文档内容
高考解密08 水溶液中的离子反应与平衡
A 组 基础练
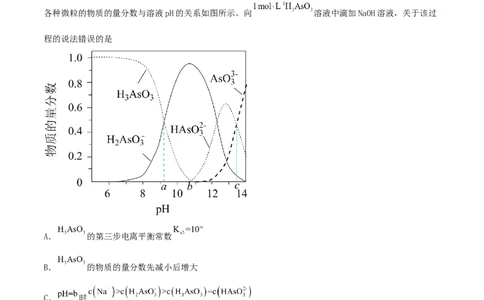
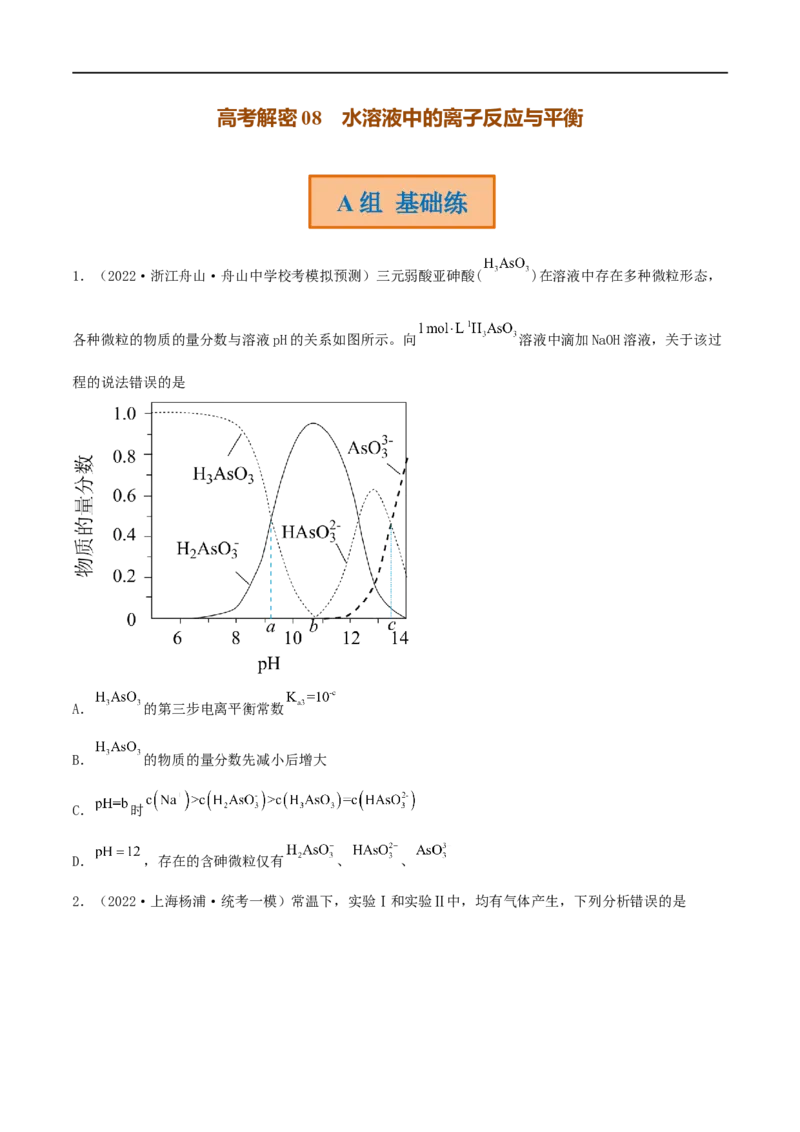
1.(2022·浙江舟山·舟山中学校考模拟预测)三元弱酸亚砷酸( )在溶液中存在多种微粒形态,
各种微粒的物质的量分数与溶液pH的关系如图所示。向 溶液中滴加NaOH溶液,关于该过
程的说法错误的是
A. 的第三步电离平衡常数
B. 的物质的量分数先减小后增大
C. 时
D. ,存在的含砷微粒仅有 、 、
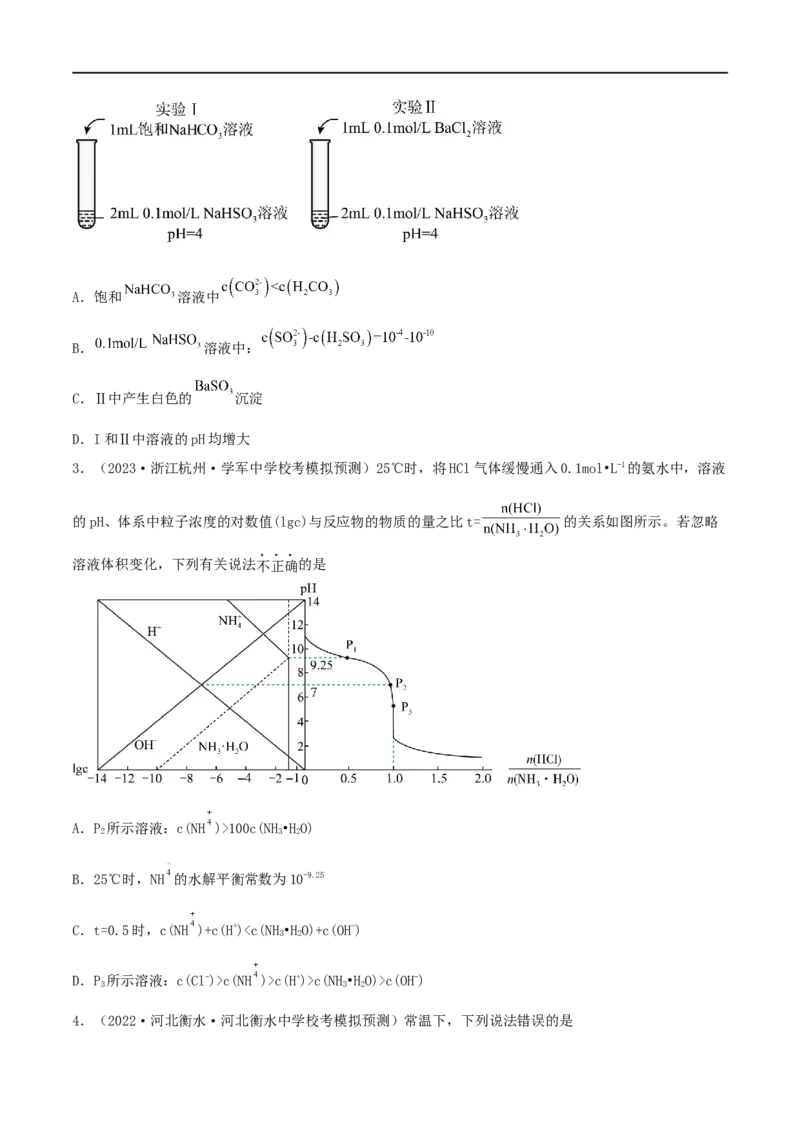
2.(2022·上海杨浦·统考一模)常温下,实验Ⅰ和实验Ⅱ中,均有气体产生,下列分析错误的是A.饱和 溶液中
B. 溶液中:
C.Ⅱ中产生白色的 沉淀
D.I和Ⅱ中溶液的pH均增大
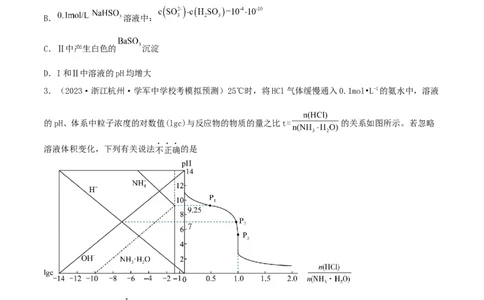
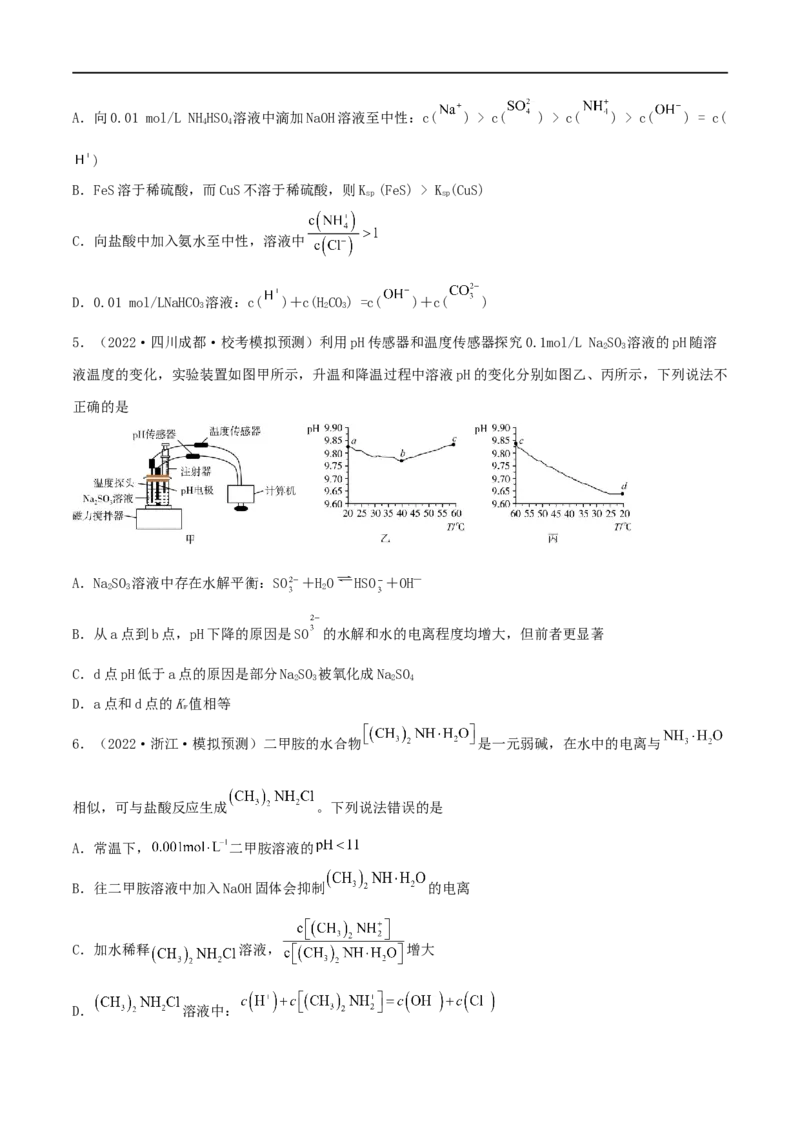
3.(2023·浙江杭州·学军中学校考模拟预测)25℃时,将HCl气体缓慢通入0.1mol•L-1的氨水中,溶液
的pH、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比t= 的关系如图所示。若忽略
溶液体积变化,下列有关说法不正确的是
A.P 所示溶液:c(NH )>100c(NH•HO)
2 3 2
B.25℃时,NH 的水解平衡常数为10-9.25
C.t=0.5时,c(NH )+c(H+)c(NH )>c(H+)>c(NH•HO)>c(OH-)
3 3 2
4.(2022·河北衡水·河北衡水中学校考模拟预测)常温下,下列说法错误的是A.向0.01 mol/L NHHSO 溶液中滴加NaOH溶液至中性:c( ) > c( ) > c( ) > c( ) = c(
4 4
)
B.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则K (FeS) > K (CuS)
sp sp
C.向盐酸中加入氨水至中性,溶液中
D.0.01 mol/LNaHCO 溶液:c( )+c(HCO) =c( )+c( )
3 2 3
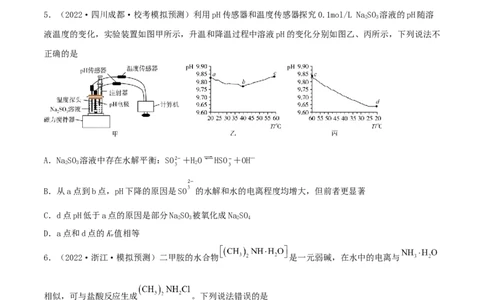
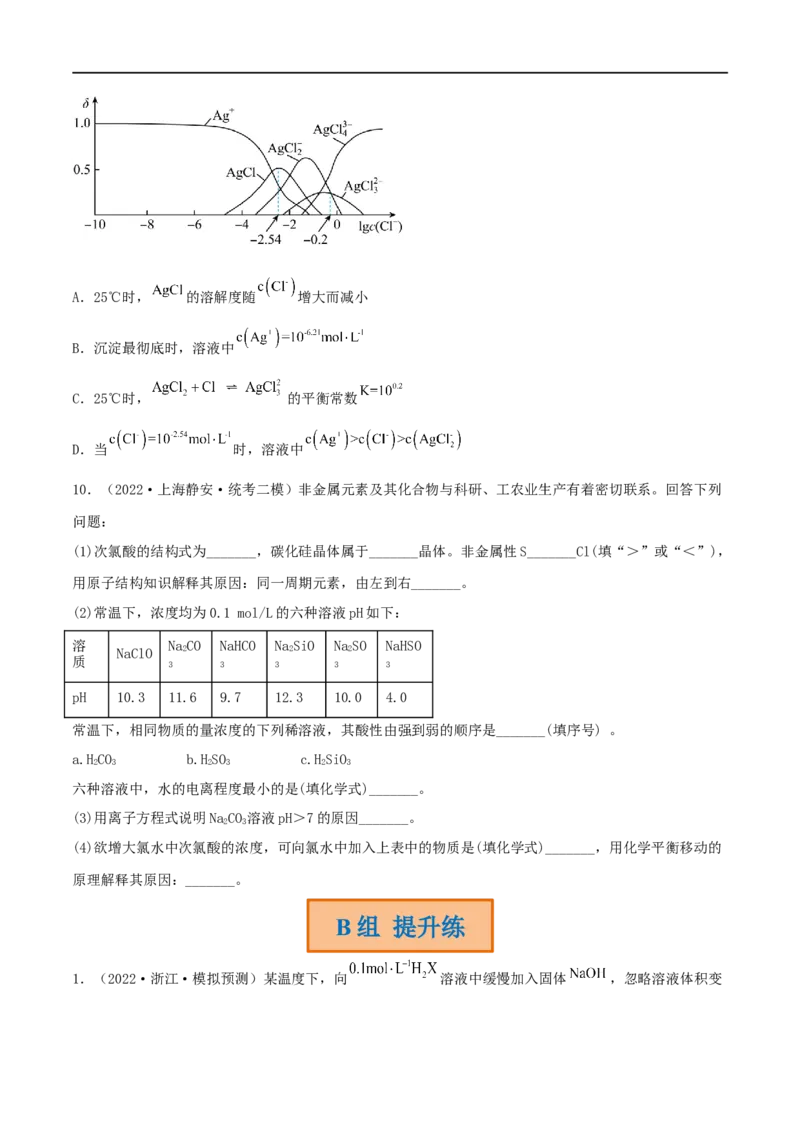
5.(2022·四川成都·校考模拟预测)利用pH传感器和温度传感器探究0.1mol/L NaSO 溶液的pH随溶
2 3
液温度的变化,实验装置如图甲所示,升温和降温过程中溶液pH的变化分别如图乙、丙所示,下列说法不
正确的是
A.NaSO 溶液中存在水解平衡:SO +HO HSO +OH—
2 3 2
B.从a点到b点,pH下降的原因是SO 的水解和水的电离程度均增大,但前者更显著
C.d点pH低于a点的原因是部分NaSO 被氧化成NaSO
2 3 2 4
D.a点和d点的K值相等
w
6.(2022·浙江·模拟预测)二甲胺的水合物 是一元弱碱,在水中的电离与
相似,可与盐酸反应生成 。下列说法错误的是
A.常温下, 二甲胺溶液的
B.往二甲胺溶液中加入NaOH固体会抑制 的电离
C.加水稀释 溶液, 增大
D. 溶液中:7.(2022·浙江·模拟预测)下列说法不正确的是
A.25℃时,浓度均为 的 溶液和 溶液,后者的pH较大
B.25℃时,pH相同的HCl溶液和 溶液,后者的 较大
C.常温下,将 的 溶液与 的NaOH溶液混合,混合溶液pH仍为9
D.相同温度下,中和相同pH、相同体积的盐酸和醋酸溶液,消耗NaOH物质的量不同
8.(2022·浙江·模拟预测)下列实验目的对应的实验方案设计、现象和结论都正确的是
选
实验目的 实验方案设计 现象和结论
项
探究 与 用 计测量酸酸、盐酸的 ,比较溶液 盐酸的 比醋酸小,则
A
酸性的强弱 大小 是弱酸
先产生白色沉淀,后产生蓝色
探究 和
向氢氧化钠溶液中先加入少量 溶液,
B 沉淀,说明 比
溶度积的
充分反应后再加入少量 溶液
大小 的溶度积小
滴入 溶液时,无明显变
向盛有 溶液的试管中滴加几滴 溶
探究 具有还原
C 液,振荡,再滴加几滴新制氯水,观察溶液颜 化,滴入新制氯水时溶液变血
性
色变化 红色, 具有还原性
准确称取3份 邻苯二甲酸氢钾,分别放
若滴定至溶液呈浅红色即达滴
标定 溶液的 入3个 锥形瓶中,加入 蒸馏
D 定终点,据此可计算出
浓度
水,加入2滴酚酞指示剂,用待标定的 溶液的准确浓度
标准溶液滴定
A.A B.B C.C D.D
9.(2022·重庆·西南大学附中校联考模拟预测)湿法提银工艺中,浸出 需加 沉淀。25℃,平衡
体系中含 微粒的分布系数 [如 ]随 的变化曲线如图所示,
已知: ,下列叙述正确的是A.25℃时, 的溶解度随 增大而减小
B.沉淀最彻底时,溶液中
C.25℃时, 的平衡常数
D.当 时,溶液中
10.(2022·上海静安·统考二模)非金属元素及其化合物与科研、工农业生产有着密切联系。回答下列
问题:
(1)次氯酸的结构式为_______,碳化硅晶体属于_______晶体。非金属性S_______Cl(填“>”或“<”),
用原子结构知识解释其原因:同一周期元素,由左到右_______。
(2)常温下,浓度均为0.1 mol/L的六种溶液pH如下:
溶 NaCO NaHCO NaSiO NaSO NaHSO
NaClO 2 2 2
质
3 3 3 3 3
pH 10.3 11.6 9.7 12.3 10.0 4.0
常温下,相同物质的量浓度的下列稀溶液,其酸性由强到弱的顺序是_______(填序号) 。
a.HCO b.HSO c.HSiO
2 3 2 3 2 3
六种溶液中,水的电离程度最小的是(填化学式)_______。
(3)用离子方程式说明NaCO 溶液pH>7的原因_______。
2 3
(4)欲增大氯水中次氯酸的浓度,可向氯水中加入上表中的物质是(填化学式)_______,用化学平衡移动的
原理解释其原因:_______。
B 组 提升练
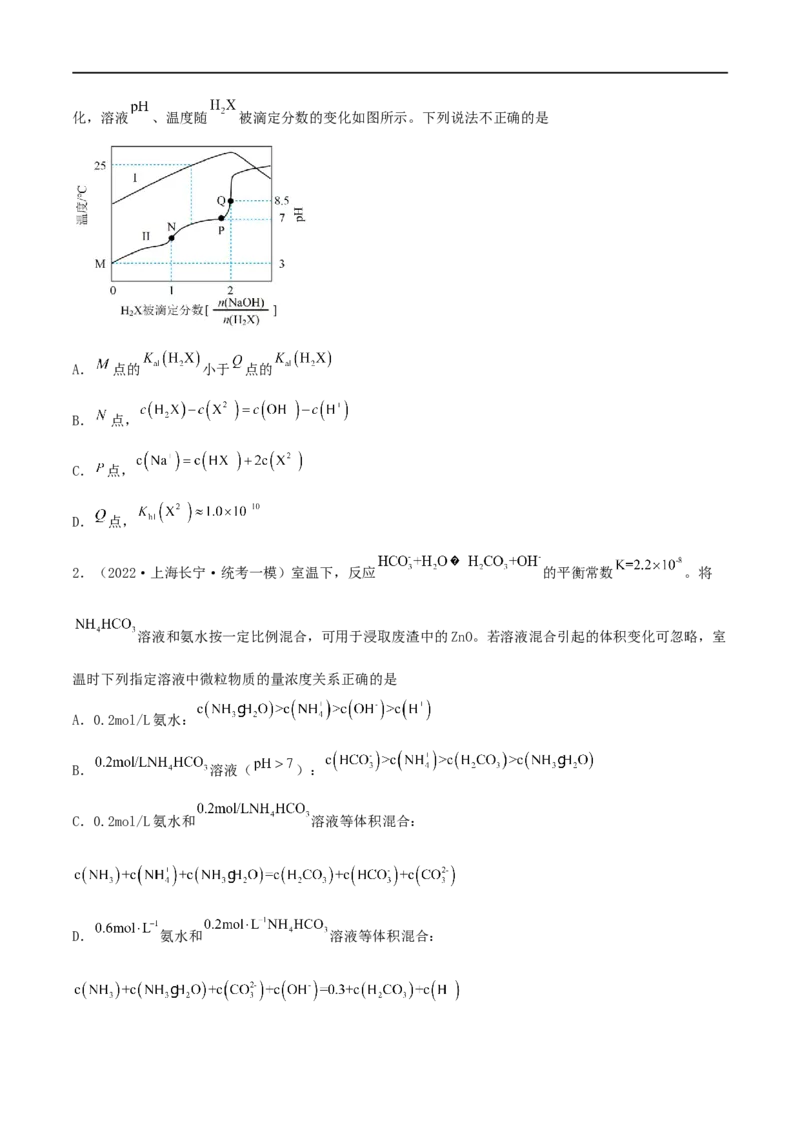
1.(2022·浙江·模拟预测)某温度下,向 溶液中缓慢加入固体 ,忽略溶液体积变化,溶液 、温度随 被滴定分数的变化如图所示。下列说法不正确的是
A. 点的 小于 点的
B. 点,
C. 点,
D. 点,
2.(2022·上海长宁·统考一模)室温下,反应 的平衡常数 。将
溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室
温时下列指定溶液中微粒物质的量浓度关系正确的是
A.0.2mol/L氨水:
B. 溶液( ):
C.0.2mol/L氨水和 溶液等体积混合:
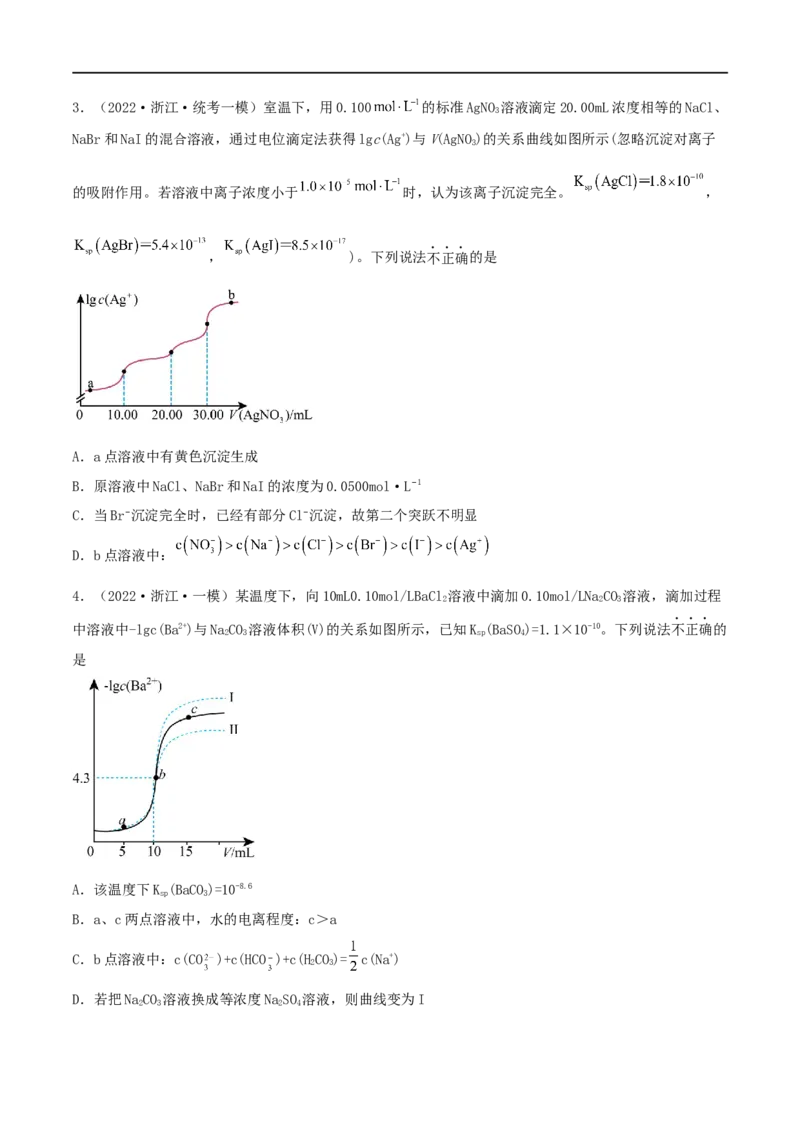
D. 氨水和 溶液等体积混合:3.(2022·浙江·统考一模)室温下,用0.100 的标准AgNO 溶液滴定20.00mL浓度相等的NaCl、
3
NaBr和NaI的混合溶液,通过电位滴定法获得lgc(Ag+)与V(AgNO)的关系曲线如图所示(忽略沉淀对离子
3
的吸附作用。若溶液中离子浓度小于 时,认为该离子沉淀完全。 ,
, )。下列说法不正确的是
A.a点溶液中有黄色沉淀生成
B.原溶液中NaCl、NaBr和NaI的浓度为0.0500mol·L−1
C.当Br−沉淀完全时,已经有部分Cl−沉淀,故第二个突跃不明显
D.b点溶液中:
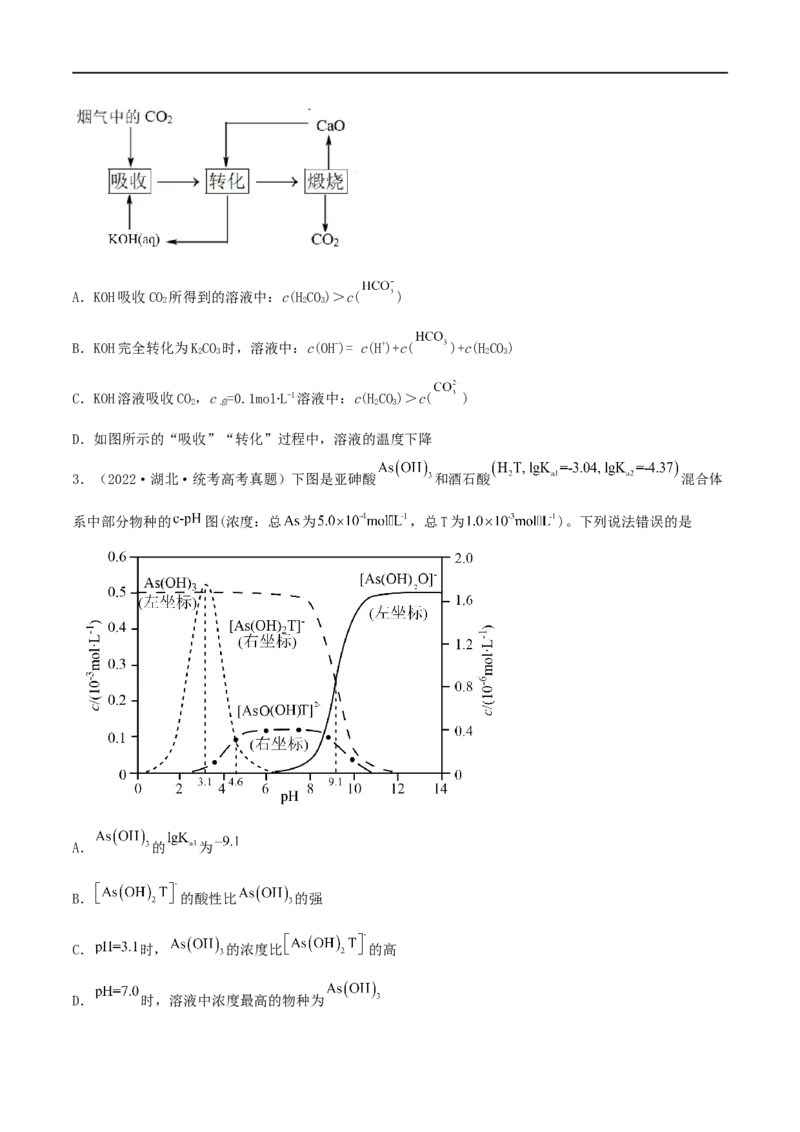
4.(2022·浙江·一模)某温度下,向10mL0.10mol/LBaCl 溶液中滴加0.10mol/LNaCO 溶液,滴加过程
2 2 3
中溶液中-lgc(Ba2+)与NaCO 溶液体积(V)的关系如图所示,已知K (BaSO)=1.1×10-10。下列说法不正确的
2 3 sp 4
是
A.该温度下K (BaCO)=10-8.6
sp 3
B.a、c两点溶液中,水的电离程度:c>a
C.b点溶液中:c(CO )+c(HCO )+c(HCO)= c(Na+)
2 3
D.若把NaCO 溶液换成等浓度NaSO 溶液,则曲线变为I
2 3 2 45.(2022·江苏·模拟预测)在含砷废水中,砷元素多以+3和+5价的形式存在。工业上常利用
磁性纳米盘等吸附剂处理含砷废水,实现水体达标排放。
(1) 水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关
系分别如图1所示。
图1
① 分子中 的空间构型为_______,将NaOH溶液滴入 溶液中,初始反应的离子方程式
为_______。
② 第一步电离方程式 ,其电离常数为 _______。
(2)① 磁性纳米盘制备:在一定条件,将 的 和PVP溶于水中并加热,
滴加过量NaOH溶液生成 ,再加入amL 的 溶液。充分反应后(
,未配平),可制得 磁性纳米盘。制备过
程中需严格控制 溶液的用量,则a=_______。
② 磁性纳米盘对酸性水中三价砷的去除能力远比五价砷的弱,可利用其中的 将酸性废
水中的 氧化成 除去,反应过程中生成 ,则反应的离子方程式为_______。③ 磁性纳米盘处理含砷废水时,水中 、 、 和 对 的吸附率的影响如图
2。 对 吸附去除几乎没有影响, 对 吸附去除影响较大。请解释 抑制 吸附去
除的可能原因_______。
C 组 真题练
1.(2022·湖北·统考高考真题)根据酸碱质子理论,给出质子 的物质是酸,给出质子的能力越强,
酸性越强。已知: , ,下列酸性强弱顺序正确
的是
A. B.
C. D.
2.(2022·江苏·高考真题)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收
2
CO,若通入CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(HCO)+c( )
2 2 2 总 2 3
+c( )。HCO 电离常数分别为K=4.4×10-7、K=4.4×10-11。下列说法正确的是
2 3 a1 a2A.KOH吸收CO 所得到的溶液中:c(HCO)>c( )
2 2 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c( )+c(HCO)
2 3 2 3
C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(HCO)>c( )
2 总 2 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
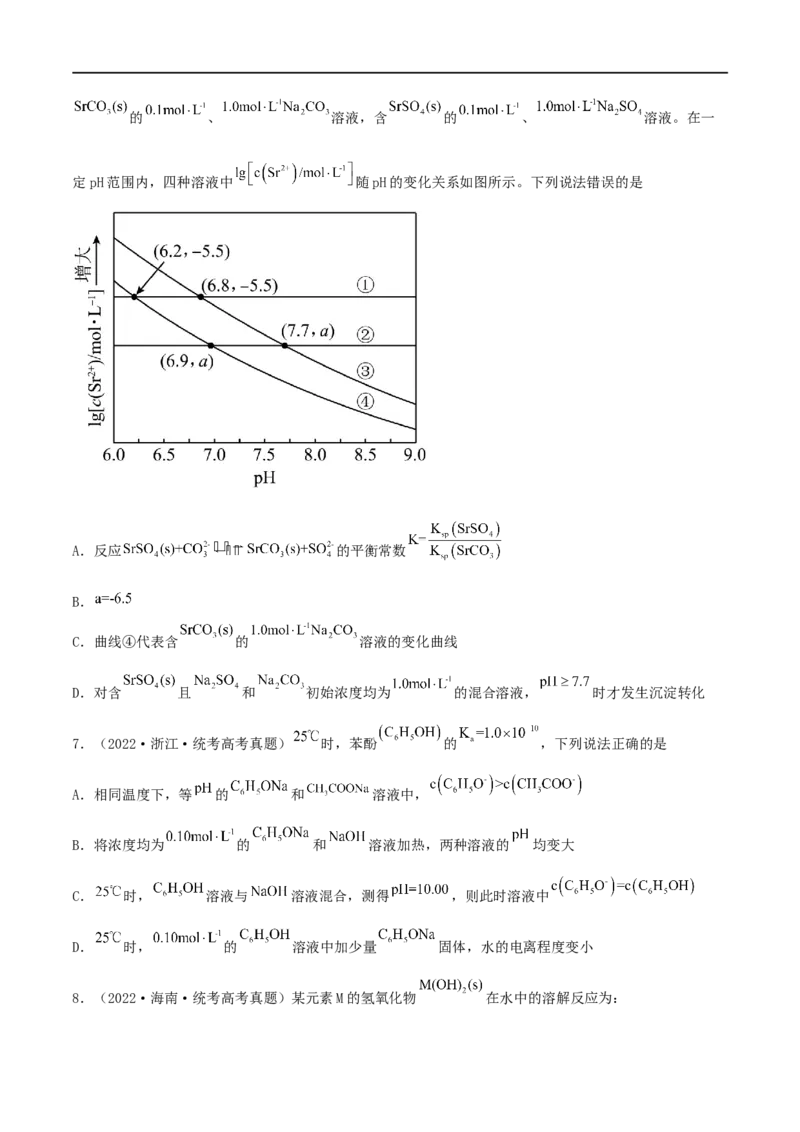
3.(2022·湖北·统考高考真题)下图是亚砷酸 和酒石酸 混合体
系中部分物种的 图(浓度:总 为 ,总T为 )。下列说法错误的是
A. 的 为
B. 的酸性比 的强
C. 时, 的浓度比 的高
D. 时,溶液中浓度最高的物种为4.(2022·辽宁·统考高考真题)甘氨酸 是人体必需氨基酸之一、在 时,
、 和 的分布分数【如 】与溶
液 关系如图。下列说法错误的是
A.甘氨酸具有两性
B.曲线c代表
C. 的平衡常数
D.
5.(2022·山东·高考真题)实验室用基准 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,
并以盐酸滴定 标准溶液。下列说法错误的是
A.可用量筒量取 标准溶液置于锥形瓶中
B.应选用配带塑料塞的容量瓶配制 标准溶液
C.应选用烧杯而非称量纸称量 固体
D.达到滴定终点时溶液显橙色
6.(2022·山东·高考真题)工业上以 为原料生产 ,对其工艺条件进行研究。现有含的 、 溶液,含 的 、 溶液。在一
定pH范围内,四种溶液中 随pH的变化关系如图所示。下列说法错误的是
A.反应 的平衡常数
B.
C.曲线④代表含 的 溶液的变化曲线
D.对含 且 和 初始浓度均为 的混合溶液, 时才发生沉淀转化
7.(2022·浙江·统考高考真题) 时,苯酚 的 ,下列说法正确的是
A.相同温度下,等 的 和 溶液中,
B.将浓度均为 的 和 溶液加热,两种溶液的 均变大
C. 时, 溶液与 溶液混合,测得 ,则此时溶液中
D. 时, 的 溶液中加少量 固体,水的电离程度变小
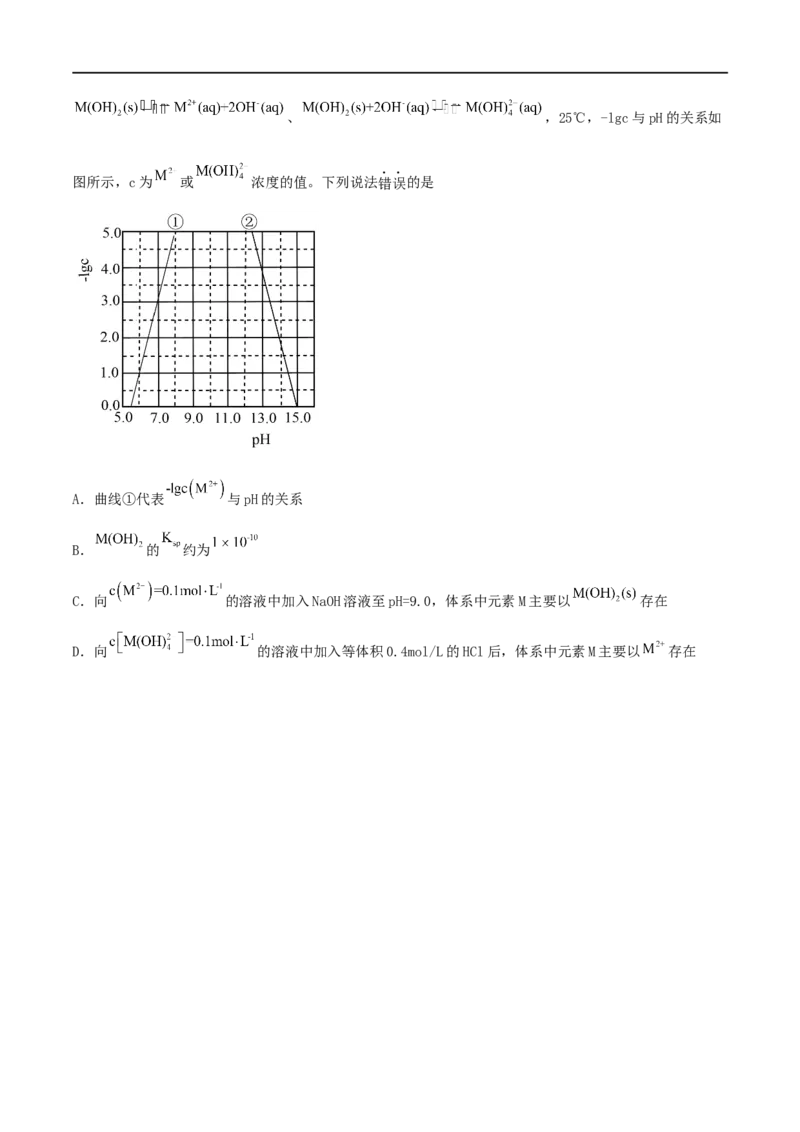
8.(2022·海南·统考高考真题)某元素M的氢氧化物 在水中的溶解反应为:、 ,25℃,-lgc与pH的关系如
图所示,c为 或 浓度的值。下列说法错误的是
A.曲线①代表 与pH的关系
B. 的 约为
C.向 的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以 存在
D.向 的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 存在