文档内容
离子反应
【学习目标】
1.了解电离、强弱电解质的概念;
2.了解离子反应的概念,掌握离子反应发生的条件,能正确书写简单的离子方程式。
【学习重点】
离子共存,离子方程式的正误判断是本节的重点内容;
【学习难点】
离子方程式的书写或判断正误及离子推断是本节的难点。
【学习过程】
一、电解质的电离
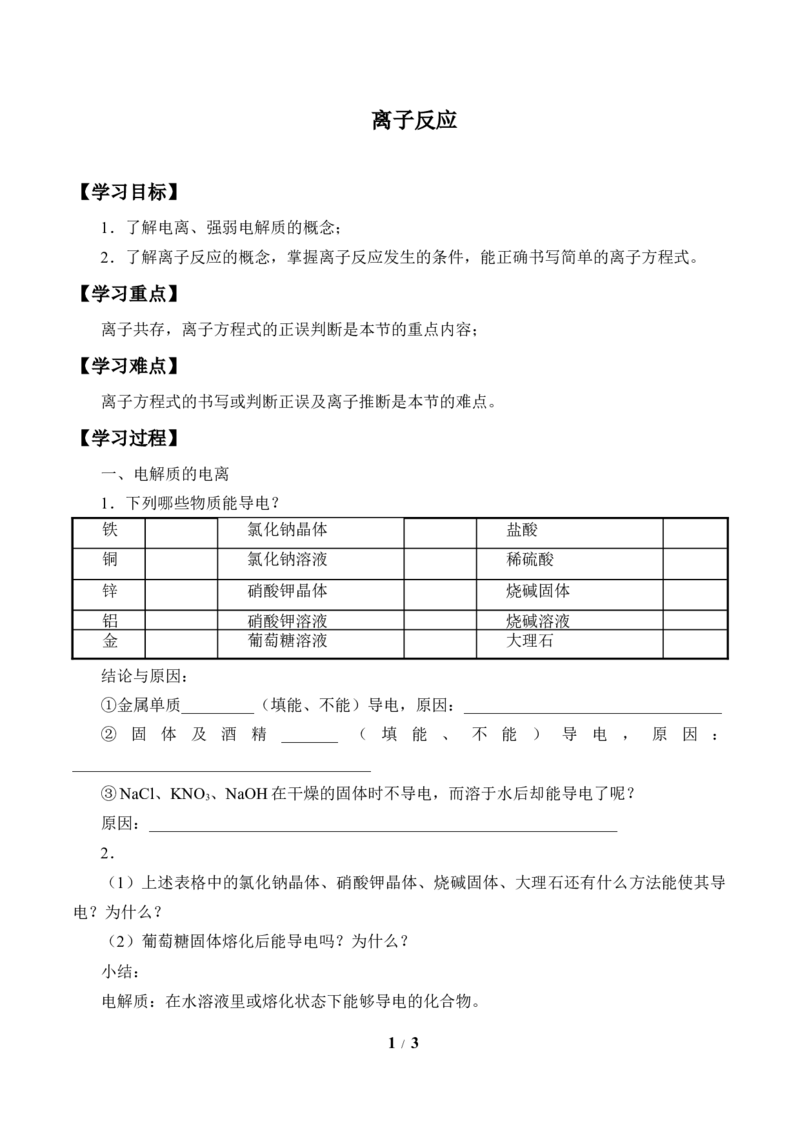
1.下列哪些物质能导电?
铁 氯化钠晶体 盐酸
铜 氯化钠溶液 稀硫酸
锌 硝酸钾晶体 烧碱固体
铝 硝酸钾溶液 烧碱溶液
金 葡萄糖溶液 大理石
结论与原因:
①金属单质_________(填能、不能)导电,原因:________________________________
② 固 体 及 酒 精 _______ ( 填 能 、 不 能 ) 导 电 , 原 因 :
_____________________________________
③NaCl、KNO 、NaOH在干燥的固体时不导电,而溶于水后却能导电了呢?
3
原因:__________________________________________________________
2.
(1)上述表格中的氯化钠晶体、硝酸钾晶体、烧碱固体、大理石还有什么方法能使其导
电?为什么?
(2)葡萄糖固体熔化后能导电吗?为什么?
小结:
电解质:在水溶液里或熔化状态下能够导电的化合物。
1 / 3非电解质:在水溶液里和熔化状态下都不能导电的化合物。
二、离子反应
1.定义:
2.表示:离子反应方程式
步骤:
写出下列反应的离子方程式
(1)硫酸与氢氧化钠溶液反应
(2)盐酸与氢氧化钡溶液反应
(3)氯化钡溶液与稀硫酸反应
(4)氢氧化钡溶液与硫酸钠溶液
3.含义:①_______ ②________
判断下列溶液中的反应是否能够进行,如果能则写出离子反应方程式。
(1)硫酸与氯化钠溶液混合
(2)盐酸与碳酸氢钠溶液混合
(3)氯化银放入稀硫酸溶液中
(4)锌放入稀硫酸溶液中
4.实质:
5.应用:化学反应能否进行、离子共存问题
知识巩固
①溶液中下列离子能大量共存的一组是( )
A.H+、 K+、 O2-、 SO 2-
4
B.K+、 Mg2+、 OH-、 NO3-
C.Na+、 Ca2+、 Cl-、 CO 2-
3
D.Na+、 NH +、 Cl-、 SO 2-
4 4
②有同学欲配制含有四种不同离子的无色溶液,下列能配制成的是( )
A.Fe2+、 H+、 NO -、 Cl-
3
B.Ca2+ 、 H+、 Cl-、 HCO -
3
C.Mg2+、 Al3+、 Cl-、 SO 2-
4
D.Na+、 NH + 、 OH- 、 NO -
4 3
③下列反应属于离子反应的是( )
A.高锰酸钾加热分解制取O
2
2 / 3B.H 和O 反应生成H O
2 2 2
C.Zn片投入稀硫酸溶液中
D.NH 遇HCl气体生成白烟(NH Cl)
3 4
归纳总结:
离子方程式书写的基本要求
(1)合事实:离子反应要符合客观事实;
(2)式正确:化学式与离子符号使用正确合理;
(3)号实际:“=” “ ”“→” “↓” “↑”等符号符合实际;
(4)看条件:看清条件中各物质反应的配比;
(5)三守恒:两边原子数、电荷数必须守恒、氧化还原反应电子得失守恒。
3 / 3