文档内容
第3讲 燃烧热
【学习目标】
1、理解燃烧热的概念
2、学会利用燃烧热进行相关的计算
3、了解家用燃料和火箭推进剂燃料的选择。
【学习重难点】
重点:燃烧热的概念及其计算
难点:燃烧热的相关计算
【自主预习】
1、请结合以下数据计算2H(g)+O(g)=2HO(g)的反应热 ,写出该反应的热化学方程式?
2 2 2
①断开1molH-H键要吸收436kJ的能量
②断开1molO-O键要吸收498kJ的能量
③形成2molH—O键要放出431kJ的能量
2.燃烧热定义: ,1mol纯物质完全燃烧生成 时所放出的热量。
【合作探究】
一.理解燃烧热的概念
1、燃烧热的定义:
【思考讨论1】我们知道物质燃烧都会放出热量,那么是不是物质燃烧放出的热量就叫燃烧热呢?
①研究条件:
②反应物及其物质的量:
③反应程度:
④生成物:
⑤燃烧热与物质的多少无关,只与物质的种类有关
⑥符号: 单位:
【思考讨论2】燃烧放出的热量与燃烧热有什么不同?
【思考讨论3】可燃物的物质的量发生变化,其燃烧热变吗?
2、燃烧热表示的意义:
【想一想】1、已知CH 的燃烧热为890.31KJ/mol,表示的含义是什么?
4
【写一写】2、已知CH 的燃烧热为890.31KJ/mol,表示甲烷燃烧热的热化学方程式:
4
【注意事项】中文叙述燃烧热、中和热时可以不带“负号”,
但凡用ΔH表示时一定要有“负号”
例:语言表述——CH4的燃烧热为890.3 kJ/mol
符号表示——△H= -890.3 kJ/mol
【知识检测】
【典例1】分析以下几个热化学方程式,哪个是表示碳的燃烧热( )
A.C(s)+1/2O(g)=CO(g) ΔH=-110.5 kJ/mol
2B.C(s)+O(g)=CO(g) ΔH=-393.5 kJ/mol
2 2
C.2H(g)+O(g)=2HO(l) ΔH=-571.6 kJ/mol
2 2 2
D.H(g)+1/2O(g)=HO(g) ΔH=-241.8 kJ/mol
2 2 2
【变式1】下列说法正确的是( )
A.1molH 完全燃烧生成HO(g)放出的热量叫H 的燃烧热
2 2 2
B.25℃、101kPa时,1molS和2molS的燃烧热相等
C.已知S(s)+ O
2
(g)=SO
3
(g) ∆H =-269.8kJ/mol,则硫生成SO
3
的反应热为269.8kJ/mol
D.25℃、101kPa时,碳的燃烧热为-393.5kJ/mol
【变式2】书写表示下列燃料燃烧热的热化学方程式
(1)1 mol 甲烷在氧气中完全燃烧释放的能量为890 kJ
(2)28 g CO在氧气中燃烧生成CO2(g)释放的能量为283 kJ
【合作探究】
二.燃烧热的相关计算【例2】 在101 kPa时,1 mol CH 完全燃烧生成CO 和液态HO,放出890.3 kJ的
4 2 2
热量,CH 的燃烧热为多少?1000 L CH(标况)燃烧后所产生的热量为多少?
4 4
[归纳]一定量可燃物完全燃烧时放出的热量
【思考讨论4】归纳一下中和热、燃烧热的异同点
燃烧热 中和热
能量变化
相同点
ΔH
反应物的量
不同点 生成物的量
反应热的定义
【知识检测】
【典例2】中和热与57.3 kJ·mol-1的关系
已知:H+(aq) + OH-(aq) = HO(l) ΔH =﹣57.3 kJ·mol-1
2
试比较下列反应中放出的热量与 57.3 kJ 的大小:
(1)浓酸与浓碱反应生成 1 mol 水,Q1 _____57.3 kJ, ΔH1 _____ ΔH;
(2)弱酸与弱碱反应生成 1 mol 水,Q2 _____57.3 kJ, ΔH2 _____ ΔH;
(3)强酸与强碱反应生成 1 mol 水和难溶性盐,Q3 _____57.3 kJ, ΔH3 _____ ΔH。【变式1】已知充分燃烧a g乙烯气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则乙烯燃
烧的热化学方程式正确的是( )
A.CH(g)+3O(g)=2CO(g)+2HO(l) ΔH=-2b kJ/mol
2 4 2 2 2
B.CH(g)+3O(g)=2CO(g)+2HO(l) ΔH=+2b kJ/mol
2 4 2 2 2
C.CH(g)+6O(g)=4CO(g)+4HO(l) ΔH=-2b kJ/mol
2 4 2 2 2
D.CH(g)+6O(g)=4CO(g)+4HO(l) ΔH=+b kJ/mol
2 4 2 2 2
【变式2】已知下列两个热化学方程式:
2H(g)+O(g) =2HO(l) △H=-571.6 kJ•mol-1
2 2 2
CH(g)+5O(g) =3CO(g)+4 HO(l) △H=-2 220 kJ•mol-1
3 8 2 2 2
(1)H 的燃烧热为______________, CH 的燃烧热为_____________
2 3 8
(2)2 g H 和2 mol CH 组成的混合气体完全燃烧放出的热量为____________
2 3 8
(3)现有H 和 CH 的混合气体5 mol,完全燃烧时放出热量3847 kJ,则混合气体中H 和CH 的体积比为
2 3 8 2 3 8
____________
【合作探究】
三.了解家用燃料和火箭推进剂燃料的选择
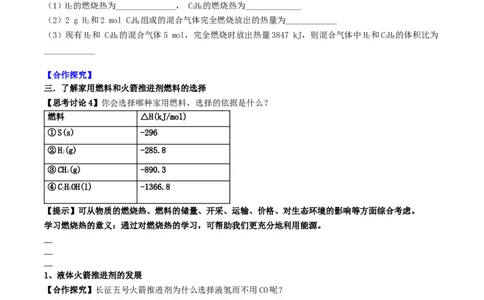
【思考讨论4】你会选择哪种家用燃料,选择的依据是什么?
燃料 △H(kJ/mol)
①S(s) -296
②H(g) -285.8
2
③CH(g) -890.3
4
④CHOH(l) -1366.8
2 5
【提示】可从物质的燃烧热、燃料的储量、开采、运输、价格、对生态环境的影响等方面综合考虑。
学习燃烧热的意义:通过对燃烧热的学习,可帮助我们更充分地利用能源。
1、液体火箭推进剂的发展
【合作探究】长征五号火箭推进剂为什么选择液氢而不用CO呢?
火箭荷载的绝大部分质量来自于推进剂,产生同样推力所需要的推进剂质量越小,火箭的荷载就越低。
计算每克液氢-液氧推进剂恰好完全反应释放的热量
2、能源
(1)定义:能源就是能提供能量的自然资源,它包括化石燃料(煤、石油、天然气)、 阳光、风力、流
水、潮汐以及柴草等。
(2)节约能源的重要措施:科学地控制燃烧反应,使燃料充分燃烧,提高能源的利用率。
(3)一级能源:来自自然界未经转化的能源。 比如:
二级能源:一级能源经过转化得到的能源形式。 比如:【知识检测】
【典例3】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水,当它们混合反应时,即产生
大量氮气和水蒸气,并放出大量热。已知0.4 mol液态肼与足量液态双氧水反应,生成氮气和水蒸气,放
出256 kJ的热量。
(1)写出该反应的热化学方程式:______________________________________________________。
(2)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是________
【变式1】(1)已知肼(NH)是一种高能燃料,将16 g气态肼在氧气中燃烧,生成氮气和水蒸气,放出267
2 4
kJ热量,试写出该反应的热化学方程式:___________________________________________________。
(2)试用化学反应能量图表示该反应过程中能量的变化。
__________________________________________________
【巩固练习】
1、下列热化学方程式中△H的绝对值能表示可燃物的燃烧热的是( )
A.H(g)+Cl(g)=2HCl(g) △H=-184.6kJ/mol
2 2
B.C(s)+ O(g)=CO(g) △H=-110.5kJ/mol
2
C.2H(g)+O(g)=2HO(l) △H=-571.6kJ/mol
2 2 2
D.CO(g)+ O(g)=CO(g) △H=-283kJ/mol
2 2
2、燃烧是人们利用热能的重要方式。下列有关燃烧热的说法正确的是( )
A.燃烧热所指的燃烧产物一定是相应元素的最高价氧化物
B.含碳物质燃烧生成 时所放出的热量是燃烧热
C.实验测定 的燃烧热时与所用 量的多少无关
D. 燃烧生成CO 时放出的热量是生成CO时放出的热量的2倍
2
3、下列有关热化学方程式的评价合理的是( )
实验事实 热化学方程式 评价
A 已知H+(aq)+OH﹣(aq)═HO HSO(aq)+Ba(OH)(aq) 正确
2 2 4 2
(l)
═BaSO(s)+2HO(l)
4 2
△H=﹣57.3 kJ•mol﹣1,将稀硫酸
△H=﹣114.6 kJ•mol﹣1
与稀氢氧化钡溶液混合
B 醋酸与稀氢氧化钠溶液混合 CHCOOH(aq)+NaOH(aq) 不正确;因为醋酸状态为
3
“aq”,而不是“l”.
═NaCl(aq)+HO(l)
2
△H=﹣57.3kJ•mol﹣1
C 160 g SO 气体与适量水恰好完全反 SO(g)+HO(l)═HSO 不正确;因为反应热为
3 3 2 2 4应生成HSO,放出热量260.6 kJ (aq) △H=﹣260.6kJ•mol﹣1
2 4
△H=﹣130.3 kJ•mol﹣1
D 已知25℃、101 kPa下,120g石墨 C(s)+O(g)═CO(g) 不正确;同素异形体要注
2 2
完全燃烧放出热量3935.1 kJ 名称:C(石墨)
△H=﹣393.51 kJ•mol﹣1
A.A B.B C.C D.D