文档内容
第一章 物质及其变化
第一节 物质的分类及转化
第三课时 物质的转化
【学习目标】1.通过回顾初中酸、碱、盐的性质荷反应类型,结合教材中的“思考与讨论”等,进一
步理解物质分类法的应用,更深入研究物质的制取方法。
2.通过对化学物质按组成和性质进行分类法的学习,进一步掌握酸、碱、盐、氧化物的概念及性
质,理解化工生成过程中条件的选择原则,会预测在一定条件下某种物质能发生的化学变化。
【学习重点】酸、碱、盐的主要性质和转化及工业生成中化工原料和条件的选择。
【学习难点】根据酸、碱、盐及氧化物的性质理解各类物质间的转化关系。
【课前预习】
旧知回顾:从 Zn、 BaC1 、 NaOH、 KClO、CuC1 、NaSO 、Na0、 H0、 HSO 等物质中,选出
2 3 2 2 4 2 2 2 4
适当的物质,按①化合反应;②分解反应;③置换反应;④复分解反应类型写出化学方程式。
新知预习: 1.O 和CO 同为酸性氧化物,根据酸性氧化物具有的通性(或CO 的性质),可推测SO 具
2 2 2 2
有 的 性 质 , 用 化 学 方 程 式 可 表 示 为 :
。
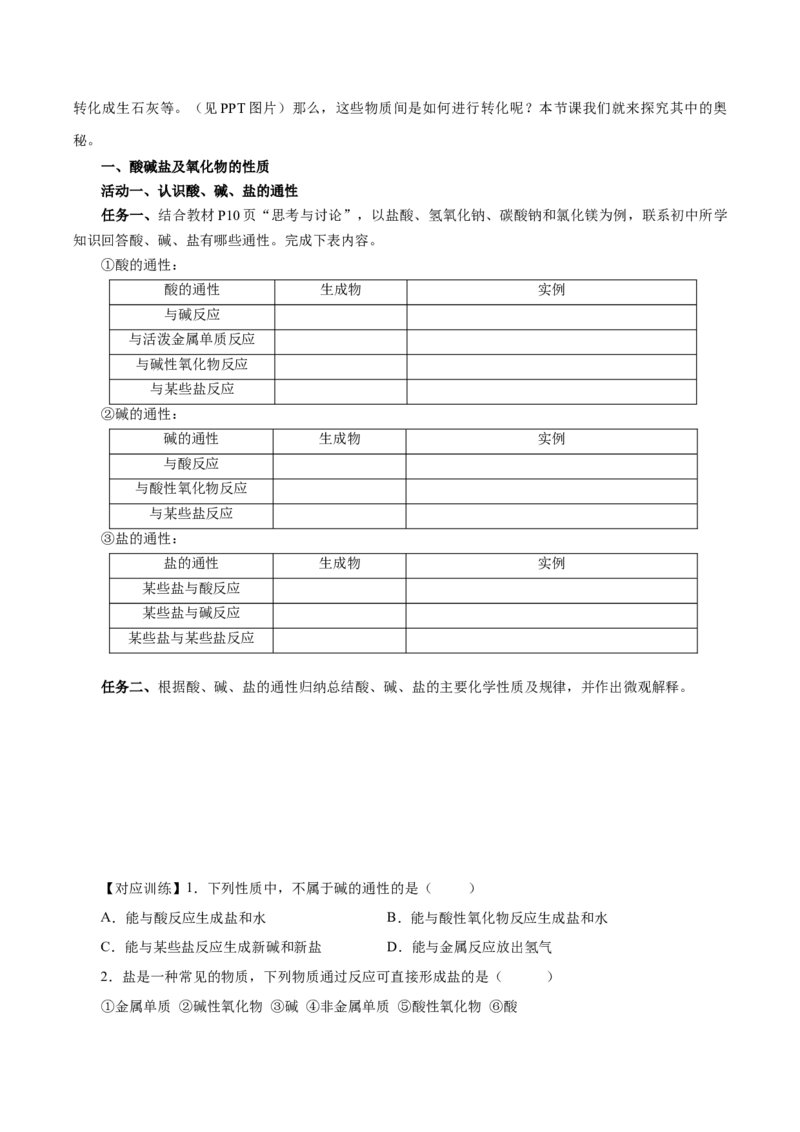
2.通过物质分类,可以建立物质间的从属关系,分析物质间的本质区别和联系,寻找各类物质之间的
转化关系。以钙为例,用化学方程式表示钙及其化合物之间的转化关系以及反应类型如下:
【课中探究】
情景导入:前面我们学习了物质的分类,知道同一类的化学物质在性质上具有一定的相似性,因此可以
从物质的性质进行分类。其实,各类物质在一定条件下还可以相互转化。我们知道世界上最奇妙的转化就
是---大自然的创造。如动植物可以转化为化石燃料、一粒种子可以转化成美丽的花朵、鸡蛋壳或贝壳可以转化成生石灰等。(见PPT图片)那么,这些物质间是如何进行转化呢?本节课我们就来探究其中的奥
秘。
一、酸碱盐及氧化物的性质
活动一、认识酸、碱、盐的通性
任务一、结合教材P10页“思考与讨论”,以盐酸、氢氧化钠、碳酸钠和氯化镁为例,联系初中所学
知识回答酸、碱、盐有哪些通性。完成下表内容。
①酸的通性:
酸的通性 生成物 实例
与碱反应
与活泼金属单质反应
与碱性氧化物反应
与某些盐反应
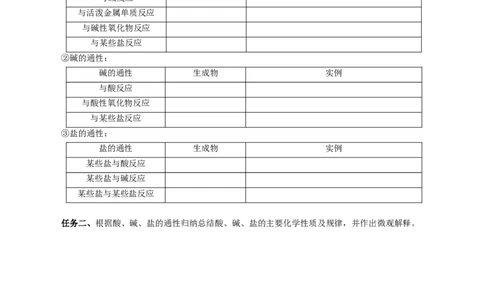
②碱的通性:
碱的通性 生成物 实例
与酸反应
与酸性氧化物反应
与某些盐反应
③盐的通性:
盐的通性 生成物 实例
某些盐与酸反应
某些盐与碱反应
某些盐与某些盐反应
任务二、根据酸、碱、盐的通性归纳总结酸、碱、盐的主要化学性质及规律,并作出微观解释。
【对应训练】1.下列性质中,不属于碱的通性的是( )
A.能与酸反应生成盐和水 B.能与酸性氧化物反应生成盐和水
C.能与某些盐反应生成新碱和新盐 D.能与金属反应放出氢气
2.盐是一种常见的物质,下列物质通过反应可直接形成盐的是( )
①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸A.①②③ B.①④⑥ C.②⑤⑥ D.①②③④⑤⑥
活动二、探究氧化物的化学性质
任务一、讨论交流:酸性氧化物和碱性氧化物有哪些通性?
任务二、讨论交流:酸性氧化物、碱性氧化物与金属氧化物和非金属氧化物有何关系?
任务三、问题探究:结合教材P10页“思考与讨论”(3),思考酸、碱、盐的主要化学性质中,涉
及哪些化学反应?
【对应训练】1.下列有关氧化物的判断正确的是( )
A.凡是含氧的化合物均可称为氧化物
B.依据性质不同氧化物只能分为酸性氧化物和碱性氧化物
C.酸性氧化物都能与碱反应生成盐和水
D.金属氧化物一定是碱性氧化物
2.北京冬奥会或第24届冬季奥林匹克运动会将在2022年2月4日至2022年2月20日在中华人民共
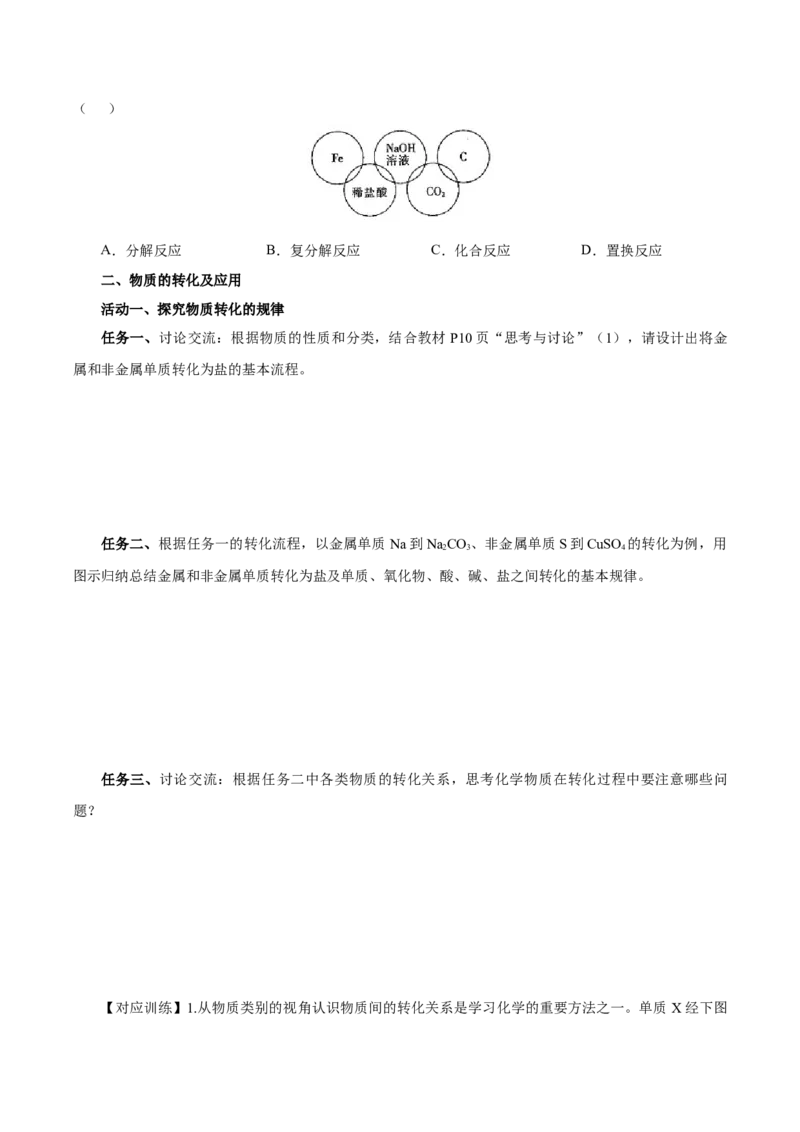
和国北京市和河北省张家口市联合举行。某同学在奥运五连环中填入了5种物质,相连环物质间能发生反
应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型是( )
A.分解反应 B.复分解反应 C.化合反应 D.置换反应
二、物质的转化及应用
活动一、探究物质转化的规律
任务一、讨论交流:根据物质的性质和分类,结合教材 P10页“思考与讨论”(1),请设计出将金
属和非金属单质转化为盐的基本流程。
任务二、根据任务一的转化流程,以金属单质Na到NaCO 、非金属单质S到CuSO 的转化为例,用
2 3 4
图示归纳总结金属和非金属单质转化为盐及单质、氧化物、酸、碱、盐之间转化的基本规律。
任务三、讨论交流:根据任务二中各类物质的转化关系,思考化学物质在转化过程中要注意哪些问
题?
【对应训练】1.从物质类别的视角认识物质间的转化关系是学习化学的重要方法之一。单质 X经下图所示过程可转化为含氧酸W。下列说法正确的是( )
X Y Z W
A.X是金属钠 B.Y一定能使品红溶液褪色
C.W的浓溶液见光一定会分解 D.Z中氧元素的质量分数一定高于Y
2.推理是学习化学的一种重要方法。以下推理正确的是( )
A.酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
B.碱中都含有氢氧根,所以碱中一定含有氢元素
C.酸能使紫色石蕊溶液变红,CO 通入紫色石蕊溶液后溶液变红,所以CO 是酸
2 2
D.碱能使无色酚酞溶液变红,所以能使无色酚酞溶液变红的都是碱
活动二、物质转化的应用
任务一、阅读教材P11页第二自然段,思考如何利用物质间的转化关系制备所需要的物质?
任务二、阅读教材P11页第三自然段,以制备氢氧化钠为例,说明在具体的生产过程中怎样选择更合
适的途径。
【对应训练】1.下列物质中不能用化合反应的方法生成的是( )
①Fe O ②HSiO ③Fe(OH) ④Cu(OH) ⑤FeCl ⑥CaSiO
3 4 2 3 3 2 2 3
A.①③④⑥ B.②④
C.②④⑤ D.①②④
2.已知:物质X与Ca(OH) 在水溶液中能发生反应,反应的化学方程式如下:
2
X+Ca(OH) =Y+Cu(OH) ↓。下列分析错误的是( )
2 2
A.X肯定不可能是酸 B.X和Y的相对分子质量之差为24
C.X可能是单质,也可能是化合物 D.Y可以是CaCl 或Ca(NO )
2 3 2
【课后巩固】1.(易)教材作业:P12习题5、6 、7、82.(易)通过下列变化,均无法得单质的是:①分解反应 ②化合反应 ③置换反应 ④复分解反应(
)
A.①② B.①③ C.③④ D.②④
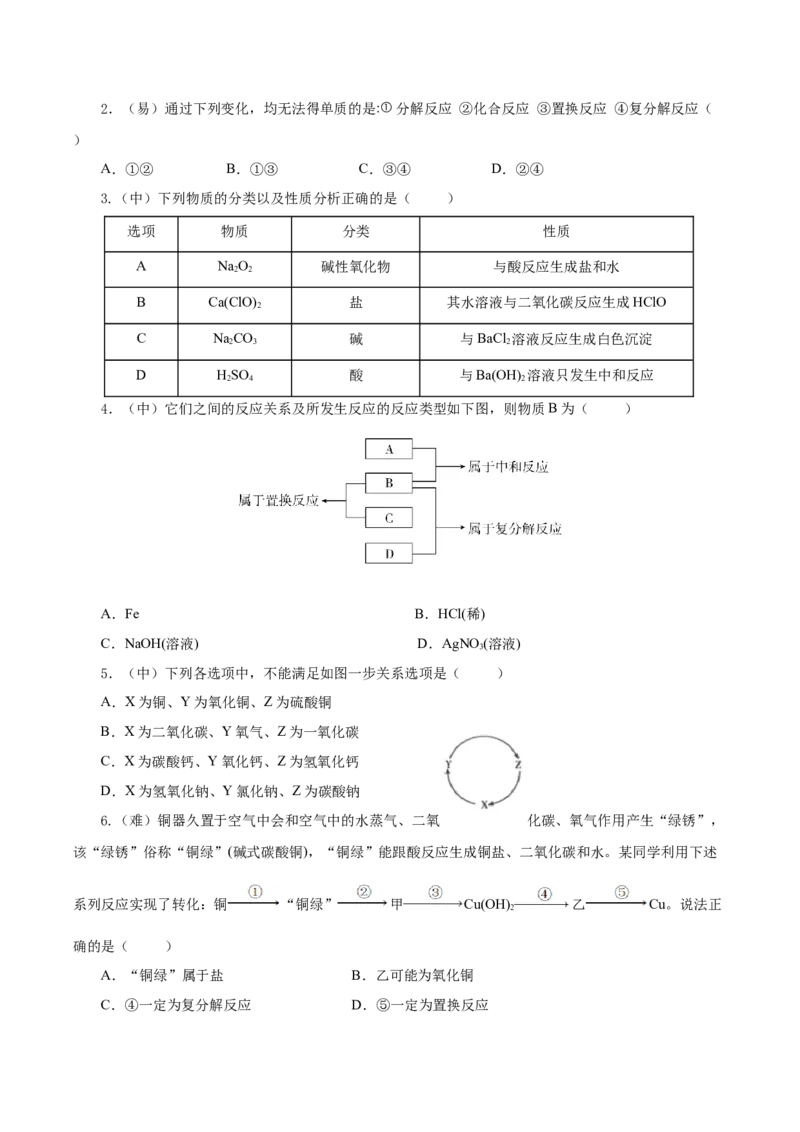
3.(中)下列物质的分类以及性质分析正确的是( )
选项 物质 分类 性质
A NaO 碱性氧化物 与酸反应生成盐和水
2 2
B Ca(ClO) 盐 其水溶液与二氧化碳反应生成HClO
2
C NaCO 碱 与BaCl 溶液反应生成白色沉淀
2 3 2
D HSO 酸 与Ba(OH) 溶液只发生中和反应
2 4 2
4.(中)它们之间的反应关系及所发生反应的反应类型如下图,则物质B为( )
A.Fe B.HCl(稀)
C.NaOH(溶液) D.AgNO(溶液)
3
5.(中)下列各选项中,不能满足如图一步关系选项是( )
A.X为铜、Y为氧化铜、Z为硫酸铜
B.X为二氧化碳、Y氧气、Z为一氧化碳
C.X为碳酸钙、Y氧化钙、Z为氢氧化钙
D.X为氢氧化钠、Y氯化钠、Z为碳酸钠
6.(难)铜器久置于空气中会和空气中的水蒸气、二氧 化碳、氧气作用产生“绿锈”,
该“绿锈”俗称“铜绿”(碱式碳酸铜),“铜绿”能跟酸反应生成铜盐、二氧化碳和水。某同学利用下述
系列反应实现了转化:铜 “铜绿” 甲 Cu(OH) 乙 Cu。说法正
2
确的是( )
A.“铜绿”属于盐 B.乙可能为氧化铜
C.④一定为复分解反应 D.⑤一定为置换反应7.(难)如图,箭头方向表示在通常条件下能与某种常见试剂发生转化,6步转化均能一步实现的一
组物质是( )
物质选项 W X Y Z
A Cu
B Na NaOH
C
D S
8.(中)牙膏中的摩擦剂碳酸钙可用石灰石来制备。某学生设计了一种制备碳酸钙的实验方案,其
流程图如下:
――→――→――――――――――→
(1)下列物质中,属于盐的是________。
A.CaCO B.CaO C.Ca(OH) D.NaCO
3 2 2 3
(2)请写出上述制备流程中有关反应的化学方程式,并写出基本反应类型。
①__________________________________,_____________;
②__________________________________,_____________;
③__________________________________,_____________。
(3)请你仍以石灰石为原料(其他试剂自选),设计另外一种制碳酸钙的方案,依照上述流程写出你的制
备流程图。
你所设计方案的优点是_______________________________________。
【反思总结】
。