文档内容
第一章 原子结构与性质
第一节 原子结构
第二课时 构造原理与电子排布式
基础达标
1.观察1s轨道电子云示意图,判断下列说法正确的是( )
A.一个小黑点表示1个自由运动的电子
B.1s轨道的电子云为圆形
C.电子在1s轨道上运动像地球围绕太阳旋转
D.1s轨道电子云的点的疏密表示电子在某一位置出现概率的大小
2.下列关于电子云的说法中,正确的是( )
A.电子云表示电子在原子核外运动的轨迹
B.电子云表示电子在核外单位体积的空间出现的机会的多少
C.电子云界面图中的小点越密表示该核外空间的电子越多
D.电子云可表示电子在核外运动的方向
3.“各能级最多容纳的电子数是该能级原子轨道数的两倍”支撑这一结论的理论是(
)
A.构造原理 B.泡利原理 C.洪特规则 D.能量最低原理
4.某原子核外电子排布为ns2np7,它违背了( )
A.能量最低原理 B.泡利不相容原理 C.洪特规则 D.洪特规则特例
5.在d轨道中电子排布成 ,而不排布成 ,遵循的是(
)
A.能量最低原理 B.泡利原理 C.原子轨道构造原理 D.洪特规则
6.下列离子中d轨道达半充满状态的是( )
A. Cr3+ B. Cu+ C. Co3+ D.Fe3+
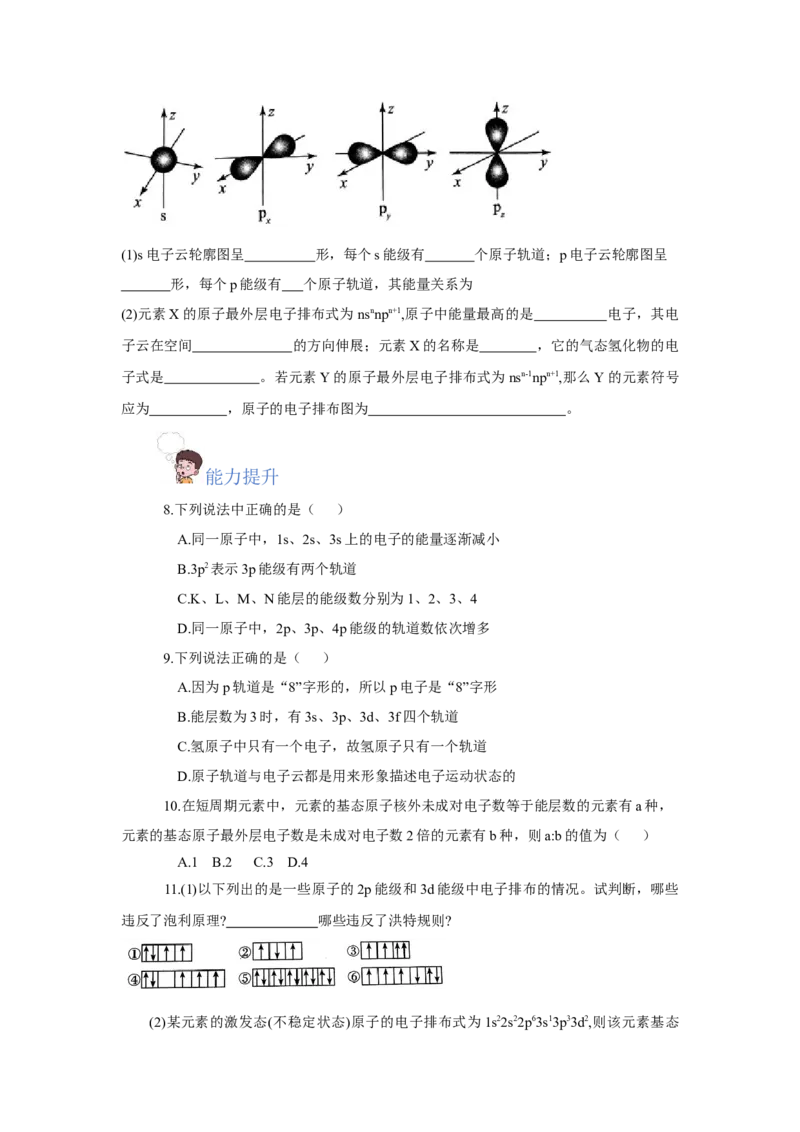
7.如图所示是s能级和p能级的电子云轮廓图,试回答下列问题。(1)s电子云轮廓图呈 形,每个s能级有 个原子轨道;p电子云轮廓图呈
形,每个p能级有 个原子轨道,其能量关系为
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是 电子,其电
子云在空间 的方向伸展;元素X的名称是 ,它的气态氢化物的电
子式是 。若元素Y的原子最外层电子排布式为nsn-1npn+1,那么Y的元素符号
应为 ,原子的电子排布图为 。
能力提升
8.下列说法中正确的是( )
A.同一原子中,1s、2s、3s上的电子的能量逐渐减小
B.3p2表示3p能级有两个轨道
C.K、L、M、N能层的能级数分别为1、2、3、4
D.同一原子中,2p、3p、4p能级的轨道数依次增多
9.下列说法正确的是( )
A.因为p轨道是“8”字形的,所以p电子是“8”字形
B.能层数为3时,有3s、3p、3d、3f四个轨道
C.氢原子中只有一个电子,故氢原子只有一个轨道
D.原子轨道与电子云都是用来形象描述电子运动状态的
10.在短周期元素中,元素的基态原子核外未成对电子数等于能层数的元素有a种,
元素的基态原子最外层电子数是未成对电子数2倍的元素有b种,则a:b的值为( )
A.1 B.2 C.3 D.4
11.(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些
违反了泡利原理? 哪些违反了洪特规则?
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为 其最高价氧化物对应水化物的化学式是
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列。
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是 (填序号)
直击高考
12.具有如下电子层结构的原子,其相应元素一定属于同一主族的是( )
A.3p轨道上有2个未成对电子的原子和4p轨道上有2个未成对电子的原子
B.3p轨道上只有1个空轨道的原子和4p轨道上只有1个空轨道的原子
C.最外层电子排布式为1s2的原子和最外层电子排布式为2s22p6的原子
D.最外层电子排布式为1s2的原子和最外层电子排布式为2s2的原子
13.已知A原子中只含1个电子;B原子的3p轨道上得到个电子后不能容纳外来电子;
C原子的2p轨道上有1个电子的自旋方向与其他电子的自旋方向相反;D原子的第三能层
上有8个电子,第四能层上只有1个电子;E原子的最外层电子排布式为3s23p6。
(1)按要求书写下列图式
①B原子的结构示意图:
②C原子的电子排布图:
③D原子的核外电子排布式:
(2)写出由上述元素组成的物质制得A的单质的化学方程式:
(至少写出2个)。
(3)要证明太阳光中含有E元素,可采用的方法是