文档内容
第二章 化学物质及其变化
第三节 氧化还原反应
第一课时 氧化还原反应
【学习目标】1.通过思考交流、归纳小结,熟记常见元素的化合价,能从化合价升降角度认识氧化
还原反应的特征,并能正确判断氧化还原反应。
2.通过阅读分析、归纳小结,从电子转移角度认识氧化还原反应的本质。能从宏观和微观相结合的
角度理解氧化还原反应与四种基本反应类型的关系。
3.通过分析判断、讨论交流,认识元素在物质中可以具有不同价态,还可通过氧化还原反应实现含
有不同价态同种元素的物质的相互转化。
【学习重点】氧化还原反应的特征、本质及判断。
【学习难点】用电子转移的观点理解氧化还原反应
【课前预习】
旧知回顾:1.标出下列物质中加粗元素的化合价,并指出常见元素化合价的特点和规律。
H Na CO HO CuO FeO MnO HSO Al(OH) KMnO KClO NaSO
2 2 2 2 2 3 2 2 3 3 4 3 2 2 3
【答案要点】①元素化合价(略)
②化合价特点:+1价钾钠银铵氢,+2价钡钙镁铜汞锌;二三铁、二四碳,三铝四硅五价磷,;氟、氯、
溴、碘-1价氧硫-2要记清;氢氧根、硝酸根(OH-、NO -)-1价,硫酸根、碳酸根(SO 2-、CO2-)-2价,
3 4 3
③化合价规律:化合物各元素化合价代数和为零;单质元素化合价是零。
2.从得失氧的角度看,木炭还原氧化铜:2CuO+C\o(\s\up6(_____)2Cu+CO ↑的反应中,氧化铜 失去氧
2
变成单质铜,发生了 还原 反应,碳单质 得到氧 变成了二氧化碳,发生了 氧化 反应。
新知预习:1.氧化反应和还原反应是同时发生的,这样的反应称为氧化还原反应,氧化还原反应的特
征是化学反应前后有元素化合价发生变化。氧化反应表现为被氧化的元素化合价 升高 ,其实质是该元素
的原子 失去 电子的过程;还原反应表现为被还原的元素化合价 降低 ,其实质是该元素的原子 得
到 电子的过程。
2.对于反应Fe + CuCl = FeCl + Cu ,从元素化合价升降的角度看CuCl 中铜元素化合价 降低 ,发
2 2 2
生 还原 反应,被Fe 还原 ,得到Cu,Fe中Fe元素化合价 升高 ,发生 氧化 反应,被CuCl 氧化 ,
2
得到HO。
2
【课中探究】
情景导入:苹果削皮后放置一段时间会变黄色(或褐色)、喝红酒之前要先把红酒倒入醒酒器中,敞
口放置一段时间,喝起来更加绵柔滑润,更加可口、家中炒菜的铁锅或钢铁会生锈、补充维生素可以延缓皮肤老化、长久放置的食物会腐败变质等等。以上都是生活中不起眼的小常识,但是在这些常识中实际蕴
含着一些重要的化学理论。本节课,我们就要以这些常识为开端,学习一种新的反应类型。(见PPT图
片)
一、氧化还原反应的特征
活动一、认识氧化还原反应
任务一、回顾初中所学氧化反应和还原反应的概念,结合教材P22页“思考与讨论(1)”, 回答什
么是氧化还原反应?并完成下表内容。
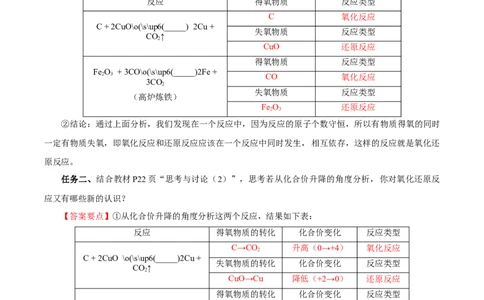
【答案要点】①从得失氧的角度来定义氧化反应和还原反应,分析结果如下表:
反应 得氧物质 反应类型
C 氧化反应
C + 2CuO\o(\s\up6(_____) 2Cu +
失氧物质 反应类型
CO↑
2
CuO 还原反应
得氧物质 反应类型
Fe O + 3CO\o(\s\up6(_____)2Fe +
2 3 CO 氧化反应
3CO
2
失氧物质 反应类型
(高炉炼铁)
Fe O 还原反应
2 3
②结论:通过上面分析,我们发现在一个反应中,因为反应的原子个数守恒,所以有物质得氧的同时
一定有物质失氧,即氧化反应和还原反应应该在一个反应中同时发生,相互依存,这样的反应就是氧化还
原反应。
任务二、结合教材P22页“思考与讨论(2)”,思考若从化合价升降的角度分析,你对氧化还原反
应又有哪些新的认识?
【答案要点】①从化合价升降的角度分析这两个反应,结果如下表:
反应 得氧物质的转化 化合价变化 反应类型
C→CO 升高(0→+4) 氧化反应
2
C + 2CuO \o(\s\up6(_____)2Cu +
失氧物质的转化 化合价变化 反应类型
CO↑
2
CuO→Cu 降低(+2→0) 还原反应
得氧物质的转化 化合价变化 反应类型
Fe O + 3CO\o(\s\up6(_____)2Fe +
2 3 CO→CO 升高(+2→+4) 氧化反应
3CO 2
2
失氧物质的转化 化合价变化 反应类型
(高炉炼铁)
Fe O→Fe 降低(+3→0) 还原反应
2 3
②结论:在氧化还原反应中,得氧的反应,有元素的化合价升高,发生了氧化反应;失氧的反应,元
素的化合价降低,发生了还原反应。
任务三、问题探究:分析反应Cl+H O===HCl+HClO和2KMnO \o(\s\up6(_____)KMnO +MnO +
2 2 4 2 4 2
O↑,还可以得出什么结论?
2【答案要点】①特点:反应Cl+H O===HCl+HClO中只有氯元素化合价变化:Cl(0价)→HCl(-1
2 2 2
价),同时Cl(0价)→HClO(+1);反应2KMnO \o(\s\up6(_____)KMnO +MnO +O↑中,其反应物
2 4 2 4 2 2
KMnO 中的锰元素化合价降低:KMnO (+7价)→KMnO (+6价)和MnO (+4价),而氧元素化合价
4 4 2 4 2
升高:KMnO (-2价)→O(0价)。
4 2
②结论:a.一种元素被氧化,不一定有另一种元素被还原。如;Cl+H O===HCl+HClO中氯元素既被
2 2
氧化又被还原;
b.一种反应物不一定只表现出一种性质。如;2KMnO \o(\s\up6(_____)KMnO +MnO +O↑中同种物质
4 2 4 2 2
既有元素化合价升高,又有降低;
c.有单质参加或生成的反应不一定是氧化还原反应。如3O 2O,反应前后无元素化合价变化;
2 3
d.某种物质由化合态变为游离态,不一定是被还原,如HCl→Cl 是被氧化。
2
【对应练习】1.氧化还原反应在生产、生活中具有广泛的用途。下列生产、生活中的事例不属于氧
化还原反应的是( )
A.金属冶炼 B.燃放鞭炮
C.食物腐败 D.点制豆腐
【答案】D
【解析】A.金属冶炼是金属元素的化合物转化为单质的过程,有元素化合价的变化,属于氧化还原
反应,A不符合题意;B.燃放鞭炮属于燃烧反应,产生了新的物质,其中有元素化合价的变化,因此反
应为氧化还原反应,B不符合题意;C.食物腐败是缓慢氧化反应,存在元素化合价的变化,属于氧化还
原反应,C不符合题意;D.点制豆腐时蛋白质发生聚沉,没有元素化合价的变化,因此没有发生氧化还
原反应,D符合题意;故合理选项是D。
2.下列说法正确的是( )
A.化合价升高的反应是还原反应
B.氧化还原反应一定有氧元素参加
C.氧化反应与还原反应同时发生
D.反应物要么发生氧化反应,要么发生还原反应
【答案】C
【解析】元素化合价升高的反应为氧化反应;只要有元素化合价升降(或电子转移)的反应就是氧化还
原反应,与是否有氧元素参加无关;氧化反应与还原反应一定同时发生;反应物中有些物质可能既不发生
氧化反应也不发生还原反应,如反应HCl+NaOH===NaCl+HO,为非氧化还原反应,HCl和NaOH既没
2
有发生氧化反应也没有发生还原反应,但在 Cl +HO=HCl+HClO中,Cl 既发生氧化反应又发生还原反
2 2 2
应。
活动二、探究氧化还原反应的特征任务一、讨论交流:从得失氧和化合价变化对比分析CuO+ H \o(\s\up6(_____)Cu+ H O和CuSO +Fe
2 2 4
===Cu+ FeSO 两个反应,你发现它们有什么相同点和不同点?由此可得出什么结论?
4
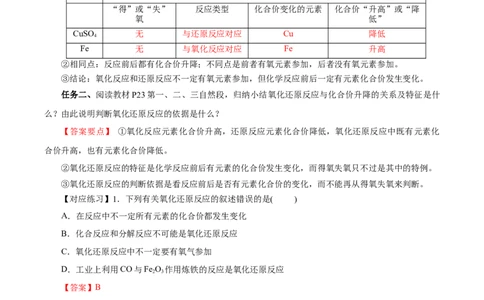
【答案要点】①对比分析两个反应 结果如下表:
反应 CuO+ H \o(\s\up6(_____)Cu+ HO
2 2
“得”或“失” 反应类型 化合价变化的元素 化合价“升高”或“降
氧 低”
CuO 失 还原 Cu 降低
H 得 氧化 H 升高
2
反应 CuSO +Fe ===Cu+ FeSO
4 4
“得”或“失” 反应类型 化合价变化的元素 化合价“升高”或“降
氧 低”
CuSO 无 与还原反应对应 Cu 降低
4
Fe 无 与氧化反应对应 Fe 升高
②相同点:反应前后都有化合价升降;不同点是前者有氧元素参加,后者没有氧元素参加。
③结论:氧化反应和还原反应不一定有氧元素参加,但化学反应前后一定有元素化合价发生变化。
任务二、阅读教材P23第一、二、三自然段,归纳小结氧化还原反应与化合价升降的关系及特征是什
么?由此说明判断氧化还原反应的依据是什么?
【答案要点】 ①氧化反应元素化合价升高,还原反应元素化合价降低,氧化还原反应中既有元素化
合价升高,也有元素化合价降低。
②氧化还原反应的特征是化学反应前后有元素的化合价发生变化,而得氧失氧只不过是其中的特例。
③氧化还原反应的判断依据是看反应前后是否有元素化合价的变化,而不能再从得氧失氧来判断。
【对应练习】1.下列有关氧化还原反应的叙述错误的是( )
A.在反应中不一定所有元素的化合价都发生变化
B.化合反应和分解反应不可能是氧化还原反应
C.氧化还原反应中不一定要有氧气参加
D.工业上利用CO与Fe O 作用炼铁的反应是氧化还原反应
2 3
【答案】B
【解析】A项,氧化还原反应中不一定所有元素的化合价都发生变化,如2HS+SO==3S↓+2HO中,
2 2 2
H、O元素的化合价不变,故A正确;B项,化合反应、分解反应中若存在化合价变化,则属于氧化还原
反应,如氢气与氧气的反应为化合反应、氯酸钾分解为分解反应,两个反应都属于氧化还原反应,故B错
误;C项,氧化还原反应中不一定有氧气参与,如氢气与氯气、Cu与硫单质的反应都是氧化还原反应,故
C正确;D项,工业上利用CO与Fe O 作用炼铁,反应中C、Fe元素存在化合价变化,属于氧化还原反
2 3
应,故D正确;故选B。
2.下列物质的制备涉及的反应属于氧化还原反应的是( )A.实验室中用NaHCO 制备纯碱 B.实验室中用石灰石制备CO
3 2
C.实验室中加热高锰酸钾制备O D.实验室中用CuO制备CuSO
2 4
【答案】C
【解析】A.加热NaHCO 制备NaCO 的方程式为2 NaHCO NaCO+H O +CO ,反应中不存在
2 3 3 2 3 2 2
元素化合价的变化,不是氧化还原反应,故A不选;B.实验室中用石灰石制备CO 的方程式为
2
CaCO +2H+==CO ↑+HO+Ca2+,反应中不存在元素化合价的变化,不是氧化还原反应,故B不选;C.实
3 2 2
验室中加热高锰酸钾制备O 的方程式为2KMnO KMnO +MnO+O ↑,反应中存在元素化合价的变
2 4 2 4 2 2
化,属于氧化还原反应,故C选;D.实验室中用CuO制备CuSO 的化学方程式为
4
CuO+H SO ==CuSO +H O,不存在元素化合价的变化,不是氧化还原反应,故D不选;故选C。
2 4 4 2
二、氧化还原反应的本质
活动一、探究氧化还原反应中引起元素化合价的因素
任务一、阅读教材P23页第四自然段和P24页内容,以反应2Na+Cl 2NaCl和H+Cl=====2HCl
2 2 2
为例,完成表格内容。
【答案要点】①反应2Na+Cl 2NaCl:
2
元素 原子结构 初始价态 最终价态 化合价变 电子转 被氧化或 发生反应
化情况 移情况 被还原 类型
示意图
钠元素 0 +1 升1 ♦失去 被氧化 氧化反应
1
氯元素 0 -1 降1 ♦得到 被还原 还原反应
1
②反应H+Cl=====2HCl:
2 2
元素 原子结构 初始价态 最终价态 化合价变 电 子 转 被氧化或 发生反应
示意图 化情况 移情况 被还原 类型
氢元素 0 +1 升1 ♦偏离 被氧化 氧化反应
1
氯元素 0 -1 降1 ♦偏向 被还原 还原反应
1③结论: 、
任务二、讨论结论:由上面两个反应的分析可知,在氧化还原反应中引起元素化合价发生变化的原因
是什么?
【答案要点】①反应2Na+Cl 2NaCl中,引起元素化合价发生变化的原因是不稳定的钠原子失去1
2
个电子形成稳定的钠离子,不稳定的氯原子得到1个电子形成稳定的氯离子。
②反应H+Cl=====2HCl中,引起元素化合价发生变化的原因是不稳定的氢、氯两种原子均易得到1
2 2
个电子形成稳定结构,于是两种原子便不能通过得失电子,而是采用形成共用电子对的方式形成稳定结
构,但由于氯原子吸电子能力强于氢原子,因此,共用电子对偏向氯原子,偏离氢原子。
③电子的得与失和形成共用电子对时电子对的偏移统称为电子的转移,即电子的转移是氧化还原反应
中元素化合价变化的原因。
【对应练习】1.下列变化过程发生还原反应的是( )
A.SO →HSO B.HCl→Cl
2 2 3 2
C.N→NH D.Fe(OH) →Fe(OH)
2 3 2 3
【答案】C
【解析】SO →HSO ,元素的化合价不变,不发生氧化还原反应,故A错误;HCl→Cl ,氯元素的化
2 2 3 2
合价升高,发生氧化反应,故B错误;N→NH ,氮元素的化合价降低,发生还原反应,故 C正确;
2 3
Fe(OH) →Fe(OH) ,铁元素的化合价升高,发生氧化反应,故D错误。
2 3
2.已知X、Y中含有相同的元素,Z、W中也含有相同的元素,根据反应X+HO→Y+H ;
2 2
Z+H O→W+O(方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为( )
2 2
A.X>Y、Z>W B.X<Y、Z<W
C.X>Y、Z<W D.X<Y、Z>W
【答案】D
【解析】X+HO→Y+H 中H元素化合价降低,根据氧化还原反应中化合价有升必有降可知,X中某
2 2
元素化合价低于Y,Z+H O→W+O 中O元素化合价升高,则Z中某元素化合价高于W,因此X、Y中及
2 2
Z、W中相同元素的化合价的高低顺序为X<Y、Z>W,故答案为D。
活动二、探究氧化还原反应的本质
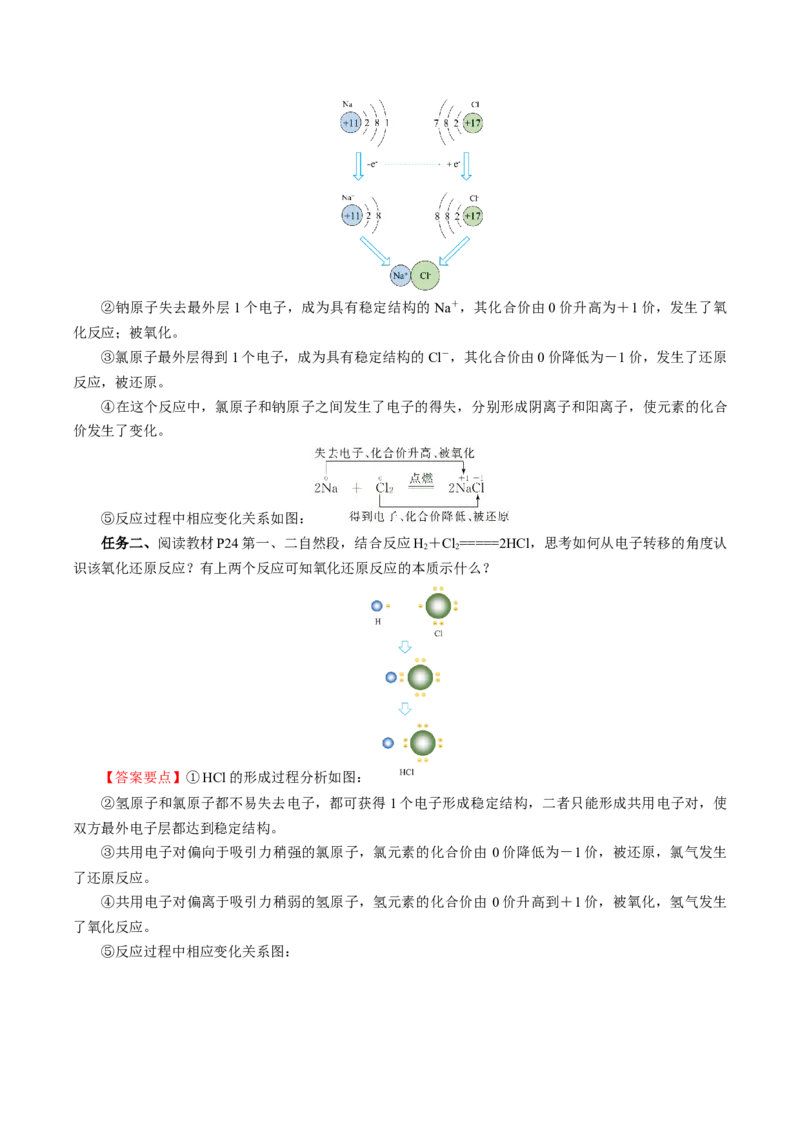
任务一、阅读教材P23最后自然段,观察教材P23图1-13 NaCl的形成过程,思考如何从电子转移的
角度认识该氧化还原反应?
【答案要点】①NaCl的形成过程的微观分析如图:2Na+Cl=====2NaCl
2②钠原子失去最外层1个电子,成为具有稳定结构的Na+,其化合价由0价升高为+1价,发生了氧
化反应;被氧化。
③氯原子最外层得到1个电子,成为具有稳定结构的Cl-,其化合价由0价降低为-1价,发生了还原
反应,被还原。
④在这个反应中,氯原子和钠原子之间发生了电子的得失,分别形成阴离子和阳离子,使元素的化合
价发生了变化。
⑤反应过程中相应变化关系如图:
任务二、阅读教材P24第一、二自然段,结合反应H+Cl=====2HCl,思考如何从电子转移的角度认
2 2
识该氧化还原反应?有上两个反应可知氧化还原反应的本质示什么?
【答案要点】①HCl的形成过程分析如图:
②氢原子和氯原子都不易失去电子,都可获得1个电子形成稳定结构,二者只能形成共用电子对,使
双方最外电子层都达到稳定结构。
③共用电子对偏向于吸引力稍强的氯原子,氯元素的化合价由 0价降低为-1价,被还原,氯气发生
了还原反应。
④共用电子对偏离于吸引力稍弱的氢原子,氢元素的化合价由 0价升高到+1价,被氧化,氢气发生
了氧化反应。
⑤反应过程中相应变化关系图:该反应生成的氯化氢分子因共用电子对偏移,而使元素的化合价发生了变化。
⑥结论:a.凡是有电子转移(得失或偏移)的反应都是氧化还原反应。失去电子(或偏离电子对)发生氧化
反应,得到电子(或偏向电子对)发生还原反应。
b.氧化还原反应的本质是电子的转移(电子得失或共用电子对偏移)。失电子(或电子对偏离),
化合价升高,被氧化,发生氧化反应;得电子(或电子对偏向),化合价降低,被还原,发生还原反应。
【对应练习】1.下列有关氧化还原反应的叙述正确的是( )
A.元素化合价升高的反应是还原反应
B.物质在变化中失去了电子,此物质中的某一元素化合价降低
C.有电子转移的反应就是氧化还原反应
D.有化合价升降的反应,不一定是氧化还原反应
【答案】C
【解析】元素化合价升高的反应为氧化反应,A项错误;失去电子应表现为化合价升高,B项错误;
有化合价升降的反应一定是氧化还原反应,D项错误。
2.下列反应中,电子转移发生在同种物质的同种元素之间的是( )
A.2HS+SO =3S+2HO B.2KMnO \o(\s\up6(_____)KMnO +MnO +O↑
2 2 2 4 2 4 2 2
C.2KClO\o(\s\up6(_____)2KCl+3O↑ D.Cu O+HSO =CuSO+Cu+HO
3 2 2 2 4 4 2
【答案】D
【解析】电子转移发生在同一物质同种元素之间,说明该反应物中的同一种元素在化学反应中一部分
化合价升高、一部分化合价降低,则该反应物既是还原剂又是氧化剂,据此分析解答。A.该反应中S元
素化合价由-2价、+4价变为0价,该反应中发生电子转移在同一元素之间,但不是同一种物质之间,故A
错误;B.该反应中Mn元素化合价由+7价变为+6价、+4价,O元素化合价由-2价变为0价,发生电子转
移在同一种物质之间,高锰酸钾既是氧化剂又是还原剂,但是不同元素之间,故B错误;C.该反应中Cl
元素化合价由+5价变为-1价、O元素化合价由-2价变为0价,发生电子转移在同一种物质之间但是在不同
元素之间,故C错误;D.该反应中Cu元素化合价由+1价变为0价、+2价,发生电子转移在同一种物质
之间且同一种元素之间,符合条件,故D正确。答案选D。
活动三、探究氧化还原反应与四种基本反应类型的关系
任务一、分析下表中的化学反应,思考它们与四种基本反应类型的关系,并判断是否是氧化还原反
应,由此,可以得出什么结论?
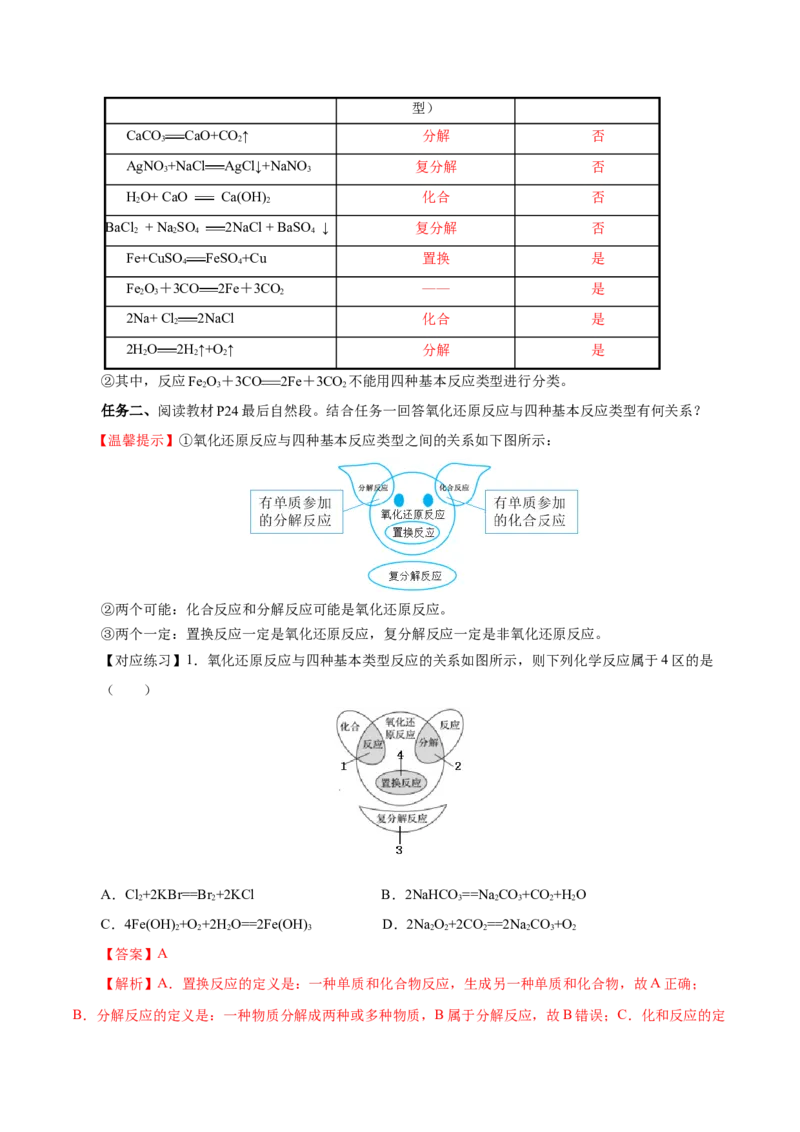
【答案要点】①化学反应的分类如下表:
化学反应(反应条件未标) 反应类型(四个基本类 是否是氧化还原反应型)
CaCO CaO+CO ↑ 分解 否
3 2
AgNO+NaCl AgCl↓+NaNO 复分解 否
3 3
HO+ CaO Ca(OH) 化合 否
2 2
BaCl + Na SO 2NaCl + BaSO ↓ 复分解 否
2 2 4 4
Fe+CuSO FeSO +Cu 置换 是
4 4
Fe O+3CO 2Fe+3CO —— 是
2 3 2
2Na+ Cl 2NaCl 化合 是
2
2HO 2H↑+O ↑ 分解 是
2 2 2
②其中,反应Fe O+3CO 2Fe+3CO 不能用四种基本反应类型进行分类。
2 3 2
任务二、阅读教材P24最后自然段。结合任务一回答氧化还原反应与四种基本反应类型有何关系?
【温馨提示】①氧化还原反应与四种基本反应类型之间的关系如下图所示:
②两个可能:化合反应和分解反应可能是氧化还原反应。
③两个一定:置换反应一定是氧化还原反应,复分解反应一定是非氧化还原反应。
【对应练习】1.氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于4区的是
( )
A.Cl+2KBr==Br+2KCl B.2NaHCO ==Na CO+CO +H O
2 2 3 2 3 2 2
C.4Fe(OH) +O +2H O==2Fe(OH) D.2NaO+2CO ==2Na CO+O
2 2 2 3 2 2 2 2 3 2
【答案】A
【解析】A.置换反应的定义是:一种单质和化合物反应,生成另一种单质和化合物,故A正确;
B.分解反应的定义是:一种物质分解成两种或多种物质,B属于分解反应,故B错误;C.化和反应的定义是:两种或多种物质反应生成一种物质,C属于化和反应,故C错误;D.该反应反应物中没有单质参
与反应,不属于置换反应,属于氧化还原反应,故D错误;故答案为A。
2.海水提溴过程中,将溴吹入吸收塔,使溴蒸气和吸收剂二氧化硫发生作用以达到富集的目的,化
学反应为Br +SO +2HO===2HBr+HSO ,下列说法正确的是( )
2 2 2 2 4
A.溴发生了还原反应
B.二氧化硫在反应中被还原
C.溴在反应中失去电子
D.该反应既是化合反应又是氧化还原反应
【答案】A
【解析】该反应为氧化还原反应,溴在反应中得到电子发生还原反应,溴被还原。
【课后巩固】1.(易)教材作业:P27页练习1、5、6、9
2.(易)下列关于氧化还原反应的叙述中,正确的是( )
A.一种元素被氧化,肯定有另一种元素被还原
B.氧化还原反应的实质是电子的转移
C.阳离子只有氧化性,阴离子只有还原性
D.氧化还原反应中,得电子越多,氧化性越强
【答案】B
【解析】A.一种元素被氧化,也可以是同一种元素被还原,例如归中和岐化反应,故A错误;B.
氧化还原反应的实质就是电子的转移,B项正确;C.阳离子也可能有还原性,例如:亚铁离子处于铁元
素的中间价,既有氧化性又有还原性,C项错误;D.氧化还原反应中,越容易得电子,其物质的氧化性
越强,越容易失去电子,物质的还原性越强,并非是通过得失电子的数目去衡量氧化(还原)性强弱的,
故D错误;故答案为B。
3.(易)下列说法正确的是( )
A.所有元素化合价都发生变化的化学反应才是氧化还原反应
B.氧化还原反应的特征是元素化合价升降,本质是电子得失
C.氧化还原反应中,一种元素化合价升高,必然有另一种元素化合价降低
D.氧化还原反应中一定存在电子转移
【答案】D
【解析】凡有元素化合价升降的化学反应都是氧化还原反应,此过程并不一定所有元素化合价都要发
生变化,A项错误;氧化还原反应的特征是元素化合价升降,本质是电子转移(包括电子得失和共用电子对
偏移),B项错误,D项正确;氧化还原反应中,发生化合价变化的元素可以是一种或多种,如Cl +
2
HO===HCl+HClO,其中只有氯元素的化合价发生变化,C项错误。
2
4.(中)在反应中,元素X的原子将电子转移给元素Y的原子,则下列说法正确的是( )
①元素X被氧化②元素Y被氧化③元素X发生还原反应 ④元素Y发生还原反应.A.①② B.③④ C.②③ D.①④
【答案】D
【解析】反应中,元素X的原子将电子转移给元素Y的原子,则X失去电子,Y得到电子,则X被氧
化,发生氧化反应,①正确,③错误;Y被还原,发生还原反应,②错误,④正确;故选D。
5.(中)属于氧化还原反应的离子方程式的是( )
A.CaCO +2H+=Ca2++CO↑+HO B.Fe2++2OH-=Fe(OH) ↓
3 2 2 2
C.HCO+H+=CO ↑+HO D.2Na+2HO=2Na++2OH+H↑
2 2 2 2
【答案】D
【解析】A.在反应CaCO +2H+=Ca2++CO↑+HO中,元素化合价都没有发生变化,因此反应不属
3 2 2
于氧化还原反应,A不符合题意;B.在反应Fe2++2OH-=Fe(OH) ↓中,元素化合价都没有发生变化,因此
2
反应不属于氧化还原反应,B不符合题意;C.在反应HCO+H+=CO +HO中,元素化合价都没有发生
2 2
变化,因此反应不属于氧化还原反应,C不符合题意;D.在反应2Na+2HO=2Na++2OH+H↑中,Na元
2 2
素化合价升高,H元素化合价降低,有元素化合价的变化,因此反应属于氧化还原反应,D符合题意;故
合理选项是D。
6.(中)下列有关叙述、对应的方程式,所属基本反应类型都正确的是( )
A.拉瓦锡研究空气成分HgO\o(\s\up6(_____)Hg+O↑ 分解反应
2
B.生石灰作干燥剂CaO+H O=Ca(OH) 化合反应
2 2
C.三氧化硫与氢氧化钠溶液反应SO +NaOH=Na SO +H O 复分解反应
3 2 3 2
D.葡萄糖在人体内氧化C H O+6O 6CO+6H O 氧化反应
6 12 6 2 2 2
【答案】B
【解析】A.该方程式没有配平,方程式为2HgO 2Hg+O↑,A错误;B.反应CaO+H O=Ca(OH)
2 2 2
是由两种或两种以上的物质反应生成一种新物质的反应,属于化合反应,B正确;C.SO 与NaOH反应生
3
成NaSO 和HO,方程式为SO +2NaOH=Na SO +H O,C错误;D.氧化反应不属于四种基本反应类型,
2 4 2 3 2 4 2
D错误;故选B。
7.(难)硫酸盐(含SO、HSO -)气溶胶是PM2.5的成分之一、近期科研人员提出了雾霾微颗粒中硫酸
4
盐生成的转化机理,其主要过程示意图如图:下列说法错误的是( )
A.过程I中的离子方程式为NO +SO==NO -+SO-
2 2 3
B.硫酸盐气溶胶呈酸性
C.过程III的反应没有电子转移
D.雾霾微颗粒中既含有硫酸盐,也含有亚硝酸盐(或硝酸盐)
【答案】C
【解析】A.过程Ⅰ中NO 得到SO失去的电子生成SO -和NO -,离子方程式为NO +SO==NO -
2 3 2 2 2
+SO-,A正确;B.转化过程有水参与,硫酸盐气溶胶中HSO -可以产生氢离子,显酸性,B正确;C.过
3 4
程Ⅲ的反应有电子转移,NO 生成HNO,化合价降低,得到电子,C错误;D.过程Ⅰ有亚硝酸根生成,
2 2
可继续被氧化成硝酸根,所以雾霾微颗粒中既含有硫酸盐,也含有亚硝酸盐(或硝酸盐),D正确;综上所
述答案为C。
8.(中)(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸
钠(NaNO )可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过
2
程中Fe2+发生__________反应,说明亚硝酸钠具有__________性;误食亚硝酸钠中毒,可服维生素C缓
解,说明维生素C具有________性。
(2)盐酸在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下三个反应,有关判断
正确的是( )
①Zn+2HCl ZnCl+H ↑ ②NaOH+HCl NaCl+H O ③2HCl\o(\s\up6(_____) H↑+Cl↑
2 2 2 2 2
选项 有关判断
A 反应①是置换反应,HCl表现还原性
B 反应②是复分解反应,HCl表现氧化性
C 反应①③都属于氧化还原反应
D 反应②中有电子的转移
(3)A图是“四种基本反应类型与氧化还原反应的关系”图,请在A图中用阴影部分表示反应:H +
2
CuO\o(\s\up6(_____)Cu + H O所属的区域。
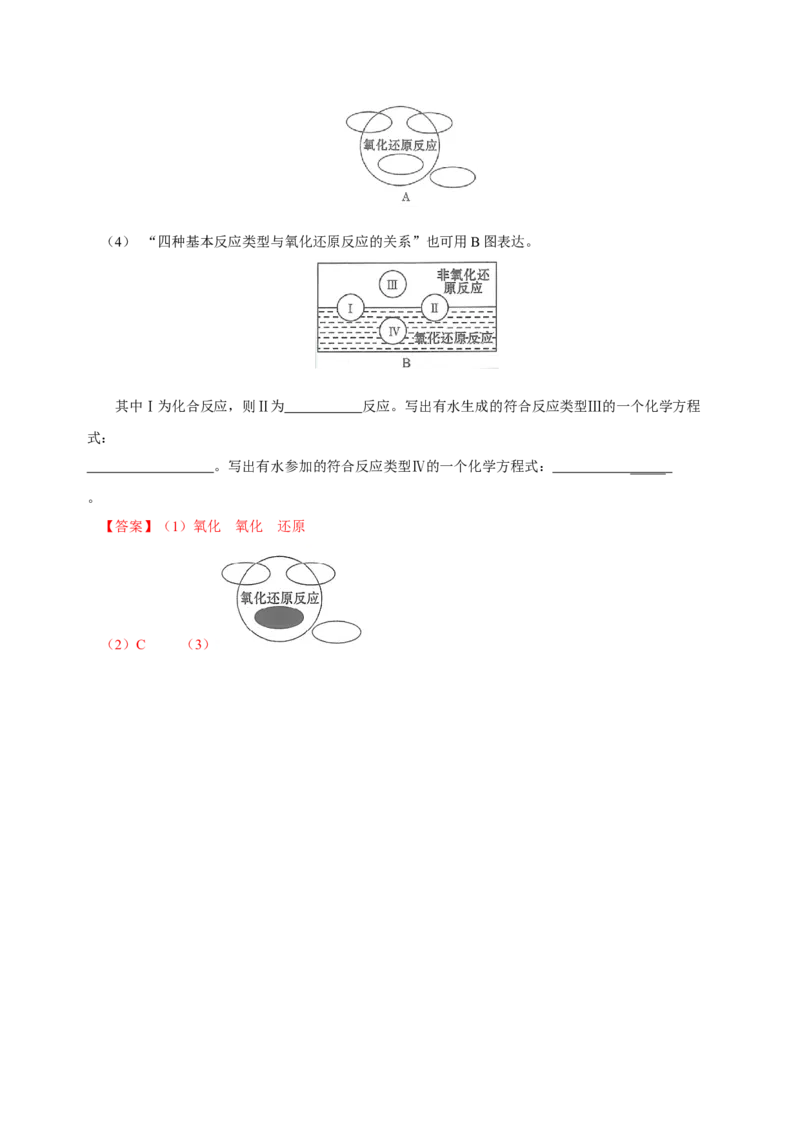
2(4) “四种基本反应类型与氧化还原反应的关系”也可用B图表达。
其中Ⅰ为化合反应,则Ⅱ为 反应。写出有水生成的符合反应类型Ⅲ的一个化学方程
式:
。写出有水参加的符合反应类型Ⅳ的一个化学方程式: ____ _
。
【答案】(1)氧化 氧化 还原
(2)C (3)