文档内容
第二章 化学反应速率与化学平衡
课
第一节 化学反应速率
题
课时2 影响化学反应速率的因素
1、理解浓度、压强、温度和催化剂等条件对化学反应速率的影响。
知识与技能 2、使学生能初步运用有效碰撞、碰撞的取向和活化分子等来解释浓
度、压强、温度和催化剂等条件对化学反应速率的影响。
教
1、掌握运用浓度、压强、温度和催化剂等条件比较反应速率大小的方
学
法;
目 过程与方法
2、通过识别有关化学反应速度与压强、温度或浓度等的图像,提高识
标
图析图能力,培养从图像中挖掘化学信息的能力。
情感态度 1、通过实验培养学生严谨的科学态度,知道科学研究的一般方法。
与价值观 2、通过目前催化剂研究的遗憾,激发学生投身科学的激情。
教
学
压强对化学速率的影响,用活化分子理论解释外界条件对化学反应速率的影响。
重
点
教
学
压强对化学速率的影响,用活化分子理论解释外界条件对化学反应速率的影响。
难
点
教
学
设
教
《化学反应速率与限度》是人教版高中化学必修二第二章《化学反应与能量》第 3
材
分 节《化学反应速率与限度》第 1节课的教学内容,主要学习化学反应速率的概念、影
析
响化学反应速率的因素,了解控制反应条件在生产生活和科学研究中的作用。本节内
容是对前两节内容的拓展和延伸。通过学习使学生对化学反应特征的认识更深入、更
全面,在头脑中建立起一个有关化学反应与能量的完整而又合理的知识体系。本节内
容是后面学习化学反应限度概念的基础。
我们的学生基础较差,特别是对实验现象的概括叙述不规范,需要老师规范学生
分 学
的用语,本节学生掌握化学反应速率的概念以及计算应该没问题,让学生自己总结影
析 情
响化学反应速率的因素会有一些困难。
以培养学生自主获取新知识的能力为目的来设计教学,采用发现,探究的教学模
想
教
法 式,其设计的教学指导思想,是由浅入深,从学生日常生活中的化学现象和实验中抽
设
象出有关的概念和原理。形成一个由宏观到微观、由感性到理性、由简单到复杂的科
计
学探究过程。
教学环节 教 学 内 容 设计意图
教师活动设计 学生活动[导入]有些反应速率很快,如盐酸与氢氧化钠的中和反应,而有些反应 培养观察
速率很慢,如石油的形成。可见,不同物质化学反应速率相差很大, 实验能力
决定化学反应速率的因素是反应物本身的性质。 学生观察
[板书]
培养概括
一、决定化学反应速率的因素:反应物本身的性质
能力
二、外界条件对化学反应速率的影响: 学生讨论
(一)浓度对化学反应速率的影响 思 考 问
[演示]课本20页实验2-2草酸与酸性高锰酸钾的反应 题。
4mL 0.01mol/L KMnO 4mL 0.01mol/L KMnO
加入试剂 4 4
2mL 0.1mol/L H C O 2mL 0.2mol/L H C O
2 2 4 2 2 4
实验现象 引入新课
褪色时间
明确要学
在其它条件相同时,增大反应物浓度,反应速率增
结论 习的内容
大。
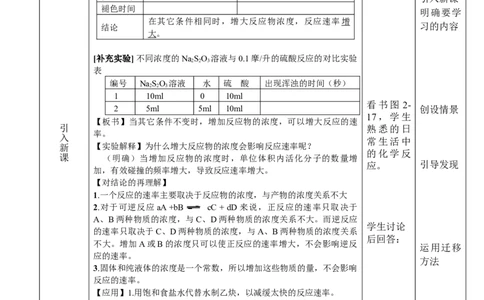
[补充实验] 不同浓度的NaSO 溶液与0.1摩/升的硫酸反应的对比实验
2 2 3
表
编号 NaSO 溶液 水 硫 酸 出现浑浊的时间(秒)
2 2 3
1 10ml 0 10ml
看书图 2-
2 5ml 5ml 10ml 创设情景
17,学生
【板书】当其它条件不变时,增加反应物的浓度,可以增大反应的速
引 熟悉的日
率。
入
常生活中
新 【实验解释】为什么增大反应物的浓度会影响反应速率呢?
的化学反
课 (明确)当增加反应物的浓度时,单位体积内活化分子的数量增
应。 引导发现
加,有效碰撞的频率增大,导致反应速率增大。
【对结论的再理解】
1.一个反应的速率主要取决于反应物的浓度,与产物的浓度关系不大
2.对于可逆反应aA +bB cC + dD 来说,正反应的速率只取决于
A、B两种物质的浓度,与C、D两种物质的浓度关系不大。而逆反应
学生讨论
的速率只取决于C、D两种物质的浓度,与A、B两种物质的浓度关系
后回答:
不大。增加A或B的浓度只可以使正反应的速率增大,不会影响逆反
运用迁移
应的速率。
方法
3.固体和纯液体的浓度是一个常数,所以增加这些物质的量,不会影响
反应的速率。
【应用】1.用饱和食盐水代替水制乙炔,以减缓太快的反应速率。
2. 制Fe(OH) 时,通过降低NaOH溶液的含氧量(给溶液加
2
热)来降低Fe(OH) 被氧化的速率。
2
学生掌握
(二)压强对化学反应速率的影响
【提出问题】压强是怎样对化学反应速率进行影响的?
【收集事实】途径:已有的实验知识
(提出以下几个实验)对比
1. 10ml、0.1mol/L的NaSO 溶液与0.1摩/升的硫酸10毫升反应的实
2 2 3
学生思考
验。
2. CaO固体与SiO 固体在高温下反应生成CaSiO 。
2 33. SO 与O 在一密闭容器内反应生成SO 。
2 2 3
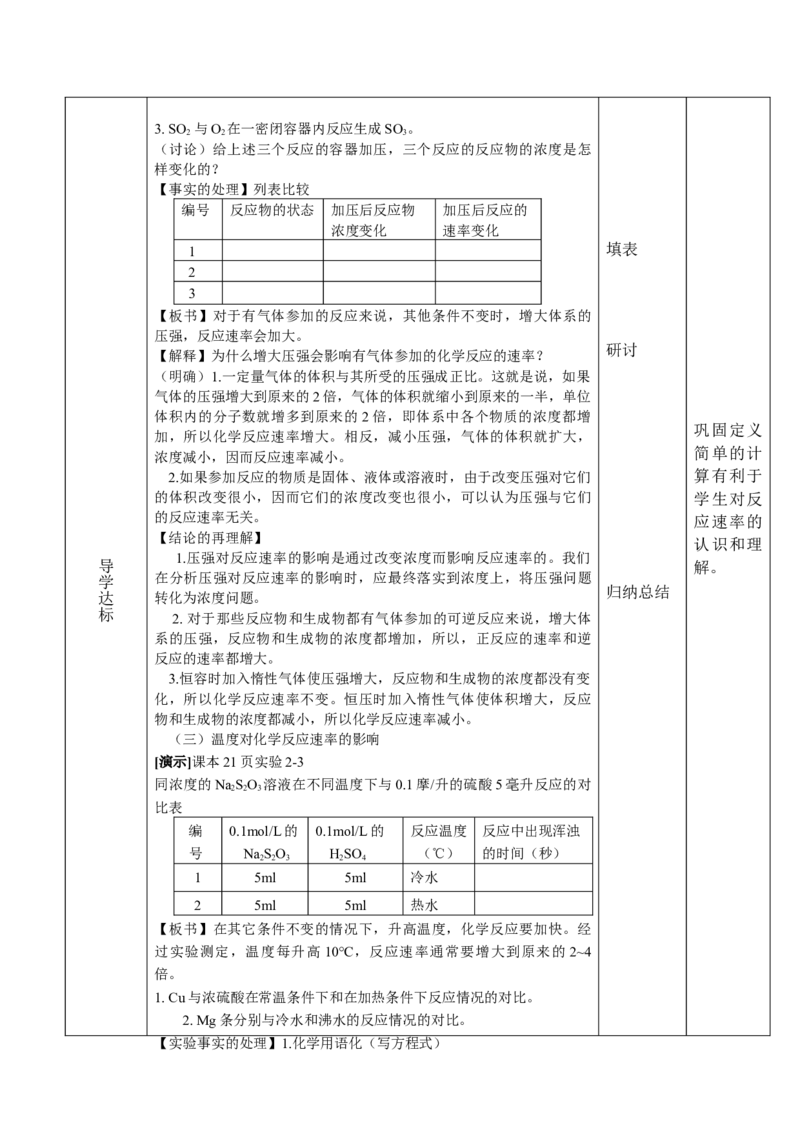
(讨论)给上述三个反应的容器加压,三个反应的反应物的浓度是怎
样变化的?
【事实的处理】列表比较
编号 反应物的状态 加压后反应物 加压后反应的
浓度变化 速率变化
填表
1
2
3
【板书】对于有气体参加的反应来说,其他条件不变时,增大体系的
压强,反应速率会加大。
研讨
【解释】为什么增大压强会影响有气体参加的化学反应的速率?
(明确)1.一定量气体的体积与其所受的压强成正比。这就是说,如果
气体的压强增大到原来的2倍,气体的体积就缩小到原来的一半,单位
体积内的分子数就增多到原来的 2倍,即体系中各个物质的浓度都增
巩固定义
加,所以化学反应速率增大。相反,减小压强,气体的体积就扩大,
简单的计
浓度减小,因而反应速率减小。
2.如果参加反应的物质是固体、液体或溶液时,由于改变压强对它们 算有利于
的体积改变很小,因而它们的浓度改变也很小,可以认为压强与它们 学生对反
的反应速率无关。 应速率的
【结论的再理解】
认识和理
1.压强对反应速率的影响是通过改变浓度而影响反应速率的。我们
导 解。
学 在分析压强对反应速率的影响时,应最终落实到浓度上,将压强问题
归纳总结
达 转化为浓度问题。
标
2. 对于那些反应物和生成物都有气体参加的可逆反应来说,增大体
系的压强,反应物和生成物的浓度都增加,所以,正反应的速率和逆
反应的速率都增大。
3.恒容时加入惰性气体使压强增大,反应物和生成物的浓度都没有变
化,所以化学反应速率不变。恒压时加入惰性气体使体积增大,反应
物和生成物的浓度都减小,所以化学反应速率减小。
(三)温度对化学反应速率的影响
[演示]课本21页实验2-3
同浓度的NaSO 溶液在不同温度下与0.1摩/升的硫酸5毫升反应的对
2 2 3
比表
编 0.1mol/L的 0.1mol/L的 反应温度 反应中出现浑浊
号 NaSO HSO (℃) 的时间(秒)
2 2 3 2 4
1 5ml 5ml 冷水
2 5ml 5ml 热水
【板书】在其它条件不变的情况下,升高温度,化学反应要加快。经
过实验测定,温度每升高10℃,反应速率通常要增大到原来的 2~4
倍。
1. Cu与浓硫酸在常温条件下和在加热条件下反应情况的对比。
2. Mg条分别与冷水和沸水的反应情况的对比。
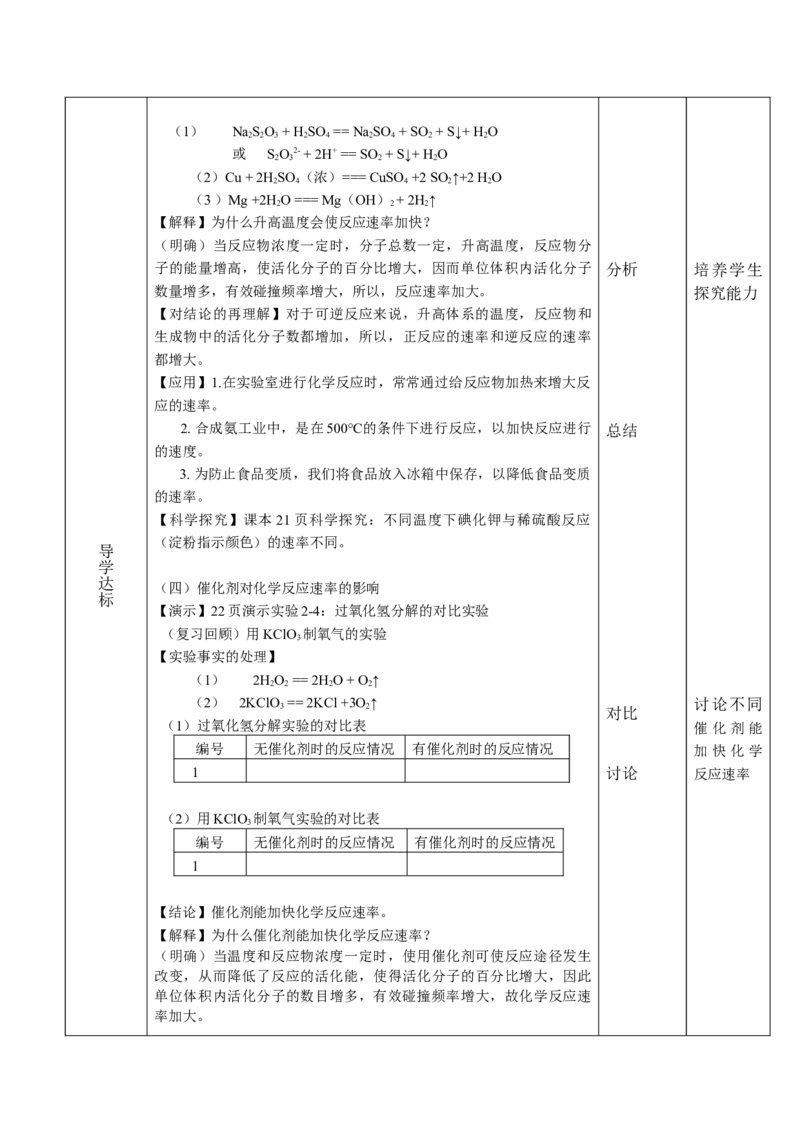
【实验事实的处理】1.化学用语化(写方程式)(1) NaSO + H SO == Na SO + SO + S↓+ H O
2 2 3 2 4 2 4 2 2
或 SO2- + 2H+ == SO + S↓+ H O
2 3 2 2
(2)Cu + 2H SO (浓)=== CuSO +2 SO↑+2 H O
2 4 4 2 2
(3 )Mg +2H O === Mg(OH) + 2H ↑
2 2 2
【解释】为什么升高温度会使反应速率加快?
(明确)当反应物浓度一定时,分子总数一定,升高温度,反应物分
子的能量增高,使活化分子的百分比增大,因而单位体积内活化分子 分析 培养学生
数量增多,有效碰撞频率增大,所以,反应速率加大。 探究能力
【对结论的再理解】对于可逆反应来说,升高体系的温度,反应物和
生成物中的活化分子数都增加,所以,正反应的速率和逆反应的速率
都增大。
【应用】1.在实验室进行化学反应时,常常通过给反应物加热来增大反
应的速率。
2. 合成氨工业中,是在500℃的条件下进行反应,以加快反应进行 总结
的速度。
3. 为防止食品变质,我们将食品放入冰箱中保存,以降低食品变质
的速率。
【科学探究】课本21页科学探究:不同温度下碘化钾与稀硫酸反应
(淀粉指示颜色)的速率不同。
导
学
达
(四)催化剂对化学反应速率的影响
标
【演示】22页演示实验2-4:过氧化氢分解的对比实验
(复习回顾)用KClO 制氧气的实验
3
【实验事实的处理】
(1) 2HO == 2H O + O↑
2 2 2 2
(2) 2KClO == 2KCl +3O ↑ 讨论不同
3 2 对比
(1)过氧化氢分解实验的对比表 催 化 剂 能
编号 无催化剂时的反应情况 有催化剂时的反应情况 加 快 化 学
1 讨论 反应速率
(2)用KClO 制氧气实验的对比表
3
编号 无催化剂时的反应情况 有催化剂时的反应情况
1
【结论】催化剂能加快化学反应速率。
【解释】为什么催化剂能加快化学反应速率?
(明确)当温度和反应物浓度一定时,使用催化剂可使反应途径发生
改变,从而降低了反应的活化能,使得活化分子的百分比增大,因此
单位体积内活化分子的数目增多,有效碰撞频率增大,故化学反应速
率加大。【结论】1.催化剂改变化学反应速率的原因仅仅是改变始态到终态的途
径,不改变反应的结果。例:
(1)在加热条件下: 2Cu + O == 2CuO
2
2CuO +2 CH CHOH == 2Cu +2 CHCHO + 2H O
3 2 3 2
(2)氮的氧化物破坏臭氧: NO + O == NO + O
3 2 2
NO + O ==NO + O
2 2
2. 能加快反应速率的催化剂叫正催化剂;能减慢化学反应速率的催化
剂叫负催化剂。如不作特殊说明,均指正催化剂。
自我总结 能力拓展
3. 对可逆反应而言,正催化剂使正、逆反应速率都加快,且加快的程
度相同。相反,负催化剂使正、逆反应速率都减小,且减小的程度相
同。
【应用】催化剂在现代化学和化工生产中占有极为重要的地位。大约
85%的反应需要催化剂。尤其是现代大型化工业、石油工业中,很多反
应还必须使用性能良好的催化剂。例;接触法制硫酸工业。
(五)其它因素对化学反应速率的影响
光、磁场、超声波、颗粒大小、溶剂性质…等
作
下发习题
业
设
计
一、决定化学反应速率的因素:反应物本身的性质
二、外界条件对化学反应速率的影响:
(一)浓度对化学反应速率的影响
当其它条(二)压强对化学反应速率的影响
件不变时,增加反应物的浓度,可以增大反应的速率。
板 (二)压强对化学反应速率的影响
书
对于有气体参加的反应来说,其他条件不变时,增大体系的压强,反应速率会加大。
设
计 (三)温度对化学反应速率的影响
在其它条件不变的情况下,升高温度,化学反应要加快。经过实验测定,温度每升高 10℃,反应
速率通常要增大到原来的2~4倍。
(四)催化剂对化学反应速率的影响
(五)其它因素对化学反应速率的影响
光、磁场、超声波、颗粒大小、溶剂性质…等