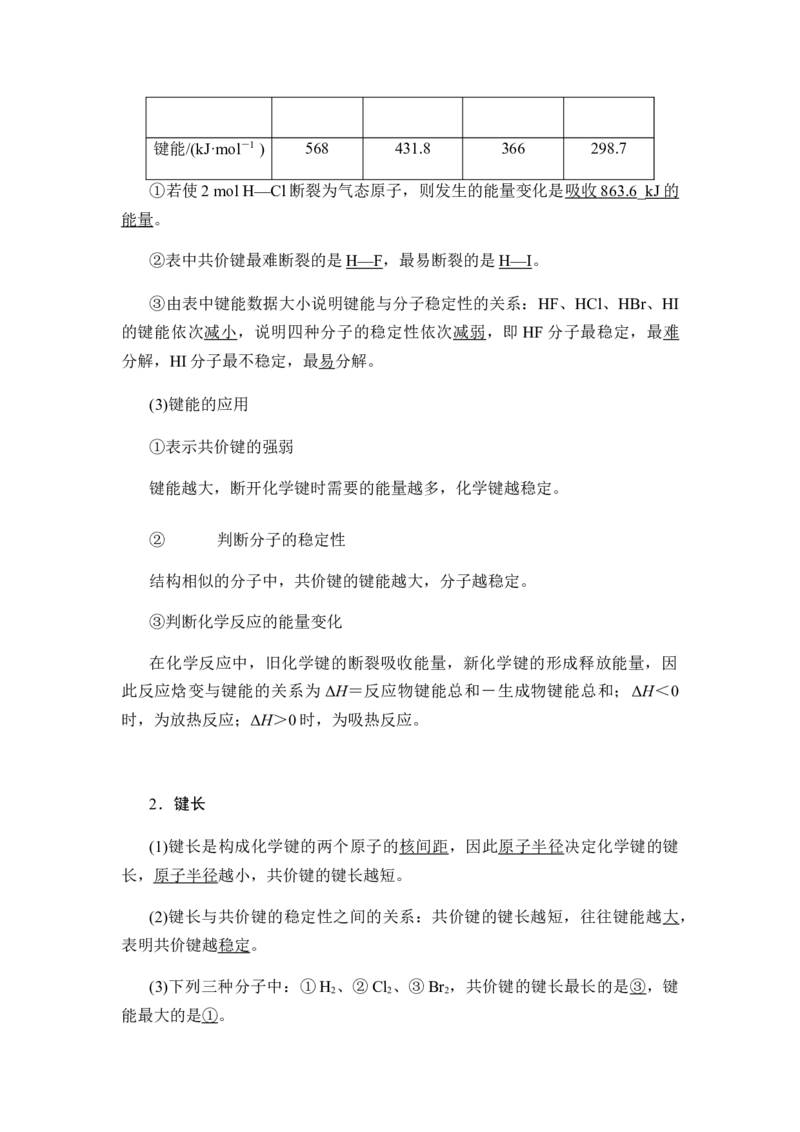文档内容
第二章 分子的结构与性质
第一节 共价键
一、共价键
1.共价键的概念和特征
原子间通过共用电子对所形成的相互作用。
【注】所有共价键都有饱和性,并不是所有共价键都具有方向性,如两个s电
子形成共价键时就没有方向性。
2. 形成条件
同种非金属元素或者不同种非金属元素原子之间,某些金属原子与非金属
原子之间形成共价键。如AlCl 、BeCl 、FeCl 等所含化学键为共价键。
3 2 3
3.共价键的类型(按成键原子的原子轨道重叠方式分类)
(1)σ键
形成 由成键原子的s轨道或p轨道重叠形成
s-s型
类
型 s-p型
p-p型以形成化学键的两原子核的连线为轴做旋转操作,共价键的
特征
电子云的图形不变,这种特征称为轴对称
(2)π键
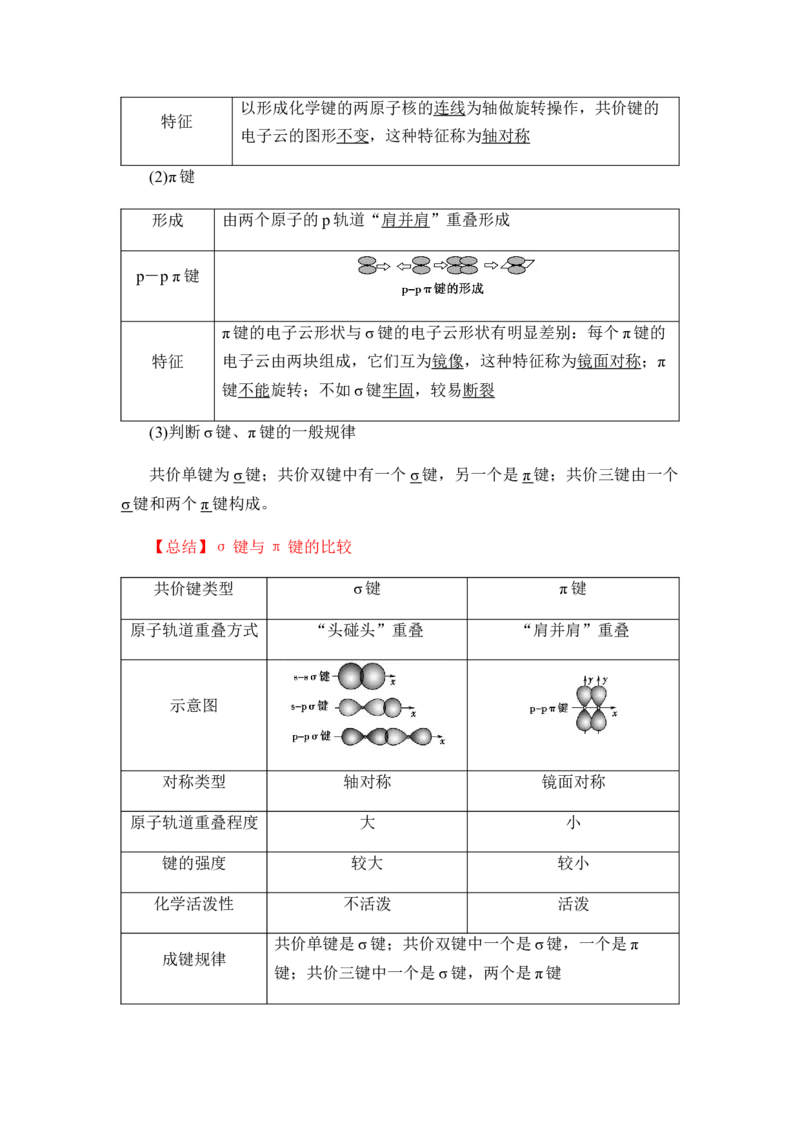
形成 由两个原子的p轨道“肩并肩”重叠形成
p-p π键
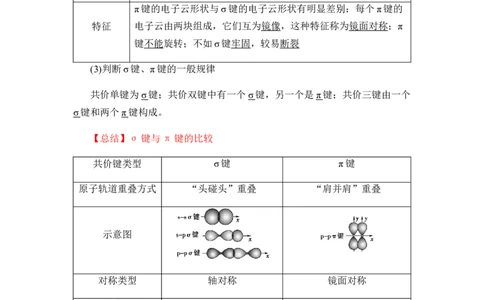
π键的电子云形状与σ键的电子云形状有明显差别:每个π键的
特征 电子云由两块组成,它们互为镜像,这种特征称为镜面对称;π
键不能旋转;不如σ键牢固,较易断裂
(3)判断σ键、π键的一般规律
共价单键为σ 键;共价双键中有一个σ 键,另一个是π 键;共价三键由一个
σ 键和两个π 键构成。
【总结】σ键与π键的比较
共价键类型 σ键 π键
原子轨道重叠方式 “头碰头”重叠 “肩并肩”重叠
示意图
对称类型 轴对称 镜面对称
原子轨道重叠程度 大 小
键的强度 较大 较小
化学活泼性 不活泼 活泼
共价单键是σ键;共价双键中一个是σ键,一个是π
成键规律
键;共价三键中一个是σ键,两个是π键【注】①s轨道与s轨道形成σ键时,电子并不是只在两核间运动,只是电子在
两核间出现的概率大。
②因s轨道是球形的,故 s轨道与s轨道形成σ键时,无方向性。两个 s轨
道只能形成σ键,不能形成π键。
③两个原子间可以只形成σ键,但不能只形成π键。
例1.有关CH ===CH—C≡N分子中所含化学键数目的说法正确的是( )
2
A.3个σ键,3个π键 B.4个σ键,3个π键
C.6个σ键,2个π键 D.6个σ键,3个π键
【答案】D [共价单键为σ键,双键中含1个σ键和1个π键,三键中含1
个σ键和2个π键,故CH ===CH—C≡N分子中含6个σ键和3个π键。]
2
例2.关于σ键和π键的比较,下列说法不正确的是( )
A.σ键是轴对称的,π键是镜面对称的
B.σ键是“头碰头”式重叠,π键是“肩并肩”式重叠
C.σ键不能断裂,π键容易断裂
D.氢原子只能形成σ键,氧原子可以形成σ键和π键
【答案】C [σ键较稳定,不易断裂,而不是不能断裂。]
二、键参数——键能、键长与键角
1.键能
(1)键能是指气态分子中1 mol化学键解离成气态原子所吸收的能量。键能
的单位是 kJ·mol - 1 。键能通常是298.15_ K 、 101 _kPa 条件下的标准值。例如,H
—H的键能为436.0 kJ·mol—1。
(2)下表中是H—X的键能数据
共价键 H—F H—Cl H—Br H—I键能/(kJ·mol-1 ) 568 431.8 366 298.7
①若使2 mol H—Cl断裂为气态原子,则发生的能量变化是 吸收 863. 6_ kJ 的
能量。
②表中共价键最难断裂的是H—F,最易断裂的是H—I。
③由表中键能数据大小说明键能与分子稳定性的关系:HF、HCl、HBr、HI
的键能依次减小,说明四种分子的稳定性依次减弱,即HF分子最稳定,最难
分解,HI分子最不稳定,最易分解。
(3)键能的应用
①表示共价键的强弱
键能越大,断开化学键时需要的能量越多,化学键越稳定。
② 判断分子的稳定性
结构相似的分子中,共价键的键能越大,分子越稳定。
③判断化学反应的能量变化
在化学反应中,旧化学键的断裂吸收能量,新化学键的形成释放能量,因
此反应焓变与键能的关系为 ΔH=反应物键能总和-生成物键能总和;ΔH<0
时,为放热反应;ΔH>0时,为吸热反应。
2.键长
(1)键长是构成化学键的两个原子的核间距,因此原子半径决定化学键的键
长,原子半径越小,共价键的键长越短。
(2)键长与共价键的稳定性之间的关系:共价键的键长越短,往往键能越大,
表明共价键越稳定。
(3)下列三种分子中:①H 、②Cl 、③Br ,共价键的键长最长的是③,键
2 2 2
能最大的是①。(4)键长的应用
①一般键长越短,键能越大,共价键越稳定,分子越稳定。
②键长的比较方法
a.根据原子半径比较,同类型的共价键,成键原子的原子半径越小,键长
越短。
b.根据共用电子对数比较,相同的两个原子间形成共价键时,单键键长>
双键键长>三键键长。
3.键角
(1)键角是指在多原子分子中,两个相邻共价键之间的夹角。在多原子分子
中的键角是一定的,这表明共价键具有方向性。键角是描述分子空间结构的重
要参数。
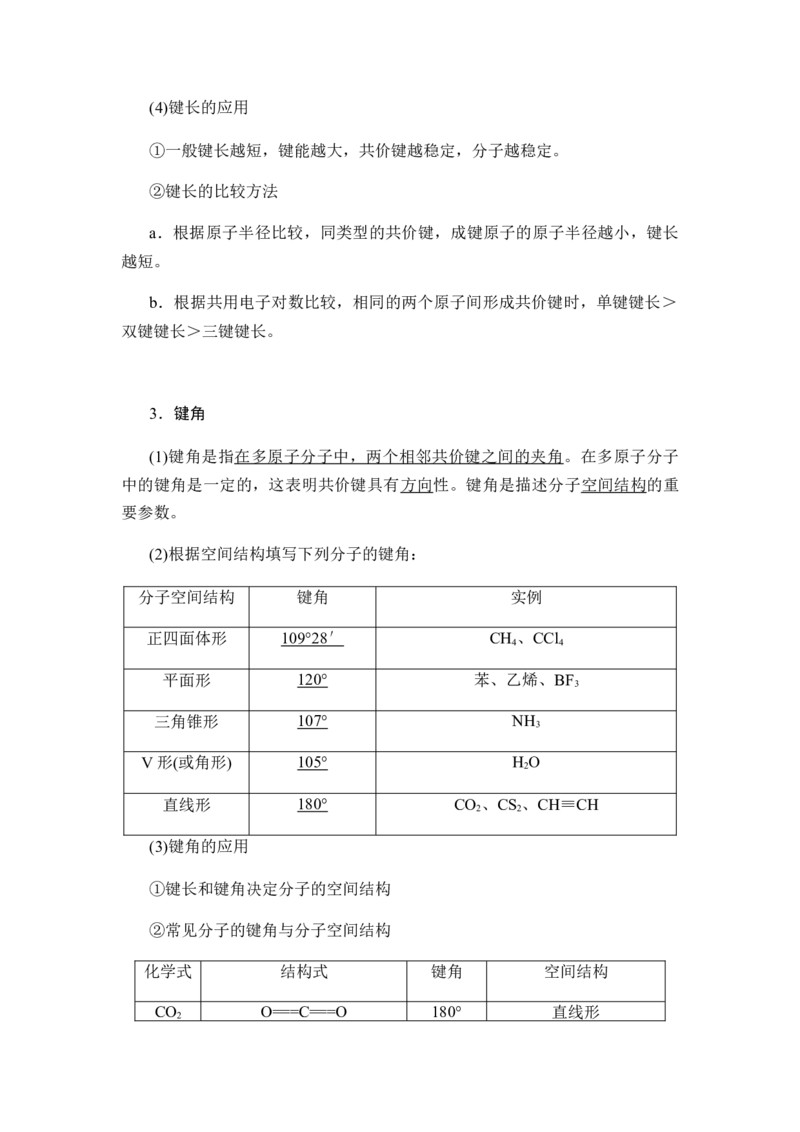
(2)根据空间结构填写下列分子的键角:
分子空间结构 键角 实例
正四面体形 109°28 ′ CH 、CCl
4 4
平面形 120° 苯、乙烯、BF
3
三角锥形 107° NH
3
V形(或角形) 105° H O
2
直线形 180° CO 、CS 、CH≡CH
2 2
(3)键角的应用
①键长和键角决定分子的空间结构
②常见分子的键角与分子空间结构
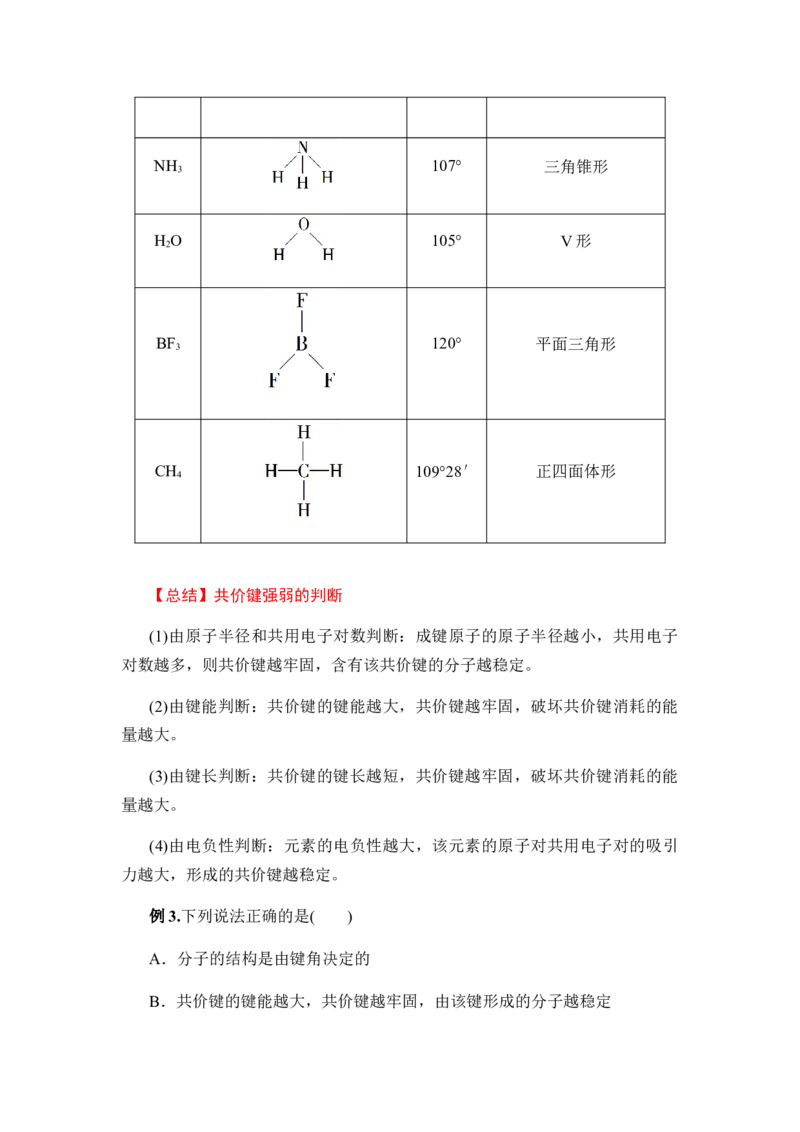
化学式 结构式 键角 空间结构
CO O===C===O 180° 直线形
2NH 107° 三角锥形
3
H O 105° V形
2
BF 120° 平面三角形
3
CH 109°28′ 正四面体形
4
【总结】共价键强弱的判断
(1)由原子半径和共用电子对数判断:成键原子的原子半径越小,共用电子
对数越多,则共价键越牢固,含有该共价键的分子越稳定。
(2)由键能判断:共价键的键能越大,共价键越牢固,破坏共价键消耗的能
量越大。
(3)由键长判断:共价键的键长越短,共价键越牢固,破坏共价键消耗的能
量越大。
(4)由电负性判断:元素的电负性越大,该元素的原子对共用电子对的吸引
力越大,形成的共价键越稳定。
例3.下列说法正确的是( )
A.分子的结构是由键角决定的
B.共价键的键能越大,共价键越牢固,由该键形成的分子越稳定C.CF 、CCl 、CBr 、CI 中C—X(X=F、Cl、Br、I)的键长、键角均相等
4 4 4 4
D.H O分子中两个O—H的键角为180°
2
【答案】B [分子的结构是由键角、键长共同决定的,A项错误;由于F、
Cl、Br、I的原子半径不同,故C—X(X=F、Cl、Br、I)键的键长不相等,C项
错误;H O分子中两个O—H的键角为105°,D项错误。]
2
例4.下列事实不能用键能的大小来解释的是( )
A.氮元素的电负性较大,但N 的化学性质很稳定
2
B.稀有气体一般难发生反应
C.HF、HCl、HBr、HI的稳定性逐渐减弱
D.HF比H O稳定
2
【答案】B [由于N 分子中存在三键,键能很大,破坏共价键需要很大的
2
能量,所以N 的化学性质很稳定;稀有气体都为单原子分子,没有化学键;卤
2
族元素从F到I,原子半径逐渐增大,其氢化物中化学键的键长逐渐变长,键能
逐渐变小,所以稳定性:HF>HCl>HBr>HI;由于H—F的键能大于H—O,
所以稳定性:HF>H O。]
2