文档内容
第二章 分子结构与性质
第二节 分子的空间结构
第一课时 分子结构的测定、多样的分子空间结构、价层电子对互斥模型
基础达标
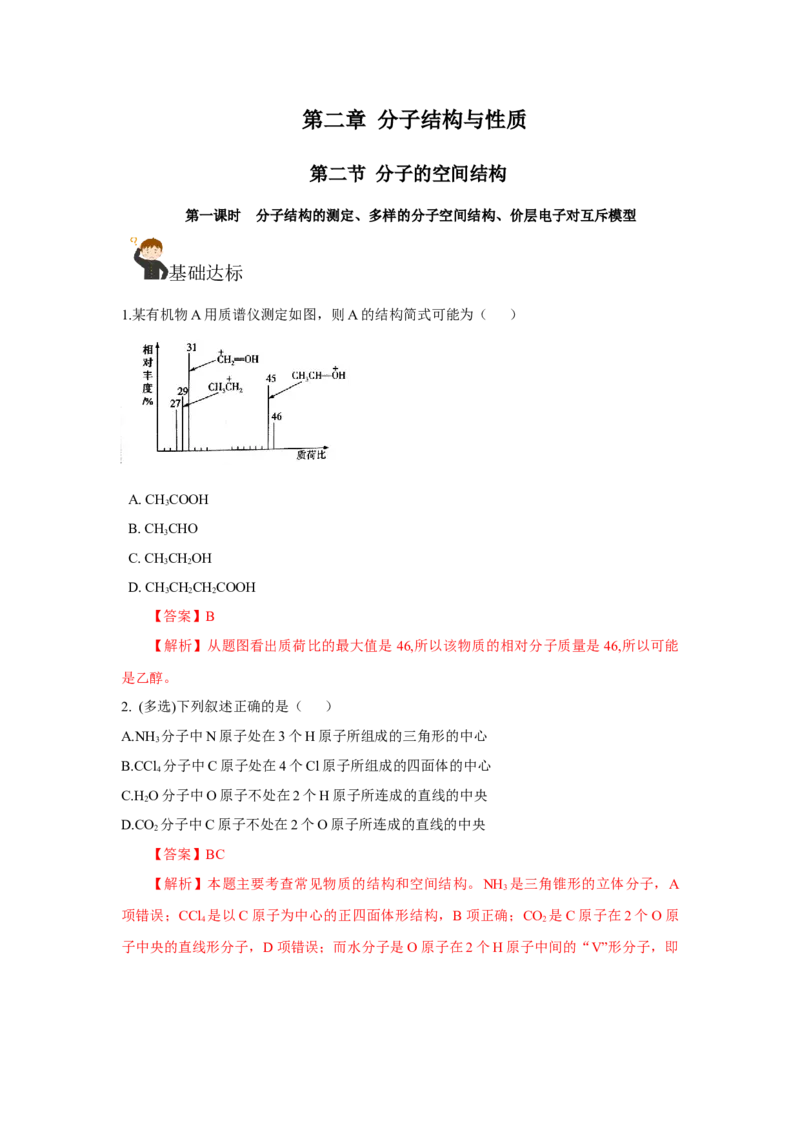
1.某有机物A用质谱仪测定如图,则A的结构简式可能为( )
A. CH COOH
3
B. CHCHO
3
C. CH CHOH
3 2
D. CH CHCHCOOH
3 2 2
【答案】B
【解析】从题图看出质荷比的最大值是 46,所以该物质的相对分子质量是 46,所以可能
是乙醇。
2. (多选)下列叙述正确的是( )
A.NH 分子中N原子处在3个H原子所组成的三角形的中心
3
B.CCl 分子中C原子处在4个Cl原子所组成的四面体的中心
4
C.H O分子中O原子不处在2个H原子所连成的直线的中央
2
D.CO 分子中C原子不处在2个O原子所连成的直线的中央
2
【答案】BC
【解析】本题主要考查常见物质的结构和空间结构。NH 是三角锥形的立体分子,A
3
项错误;CCl 是以C原子为中心的正四面体形结构,B项正确;CO 是C原子在2个O原
4 2
子中央的直线形分子,D项错误;而水分子是O原子在2个H原子中间的“V”形分子,即,C项正确。
3.下列微粒中,含有孤电子对的是( )
A. SO B. BF C. HO+ D. NH +
3 3 3 4
【答案】C
【解析】HO+中的中心原子是O,最外层有6个电子,与H原子形成3个共价键,所以
3
O有1对孤电子对。
4.下列分子的中心原子,带有一对孤电子对的是( )
A. XeO B. BeCl C. CH D. PCl
4 2 4 3
【答案】D
【解析】按照孤电子对的计算方法进行求解。A. XeO 中Xe的孤电子对数= 1/2(8-4 ×
4
2) = 0; B.BeCl 中Be的孤电子对数= 1/2 (2-2 × 1) = 0; C.CH 中C的孤电子对数= 1/2(4- 4×1)
2 4
= 0; D.PCl 中P的孤电子对数= 1/2 (5-3 × 1) =1。
3
5.下列分子或离子中,VSEPR模型名称与分子或离子的空间结构名称不一致的是( )
A. H O B. CO C. CO 2— D. CCl
2 2 3 4
【答案】A
【解析】A.水分子中,价层电子对数=2+1/2×(6-2×1)=4, VSEPR模型为正四面体形结构,
含有2对孤电子对,略去孤电子对后,实际上其空间结构是V形,VSEPR模型与分子空间
结构名称不一致,A符合题意;B.CO 分子中,每个O原子和C原子形成两个共用电子对,
2
所以C原子价层电子对数是2,且不含孤电子对,为直线形结构,VSEPR模型与分子空间结
构名称一致,B不符合题意;C. CO2—的中心原子C原子上含有3个σ键,中心原子上的孤
3
电子对数=1/2×(4+2-2×3)=0,所以CO2—的空间结构是平面三角形,VSEPR模型与分子空间
3
结构名称一致,C不符合题意;D.CCl 分子中,中心原子C原子价层电子对数=σ键电子对
4
数+孤电子对数=4+1/2×(4-1×4)=4, VSEPR模型为正四面体形结构,中心原子不含有孤电子
对,其分子的空间结构为正四面体形结构,VSEPR模型与分子空间结构名称一致,D不符
合题意。
6.若AB 的中心原子A没有未用于形成共价键的孤电子对,运用价层电子对互斥模型,下
n
列说法正确的是( )
A.若n=2,则分子的空间结构为V形 B.若n=3,则分子的空间结构为三角锥形
C.若n=4,则分子的空间结构为正四面体形 D.以上说法都不正确【答案】C
【解析】若中心原子A没有未用于成键的孤电子对,则根据斥力最小的原则,当n=2
时,分子的空间结构为直线形;n=3时,分子的立体结构为平面三角形;n=4时,分子的
空间结构为正四面体形。
7.对CO 和SO 的说法正确的是( )
2 2
A.都是AB 型,所以都是直线形 B.C原子和S原子上都没有孤电子对
2
C.CO 是直线形结构,SO 是V形结构 D.都含有极性共价键和非极性共价键
2 2
【答案】C
【解析】CO 的中心原子C原子上含有2个σ键,中心原子上的孤电子对数=1/2×(4-
2
2×2)=0,所以CO 的空间结构是直线形,SO 的中心原子S原子上含有2个σ键,中心原子
2 2
上的孤电子对数=1/2×(6-2×2)=1,所以SO 的空间结构是V形,A错;C对。C原子没有孤电
2
子对,S原子上有1对孤电子对,B错;两个物质都有极性共价键,没有非极性共价键,D
错。
8.下列分子或离子的中心原子上未用于成键的价电子对最多的是( )
A. H O B. NH C. NH + D. PCl
2 3 4 3
【答案】A
【解析】A项,氧原子有两对未成键的价电子对;B项,氮原子有一对未成键的价电子
对;C项,NH +的中心原子的价电子全部参与成键;D项,磷原子有一对未成键的价电子
4
对。
9.下列分子中键角最大的是( )
A. H S B. H O C. CCl D. NH
2 2 4 3
【答案】C
【解析】题中四种物质中的中心原子的价层电子对数都是 4,CCl 中不存在孤电子对,键
4
角为109º28´;NH 中存在1对孤电子对,HS和HO中存在2对孤电子对,由于孤电子对的
3 2 2
排斥作用,导致NH 、HS和HO的键角小于109º28´。
3 2 2
能力提升
10.下列说法不正确的是( )
A.蛋白质、棉花、PVC、淀粉都是由高分子构成的物质
B.乙醇和二甲醚互为同分异构体,可利用红外光谱法鉴别两者
C.双原子或多原子形成的气体单质分子中,一定有σ键,可能有π键D.P 和CH 都是正四面体形分子且键角都为109°28´
4 4
【答案】D
【解析】P 和CH 都是正四面体形分子,其中P 中键角为60°CH 中键角为109°28´,所
4 4 4 4
以D不正确。
11.(多选)右表是元素周期表中短周期的一部分。A、D两种元素原子的核内质子数之和为
23。下列有关说法中不正确的是( )
A.原子半径:A>B
B.C的气态氢化物的分子空间结构为平面三角形
C.最高价氧化物对应水化物的酸性:D