文档内容
第二章 分子结构与性质
第二节 分子的空间结构
2.2.1 分子结构的测定与多样性 价层电子对互斥模型
1.了解分子结构的测定方法。
2.认识共价分子结构的多样性和复杂性。
3.理解价层电子对互斥理论的含义。
4.能根据有关理论判断简单分子或离子的空间结构。
教学重点:价层电子对互斥理论
教学难点:价层电子对互斥理论
一、分子结构的测定
1.红外光谱仪
分子中的原子不是固定不动的,而是不断地________的。当一束红外线透过分子时,分子会
________跟它的某些化学键的________频率相同的红外线,再记录到图谱上呈现吸收峰。可分析出
分子中含有何种________或官能团的信息。
2.质谱仪:
现代化学常利用质谱仪测定分子的________。
二、多样的分子空间构型
1.三原子分子的空间构型
物质 化学式 空间结构 结构式 键角 空间结构模型
二氧化碳 CO 180°
2
水 HO 105°
2
2.四原子分子的空间构型
物质 化学式 空间结构 结构式 键角 空间结构模型
甲醛 CHO 120°
2氨 NH 107°
3
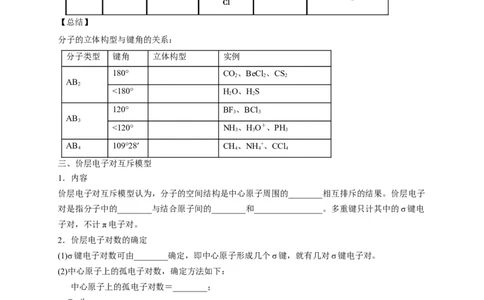
3.五原子分子的空间构型
物质 化学式 空间结构 结构式 键角 空间结构模型
甲烷 CH 109°28′
4
四氯
CCl 109°28′
化碳 4
【总结】
分子的立体构型与键角的关系:
分子类型 键角 立体构型 实例
180° CO、BeCl 、CS
2 2 2
AB
2
<180° HO、HS
2 2
120° BF、BCl
3 3
AB
3
<120° NH 、HO+、PH
3 3 3
AB 109°28′ CH、NH +、CCl
4 4 4 4
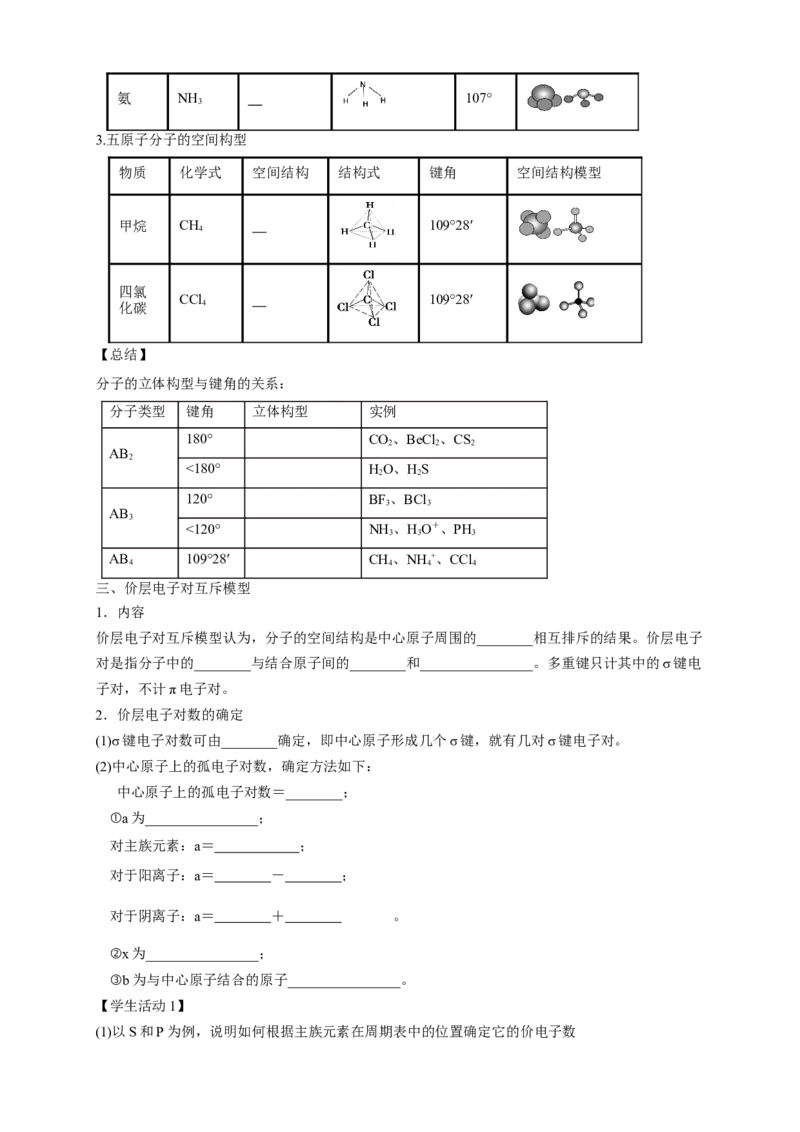
三、价层电子对互斥模型
1.内容
价层电子对互斥模型认为,分子的空间结构是中心原子周围的________相互排斥的结果。价层电子
对是指分子中的________与结合原子间的________和________________。多重键只计其中的σ键电
子对,不计π电子对。
2.价层电子对数的确定
(1)σ键电子对数可由________确定,即中心原子形成几个σ键,就有几对σ键电子对。
(2)中心原子上的孤电子对数,确定方法如下:
中心原子上的孤电子对数=________;
①a为________________;
对主族元素:a= ;
对于阳离子:a= - ;
对于阴离子:a= + 。
②x为________________;
③b为与中心原子结合的原子________________。
【学生活动1】
(1)以S和P为例,说明如何根据主族元素在周期表中的位置确定它的价电子数_____________________________________________________________________________________
_____________________________________________________________________________________
(2)以N和Cl为例,说明如何根据主族元素在周期表中的位置确定它最多能接受的电子数。
_____________________________________________________________________________________
_____________________________________________________________________________________
(3) 计算HO、NH 、SO 、NH +、CO分子的孤电子对数。
2 3 3 4
分子或离子 中心原子 a x b 中心原子数的孤电子对数
HO
2
NH
3
SO
3
NH +
4
CO
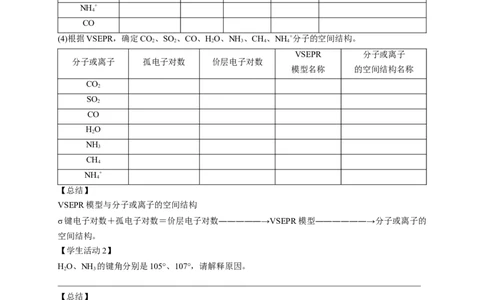
(4)根据VSEPR,确定CO、SO 、CO、HO、NH 、CH、NH +分子的空间结构。
2 2 2 3 4 4
VSEPR 分子或离子
分子或离子 孤电子对数 价层电子对数
模型名称 的空间结构名称
CO
2
SO
2
CO
HO
2
NH
3
CH
4
NH +
4
【总结】
VSEPR模型与分子或离子的空间结构
σ键电子对数+孤电子对数=价层电子对数―――――→VSEPR模型――――――→分子或离子的
空间结构。
【学生活动2】
HO、NH 的键角分别是105°、107°,请解释原因。
2 3
_____________________________________________________________________________________
【总结】
价层电子对之间的斥力
①电子对之间的夹角越小,斥力越大。
②分子中电子对之间的斥力大小顺序:孤电子对-孤电子对>孤电子对-成键电子对
>成键电子-成键电子。
③由于三键、双键比单键包含的电子多,所以斥力大小顺序:三键>双键>单键 。
1. 下列离子的VSEPR模型与离子的空间立体构型一致的是A. B. C. D.
2. 用短线“ ”表示共用电子对,用“ ”表示未成键孤对电子的式子叫路易斯结构式.R分子
的路易斯结构式可以表示为 ,则以下叙述错误的是
A. R为三角锥形 B. R可以是
C. R是极性分子 D. 键角小于
3. R模型预测下列分子或离子的立体结构,其中正确的是
A. 与 为角形 形 B. 与 为直线形
C. 与 为三角锥形 D. 与 为平面三角形
4. 已知原子总数和价电子总数相同的离子或分子结构相似,如 、 都是平面三角形。那
么下列分子或离子中与 有相似结构的是
A. B. C. D.
5. 根据VSEPR理论判断下列各组分子或离子结构相同的是
A. 和 B. 和 C. 和 D. 和