文档内容
第二节 氯及其化合物
第3课时 氯气的实验室制备
基础巩固
1.在实验室利用浓盐酸和二氧化锰制氯气,制备装置中应使用分液漏斗而不能使用长颈漏斗,下列有关
理由叙述错误的是( )
A.防止氯气扩散到空气中造成污染
B.便于控制加入盐酸的量
C.分液漏斗加入液体快
D.尽量避免氯化氢挥发到空气中
2.下列有关实验室制取氯气的说法不正确的是
A.可用二氧化锰和稀盐酸加热反应生成氯气
B.干燥氯气时常用浓硫酸作干燥剂
C.多余的氯气用氢氧化钠溶液吸收
D.收集氯气用向上排空气法
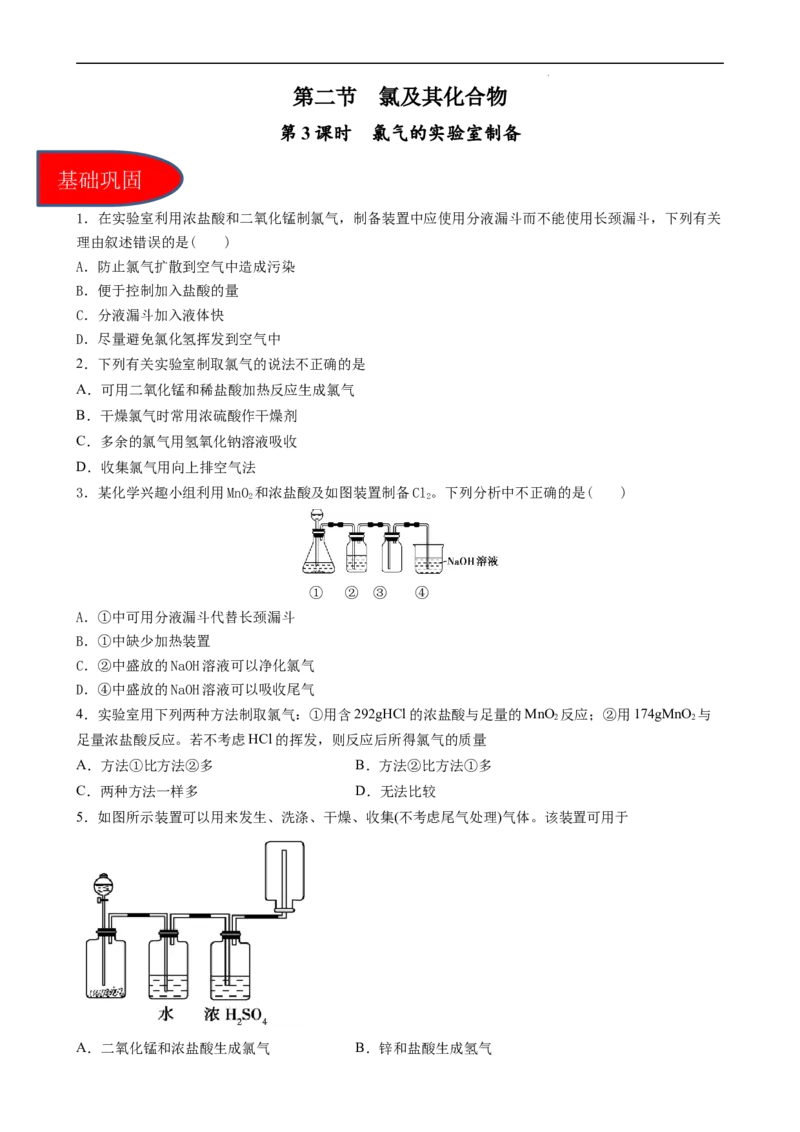
3.某化学兴趣小组利用MnO 和浓盐酸及如图装置制备Cl。下列分析中不正确的是( )
2 2
① ② ③ ④
A.①中可用分液漏斗代替长颈漏斗
B.①中缺少加热装置
C.②中盛放的NaOH溶液可以净化氯气
D.④中盛放的NaOH溶液可以吸收尾气
4.实验室用下列两种方法制取氯气:①用含292gHCl的浓盐酸与足量的MnO 反应;②用174gMnO 与
2 2
足量浓盐酸反应。若不考虑HCl的挥发,则反应后所得氯气的质量
A.方法①比方法②多 B.方法②比方法①多
C.两种方法一样多 D.无法比较
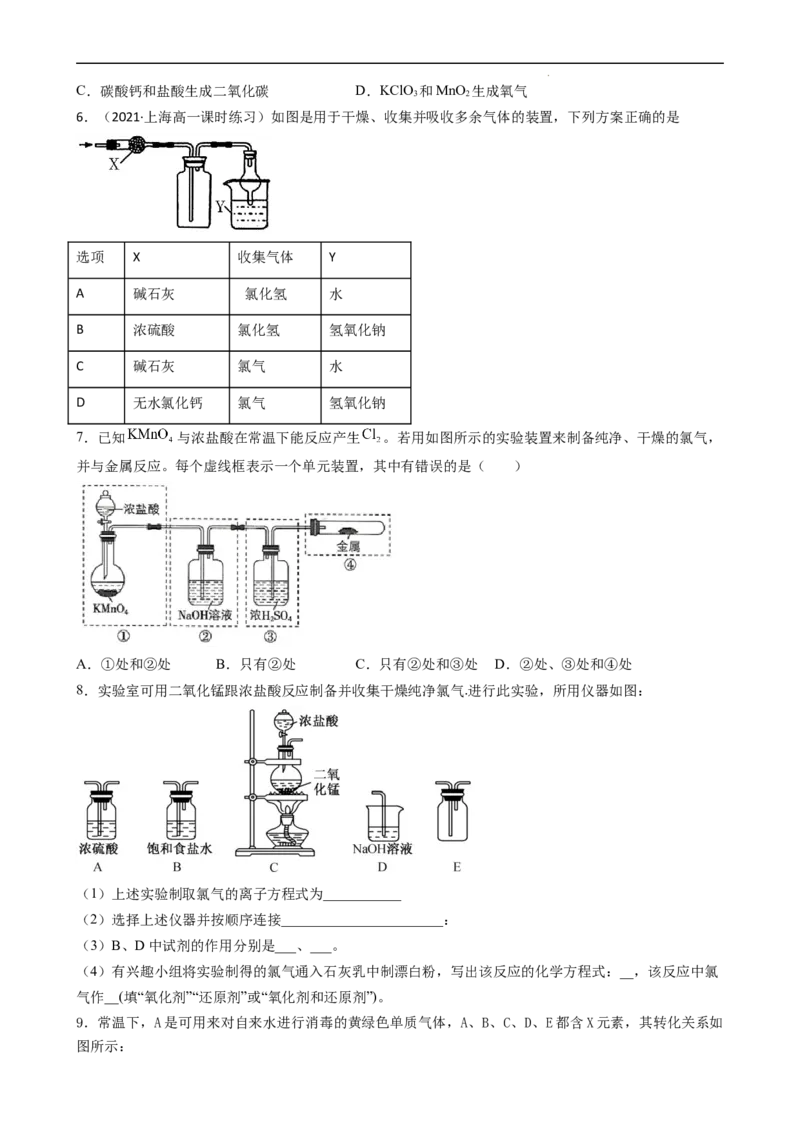
5.如图所示装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于
A.二氧化锰和浓盐酸生成氯气 B.锌和盐酸生成氢气
学科网(北京)股份有限公司C.碳酸钙和盐酸生成二氧化碳 D.KClO 和MnO 生成氧气
3 2
6.(2021·上海高一课时练习)如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是
选项 X 收集气体 Y
A 碱石灰 氯化氢 水
B 浓硫酸 氯化氢 氢氧化钠
C 碱石灰 氯气 水
D 无水氯化钙 氯气 氢氧化钠
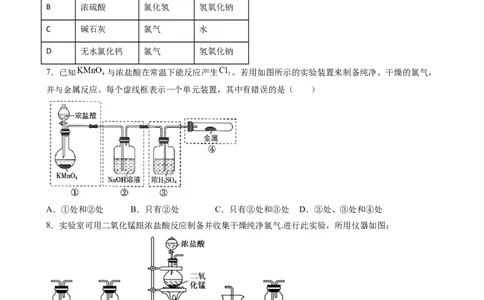
7.已知 与浓盐酸在常温下能反应产生 。若用如图所示的实验装置来制备纯净、干燥的氯气,
并与金属反应。每个虚线框表示一个单元装置,其中有错误的是( )
A.①处和②处 B.只有②处 C.只有②处和③处 D.②处、③处和④处
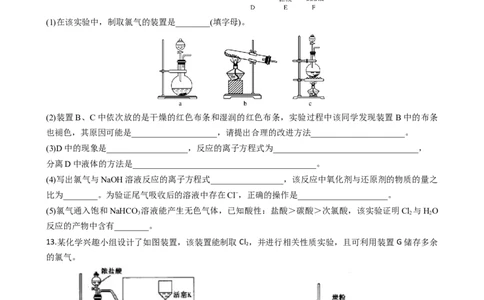
8.实验室可用二氧化锰跟浓盐酸反应制备并收集干燥纯净氯气.进行此实验,所用仪器如图:
(1)上述实验制取氯气的离子方程式为___________
(2)选择上述仪器并按顺序连接_______________________:
(3)B、D中试剂的作用分别是___、___。
(4)有兴趣小组将实验制得的氯气通入石灰乳中制漂白粉,写出该反应的化学方程式:__,该反应中氯
气作__(填“氧化剂”“还原剂”或“氧化剂和还原剂”)。
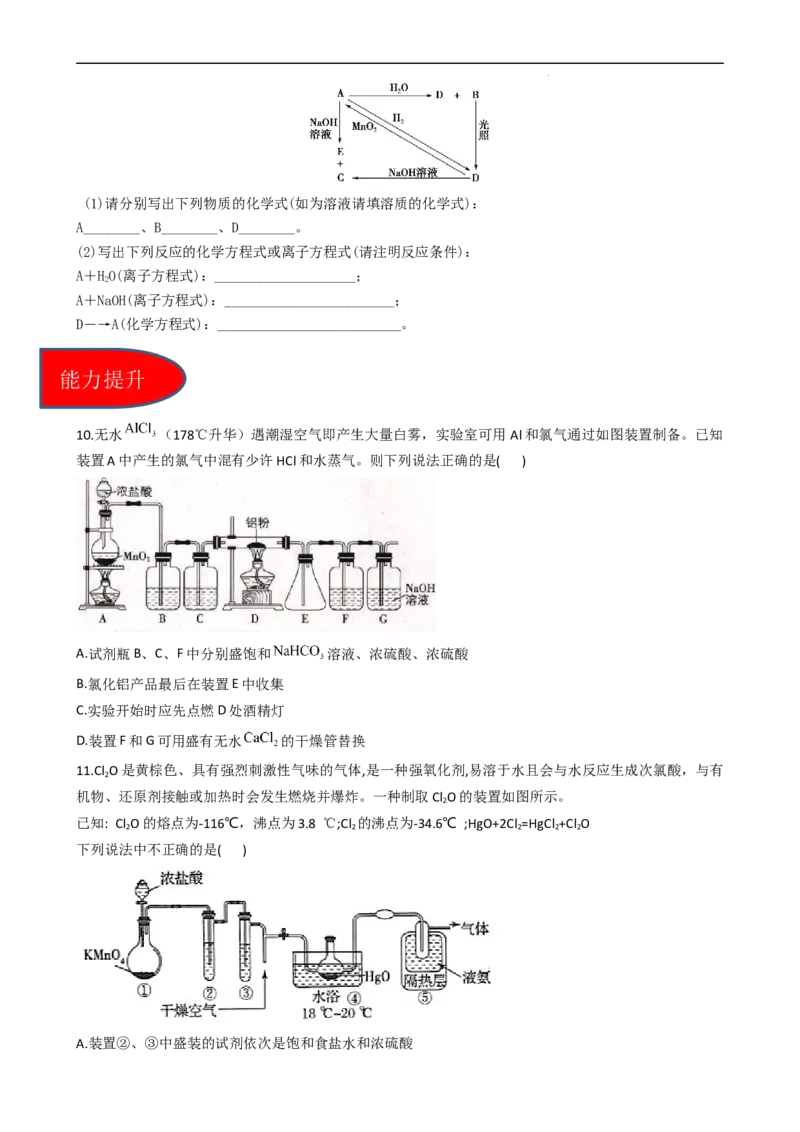
9.常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如
图所示:
学科网(北京)股份有限公司(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):
A+HO(离子方程式):____________________;
2
A+NaOH(离子方程式):________________________;
D―→A(化学方程式):__________________________。
能力提升
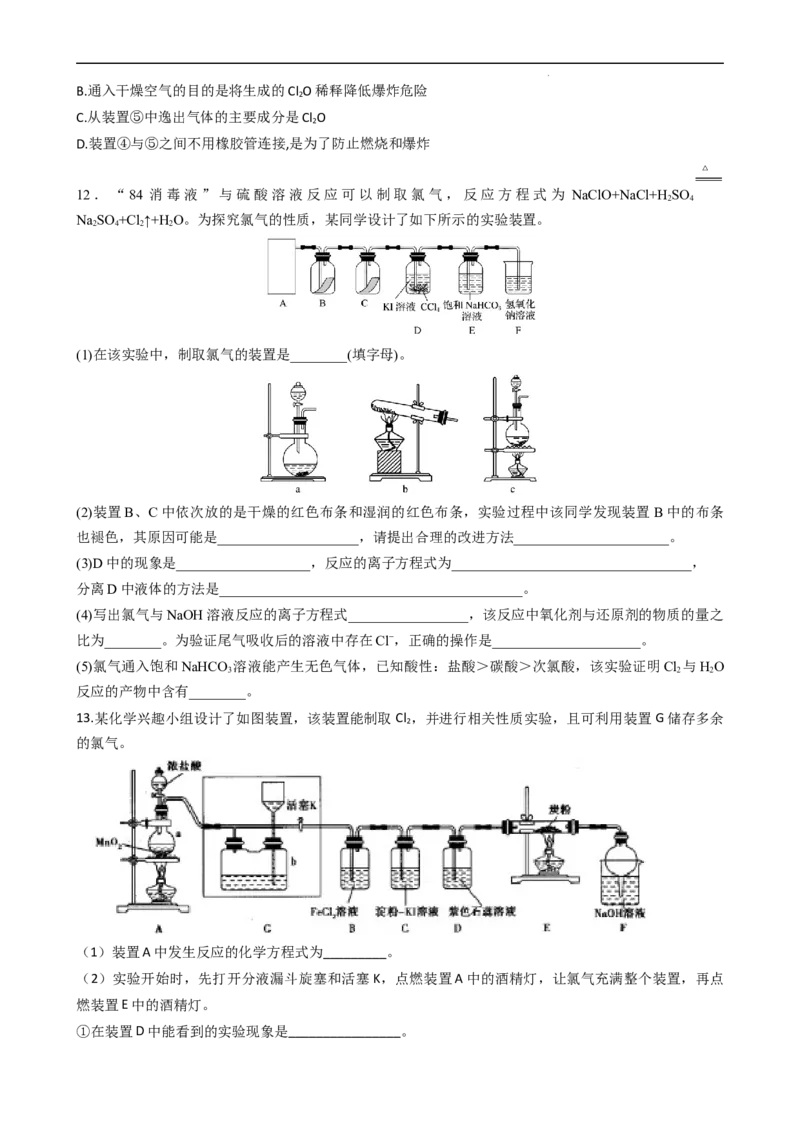
10.无水 (178℃升华)遇潮湿空气即产生大量白雾,实验室可用 Al和氯气通过如图装置制备。已知
装置A中产生的氯气中混有少许HCl和水蒸气。则下列说法正确的是( )
A.试剂瓶B、C、F中分别盛饱和 溶液、浓硫酸、浓硫酸
B.氯化铝产品最后在装置E中收集
C.实验开始时应先点燃D处酒精灯
D.装置F和G可用盛有无水 的干燥管替换
11.Cl O是黄棕色、具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有
2
机物、还原剂接触或加热时会发生燃烧并爆炸。一种制取Cl O的装置如图所示。
2
已知: Cl O的熔点为-116℃,沸点为3.8 ℃;Cl 的沸点为-34.6℃ ;HgO+2Cl =HgCl +Cl O
2 2 2 2 2
下列说法中不正确的是( )
A.装置②、③中盛装的试剂依次是饱和食盐水和浓硫酸
学科网(北京)股份有限公司B.通入干燥空气的目的是将生成的Cl O稀释降低爆炸危险
2
C.从装置⑤中逸出气体的主要成分是Cl O
2
D.装置④与⑤之间不用橡胶管连接,是为了防止燃烧和爆炸
12.“84 消毒液”与硫酸溶液反应可以制取氯气,反应方程式为 NaClO+NaCl+H SO
2 4
NaSO +Cl↑+H O。为探究氯气的性质,某同学设计了如下所示的实验装置。
2 4 2 2
(1)在该实验中,制取氯气的装置是________(填字母)。
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置 B中的布条
也褪色,其原因可能是____________________,请提出合理的改进方法______________________。
(3)D中的现象是___________________,反应的离子方程式为__________________________________,
分离D中液体的方法是___________________________________________。
(4)写出氯气与NaOH溶液反应的离子方程式_________________,该反应中氧化剂与还原剂的物质的量之
比为________。为验证尾气吸收后的溶液中存在Cl−,正确的操作是_____________________。
(5)氯气通入饱和NaHCO 溶液能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验证明Cl 与HO
3 2 2
反应的产物中含有________。
13.某化学兴趣小组设计了如图装置,该装置能制取Cl ,并进行相关性质实验,且可利用装置G储存多余
2
的氯气。
(1)装置A中发生反应的化学方程式为_________。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃装置A中的酒精灯,让氯气充满整个装置,再点
燃装置E中的酒精灯。
①在装置D中能看到的实验现象是________________。
学科网(北京)股份有限公司②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为 CO 和HCl,写出E中发生反应的化学
2
方程式为_________。
③利用装置G储存多余的氯气的操作和现象是_________。
(3)储气瓶b内盛放的试剂是___________________。
(4)装置B中发生反应的离子方程式为__________。
学科网(北京)股份有限公司学科网(北京)股份有限公司