文档内容
第二章 分子结构与性质
第三节 分子结构与物质性质
2.3.2分子间的作用力 分子的手性
本节是在学习了共价键和分子的立体构型的基础上,进一步来认识分子的一些性质,包括共价
键的极性和非极性,并由此引出一些共价分子的性质及其应用;范德华力、氢键及其对物质性质的
影响,特别是物质的熔沸点及溶解性等;教学时要注意引导学生运用“物质结构决定物质性质,性
质反映结构”的观念来理解和解释分子的性质。
课程目标 学科素养
1.认识分子间存在相互作用,知道范德华力和氢键 a.模型认知:通过范德华力、氢键对物质性
质影响的探析,形成“结构决定性质”的模
是两种常见的分子间作用力。
型认知。能从微观角度理解分子的手性,形
2.了解分子内氢键和分子内氢键在自然界中的广泛 成判断手性分子的思维模型。
存在及重要作用。
3.掌握物质的溶解性与分子结构的关系,了解“相
似相溶”规律。
4.结合实例初步认识分子的手性对其性质的影响。
教学重点:范德华力、氢键对物质性质的影响,物质的溶解性与分子结构的关系
教学难点:范德华力、氢键对物质性质的影响
多媒体调试、讲义分发
【新课导入】
【展示】
展示干冰、二氧化碳气体,固态水、液态水、气态水
【学生活动】
气体在加压或降温时为什么会变成液体或固体【讲解】
因为分子间存在间隔,气体分子间的间隔大,液体、固体分子间的间隙小。因此气体加压或降温后
会变成液体、固体。
【追问】
为什么水三态之间的转化会伴随着能量的变化?
【猜想】
分子之间可能存在着某种力,需要克服这种作用力,实现水三态之间的转化。
【新课讲授】
一.范德华力及其物质性质的影响
降温加压时气体会液化,降温时液体会凝固,这些事实表明,分子之间存在着相互作用力。范德华
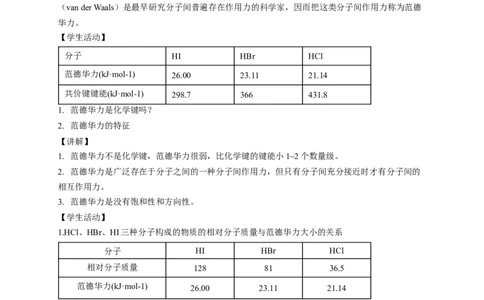
(van der Waals)是最早研究分子间普遍存在作用力的科学家,因而把这类分子间作用力称为范德
华力。
【学生活动】
分子 HI HBr HCl
范德华力(kJ·mol-1) 26.00 23.11 21.14
共价键键能(kJ·mol-1) 298.7 366 431.8
1. 范德华力是化学键吗?
2. 范德华力的特征
【讲解】
1. 范德华力不是化学键,范德华力很弱,比化学键的键能小1~2个数量级。
2. 范德华力是广泛存在于分子之间的一种分子间作用力,但只有分子间充分接近时才有分子间的
相互作用力。
3. 范德华力是没有饱和性和方向性。
【学生活动】
1.HCl、HBr、HI三种分子构成的物质的相对分子质量与范德华力大小的关系
分子 HI HBr HCl
相对分子质量 128 81 36.5
范德华力(kJ·mol-1)
26.00 23.11 21.14
【结论】
一般地,组成和结构相似的分子,相对分子质量越大,范德华力越大。即范德华力:HCl< HBr <
HI。
【学生活动】
2.CO、N 的相对分子质量、分子的极性、范德华力的关系
2
分子 相对分子质量 分子的极性 范德华力(kJ·mol-1)
CO 28 极性 8.75
N 28 非极性 8.50
2
【结论】相对分子质量相同或相近时,分子的极性越大,范德华力越大。如CO为极性分子,N 为非极性分
2
子,范德华力:CO>N。
2
【学生活动】
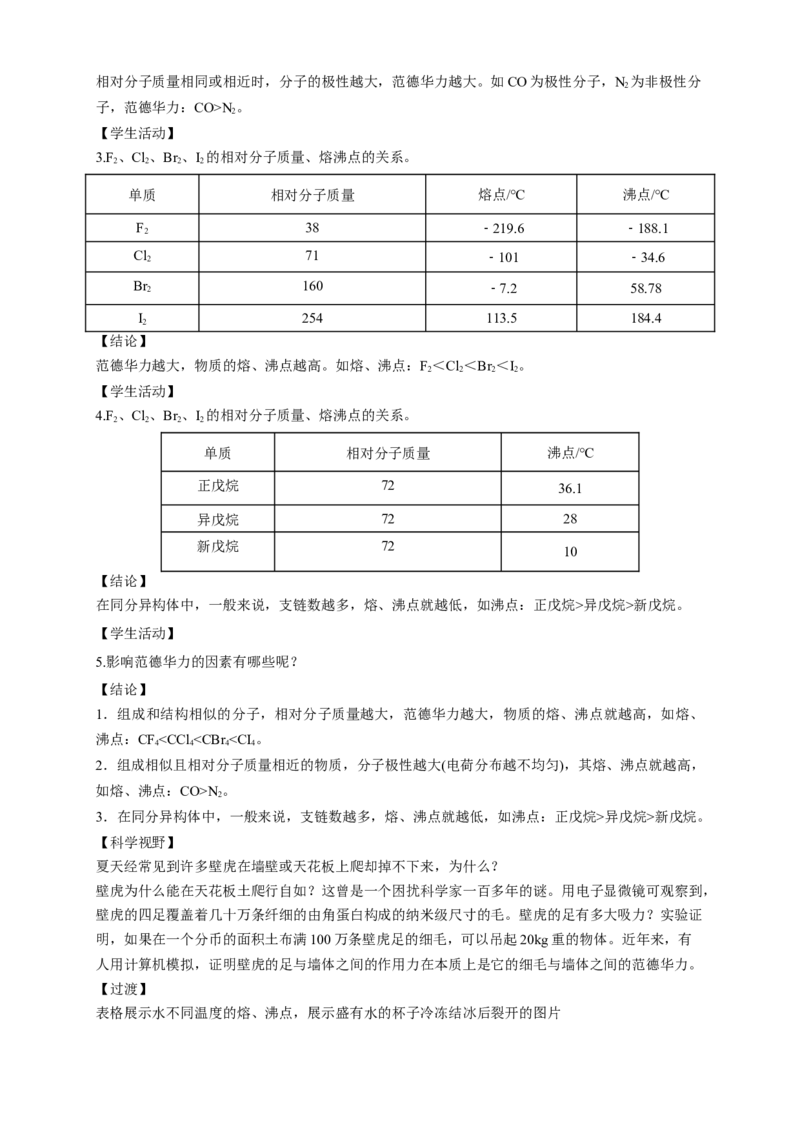
3.F、Cl、Br 、I 的相对分子质量、熔沸点的关系。
2 2 2 2
单质 相对分子质量 熔点/℃ 沸点/℃
F 38 ﹣219.6 ﹣188.1
2
Cl
2
71 ﹣101 ﹣34.6
Br 2 160 ﹣7.2 58.78
I 254 113.5 184.4
2
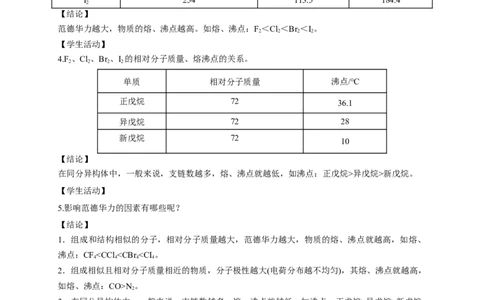
【结论】
范德华力越大,物质的熔、沸点越高。如熔、沸点:F<Cl<Br <I。
2 2 2 2
【学生活动】
4.F、Cl、Br 、I 的相对分子质量、熔沸点的关系。
2 2 2 2
单质 相对分子质量 沸点/℃
正戊烷 72 36.1
异戊烷 72 28
新戊烷 72
10
【结论】
在同分异构体中,一般来说,支链数越多,熔、沸点就越低,如沸点:正戊烷>异戊烷>新戊烷。
【学生活动】
5.影响范德华力的因素有哪些呢?
【结论】
1.组成和结构相似的分子,相对分子质量越大,范德华力越大,物质的熔、沸点就越高,如熔、
沸点:CFN。
2
3.在同分异构体中,一般来说,支链数越多,熔、沸点就越低,如沸点:正戊烷>异戊烷>新戊烷。
【科学视野】
夏天经常见到许多壁虎在墙壁或天花板上爬却掉不下来,为什么?
壁虎为什么能在天花板土爬行自如?这曾是一个困扰科学家一百多年的谜。用电子显微镜可观察到,
壁虎的四足覆盖着几十万条纤细的由角蛋白构成的纳米级尺寸的毛。壁虎的足有多大吸力?实验证
明,如果在一个分币的面积土布满100万条壁虎足的细毛,可以吊起20kg重的物体。近年来,有
人用计算机模拟,证明壁虎的足与墙体之间的作用力在本质上是它的细毛与墙体之间的范德华力。
【过渡】
表格展示水不同温度的熔、沸点,展示盛有水的杯子冷冻结冰后裂开的图片水的熔点(℃) 水的沸点(℃) 水在0 ℃时密度(g/ml) 水在4 ℃时密度(g/ml)
0.00 100.00 0.9998 1.0000
【思考】
常见物质中,水是熔沸点较高的液体之一?
冰的密度比液态水的密度小?
二、氢键及其对物质性质的影响
1.定义:已经与电负性很大的原子形成共价键的氢原子与另一个电负性很大的原子之间的作用力
2.定义阐述:当氢原子与电负性大的X原子以共价键结合时,它们之间的共用电子对强烈地偏向
X,使H几乎成为“裸露”的质子,这样相对显正电性的H与另一分子中相对显负电性的X(或Y)
中的孤对电子接近并产生相互作用,这种相互作用称氢键。
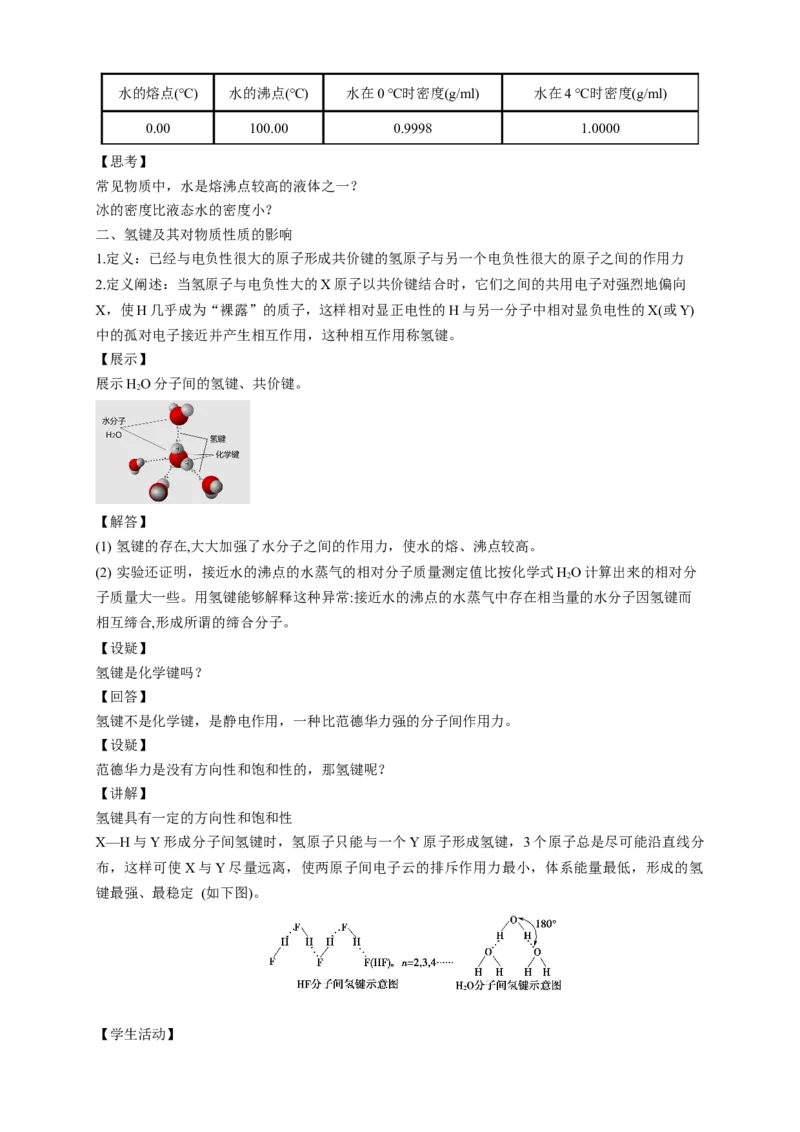
【展示】
展示HO分子间的氢键、共价键。
2
【解答】
(1) 氢键的存在,大大加强了水分子之间的作用力,使水的熔、沸点较高。
(2) 实验还证明,接近水的沸点的水蒸气的相对分子质量测定值比按化学式HO计算出来的相对分
2
子质量大一些。用氢键能够解释这种异常:接近水的沸点的水蒸气中存在相当量的水分子因氢键而
相互缔合,形成所谓的缔合分子。
【设疑】
氢键是化学键吗?
【回答】
氢键不是化学键,是静电作用,一种比范德华力强的分子间作用力。
【设疑】
范德华力是没有方向性和饱和性的,那氢键呢?
【讲解】
氢键具有一定的方向性和饱和性
X—H与Y形成分子间氢键时,氢原子只能与一个Y原子形成氢键,3个原子总是尽可能沿直线分
布,这样可使X与Y尽量远离,使两原子间电子云的排斥作用力最小,体系能量最低,形成的氢
键最强、最稳定 (如下图)。
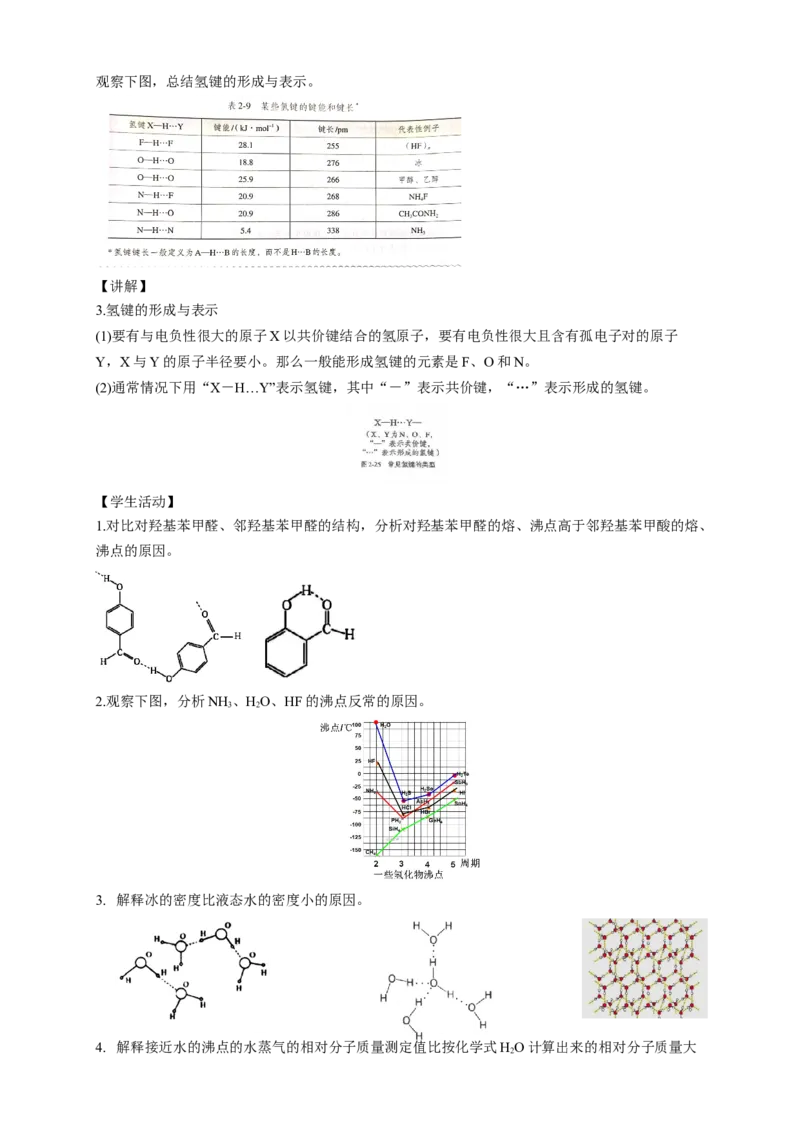
【学生活动】观察下图,总结氢键的形成与表示。
【讲解】
3.氢键的形成与表示
(1)要有与电负性很大的原子X以共价键结合的氢原子,要有电负性很大且含有孤电子对的原子
Y,X与Y的原子半径要小。那么一般能形成氢键的元素是F、O和N。
(2)通常情况下用“X-H…Y”表示氢键,其中“-”表示共价键,“…”表示形成的氢键。
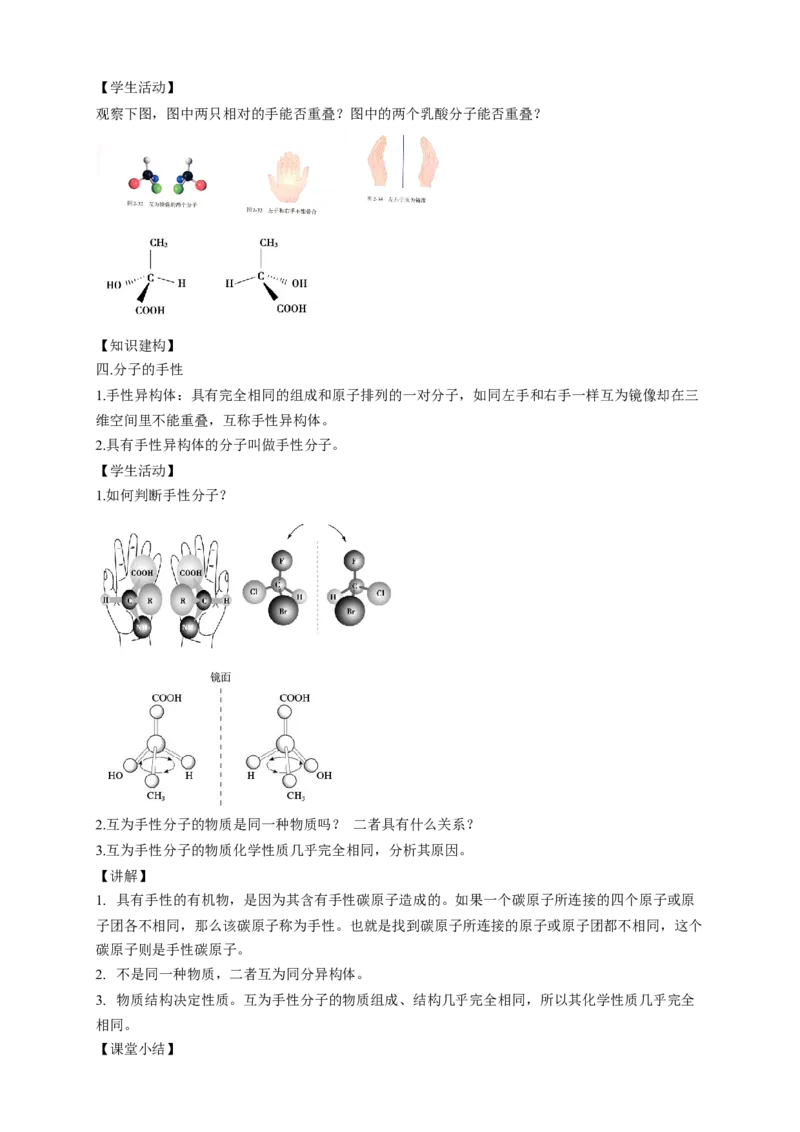
【学生活动】
1.对比对羟基苯甲醛、邻羟基苯甲醛的结构,分析对羟基苯甲醛的熔、沸点高于邻羟基苯甲酸的熔、
沸点的原因。
2.观察下图,分析NH 、HO、HF的沸点反常的原因。
3 2
3. 解释冰的密度比液态水的密度小的原因。
4. 解释接近水的沸点的水蒸气的相对分子质量测定值比按化学式HO计算出来的相对分子质量大
2一些的原因。
5. 解释氨气分子为什么极易溶于水原因。
6. 邻苯二甲酸的电离平衡常数K 比对苯二甲酸的电离平衡常数K 大
a1 a1
【讲解】
1. 氢键不仅存在于分子内,也存在于分子间。 互为同分异构体的物质,能形成分子内氢键
的,其熔沸点比能形成分子间氢键的物质的低。由于邻羟基苯甲醛能形成分子内氢键,而对羟基苯
甲醛能形成分子间氢键,当对羟基苯甲醛熔化时,需要较多的能量克服分子间氢键,所以对羟基苯
甲醛的熔沸点高于邻羟基苯甲醛的熔、沸点。
【总结】
4.氢键的类型
(1)分子间氢键,如水中O—H…O—。
(2)分子内氢键,如
2. NH 、HO、HF的沸点反常的原因:由于它们各自的分子间形成了氢键。
3 2
3. 常温下液态水中除了含有简单HO外,还含有通过氢键联系在一起的缔合分子(H O) 、
2 2 2
(H O) ……(H O) 等。一个水分子的氧原子与另一个水分子的氢原子沿该氧原子的一个sp3杂化轨
2 3 2 n
道的方向形成氢键,因此当所有HO全部缔合——结冰后,所有的HO按一定的方向全部形成了
2 2
氢键,成为晶体,因此在冰的结构中形成许多空隙,体积膨胀,密度减小。故冰的体积大于等质量
的水的体积,冰的密度小于水的密度。
4. 接近水的沸点的水蒸气中存在相当量的水分子因氢键而相互缔合形成所谓的缔合分子。
5. NH 与HO间能形成氢键,且都是极性分子,所以NH 极易溶于水。氨气,低级醇、醛、酮等
3 2 3
分子都与水分子形成氢键,均可溶于水。
6. 邻苯二甲酸存在分子内氢键,邻苯二甲酸的电离平衡常数K 比对苯二甲酸的电离平衡常数K
a1 a1
大
【总结】
5.氢键对物质性质的影响
(1).对物质熔、沸点的影响:分子间存在氢键的物质,物质的熔、沸点明显高,如NH >PH ;同分
3 3
异构体分子间形成氢键的物质比分子内形成氢键的物质熔、沸点高,如邻羟基苯甲酸<对羟基苯甲
酸
(2).对物质溶解度的影响:溶剂和溶质之间形成氢键使溶质的溶解度增大,如 NH 、甲醇、甲酸等
3
易溶于水。
(3).对物质密度的影响:氢键的存在会使某些物质的密度反常,如水的密度比冰的密度大。
(4).氢键对物质电离性质的影响:如邻苯二甲酸的电离平衡常数 K 与对苯二甲酸的电离平衡常数
a1
K 相差较大。
a1
【知识构建】
范德华力、氢键、化学键的比较
范德华力 氢键 共价键
概念 物质分子之间普遍存在的 已经与电负性很强的原子形 原子间通过共用电子对成共价键的氢原子与另一个
一种作用力 电负性很强的原子之间的静 所形成的相互作用
电作用
作用粒
分子 H与N、O、F 原子
子
特征 无方向性和饱和性 有方向性和饱和性 有方向性和饱和性
强度 共价键>氢键>范德华力
①随分子极性的增大而增
对于 成键原子半径和共用
影响强 大
X—H…Y,X、Y的电负性越 电子对数目。键长越
度的因 ②组成和结构相似的分子
大,Y原子的半径越小,作用越 短,键能越大,共价
素 构成的物质,相对分子质
强 键越稳定
量越大,范德华力越大
①影响物质的熔点、沸
①分子间氢键的存在,使物质的
点、溶解度等物理性质
对物质 熔、沸点升高,在水中的溶解度
②组成和结构相似的物 共价键键能越大,分
性质的 增大。如熔、沸点:HO>HS
2 2
质,随相对分子质量的增 子稳定性越强
影响 ②分子内存在氢键时,降低物质
大,物质的熔、沸点升
的熔、沸点
高。如CF