文档内容
3.1.2 晶胞(分层作业)
1.所列图形表示的晶体结构中,符合晶胞特点的是
A. B.
C. D.
【答案】A
【解析】晶胞特点是周期性有序无隙并置排列,具有对称性,根据图中信息B、C、D都不满足,只有A满足
条件,故A符合题意。
综上所述,答案为A。
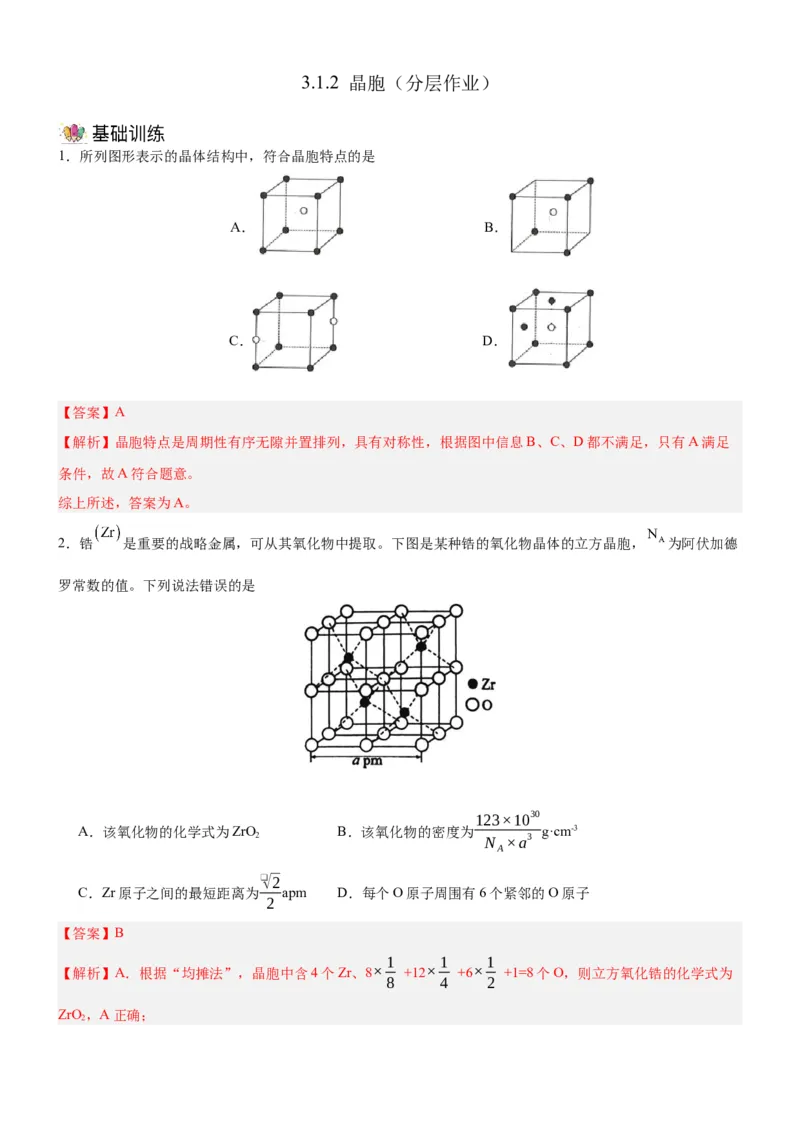
2.锆 是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立方晶胞, 为阿伏加德
罗常数的值。下列说法错误的是
123×1030
A.该氧化物的化学式为ZrO B.该氧化物的密度为 g·cm-3
2 N ×a3
A
❑√2
C.Zr原子之间的最短距离为 apm D.每个O原子周围有6个紧邻的O原子
2
【答案】B
1 1 1
【解析】A.根据“均摊法”,晶胞中含4个Zr、8× +12× +6× +1=8个O,则立方氧化锆的化学式为
8 4 2
ZrO,A正确;
24M
492
B.结合A分析可知,晶体密度为 N 1030g·cm-3= × 1030g·cm-3,B错误;
A × a3N
a3 A
❑√2
C.Zr原子之间的最短距离为面对角线的一半,即 apm,C正确;
2
D.每个O原子在xyz轴上各有2个紧邻的氧原子,则周围有6个紧邻的O原子,D正确;
故选B。
3.已知两种短周期元素X、Y的原子价层电子排布式分别为3s1、nsnnp2n。这两种元素组成的一种晶胞结构如图
所示,晶胞参数a=0.566nm。下列叙述错误的是
A.该晶体的化学式为NaO B.氧离子的配位数为4
2
C.该晶体为离子晶体 D.该晶体的密度为2.27 g⋅cm-3
【答案】B
【分析】短周期元素X原子价层电子排布式分别为3s1,X为Na元素;短周期元素Y的原子价层电子排布式为
nsnnp2n,n=2,则Y是O元素。离子半径Na+”“<”或“=”),其键角差异的原因是
。
(5) 可由Mg和 反应制得。一种 晶体的结构中有顶角相连的硅氧四面体形成螺旋上升的长链(如
下图)。其中Si原子的杂化轨道类型是 。
(6) 晶体的晶胞示意图如下。每个Mg原子位于Si原子组成的四面体的中心。则1个Si原子周围有
个紧邻的Mg原子。已知 的晶胞边长为 ,阿伏加德罗常数的值为 ,则 晶体的密度为
。
【答案】(1) 第三周期第ⅣA族 3p
(2)O>N>H
(3)c
(4) 高 SiH 和CH 为结构相似的分子,相对分子质量SiH>CH ,分子间范德华力SiH 和CH >
4 4 4 4 4 4
SiH 与NH 的中心原子上价层电子对数均为4,但NH 中心原子N原子上含有一对孤对电子,孤对电子与成键
4 3 3
电子之间的排斥力强于成键电子与成键电子之间的斥力,导致SiH 中H—Si—H的键角大于NH 中H—N—H的
4 3
键角(5)sp3
304
(6) 8
a3×N
A
【解析】(1)硅在元素周期表中位于第三周期第ⅣA族;基态硅原子的核外电子排布式为1s22s22p63s23p2,占
据的最高能级为3p能级。
(2)同周期从左到右主族元素的电负性逐渐增大,元素的非金属性越强、电负性越大,则电负性O>N>H。
(3) 电离最外层一个电子是氮的第二电离能, 电离最外层一个电子是氮
的第一电离能, 为激发态的氮原子,故电离最外层一个电子所需能量由小到大的顺
序为c<b<a;答案选c。
(4)①SiH、CH 都为分子晶体,SiH 和CH 的结构相似,相对分子质量SiH>CH,分子间范德华力SiH>
4 4 4 4 4 4 4
CH,故SiH 的沸点比CH 的高。
4 4 4
1 1
②SiH 中中心原子Si的孤电子对数为 ×(4-4×1)=0、价层电子对数为4,NH 中中心原子N上的孤电子对数为
4 2 3 2
×(5-3×1)=1、价层电子对数为4,即两者中心原子上价层电子对数均为4,但NH 中心原子N原子上含有一对孤
3
对电子,孤对电子与成键电子之间的排斥力强于成键电子与成键电子之间的斥力,导致SiH 中H—Si—H的键
4
角大于NH 中H—N—H的键角。
3
(5)由图可知,Si形成4个Si—Oσ键,Si上没有孤电子对,Si的价层电子对数为4,Si原子采取sp3杂化。
(6)以面心Si为研究对象,由于每个Mg原子位于Si原子组成的四面体的中心,则1个Si原子周围有8个紧
4×76
邻的Mg原子;根据“均摊法”,1个晶胞中含4个“MgSi”,1个晶胞的质量为 g,晶胞的边长为
2 N
A
4×76 304
acm,晶胞的体积为a3cm3,MgSi晶体的密度为 g÷a3cm3= g/cm3。
2 N a3×N
A A
8.过氧化钙晶体的晶胞结构如下图所示,已知该晶胞的密度是ρg·cm−3(N 表示阿伏伽德罗常数)。下列表述不
A
正确的是A.基态Ca2+的电子排布式:1s22s22p63s23p6
B.过氧化钙电子式:
C.晶体中Ca2+紧邻6个O
D.晶胞结构中最近的两个Ca2+间的距离为: nm
【答案】D
【解析】A.Ca原子序数20,基态Ca2+的核外电子排布式:1s22s22p63s23p6,A正确;
B.过氧化钙为离子化合物,电子式: ,B正确;
C.根据晶胞结构,与Ca2+紧邻6个O2- ,C正确;
2
1 1
D.晶胞结构中最近的两个Ca2+间的距离为面对角线的一半。晶胞中含钙离子数目:8× +6× = 4,含过氧
8 2
1 4×72
根离子数目:12× +1 = 4,假设晶胞棱长为a,晶胞密度为ρg·cm−3,根据晶胞密度计算公式:ρ=
4 a3×N
A
√ 4×72 √ 4×72 ❑√2 √ 4×72
g·cm−3,解得a= 3 cm= 3 ×107nm,即晶胞结构中最近的两个Ca2+间的距离: ×3 ×
ρ×N ρ×N 2 ρ×N
A A A
107nm,D错误;
答案选D。
9.经理论计算预测,一种由汞(Hg)、锗(Ge)、锑(Sb形成的新物质X为潜在的拓扑绝缘体材料。X的晶体可视
为金刚石晶体中的C原子被Hg、Ge和Sb取代后形成。其晶胞如图所示,下列说法正确的A. 、 、 三种元素都位于周期表的ds区
B.设X的最简式的式量为Mr,则X晶体的密度为
C.晶体中与 距离最近的 的数目为6
D.X晶体是一种合金,内部有自由电子,是电的良导体
【答案】B
【解析】A.Hg元素位于周期表的ds区,Ge、Sb两种元素都位于周期表的p区,A错误;
1 1 1 1
C.根据均摊法,X晶胞中Hg的个数为4× +6× =4,Ge的个数为8× +4× +1=4,Sb的个数为8,则
4 2 8 2
M
r×4
晶体的化学式为HgGeSb ,设X的最简式的式量为Mr,则X晶体的密度为ρ= N g·cm-3=
2 A
x2y×10−21
4M
r
g·cm-3,B正确;
N x2y×10−21
A
C.由图可知,离面心Hg原子最近的Sb原子有4个,C错误;
D.由题干可知,新物质X为潜在的拓扑绝缘体材料,不是电的良导体,D错误;
故选B。
10.已知: , 晶胞如图所示,晶胞边长为a pm,设 为阿伏加
德罗常数的值。下列叙述错误的是A.该晶胞中含有4个FeS
2
B.离Fe2+最近的S2- 有12个
2
C.该晶体的密度为
D.上述反应中,每生成 ,转移电子数为
【答案】B
1
【解析】A.根据晶胞结构可知,小黑球为Fe2+位于棱上和体心,数目为12× +1=4,小灰球为S2- 位于顶点和
4 2
1 1
面心,数目为8× +6× =4,根据化学式为FeS 可知该晶胞中含有4个FeS,A正确;
8 2 2 2
B.根据晶胞结构可知,与Fe2+(位于体心的小黑球)距离最近且相等的S2- 有6个,则Fe2+的配位数为6,B错
2
误;
1 1 1
C.在晶胞中,含Fe2+个数为12× +1=4,含S2- 个数为8× +6× =4,则FeS 晶胞密度为
4 2 8 2 2
4×120g/mol
N mol−1×(a×10−10cm) 3
A
120×4
= g·cm-3,C正确;
a3×10−30·N
A
D.根据方程式中O 的变化可知O化合价降低为-2价,那么消耗1molO 转移4mole-,由此可得
2 2
7O~2FeSO ~28e-,计算可知每生成1molFeSO ,转移电子数为14N ,D正确;
2 4 4 A
故答案选B。
11.科学工作者发现了一种光解水的催化剂,其品胞结构如图所示,已知晶胞参数为 。下列说法中正确的
是A.Ce与O的数目之比为 B.Ce在晶胞中的配位数为4
C.Ce与O最近的距离为 D.该晶体的摩尔体积为
【答案】C
1 1
【解析】A.据“均摊法”,晶胞中,Ce的个数为8× +6× =4,O的个数为8,则晶胞中Ce与O的个数比为
8 2
1:2,A错误;
B.以底面面心的Ce为例,上、下层各有4个氧原子,故Ce在晶胞中的配位数为8,B错误;
√33
C.Ce与O的最近距离为体对角线的四分之一,为 apm,C正确;
4
1 a3·10−36N
D.1个晶胞体积为a3×10-36m3,含有4个Ce和8个O,则该晶体的摩尔体积为 ×a3×10-36m3×N = A
4 A 4
m3·mol-1,D错误;
答案选C。
12. 晶胞结构中 的位置如图1所示。 位于 所构成的四面体中心,其晶胞俯视图如图2所示。若晶
胞参数为 ,阿伏加德罗常数的数值为 ,下列说法正确的是
A. 晶胞中, 的配位数为8 B. 晶体的密度为
C. 晶胞中, 之间的最短距离为 D. 晶胞中, 填充了8个四面体空隙
【答案】B1 1
【分析】该晶胞中S2-个数=8× +6× =4,S2-所构成的四面体空隙有8个,根据化学式CuS可以判断有4个空
8 2
隙填充了Cu2+,Cu2+之间的最短距离为晶胞面角线的一半。
【解析】A.由上述分析可知,Cu2+填充在,S2-所构成的四面体空隙中,故Cu2+的配位数为4,故A错误;
4×(64+32)
B.上述晶胞含有4个CuS,故1个晶胞的质量等于 g,1个晶胞的体积为a3×10-30cm3,晶体的密度
N
A
96×4×1030
为 g·cm-3,故B正确;
N ×a3
A
√22
C.CuS晶胞中,Cu2+之间的最短距离为晶胞面角线的一半,即 apm,故C错误;
2
D.由分析可知,Cu2+填充了4个四面体空隙,故D错误。
答案选B。
13.铁有δ、γ、α三种同素异形体,其晶胞结构如图所示,下列判断正确的是
A.δ、γ、α铁晶体中存在金属阳离子和阴离子
B. 晶胞中所含有的铁原子数为9
C.δ、α两种晶胞中铁原子周围等距离且最近的铁原子个数之比为3∶1
D.若 晶胞棱长为acm, 晶胞棱长为bcm,则两种晶体的密度比为
【答案】D
【解析】A.金属晶体中存在金属阳离子和自由电子,不存在阴离子,A错误;
1
B.根据“均摊法”,晶胞中含8× +1=2个Fe,B错误;
8
C.由图可知,δ-Fe晶胞中Fe原子的配位数为8,α-Fe晶胞中铁原子的配位数为6,故二者晶胞中铁原子周围
等距离且最近的铁原子个数之比为8∶6=4∶3,C错误;
4M
1 1 1
D.根据“均摊法”, γ-Fe晶胞中含8× +6× =4个Fe,α-Fe晶胞中含8× =1个Fe,则晶体密度比为 N :
8 2 8 A
a3M
N =4b3:a3,D正确;
A
b3
故选D。
14.氮化铬的晶胞结构如图所示,A点分数坐标为(0,0,0)。氮化铬的晶体密度为dg/cm3,摩尔质量为Mg/
mol,晶胞参数为anm,N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.基态铬原子价电子排布图为3d54s1
B.Cr原子位于N原子构成的四面体空隙中
C.距离Cr原子最近的Cr原子有8个
D.
【答案】D
【解析】A.基态Cr原子的价电子排布图为 ,A错误;
B.由题干晶胞示意图可知,Cr原子位于N原子构成的八面体空隙中,B错误;
C.由题干晶胞示意图可知,距离体心的Cr原子最近的Cr原子位于棱心,共有12个,C错误;
1 1
D.由题干晶胞示意图可知,N原子位于顶点和面心,个数为8× +6× =4,Cr原子位于棱心和体心,个数为
8 2
1 4M m 4Mg
12× +1=4,晶胞的质量为 g,晶胞体积为(a×10-7)cm3,根据ρ= 可得,dg·cm-3= ,则
4 N V N (a×10−17 ) 3cm3
A A
√ 4M
a= 3 ×107,D正确;
N d
A
故选D。
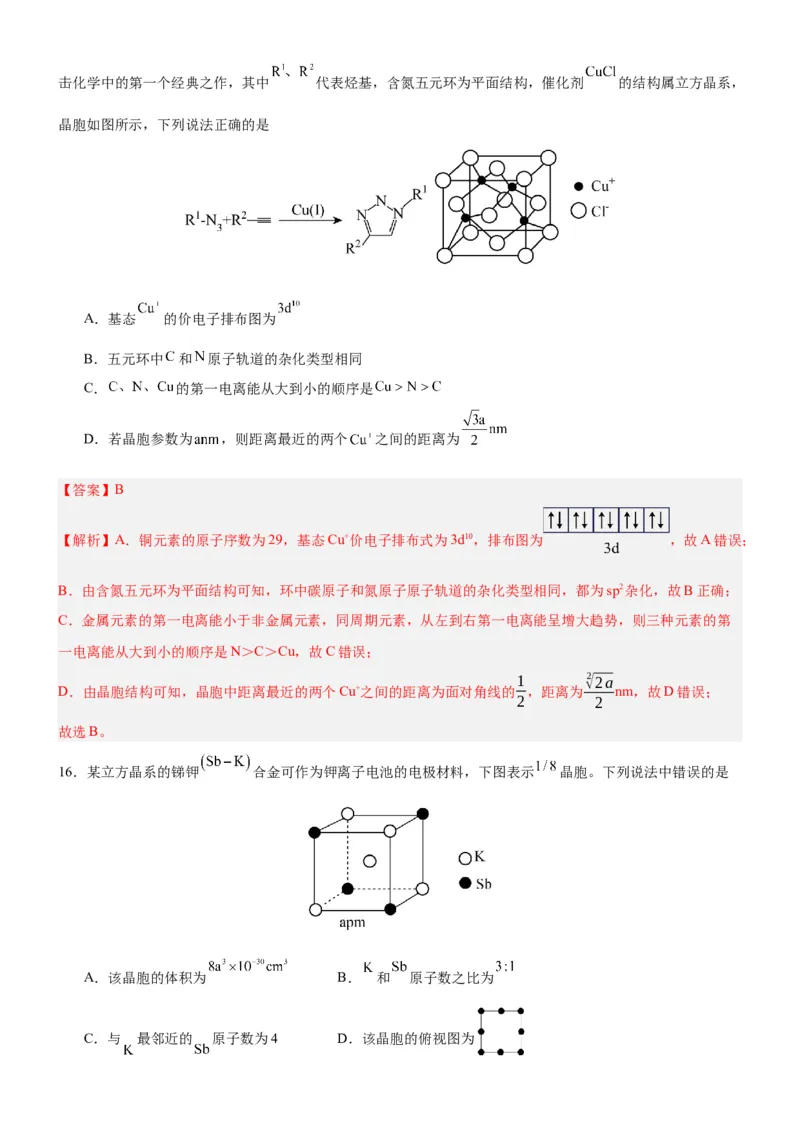
15.2022年诺贝尔化学奖授予了点击化学领域的三位科学家。一价铜催化的叠氮化物-炔烃环加成反应可谓点击化学中的第一个经典之作,其中 代表烃基,含氮五元环为平面结构,催化剂 的结构属立方晶系,
晶胞如图所示,下列说法正确的是
A.基态 的价电子排布图为
B.五元环中 和 原子轨道的杂化类型相同
C. 的第一电离能从大到小的顺序是
D.若晶胞参数为 ,则距离最近的两个 之间的距离为
【答案】B
【解析】A.铜元素的原子序数为29,基态Cu+价电子排布式为3d10,排布图为 ,故A错误;
B.由含氮五元环为平面结构可知,环中碳原子和氮原子原子轨道的杂化类型相同,都为sp2杂化,故B正确;
C.金属元素的第一电离能小于非金属元素,同周期元素,从左到右第一电离能呈增大趋势,则三种元素的第
一电离能从大到小的顺序是N>C>Cu,故C错误;
1 √22a
D.由晶胞结构可知,晶胞中距离最近的两个Cu+之间的距离为面对角线的 ,距离为 nm,故D错误;
2 2
故选B。
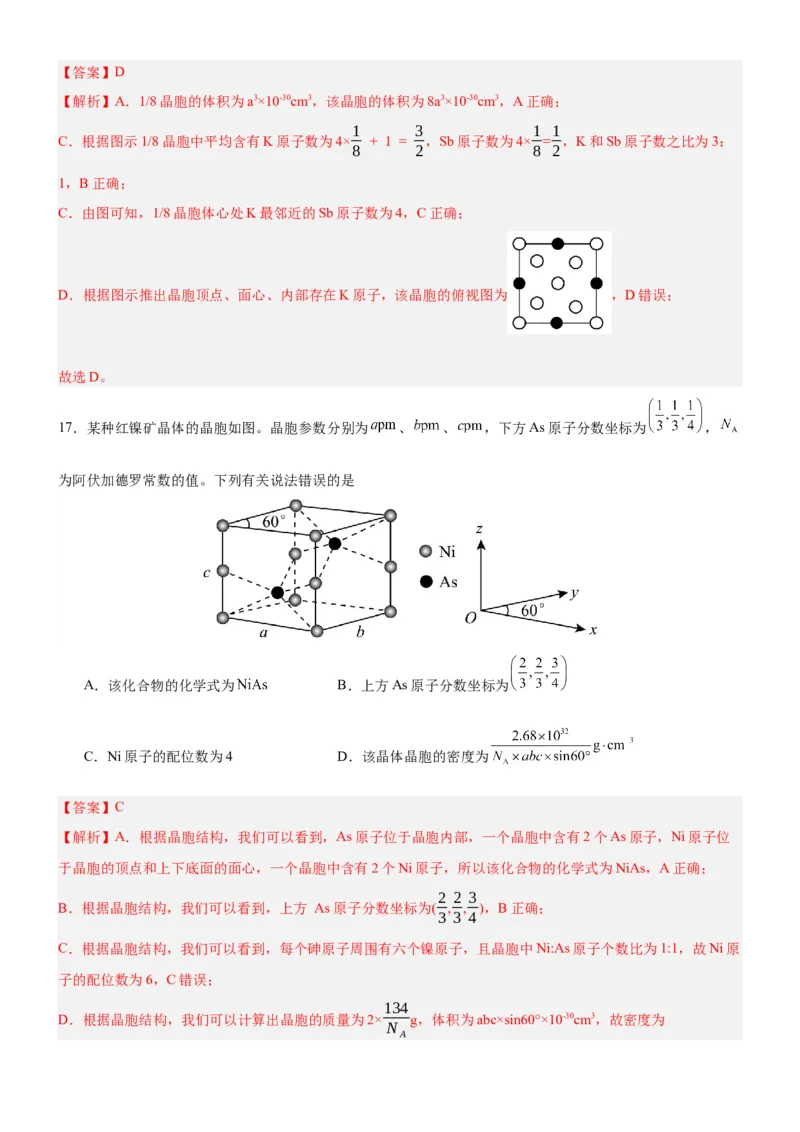
16.某立方晶系的锑钾 合金可作为钾离子电池的电极材料,下图表示 晶胞。下列说法中错误的是
A.该晶胞的体积为 B. 和 原子数之比为
C.与 最邻近的 原子数为4 D.该晶胞的俯视图为【答案】D
【解析】A.1/8晶胞的体积为a3×10-30cm3,该晶胞的体积为8a3×10-30cm3,A正确;
1 3 1 1
C.根据图示1/8晶胞中平均含有K原子数为4× + 1 = ,Sb原子数为4× = ,K和Sb原子数之比为3:
8 2 8 2
1,B正确;
C.由图可知,1/8晶胞体心处K最邻近的Sb原子数为4,C正确;
D.根据图示推出晶胞顶点、面心、内部存在K原子,该晶胞的俯视图为 ,D错误;
故选D。
17.某种红镍矿晶体的晶胞如图。晶胞参数分别为 、 、 ,下方As原子分数坐标为 ,
为阿伏加德罗常数的值。下列有关说法错误的是
A.该化合物的化学式为 B.上方As原子分数坐标为
C.Ni原子的配位数为4 D.该晶体晶胞的密度为
【答案】C
【解析】A.根据晶胞结构,我们可以看到,As原子位于晶胞内部,一个晶胞中含有2个As原子,Ni原子位
于晶胞的顶点和上下底面的面心,一个晶胞中含有2个Ni原子,所以该化合物的化学式为NiAs,A正确;
2 2 3
B.根据晶胞结构,我们可以看到,上方 As原子分数坐标为( , , ),B正确;
3 3 4
C.根据晶胞结构,我们可以看到,每个砷原子周围有六个镍原子,且晶胞中Ni:As原子个数比为1:1,故Ni原
子的配位数为6,C错误;
134
D.根据晶胞结构,我们可以计算出晶胞的质量为2× g,体积为abc×sin60°×10-30cm3,故密度为
N
A2.68×1032
g·cm-3,D正确;
N ×abc×sin60°
A
故选C。
18.铁、钨、氮三种元素组成的氮化物表现出特殊的导电性质,晶胞结构如图。
该晶体的化学式为 ;设 为阿伏加德罗常数的值,该晶体的密度 。已知:Fe-56、
N-14、W-184
56×2+184×2+14×4
【答案】 FeWN ❑√3
2 N ×(a×10−7 ) 2×c×10−7
2 A
1 1
【解析】N位于顶点、体内、棱上,则N的个数为8× +4× +2=4,Fe位于体内,个数为2,W位于体内,
8 4
m NM
个数为2,则Fe:W:N的个数比为1:1:2,则化学式为FeWN;根据密度计算公式ρ= = =
2 V N V
A
(2×56+184×2+6×14)
❑√3 g/cm3
N × (a×10−7 ) 2×c×10−7
A 2
(56×2+184×2+14×6)
故答案为:FeWN; ❑√3 。
2 N ×(a×10−7 ) 2×c×10−7
2 A
19.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
(1)距离Mg原子最近的Fe原子个数是 。(2)若该晶胞的晶胞边长为d nm,则该合金的密度为 。(不用化简)
(3)若该晶体储氢时,H 分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下H 的体积
2 2
约为 L。
【答案】(1)4
4.16×1023
(2)
N d3
A
(3)22.4
【解析】(1)由晶胞结构可知,Mg位于Fe原子围成的四面体空隙中,距离Mg原子最近的Fe原子个数是4;
1 1
(2)由晶胞结构可知,Fe位于顶点和面心,个数为:8× +6× =4;Mg位于体内,个数为8,则该晶胞的
8 2
56×4+24×8 416 4.16×1023
质量为: = g,晶胞体积为:(d×10-7)cm3,则该合金的密度为 g·cm-3;
N N N d3
A A A
1
(3)该晶体氢时,H 分子在晶胞的体心和棱心位置,则1个晶胞中H 分子个数为:1+12× =4;结合以上分
2 2 4
析吸氢后晶胞的化学式可表示为:MgFeH。则含Mg 48g的该储氢合金可储存1mol氢气,标准状况下的体积
2 2
约为22.4L。