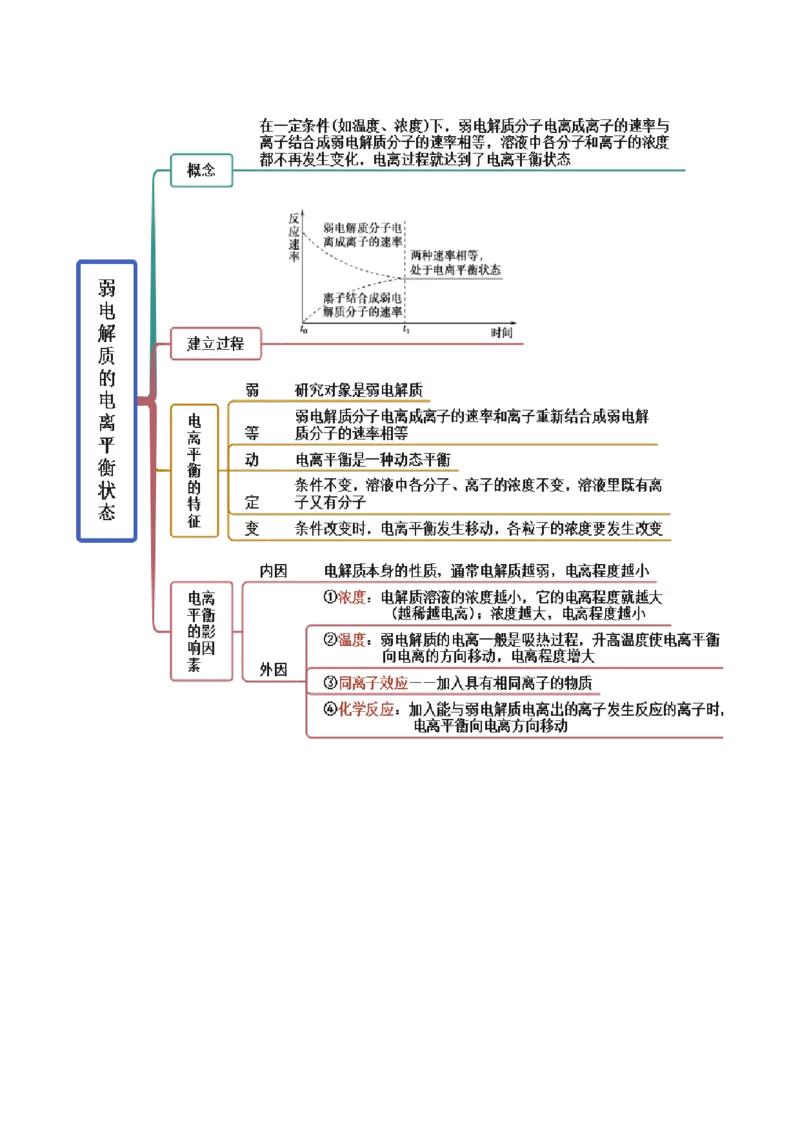
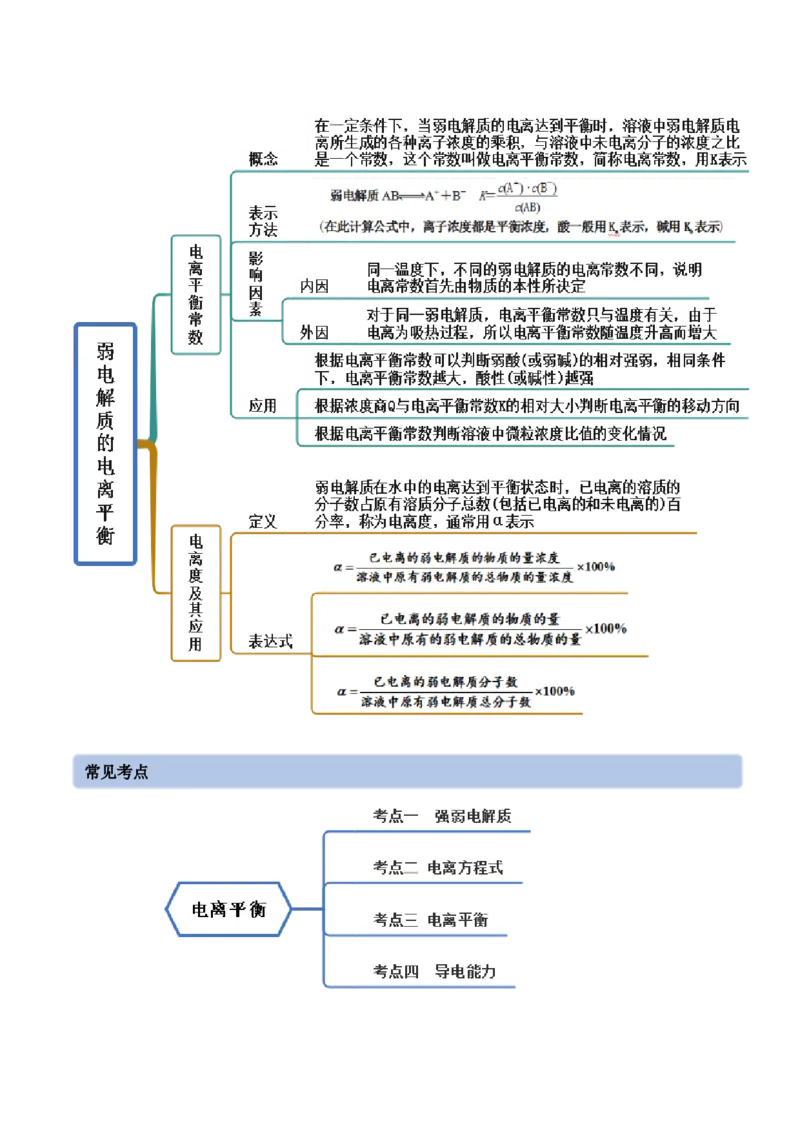
文档内容
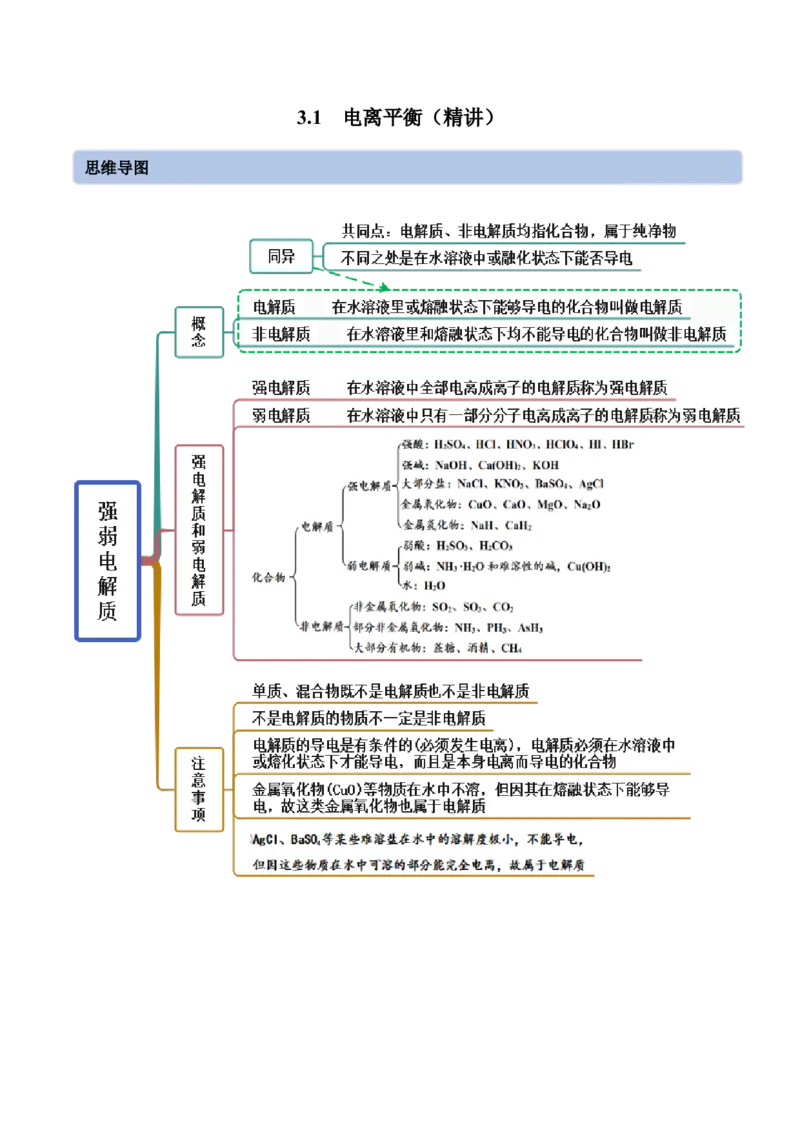
3.1 电离平衡(精讲)
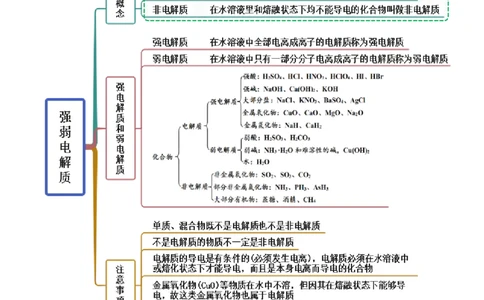
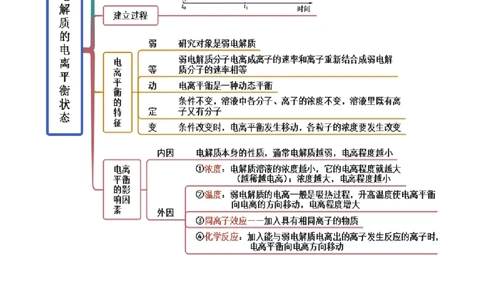
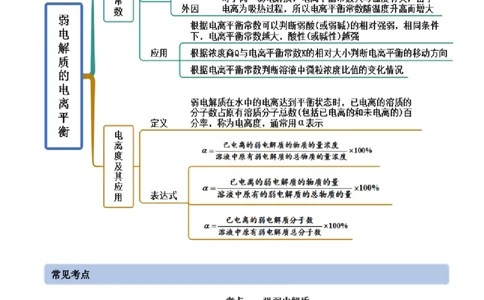
思维导图常见考点考点一 强弱电解质
【例1-1】(2022·湖南张家界·高二期末)下列物质属于弱电解质的是
A.KOH B.HSO C.HO D.SO
2 4 2 2
【例1-2】(2021·全国·高二专题练习)下列关于强、弱电解质的叙述,有错误的是
A.强电解质在溶液中完全电离,不存在电离平衡
B.在溶液中,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质
C.同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不同
D.纯净的强电解质在液态时,有的导电,有的不导电
【一隅三反】
1.(2022·四川甘孜·高二期末)下列物质属于强电解质的是
A. B. C. D.
2.(2022·四川达州·高二期末)下列物质属于弱电解质的是
A. B. C. D.
3.(2021·广西玉林·高二期中)乙酸的下列性质中,可以证明它是弱电解质的是
A.乙酸以任意比与水互溶
B.0.1mol/L乙酸溶液的c(H+)=10-3mol/L
C.10mL1mol/L乙酸恰好与10mL1mol/LNaOH溶液完全反应
D.乙酸溶液的导电性比一元强酸溶液的弱
考点二 电离方程式的书写
【例2-1】(2022·云南·澄江市第一中学)下列电离方程式中书写正确的是
A.HSO =2H++SO B.Ca(OH) =Ca2++(OH)
2 4 2
C.NH NO =NH+H++NO D.NaHCO =Na++H++CO
4 3 3 3
【例2-2】.(2021·云南·弥勒市一中)下列物质在水中的电离方程式书写正确的是
A.MgCl = Mg2+ + Cl B.NaHSO Na+ +HSO
2 4 =
C.HSO = 2H+ + SO D.Ba(OH) = Ba2+ + 2(OH)-
2 4 2【一隅三反】
1.下列物质在水中的电离方程式书写正确的是
A.KClO=K++Cl-+3O2- B.Fe(NO )=Fe2++3
3 3 3
C.NaHSO=Na++H++ D.NaHCO =Na++H++
4 3
2.下列物质在水溶液中的电离方程式书写错误的是
A.CaCl =Ca2++2Cl- B.NaOH=Na++OH-
2
C.HNO=H++ D.KClO=K++Cl++3O2-
3 3
3.(2022·新疆昌吉·高二期末)下列物质在水溶液中的电离方程式书写正确的是
A.CHCOOH H++CH COO- B.NaHSO=Na++HSO
3 3 4
C.HPO 3H++PO D.NaHCO Na++H++CO
3 4 3
4.下列电离方程式书写不正确的是
A.Ca(OH) =Ca2++2OH- B.KNO=K++NO
2 3
C.CHCOOH CHCOO-+H+ D.NaSO =Na +SO
3 3 2 3
考点三 电离平衡
【例3-1】请根据化学平衡影响因素的相关知识,分析温度、浓度等外界条件对电离平衡的影响?完成下
表:
CHCOOH CHCOO-+H+
3 3
改变条件 平衡移动方向 c(H+) c(Ac-) c(HAc) 电离程度
(1)加热 ____ ____ ____ ____ ____
(2)加盐酸 ____ ____ ____ ____ ____
(3)加NaOH(s) ____ ____ ____ ____ ____
(4)加NaAc(s) ____ ____ ____ ____ ____
(5)加CHCOOH ____ ____ ____ ____ ____
3
(6)加水 ____ ____ ____ ____ ____【例3-2】(2021·全国·高二专题练习)完成下列问题。
(1)某浓度的氨水中存在平衡:NH ·H O +OH-。如想增大 的浓度而不增大OH-的浓度,应采取的
3 2
⇌
措施是___________(填字母)。
a.适当升高温度 b.加入NH Cl固体 c.通入NH d.加入少量浓盐酸
4 3
(2)将0.1mol·L-1的CHCOOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是___________(填字母)。
3
a.电离程度增大 b.溶液中离子总数增多
c.溶液导电性增强 d.溶液中醋酸分子增多
【例3-3】(2022·宁夏·银川二中高二阶段练习)醋酸溶液中存在电离平衡:CHCOOH CHCOO-+ H+,
3 3
要使电离平衡右移且c(H+)增大,应采取的措施是
A.加入NaOH(s) B.加入盐酸 C.加蒸馏水 D.升高温度
【例3-4】(2022·内蒙古·阿拉善盟第一中学高二期末)在25℃时,用蒸馏水稀释1 mol·L-1氨水至0.01
mol·L-1,随溶液的稀释,下列各项中始终保持增大趋势的是
A. B. C. D.c(OH-)
【一隅三反】
1.某浓度的氨水中存在下列平衡:NH ·H O +OH-,如果增大 的浓度,而不增大OH-的浓
3 2
度,应采取的措施是
A.适当升高温度 B.加入NH Cl固体
4
C.通入NH D.加入少量NaOH
3
2.(2022·云南·弥勒市一中高二阶段练习)对于0.1 mol·L-1的醋酸溶液,CHCOOH CHCOO-+H+,
3 3
下列说法错误的是
A.温度降低后,溶液的酸性增强
B.温度升高后,溶液的酸性增强
C.升高温度能促进弱电解质的电离D.温度升高, 比值增大
3.(2022·辽宁·丹东市教师进修学院高二期末)分别对 稀溶液进行下列操作,一定可使
增大的是
①升温 ②恒温加少量水 ③恒温加入少量固体
④恒温加入少量固体 ⑤恒温加入少量醋酸
A.①② B.②⑤ C.①⑤ D.④⑤
4.回答下列各小题:
(1)H S溶于水的电离方程式为__________________。
2
(2)向HS溶液中加入CuSO (aq)时,电离平衡向_____移动(填“左”或“右”),c(H+)___,c(S2-)_____(填
2 4
“增大”、“减小”或“不变”);
(3)向HS溶液中加入NaOH(s)时,电离平衡向______移动(填“左”或“右”),c(H+)____,c(S2-)_____(填
2
“增大”、“减小”或“不变”);
(4)若将HS溶液加热至沸腾,c(HS)_________填“增大”、“减小”或“不变”);若要增大HS溶液中
2 2 2
c(S2-),最好加入____________。
考点四 导电能力
【例4】(2022·四川雅安·高二期末)常温下,0.1 mol∙L−1下列溶液:①HC1、②HSO 、③CHCOOH,
2 4 3
导电能力强弱顺序是
A.②>①>③ B.①=②>③ C.①>②>③ D.①=②=③
【一隅三反】
1.在CHCOOH溶液中滴入过量稀氨水,溶液的导电能力发生变化,其电流强度(I)随氨水的加入体积(V)
3
的变化曲线(如图)是
A. B.C. D.
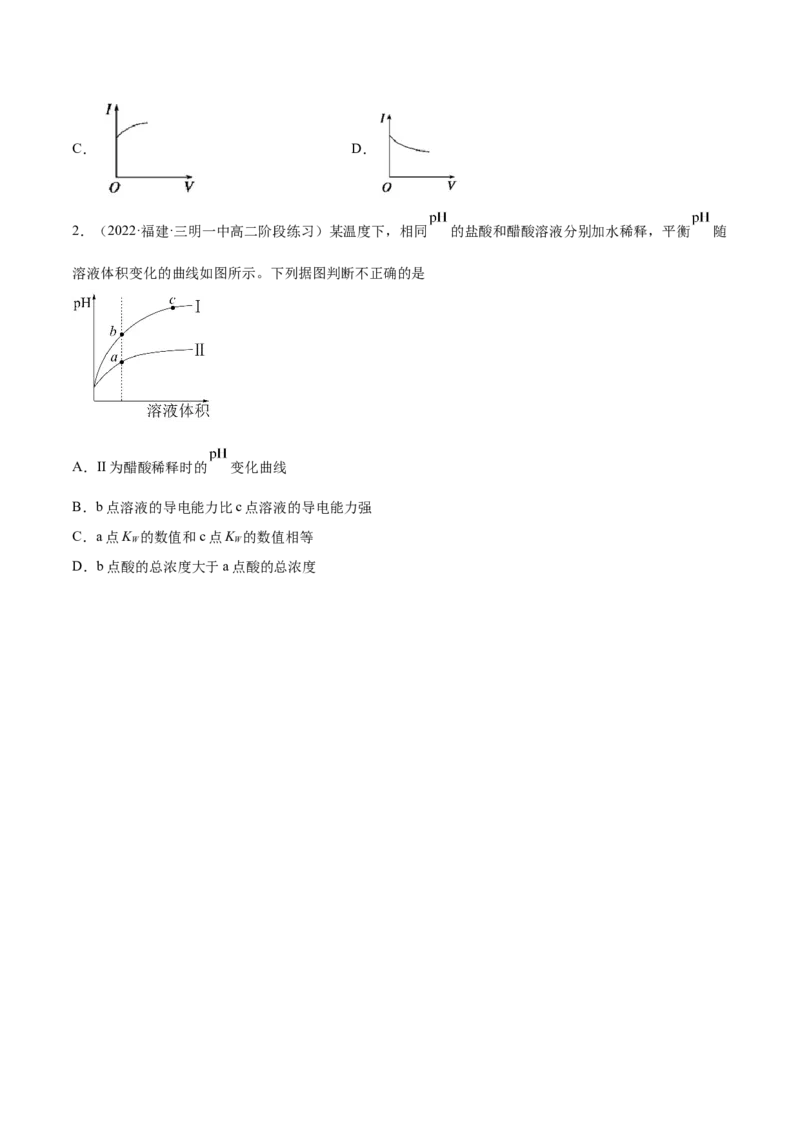
2.(2022·福建·三明一中高二阶段练习)某温度下,相同 的盐酸和醋酸溶液分别加水稀释,平衡 随
溶液体积变化的曲线如图所示。下列据图判断不正确的是
A.II为醋酸稀释时的 变化曲线
B.b点溶液的导电能力比c点溶液的导电能力强
C.a点K 的数值和c点K 的数值相等
W W
D.b点酸的总浓度大于a点酸的总浓度倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育