文档内容
3.1 铁及其化合物
【题组一 工业炼铁】
1.(2020·全国高一课时练习)北宋沈括的《梦溪笔谈》对指南针已有详细记载:“方家以磁石磨针锋,
则能指南。”磁石的主要成分是( )
A. B. C. D.
【答案】C
【解析】 叫磁性氧化铁,具有磁性,制指南针的磁石的主要成分是 ,C答案选C。
2.(2020·全国高一课时练习)指南针是我国的四大发明之一,制造指南针的磁性物质是( )
A.FeO B.Fe O C.Fe O D.Fe
2 3 3 4
【答案】C
【解析】A. FeO没有磁性,故A错误;B. Fe O 没有磁性,故B错误;C. Fe O 有磁性,可以用来制造指
2 3 3 4
南针,故C正确;D. Fe没有磁性,故D错误;故选C。
3.(2020·湖南)中国传统文化博大精深,明代方以智的《物理小识》中有关炼铁的记载:“煤则各处产
之,臭者烧熔而闭之成石,再凿而入炉曰礁,可五日不灭火,煎矿煮石,殊为省力。”下列说法中正确的
是
A.《物理小识》中记载的是以焦炭作为还原剂的方法来炼铁
B.文中说明以煤炭作为燃料被普遍使用,煤的主要成分为烃
C.生铁是指含硫、磷、碳量低的铁合金
D.工业上可通过煤的干馏获得乙烯、丙烯等化工原料
【答案】A
【解析】A.由《物理小识》中记载语句“臭者烧熔而闭之成石,再凿而入炉曰礁,可五日不灭火,煎矿
煮石”可知是以焦炭作为还原剂的方法来炼铁,A选项正确;
B.煤其主要成分为碳、氢、氧和少量的氮、硫或其它元素,而烃只由C、H两种元素组成,B选项错误;
C.生铁的含碳量比钢的含碳量较高,故生铁不是指含碳量很低的铁合金,C选项错误;
D.工业上可通过石油的裂化、裂解获得乙烯、丙烯等化工原料,D选项错误;
答案选A。
4.(2020·三亚华侨学校高一开学考试) 是高炉炼铁的重要反应。下列关于
该反应的说法正确的是
A.CO是氧化剂 B.CO得到电子
C. 被还原 D. 发生氧化反应
【答案】C
【解析】A.由Fe O+3CO 2Fe+3CO 反应可知,C元素的化合价由+2价变为+4价,化合价升高,
2 3 2CO发生氧化反应,CO作还原剂,故A错误;
B.由Fe O+3CO 2Fe+3CO 反应可知,C元素的化合价由+2价变为+4价,化合价升高,失去电子,
2 3 2
故B错误;
C.由Fe O+3CO 2Fe+3CO 反应可知,Fe元素的化合价由+3价变为0价,化合价降低,得到电子,
2 3 2
Fe O 被还原,故C正确;
2 3
D.由Fe O+3CO 2Fe+3CO 反应可知,Fe元素的化合价由+3价变为0价,化合价降低,Fe O 发生
2 3 2 2 3
还原反应,故D错误;
答案为C。
5.硫铁矿石(主要成分FeS)用于工业制硫酸,其排出的矿渣在一定条件下以磁性铁为主。经磁选获得
2
精矿,可直接用于高炉炼铁。已知某精矿的主要成分是磁性铁(Fe O)和Fe O 及杂质(杂质不含铁、硫、
3 4 2 3
氧元素,且杂质不耗氧)。请回答下列问题:
(1)某硫铁矿石中(杂质不含铁、硫)含硫的质量分数是0.360,则该硫铁矿石中含铁的质量分数是:
_______(用小数表示,保留3位小数)。
(2)如用上述硫铁矿石制硫酸,矿渣经磁选获得精矿,直接用于高炉炼铁,当制得98%的硫酸1.92吨时(不
考虑硫的损失),则炼铁厂(不计选矿及炼铁时铁的损耗)最多可生产含碳4%的生铁_______吨。
(3)煅烧硫铁矿常用富氧空气。从沸腾炉排出的气体成分如下表。如果精矿中铁、氧的物质的量之比为
n(Fe)∶n(O)=5∶7,则富氧空气中O 和N 的体积比为_______。
2 2
气体 SO N O
2 2 2
物质的量
10 58 6
(mol)
(4)炼铁厂生产的生铁常用于炼钢。取某钢样粉末28.12 g(假设只含Fe和C),在氧气流中充分反应,得
到CO 气体224 mL(标准状况)。
2
①计算此钢样粉末中铁和碳的物质的量之比_______(最简单的整数比)。
②再取三份不同质量的钢样粉末分别加到100 mL相同浓度的HSO 溶液中,充分反应后,测得的实验数据
2 4
如下表所示:
实验序号 I II III
加入钢样粉末的质量/g 2.812 5.624 8.436
生成气体的体积/L(标准状况) 1.120 2.240 2.800
则该硫酸溶液的物质的量浓度_______。
③若在实验II中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少? (写出必要的步骤,答
案保留3位小数)_______。
【答案】(1)0.315
(2) 0.560
(3) 39:116(4) ① 50:1 ② 1.25mol/L ③ HSO 共0.125 mol,设再加入钢样的质量为x时酸反应完,则有:
2 4
5.624g+x= ,x = 1.406 g。
a.若加入的钢样粉末过量(m≥1.406 g),HSO 全反应,则:
2 4
m(余固体) = (5.624 g + m g)-0.125 mol×56 g·mol-1 = (m-1.376)g。
b.若加入的钢样粉末少量(m<1.406 g),Fe全溶解,则剩余固体全部为碳的质量。
即:m(余固体) = (5.624 g + m g)× =(5.624 g + m g)× 。
【解析】(1)利用化学式FeS,硫的质量分数是0.360,则该硫铁矿石中含铁的质量分数为
2
=0.315。答案为:0.315;
(2)由硫铁矿石的化学式FeS,可建立关系式FeS—2HSO —Fe,最多可生产含碳4%的生铁的质量为
2 2 2 4
=0.560t。答案为:0.560;
(3)由精矿中铁、氧的物质的量之比为n(Fe)∶n(O)=5∶7,可假设化学式Fe O,写出方程式:
5 7
10FeS+27O →2Fe O+20SO,则富氧空气中O 和N 的体积比为( mol+6mol):58mol=39:116。答案
2 2 5 7 2 2 2
为:39:116;
(4)①由CO 气体224 mL,n(CO)=0.01mol,可求出钢样中含C的质量为0.12g,从而求出Fe的质量为
2 2
28g,便可计算此钢样粉末中铁和碳的物质的量之比为 =50:1。答案为:50:1;
②由表中数据可知,第III次实验中,样品过量,硫酸完全反应,由H 的体积2.8L,可求出该硫酸溶液的
2
物质的量为 =0.125mol,c(H SO )= = 1.25mol/L。答案为:1.25mol/L;
2 4
③HSO 共0.125 mol,设再加入钢样的质量为x时酸反应完,则有:
2 4
5.624g+x= ,x = 1.406 g。
a.若加入的钢样粉末过量(m≥1.406 g),HSO 全反应,则:
2 4
m(余固体) = (5.624 g + m g)-0.125 mol×56 g·mol-1 = (m-1.376)g。
b.若加入的钢样粉末少量(m<1.406 g),Fe全溶解,则剩余固体全部为碳的质量。即:m(余固体) = (5.624 g + m g)× =(5.624 g + m g)× 。答案为:
钢样过量时,剩余固体质量为(m-1.376)g;钢样不足量时,剩余固体质量为(5.624 g + m g)× 。
6.(2020·全国高一课时练习)中学化学中几种常见物质的转化关系如下:
为常见金属单质,将 的浓溶液滴入氨水中可以得到红褐色沉淀 。请回答下列问题:
(1)写出物质 的化学式:________。
(2) 、 都可用于工业上冶炼金属铁,以 为原料冶炼铁的原理是______(用化学方程式表示),若有
参加反应,转移电子的物质的量是______;写出 的另一种用途:_______。
(3)写出下列过程的离子方程式。
________; _________。
(4)制造电路板工艺中,用 溶液刻蚀铜箔,用离子方程式表示该反应原理:_____。
(5)在 溶液中加入 ,恰好使 转化为 ,写出该反应的离子方程式:____。
【答案】(1)
(2) 制造红色油漆涂料
(3)
(4)
(5)
【解析】(1) 的浓溶液滴入氨水中可以得到红褐色沉淀,可知 为 ,从而可知 为 ,
为 , 为 , 过程中 元素的化合价由+2变为+3, 被氧化, 不稳定,加
热易分解,所以 为 。(2)工业上用 炼铁的化学方程式为 ,该反应中 元素的化合价从
降低到0,故 参加反应时转移电子的物质的量为 ;已知 为 ,
为红色粉末,可用于制造红色油漆涂料。
(3) 的反应为 与盐酸的反应,对应的离子方程式为 ; 反应的离
子方程式为 。
(4)制造电路板工艺中,用 溶液刻蚀铜箔发生的反应为 ,离子方程
式为 。
(5)在 溶液中加入 ,恰好使 转化为 沉淀,可以先考虑 与水反应生成
和 ,然后再考虑 与 发生复分解反应,化学方程式分别为①
、② ,由 可以得到
总化学方程式: ,其离子方程式为
。
【题组二 铁的化学性质】
1.(2020·北京丰台·高一学业考试)常温下,下列溶液可用铁质容器盛装的是
A.稀硝酸 B.稀硫酸 C.浓硝酸 D.浓盐酸
【答案】C
【解析】A. 稀硝酸可将铁溶解为硝酸盐溶液,因此不能用铁质容器盛装,A项错误;
B. 铁可以被稀硫酸溶解,反应生成硫酸亚铁溶液和氢气,因此不能用铁质容器盛装,B项错误;
C. 浓硝酸能使铁钝化,化学反应只发生在铁表面,但不是将铁溶解,因此能用铁质容器盛装,C项正确;
D. 浓盐酸可以将铁溶解为氯化亚铁溶液,因此不能用铁质容器盛装,D项错误;
答案选C。
2.(2019·邢台市第二中学高一月考)将铁片投入下列溶液,溶液质量增加,但无气体产生的是( )
A.AgNO B.Cu(NO ) C.稀HSO D.FeCl
3 3 2 2 4 3
【答案】D
【解析】A.Fe置换出Ag,溶液质量减小,故A错误;
B.Fe置换出Cu,溶液质量减小,故B错误;C.反应生成硫酸亚铁和氢气,溶液质量增加,但生成气体,故C错误;
D.反应生成氯化亚铁,无固体析出,溶液质量增加,且没有气体生成,故D正确;答案选D。
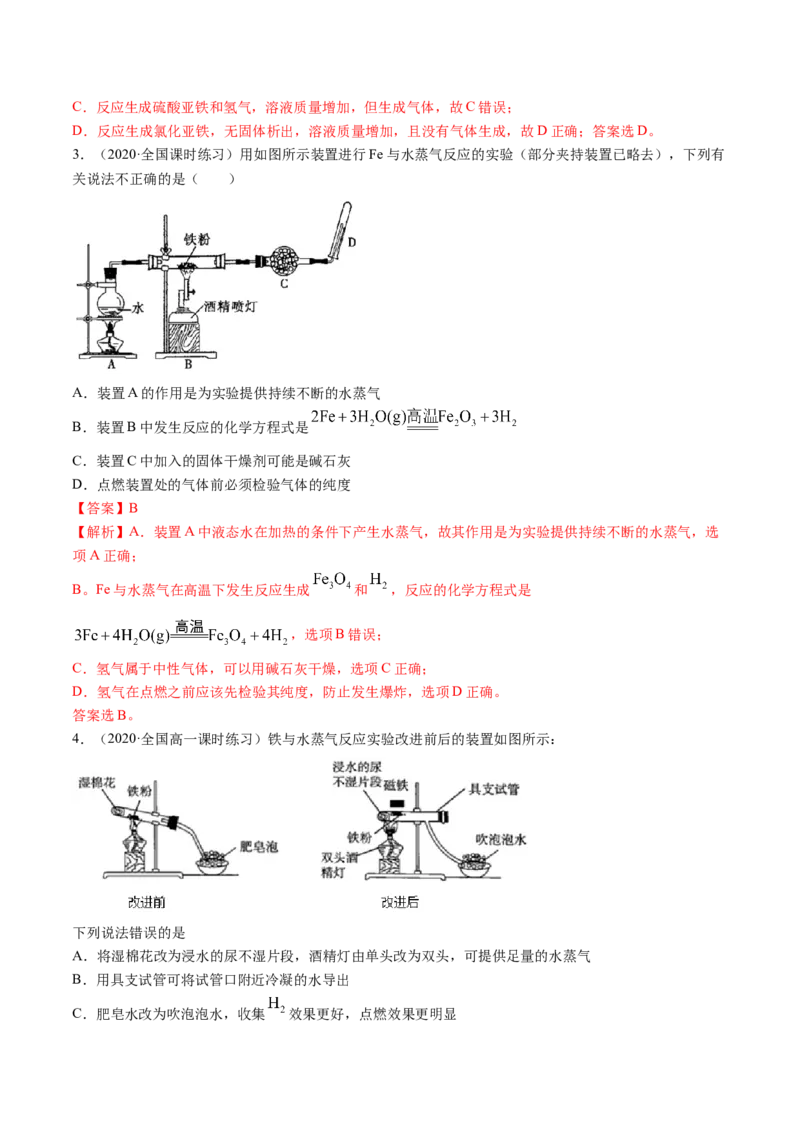
3.(2020·全国课时练习)用如图所示装置进行Fe与水蒸气反应的实验(部分夹持装置已略去),下列有
关说法不正确的是( )
A.装置A的作用是为实验提供持续不断的水蒸气
B.装置B中发生反应的化学方程式是
C.装置C中加入的固体干燥剂可能是碱石灰
D.点燃装置处的气体前必须检验气体的纯度
【答案】B
【解析】A.装置A中液态水在加热的条件下产生水蒸气,故其作用是为实验提供持续不断的水蒸气,选
项A正确;
B。Fe与水蒸气在高温下发生反应生成 和 ,反应的化学方程式是
,选项B错误;
C.氢气属于中性气体,可以用碱石灰干燥,选项C正确;
D.氢气在点燃之前应该先检验其纯度,防止发生爆炸,选项D正确。
答案选B。
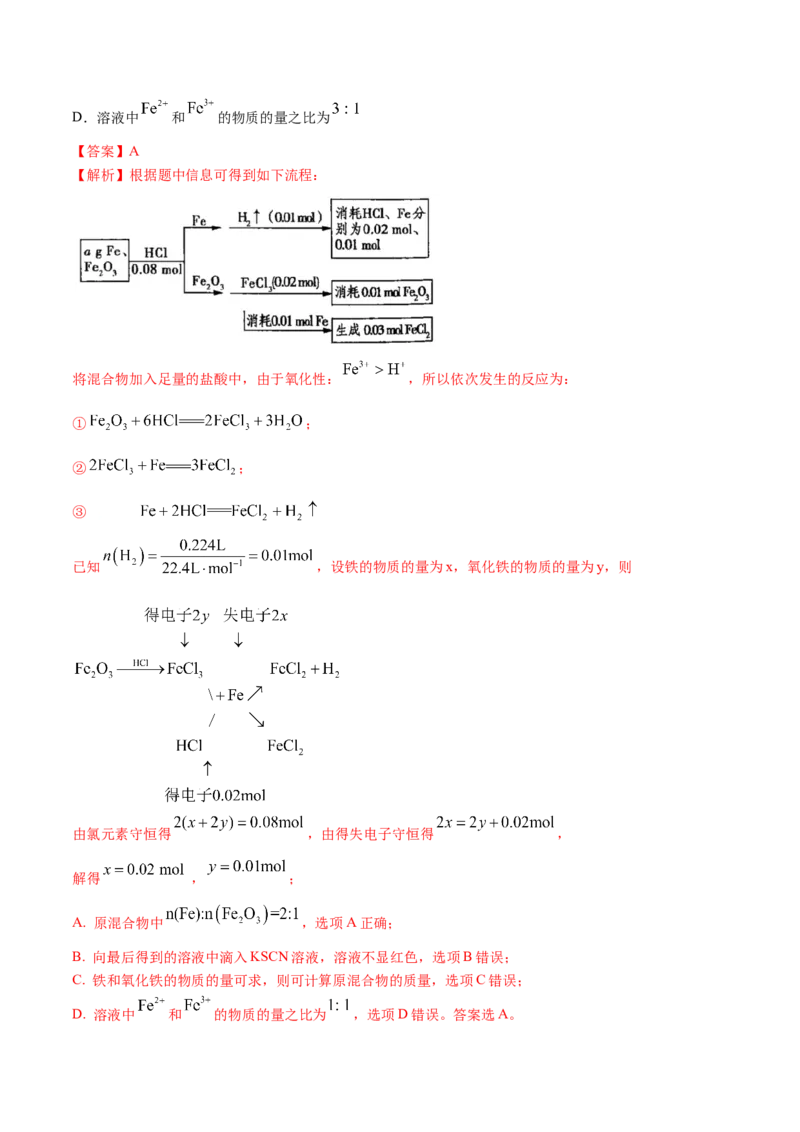
4.(2020·全国高一课时练习)铁与水蒸气反应实验改进前后的装置如图所示:
下列说法错误的是
A.将湿棉花改为浸水的尿不湿片段,酒精灯由单头改为双头,可提供足量的水蒸气
B.用具支试管可将试管口附近冷凝的水导出
C.肥皂水改为吹泡泡水,收集 效果更好,点燃效果更明显D.改进后,悬挂的磁铁能吸引铁粉,实验过程中,我们能看到具支试管中有黑色固体不断落下
【答案】D
【解析】A. 尿不湿可吸附更多的水,且不易洒出,酒精灯改为双头可增加受热面积及尿不湿的加热温度,
从而提供足够的水蒸气,A项正确;
B. 具支试管的结构中含支管,冷凝的水可从支管中流出,B项正确;
C. 泡泡水易于起泡,收集气体更容易,点燃效果更好,C项正确;
D. 磁铁可以吸引单质铁和 ,D项错误。答案选D。
5.(2020·内蒙古通辽实验中学高一期末)已知在温度低于570 ℃时,还原铁粉与水蒸气反应的产物是
FeO,高于570 ℃时,生成Fe O。老师用上图所示实验装置,完成了还原铁粉与水蒸气反应的演示实验。
3 4
甲同学为探究实验后试管内的固体含有哪些物质,进行了下列实验:
实验编号 实验操作 实验现象
黑色粉末逐渐溶解,溶液呈浅绿色;有少量气
① 取少量黑色粉末放入试管中,加入盐酸,微热
泡产生
② 向试管中滴加几滴KSCN溶液,振荡 溶液没有出现血红色
根据上述实验,下列说法不正确的是
A.试管内的固体一定含有铁粉
B.试管内的固体一定不含有Fe O
3 4
C.不能确定试管内的固体一定含有FeO
D.可通过将试管内固体彻底还原,分析其质量减小的方法来确定是否含有Fe O
3 4
【答案】B
【解析】A. 加入盐酸,黑色粉末溶解且有少量气泡产生,说明黑色粉末中含有铁粉,故A正确;
B. 铁粉能把三价铁离子还原成二价铁离子,故不能确定黑色粉末是否含有Fe O,故B错误;
3 4
C. 铁粉能把三价铁离子还原成二价铁离子,不能确定试管内的固体一定含有FeO,故C正确;
D. 若含有Fe O,通过将试管内固体彻底还原为氧化亚铁,则固体质量减小,故D正确;故选B。
3 4
6.(2020·元氏县第四中学高一期末)在常温下,Fe与水并不发生反应,但在高温下,Fe与水蒸气可以发
生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,即可以
完成高温下Fe与水蒸气的反应实验,请回答下列问题:(1)写出反应的化学方程式____。
(2)圆底烧瓶中盛装的是水,该装置受热后的主要作用是___。
(3)酒精灯和酒精喷灯点燃的顺序是先点燃___,理由是___。
(4)试管收集到的气体是__,如果要在A处点燃气体,则必须对该气体进行__。
【答案】(1)3Fe+4H O(g) Fe O+4H
2 3 4 2
(2)提供水蒸气
(3)酒精灯 产生的水蒸气赶走管内的空气,防止铁与氧气反应
(4) H 验纯
2
【解析】(1)铁与水蒸气发生氧化还原反应,生成四氧化三铁和氢气,反应的化学方程式为3Fe+4H O
2
Fe O+4H ;答案为3Fe+4H O Fe O+4H 。
3 4 2 2 3 4 2
(2)反应物为水蒸气与铁,水受热形成水蒸气,所以加热圆底烧瓶的目的就是提供水蒸气;答案为提供
水蒸气。
(3)点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防止铁与空气中的
氧气在加热的条件下反应,应该先点燃酒精灯,排掉硬质玻璃管内空气,然后再点燃酒精喷灯;答案为酒
精灯;产生的水蒸气赶走管内的空气,防止铁与氧气反应。
(4)铁与水蒸气发生氧化还原反应生成H,点燃氢气前一定要检验纯度,防止发生爆炸;答案为H,验
2 2
纯。
【题组三 铁与酸反应】
1.(2020·和林格尔县第一中学高一开学考试)等量的铁粉分别与足量的盐酸、水蒸气在一定的条件下充
分反应,则在相同的条件下,产生氢气的物质的量之比是( )
A.1:1 B.3:4 C.2:3 D.4:3
【答案】B
【解析】令Fe的物质的量为1mol,则:
Fe+2HCl=FeCl +H ↑
2 2
1mol 1mol
3Fe+4H O(g) Fe O+4H
2 3 4 21mol mol,
相同条件下体积之比等于物质的量之比,则两反应中生成氢气体积之比为1mol: mol =3:4。
答案选B。
2.(2019·全国高一课时练习)两种金属混合粉末15g,与足量的盐酸反应时生成11.2L H (标况下),符
2
合上述情况的金属混合物是( )
A.Mg、Fe B.Zn、Ag C.Fe、Zn D.Mg、Al
【答案】A
【解析】11.2L氢气的物质的量为:n= =0.5mol,假设金属都为+2价,则金属混合物的平均摩
尔质量为: =30g/mol,A.Mg的相对原子质量为24,Fe的相对原子质量为56,平均摩尔质量可
能为30g/mol,选项A正确;B.Zn的相对分子质量为65,Ag与盐酸不反应,生成0.5mol氢气所以Zn的
质量为0.5mol×65g/mol=32.5g,大于15g,不符合题意,故B错误;C.Zn的相对分子质量为65,Fe的相
对原子质量为56,平均摩尔质量大于30g/mol,选项C错误;D.Mg的相对原子质量为24,当Al的化合
价为+2价时,可看成其相对原子质量为: ×2=18g/mol,镁和铝的摩尔质量都小于30g/mol,故
D错误;答案选A。
3.(2020·全国课时练习)向=50 mL稀HSO 与稀HNO 的混合溶液中逐渐加入铁粉,假设加入铁粉的质
2 4 3
量与产生气体的体积(标准状况)之间的关系如图所示,假设C点之前每一段只对应一个反应。下列说法正
确的是( )
A.参加反应铁粉的总质量m=5.6 g
2
B.所用混合溶液中c(HNO )=0.5 mol/L
3
C.开始时产生的气体为H
2
D.AB段发生的反应为置换反应
【答案】A
【解析】A.最终生成Fe2+,根据氧化还原反应中得失电子数目相等可知3×n(NO)+2×n(H )=2n(Fe),即3×
2+2× =2n(Fe),n(Fe)=0.1mol,其质量为0.1 mol×56 g/mol=5.6 g,A正确;
B. n(NO)= =0.05mol,则所用混合溶液中c(HNO)= =1mol/L,B错误;
3
C. 反应开始时产生的气体为NO,C错误;
D. AB段发生:Fe+2Fe3+=3Fe2+,该反应为化合反应,D错误;
故合理选项是A。
4.(2020·四川高一期末)在1 L浓度为0.2 mol·L-1 Fe(NO ) 和1.5 mol·L-1 HSO 组成的混合溶液中,加入
3 3 2 4
39.2 g铁粉使其充分反应。下列有关说法正确的是
A.反应后产生标准状况下的氢气11.2 L
B.反应后的溶液中c(Fe2+)∶c(Fe3+)=2∶1
C.反应后的溶液还可以溶解16.8 g铁粉
D.反应后的溶液还可以溶解19.2g铜
【答案】D
【解析】A.分析可知,反应后不产生氢气,A错误;
B.分析可知,生成0.3molFe2+,剩余的Fe3+为0.6mol,溶液中c(Fe2+)∶c(Fe3+)=0.3∶0.6=1:2,B错误;
C.反应后的溶液,含有0.6mol Fe3+,0.6molH+还可以溶解0.6mol铁粉即33.6g,C错误;
D.反应后的溶液含有0.6molFe3+,还可以溶解0.3molCu,即19.2g,D正确;答案为D;
5.(2020·江苏广陵·扬州中学高一期中)某稀溶液中含有4molKNO 和2.5molHSO ,向其中加入
3 2 4
1.5molFe,充分反应(已知NO -被还原为NO)。下列说法正确的是( )
3
A.反应后生成NO的体积为28L
B.所得溶液中c(Fe2+):c(Fe3+)=1:1
C.所得溶液中c(NO -)=2.75mol/L
3
D.所得溶液中的溶质只有FeSO
4
【答案】B
【解析】A.分析可知,反应后生成NO的物质的量为1.25mol,标况下的体积为28L,但题目未说明是否为
标准状况,故A错误;
B.所得溶液中c(Fe2+):c(Fe3+)=0.75mol:0.75mol=1:1,故B正确;
C.未给定溶液体积,无法计算所得溶液中c(NO -),故C错误;
3
D.所得溶液中含有Fe2+、Fe3+、SO 2-、NO -,故D错误;答案为B。
4 3
【题组四 铁的氧化物】
1.(2020·全国课时练习)将ag铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加
反应的HCl的物质的量为 ,放出气体 (标准状况)。则下列判断正确的是( )
A.原混合物中
B.向最后得到的溶液中滴入KSCN溶液,溶液显红色
C.无法计算原混合物的质量D.溶液中 和 的物质的量之比为
【答案】A
【解析】根据题中信息可得到如下流程:
将混合物加入足量的盐酸中,由于氧化性: ,所以依次发生的反应为:
① ;
② ;
③
已知 ,设铁的物质的量为x,氧化铁的物质的量为y,则
由氯元素守恒得 ,由得失电子守恒得 ,
解得 , ;
A. 原混合物中 ,选项A正确;
B. 向最后得到的溶液中滴入KSCN溶液,溶液不显红色,选项B错误;
C. 铁和氧化铁的物质的量可求,则可计算原混合物的质量,选项C错误;
D. 溶液中 和 的物质的量之比为 ,选项D错误。答案选A。2.(2020·全国课时练习)现有CuO和Fe O 组成的混合物a g,向其中加入2mol/L的硫酸溶液50mL,恰
2 3
好完全反应。若将a g该混合物在足量H 中加热,使其充分反应,冷却后剩余固体质量为
2
A.1.6a g B.(a-1.6)g C.(a-3.2)g D.1.6g
【答案】B
【解析】CuO和Fe O 的混合物与硫酸反应生成硫酸盐和水,由电荷守恒,可知ag混合物中含有的O原子
2 3
的物质的量n(O)=n(SO 2-)=0.05 L×2mol/L=0.1mol,则ag混合物中氧元素的质量
4
为m(O)=0.1mol×16g/mol=1.6g,若用足量H 还原a g混合物,反应剩余固体为Cu、Fe,则金属质量为两种
2
金属氧化物的质量减去氧元素的质量,即金属质量为:m(金属)=ag-1.6g=(a-1.6)g,故合理选项是B。
3.(2020·福建厦门·高一月考)在由Fe、FeO和Fe O 组成的混合物中加入100mL2 mol•L-1的盐酸,恰好
2 3
使混合物完全溶解,并放出448mL气体(标准状况),此时溶液中无Fe3+,则下列判断正确的是
A.混合物里3种物质反应时消耗盐酸的物质的量浓度之比为1:1:3
B.反应后所得溶液中的Fe2+离子与Cl-离子的物质的量之比为2:1
C.混合物里,FeO的物质的量无法确定,但Fe比Fe O 的物质的量多
2 3
D.混合物里,Fe O 的物质的量无法确定,但Fe比FeO的物质的量多
2 3
【答案】C
【解析】混合物恰好完全溶解,且无Fe3+,故溶液中溶质为FeCl ,n(HCl)=0.2mol,n(H )=0.02mol,
2 2
n(Fe2+)=0.1mol,由反应2Fe3++Fe═3Fe2+知Fe比Fe O 的物质的量多,但FeO的物质的量无法确定;
2 3
A.根据以上分析知Fe比Fe O 的物质的量多,但FeO的物质的量无法确定,故无法确定混合物里三种物
2 3
质反应时消耗盐酸的物质的量的浓度,故A错误;B.反应后所得溶液为FeCl 溶液,阳离子与阴离子的物
2
质的量之比为1:2,故B错误;C.混合物恰好完全溶解,且无Fe3+,故溶液中溶质为FeCl ,由铁与酸反
2
应生成氢气及反应2Fe3++Fe═3Fe2+知Fe比Fe O 的物质的量多,但FeO的物质的量无法确定,故C正确;
2 3
D.FeO的物质的量无法确定,不能确定Fe与FeO的物质的量的关系,故D错误;故选C。
4.(2020·四川广元·高一期末)有一粉末,它是由铁的氧化物物中的一种或两种组成,取3.04 g粉末加热,
同时通入足量的CO使之完全反应,再用澄清石灰水把产生的气体充分吸收,产生沉淀5g,则该粉末的组
成可能是
A.只有Fe O B.只有FeO
2 3
C.等物质的量的FeO和Fe O D.等物质的量的Fe O 和Fe O
3 4 2 3 3 4
【答案】C
【解析】用澄清石灰水把产生的气体充分吸收,产生沉淀5g,则生成的CO 的物质的量为:n(CO)="n(Ca"
2 2
CO)=5g÷100g/mol=0.05mol,设铁的氧化物化学式为Fe O,设铁的氧化物物质的量为n,则有:
3 x y
Fe O+ yCO = xFe + yCO
x y 2
1 y
n 0.05 得n=0.05/y 3.04/ (56x+16y)=0.05/y ,x/y=4/5,所以Fe和O的原子个数比为
4:5,选C。
5.(2020·安徽)向一定量的Fe、FeO和Fe O 的混合物中加入4 mol/L的稀硝酸250 mL时,混合物恰好
2 3
完全溶解并放出3.36 L NO气体(标准状况)。若用足量CO在加热下还原相同质量的该混合物,则反应掉的
CO物质的量为( )
A.0.1 mol B.0.15 mol C.0.16 mol D.0.2 mol
【答案】D【解析】根据元素守恒,该反应可表示为:FeO+HNO →Fe(NO )+NO+HO,混合物中的O等于HO中的
x y 3 3 z 2 2
O减去HNO 变为NO时损失的O;后一反应可表示为:FeO+CO→Fe +CO ,反应掉的CO就等于混合物
3 x y 2
中的O;根据H元素守恒可知,HO中的O:n(HNO)÷2 =0.5mol,HNO 变为NO时损失的O:n
2 3 3
(NO)×2=0.15×2=0.3mol,所以反应的CO:0.5-0.3=0.2mol,故答案为:D。
6.(2020·全国课时练习)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过
实验来探究一红色粉末是Fe O、Cu O或二者混合物。探究过程如下:
2 3 2
查阅资料:Cu O是一种碱性氧化物, 溶于稀硫酸生成Cu和CuSO , 在空气中加热生成CuO
2 4
提出假设: 假设1:红色粉末是Fe O 假设2:红色粉末是Cu O
2 3 2
假设3:红色粉末是Fe O 和Cu O的混合物
2 3 2
设计探究实验: 取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN试剂。
(1)若假设1成立,则实验现象是_______________。
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理
吗?__________简述你的理由(不需写出反应的方程式)____________。
(3)若固体粉末完全溶解无固体存在,滴加KSCN 试剂时溶液不变红色,则证明原固体粉末是__________,
写出发生反应的离子方程式______、__________、______________。
探究延伸:
(4)如果经实验分析,确定红色粉末为Fe O 和Cu O的混合物。某实验小组欲用加热法测定Cu O的质量分
2 3 2 2
数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b > a),则混合物中Cu O的质
2
量分数为__________。
【答案】(1)溶液变为血红色
(2) 不合理 Cu能将Fe3+还原为Fe2+
(3) Fe O 和Cu O的混合物 Fe O+6H+ = 2Fe3++3H O
2 3 2 2 3 2
Cu O+2H+ =Cu + Cu2+ + H O 2 Fe3+ + Cu =2Fe2+ + Cu2+
2 2
(4)
【解析】(1)若假设1成立,金属氧化物Fe O 与稀硫酸反应:Fe O+3H SO =Fe (SO )+3H ↑,反应产生的
2 3 2 3 2 4 2 4 3 2
Fe (SO ) 与KSCN溶液反应:Fe (SO )+6KSCN=3K SO +2Fe(SCN) ,因此看到的现象是固体溶解,溶液变
2 4 3 2 4 3 2 4 3
为血红色;
(2)Fe O 与稀硫酸反应:Fe O+3H SO =Fe (SO )+3H ↑,由资料知Cu O溶于稀硫酸生成Cu和CuSO ,
2 3 2 3 2 4 2 4 3 2 2 4
Cu O+HSO =CuSO+Cu+H O,铜为红色固体不溶水,Cu与第一个反应产生的Fe (SO ) 发生反应:
2 2 4 4 2 2 4 3
Fe (SO )+Cu=2FeSO +CuSO,也会导致溶液中无Fe3+存在,溶液中无Fe3+所以滴加KSCN试剂也不变红,
2 4 3 4 4
因此不能根据滴加 KSCN 试剂后溶液不变红色,就判断证明原固体粉末中一定不含Fe O;
2 3
(3)因为Cu O溶于硫酸生成Cu和CuSO ,而HSO 不能溶解Cu,所以混合物中必须有Fe O 存在,使其生
2 4 2 4 2 3
成的Fe3+溶解产生的Cu,若固体全部溶解,则一定存在Fe O 和Cu O,涉及的反应有Fe O+6H+=2Fe3+
2 3 2 2 3
+3H O、Cu O+2H+=Cu+Cu2++H O、2Fe3++Cu=2Fe2++Cu2+;
2 2 2
(4)依据题意,固体粉末在空气中充分加热时能发生反应的物质为Cu O,最后变成CuO,增加的质量就是
2
反应的氧气的质量,根据质量差计算可以得出Cu2O的质量分数.
设样品中氧化亚铜的质量为m,2Cu O+O 4CuO 固体增加质量△m
2 2
288g 32g
m (b-a)g
m= =9(b-a)g,则混合物中Cu O的质量分数为 ×100%= ×100%。
2
【题组五 铁的氢氧化物】
1.(2020·古浪县第二中学竞赛)下列物质受热不易分解的氢氧化物是( )
A.Al(OH) B.NaOH
3
C.Mg(OH) D.Fe(OH)
2 3
【答案】B
【解析】Al(OH) 、Mg(OH) 、Fe(OH) 三种均为难溶性碱,受热易分解为相应的氧化物,NaOH为易溶性
3 2 3
碱,受热不易分解,故选B。
2.(2019·全国高一课时练习)将Fe(OH) 露置在空气中加热灼烧所得的产物为( )
2
A.FeO B.Fe O C.Fe O D.Fe(OH)
2 3 3 4 3
【答案】B
【解析】因Fe(OH) 极易被空气中的氧气氧化,当露置于空气中时,Fe(OH) 首先转化为Fe(OH) ,然后
2 2 3
Fe(OH) 分解生成Fe O 和HO。故答案选B。
3 2 3 2
3.(2020·洮南市第一中学月考)现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,
它们之间的相互转化关系如图所示 图中有些反应的生成物和反应的条件没有标出 。
请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B_______,丙__________。
(2)写出黄绿色气体乙的一种用途___________,反应过程⑦可能观察到的实验现象是______。对应的化学
方程式是_______。
(3)反应③中的离子方程式是_________。
(4)向G溶液中加入氢硫酸的离子方程式是_________。
【答案】(1)Al HCl
(2) 杀菌消毒、制漂白粉、强氧化剂 白色沉淀迅速变为灰绿色,最终变为红褐色
FeCl +2NaOH=Fe(OH) ↓+2NaCl、4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 2 2 3
(3) 2Al+2 +2H O=2 +3H ↑
2 2(4) 2 +H S=2 +S↓+2
2
【解析】(1)根据上述分析可知,物质B是Al,丙是HCl;
(2)黄绿色气体乙是Cl,该物质可以与水反应产生HCl和HClO,HClO具有强氧化性,可作氧化剂,氧化
2
一些具有还原性的物质,也用于杀菌消毒或用于物质的漂白;F是FeCl ,D是NaOH,反应过程⑦是FeCl
2 2
与NaOH溶液发生反应:FeCl +2NaOH=Fe(OH) ↓+2NaCl,Fe(OH) 不稳定,容易被溶解在溶液中的氧气氧
2 2 2
化,发生反应:4Fe(OH) +O +2H O=4Fe(OH) ,可观察到的实验现象是白色沉淀迅速变成灰绿色,最终变
2 2 2 3
成红褐色;
(3)反应③是Al与NaOH溶液发生反应产生NaAlO 和H,反应的离子方程式为:2Al+2 +2H O=2
2 2 2
+3H ↑;
2
(4)G是FeCl ,具有氧化性,硫化氢具有还原性,向G溶液中加入氢硫酸,发生氧化还原反应,铁离子被
3
还原成亚铁离子,硫化氢被氧化成硫单质,反应的离子方程式是2 +H S=2 +S↓+2 。
2
4.(2020·四川省宜宾市第四中学校高一期中)已知A是一种常见金属,F是一种红褐色沉淀。试根据图
中转化关系,回答下列问题。
(1)写出A、C、F、G的化学式:A________,C_________,F_________,G_________。
(2)检验D中阳离子的方法_____________________________________________。
(3)保存C溶液时为什么要加固体A_____________________________________。
(4)写出下列转化的离子方程式C→D:____________________________________,由E转化为F的现象
是_________________________________。
【答案】(1)Fe FeCl Fe(OH) Fe O
2 3 2 3
(2) 取D溶液少许于试管中,加入几滴KSCN溶液,溶液变红色,证明含Fe3+
(3) 防止Fe2+被O 氧化
2
(4) 2Fe2++Cl===2Fe3++2Cl- 白色沉淀迅速变为灰绿,最后变为红褐色
2
【解析】红褐色沉淀F是Fe(OH) ,由元素守恒可知,A为Fe,C为FeCl ,E为Fe(OH) ,G为氧化铁。
3 2 2
(1)A为Fe,C为FeCl ,F为Fe(OH) ,G为Fe O。(2)检验D中Fe3+的方法是取D溶液少许于试管中,
2 3 2 3
加入几滴KSCN溶液,溶液变红色,证明含Fe3+;(4)C→D的离子方程式为:2Fe2++Cl===2Fe3++2Cl
2
-;Fe(OH) 转化为Fe(OH) 的现象是白色沉淀迅速变为灰绿,最后变为红褐色。
2 3
【题组六 铁氢氧化物的制备】
1.(2020·西安市第八十五中学期末)实验室用FeCl 和烧碱制备Fe(OH),为了生成的产物不容易被氧
2 2
化,下列说法不正确的是
A.配制FeCl 和烧碱溶液所用的蒸馏水通常要煮沸
2B.可在FeCl 溶液的上面加一层苯,以隔绝空气
2
C.向FeCl 溶液中滴加烧碱溶液时,胶头滴管尖嘴不能伸入到试管内
2
D.产生Fe(OH) 沉淀后,不能震荡试管
2
【答案】C
【解析】A.FeCl 和烧碱溶液要现用现配,且配制溶液的蒸馏水要煮沸以除去氧气,确保Fe(OH) 的生成
2 2
在无氧的环境里,故A正确;
B.在FeCl 溶液的上面加一层苯或一层油,以隔绝空气防止氧气溶入,故B正确;
2
C.向FeCl 溶液中滴加烧碱溶液时,要将胶头滴管的尖嘴伸入到FeCl 溶液中,防止氢氧化钠溶液在滴入时
2 2
接触空气溶有氧气,故C错误;
D.产生Fe(OH) 沉淀后,若震荡试管,会增大沉淀与空气的接触的机会,使沉淀更易被氧化,故D正确。
2
2(2020·全国课时练习)用下面两种方法可以制得白色的 沉淀。
Ⅰ.方法一:用 溶液与不含 的蒸馏水配制的NaOH溶液反应制备 。
(1)除去蒸馏水中溶解的 常采用的________方法。
(2)生成白色 沉淀的操作是用长胶头滴管吸取不含 的NaOH溶液,插入 溶液液面下,
再挤出NaOH溶液。这样操作的理由是________________。
Ⅱ.方法二:在如图所示装置中,用不含 的NaOH溶液、铁屑、稀 制备 。
(1)在试管A中加入的试剂是________________。
(2)在试管B中加入的试剂是________________。
(3)为了制得白色 沉淀,在试管A和B中加入试剂,塞紧塞子,打开止水夹后的实验步骤是
________________。
(4)这样生成的 沉淀能较长时间保持白色,其理由是________________。
【答案】I(1)煮沸 (2)避免生成的 沉淀接触
II(1)铁屑、稀 (2) 不含 的NaOH溶液
(3) 检验试管B出口处氢气的纯度,当排出的 纯净时,再关闭止水夹(4) 两试管中充满 且外界空气不易进入,可防止 被氧化
【解析】除去或隔绝氧气的措施:煮沸:加热煮沸以除去溶解在水中的氧气;排气:利用其他气体排尽装
置中的氧气;覆盖:在液面上覆盖一层苯或煤油等,隔绝氧气。
Ⅰ.(1)常采用煮沸的方法除去蒸馏水中的 ;
(2)因为 在空气中易被 氧化为 ,所以在制备 时,若向 溶液中直接
滴加NaOH溶液,会带入空气使制取的 被氧化;若将盛有NaOH溶液的长胶头滴管插入
溶液液面下,再挤出NaOH溶液,可以防止滴加NaOH溶液时带入空气,避免生成的 接触 ;
Ⅱ.(1)在试管A中加入的试剂是铁屑、稀 ;
(2)在试管B中加入的试剂是不含 的NaOH溶液;
(3)为了制得白色 沉淀,在试管A和B中加入试剂,塞紧塞子,打开止水夹后的实验步骤是检
验试管B出口处氢气的纯度,当排出的 纯净时,再关闭止水夹;
(4)制备 时利用Fe与 反应产生的 排尽装置中的空气,收集氢气验纯后,关闭止水夹,
试管A中产生 ,压强增大,将A中溶液压入B中与NaOH溶液反应制备 , 沉淀在
的氛围中不易被氧化,能较长时间保持白色。
3.(2020·湖南开福·长沙市第七中学高一开学考试)小熊同学在学习酸碱盐有关知识时,对一些沉淀物质
的颜色产生了兴趣。老师告诉他氢氧化铜是蓝色,氢氧化铁是红褐色,让他探究氢氧化亚铁的颜色。下面
请你和他一起探究。
(查阅资料)
(1)铁有两种氢氧化物,它们可以分别由相对应的可溶性盐与碱溶液反应而制得。
(2)氢氧化亚铁在空气中立即被氧气氧化。
(3)硫酸铜溶液是蓝色,硫酸亚铁溶液是浅绿色。
(提出猜想)氢氧化亚铁是浅绿色。
(实验过程)在2支试管里分别加入少量FeCl 和FeSO 溶液,然后滴入NaOH溶液,观察现象,请补充完
3 4
成下表:
FeCl 溶液 FeSO 溶液
3 4滴入NaOH溶液 先生成魄絮状沉淀,慢慢变化,最后变成红褐色沉
生成红褐色沉淀
的现象 淀
①_____ __, FeSO +2NaOH=Fe(OH) ↓+NaSO ;4Fe(OH) +O
化学方程式 4 2 2 4 2 2
基本反应类型属于②_____反应 +2HO=③_______(完成并配平此方程式)
2
(学习交流)
(1)氢氧化亚铁是白色而不是浅绿色。
(2)小熊联系到CO 与C的化合反应,认为FeCl 溶液可以转化为FeCl 溶液,请模仿写出这个转化的化学方
2 3 2
程式:④_______。
【答案】①FeCl +3NaOH=Fe(OH) ↓+3NaCl ②复分解反应 ③ 4Fe(OH) +O +2H O=4Fe(OH)
3 3 2 2 2 3
④2FeCl +Fe=3FeCl
3 2
【解析】(1) FeCl 溶液和NaOH溶液反应的方程式:FeCl +3NaOH=Fe(OH) ↓+3NaCl,此反应属于复分解反
3 3 3
应;
(2) FeSO 溶液中滴入NaOH溶液,生成白色絮状沉淀是氢氧化亚铁沉淀,白色氢氧化亚铁在水中不稳定,
4
容易跟水中的氧气反应生成红棕色的氢氧化铁;由于氢氧化亚铁有少量溶于水中,亚铁离子显绿色,所以
溶液呈绿色,同时也会转化成黄色的铁离子,灰色就是白色、红棕、绿色、黄色的混合色;在加上这种转
化是有时间过程的,所以随着各种离子含量变化,颜色变化就由此而来了;最后变成红褐色沉淀是氢氧化
铁沉淀,根据质量守恒定律完成并配平反应的方程式,4Fe(OH) +O +2H O=4Fe(OH) ;
2 2 2 3
(3)根据CO 与C的反应,要让FeCl 溶液可以转化为FeCl 溶液,小熊的理由是:单质铁也可以将FeCl
2 3 2 3
还原成FeCl ,化学方程式是2FeCl +Fe=3FeCl 。
2 3 2
【题组七 Fe2+和Fe3+检验】
1.(2020·全国高一课时练习)向 和 的混合物中加入 足量的稀硫酸,在标准状况
下收集到 ,向反应后的溶液中滴加 溶液不变红。为中和过量的 ,并使 元素全
部转化为 沉淀,恰好消耗了 的 溶液,则该稀 的物质的量浓度
为
A. B. C. D.
【答案】B
【解析】Fe和Fe O 的混合物与足量稀HSO 反应,Fe和Fe O 均无剩余,且有H 生成,向反应后的溶液
2 3 2 4 2 3 2
中滴加KSCN溶液不变红,说明反应生成FeSO ;为了中和过量的硫酸,而且FeSO 使完全转化成
4 4
Fe(OH)2,共消耗 的 溶液 ,说明反应后的溶液中溶质只有NaSO ,根据硫元素
2 4守恒,则 ,根据钠元素守恒,则 ,则有
,故该稀硫酸的物质的量浓
度 ,B正确,故答案为:B。
2.(2020·全国课时练习)证明某溶液中含有 而不含有 的实验方法是( )
①先滴加氯水,再滴加KSCN溶液,溶液显红色
②先滴加KSCN溶液,溶液不显红色,再滴加氯水,溶液显红色
③滴加 溶液,先产生白色絮状沉淀,后沉淀迅速变成灰绿色,最后变成红褐色
④滴加KSCN溶液,溶液不显红色
A.①② B.②③ C.③④ D.①④
【答案】B
【解析】①先滴加氯水,再滴加KSCN溶液,溶液显红色,只能证明加氯水后的溶液中含有 ,无法确
定加氯水前的溶液中是否含有 、 ,①不正确;
②先滴加KSCN溶液,溶液不显红色,证明不含 ,再滴加氯水,溶液显红色,证明滴加氯水前的溶液
中含有 ,②正确;
③滴加NaOH溶液,先产生白色絮状沉淀,后沉淀迅速变成灰绿色,最后变成红褐色,能证明原溶液中含
有 而不含有 ,③正确;
④滴加KSCN溶液,溶液不显红色,只能证明原溶液中不含有 ,不能证明含有 ,④不正确。
故选B。
3.(2020·全国课时练习)下列除去括号中的杂质的方法不正确的是( )
A.FeCl 溶液(FeCl ):通入适量Cl
3 2 2
B.CO(HCl气体):通过饱和NaHCO 溶液后干燥
2 3
C.FeCl 溶液(FeCl ):加过量铜粉后过滤
2 3
D.Cl(HCl气体):通过饱和NaCl溶液后干燥
2
【答案】C
【解析】A.氯气可以和氯化亚铁反应生成氯化铁,不会引入新的杂质,A正确;
B.HCl可以和NaHCO 反应生成CO,CO 不和饱和碳酸氢钠反应,B正确;
3 2 2C.铜和氯化铁反应生成氯化亚铁和氯化铜,引入了新的杂质,C错误;
D.HCl气体可以溶解在饱和NaCl溶液中,且饱和NaCl溶液中含有较高浓度的Cl-,可以降低Cl 的溶解
2
度,D正确;故选C。
4.(2020·福建省福州第一中学高二月考)下列除去杂质的方法错误的是( )
物质 杂质 试剂 主要操作
A FeCl 溶液 CuCl Fe(足量) 过滤
2 2
B Cl HCl 饱和食盐水+浓硫酸 洗气
2
C Fe Fe O 稀盐酸(足量) 过滤
2 3
D NaCO 固体 NaHCO 无 加热
2 3 3
【答案】C
【解析】A. 与Fe反应,生成 和Cu,过滤可以除去Cu和多余的Fe,A正确;
B. 难溶于饱和食盐水,HCl极易溶于水,然后用浓硫酸干燥除去水蒸气,可以通过洗气法除去氯气中
的HCl,B正确;
C.Fe和 都能溶于盐酸,不能用盐酸除去Fe中的 ,C错误;
D. 受热分解生成碳酸钠和水和二氧化碳,除去碳酸钠中的碳酸氢钠可以用加热的方法,D正确;
答案选C。
5.(2020·全国高二开学考试)金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)下列物质中不属于合金的是_______。
A.钢 B.青铜 C.黄铜 D.水银
(2)在钠、铝、铁三种金属元素中,所形成的氧化物中适宜做耐火材料的是_______ ,向盛有硫酸铝溶液的
试管中滴加足量氨水,反应的离子方程式是_____________。
(3)乙同学为了获得持久白色的Fe (OH) 沉淀,准备用右图所示装置,用不含O 的蒸馏水配制的NaOH溶
2 2
液与新制的FeSO 溶液反应。获得不含O 的蒸馏水的方法是_______。反应开始时,打开止水夹;一段时
4 2
间后,关闭止水夹,在试管_______(填“A”或“B”) 中观察到白色的Fe(OH) 。
2(4)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出
现的是____________。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(5)电子工业常用30%的FeCl 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。请写出FeCl 溶液与铜反应
3 3
的离子方程式:__________;
(6)某研究性学习小组内测定FeCl 腐蚀铜后所得溶液的组成,进行了如下实验:①取少量待测溶液,滴入
3
KSCN溶液呈红色,该现象说明该溶液中含有的离子是_______; ②验证该溶液中含有Fe2+,正确的实验
方法是_______;A.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+;B.取适量溶液,滴
入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+;C.观察溶液是否呈浅绿色
【答案】(1)D
(2)Al O Al3++3NH·H O=3NH ++Al(OH) ↓
2 3 3 2 4 3
(3)加热煮沸 B
(4) B
(5)2Fe3++Cu=Cu2++2Fe2+
(6)Fe3+ A
【解析】(1)A.钢是铁与碳元素的合金,A错误;B.青铜是铜和锡的合金,B错误;C.黄铜是铜和锌的
合金,C错误;D.水银为汞单质,不是混合物,不属于合金,D正确;答案选D;
(2)适合作耐火材料的氧化物必须具有高熔点,氧化铝的熔点较高,所以氧化铝可以作耐火材料;铝离子和
氨水反应生成氢氧化铝沉淀和铵根,离子反应方程式为Al3++3NH·H O=3NH ++Al(OH) ↓;
3 2 4 3
(3)获得不含O 的蒸馏水的方法是煮沸,简单易操作;反应开始时,要打开止水夹,利用铁粉和稀硫酸反
2
应产生的氢气排出试管A、B中的空气,使整个装置不含氧气。在对B试管的出气管排出的氢气验纯之后,
关闭止水夹,由于产生的氢气无法排出,试管A中的压强将增大,最终将A试管中生成的FeSO 溶液压入
4
NaOH溶液中,故Fe(OH) 在B试管生成;
2
(4)A.加入铁和铜的混合物,铁首先与氯化铁反应,可能铁全部反应而铜有剩余,A正确;B.加入铁和
铜的混合物,铁首先与氯化铁反应,铜后参加反应,不会出现有铁无铜的情形,B错误;C.若氯化铁的
量少,加入的铁粉和铜粉可能剩余,C正确;D.若氯化铁的量多,加入的铁粉和铜粉全部参加反应,不
会有剩余,D正确;答案选B。
(5)氯化铁与铜反应生成氯化亚铁和氯化铜,反应的离子方程式为2Fe3++Cu=Cu2++2Fe2+;
(6)①取少量待测溶液,滴入KSCN溶液呈红色,该现象说明该溶液中含有的离子是Fe3+;②A.由于亚铁
离子具有还原性,因此取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+,A正确;B.取适量溶液,滴入氯水,再滴入KSCN溶液,若显血红色,不能证明原溶液中含有Fe2+,因为原溶液中可能含有
铁离子,B错误;C.观察溶液是否呈浅绿色,不能确定是否含亚铁离子,C错误,答案选A。