文档内容
第三章 铁 金属材料
第二节 金属材料
第二课时 新型合金 物质的量在化学方程式计算中的应用
【学习目标】1.通过阅读教材、查阅资料,了解储氢合金、钛合金等新型合金,感受化学科学对创造
更多新材料以满足人类生活需要和促进科技发展的重要作用。
2.通过联系旧知、讨论交流,从物质的量的角度认识物质的组成及化学变化,能运用物质的量与其他
物理量之间的换算关系进行有关计算。
3.通过对化学方程式本质的分析,能结合物质的量在化学方程式计算中的应用进行简单的计算,了解
常见的化学计算中常用的方法,进一步体会守恒思想,强化宏观辨识与微观探析能力。
【学习重点】物质的量在化学方程式计算中的应用
【学习难点】物质的量在化学方程式计算中的应用
【课前预习】
旧知回顾:1.生铁和钢是含碳量不同的两种 合金。生铁的含碳量为 ,钢的含碳
量为 。由于含碳量不司,钢和生铁在性能上有很大 。例如,生铁
、
,是制造 的重要材料;钢有良好的延展性,机械性能好,可以
,泛用于制造机械和交通工具等。
2. 联 系 物 质 的 量 与 气 体 体 积 、 质 量 、 微 粒 数 的 、 物 质 的 量 浓 度 的 桥 梁 分 别 是
、
。
新知预习:1.近年来,为满足某些尖端技术发展的需要,人们又设计和合成了许多 。例
如,氢能是人类未来的理想能源之一,氢能利用存在两大难题: 。H 是种
2
的气体,要利用H ,关键要解决H 的 。
2 2
2.化学方程式中各物质的化学计量数之比 组成各物质的粒子数之比,也等于
,还等于 。
【课中探究】
情景导入:在之前的学习中,我们已经学习了铁合金和铝合金,这两种合金都是常用的合金材料。而
生活中除了这些常见的合金材料以外,随着科技的不断发展,也涌现了很多具有特殊性
能的新型合金,广泛用于航空航天、生物工程和电子工业等领域。(见PPT图片)。
一、新型合金
活动一、新型合金的分类及应用任务一、阅读教材P83页内容,观察储氢合金的图片,结合教材内容思考储氢合金有何特点?
任务二、阅读教材P83页内容,思考常见新型合金的有哪些主要性能和用途?完成表格内容。
钛合金
储氢合金
形状记忆合
金
耐热合金
【对应训练】1.“双奥之城”——北京将迎来2022年冬奥会,滑雪是冬奥会的主要项目之一。下列滑
雪用品涉及到的材料属于合金的是( )
A.滑雪杖杆——铝材(铝、镁等) B.滑雪板底板——塑料
C.滑雪手套——合成橡胶 D.滑雪服面料——尼龙
2.2022年科技创新结出累累硕果,加快了实现高水平建设科技强国。 下列
有关说法错误的是( )
A.“北斗导航”系统应用一体化芯片手机,芯片成分为SiO
2
B.“奋斗者”号深海载人潜水器采用的Ti62A新型钛合金的硬度比纯钛的高
C.C919大飞机机身采用了第三代铝锂合金,具有密度低、强度高等优良特点
D.问天实验舱太阳翼配置的是三结砷化镓电池,砷化镓喻为“半导体贵族”
活动二、合金形成的条件及应用
任务一、讨论交流:根据合金的定义,你认为合金形成的条件是什么?任务二、阅读教材P84页“科学‧技术‧社会”栏目,结合P86教材习题9:我国发行的第五套人民币
中,l元 、5角 和 1角 硬币的材质分别为钢芯镀镍 (1元 )、 钢芯镀铜(5角 )和铝合金 (1角 )。 思考什
么是稀土金属,有哪些应用?选择铸造硬币的金属材料时应考虑哪些因素?
【对应训练】1.社会的进步与时代的发展充满了人类智慧的结晶。下列有关说法中错误的是
( )
A.合金为纯净物,具有许多优良的物理、化学或机械性能
B.不锈钢是最常见的一种合金钢,不容易生锈。
C.商朝的“后母戊鼎”是我国较早使用的铜制品之一
D.近年来,人们又设计和合成了许多新型合金。如储氢合金、钛合金等
2.下列说法正确的是( )
A.合金一般由多种元素组成,属于化合物
B.常温下,铝制品耐腐蚀是因为铝不活泼
C.新型储氢合金因具有较大空隙,通过物理吸附大量H 而广泛用于新能源汽车行业
2
D.合金中加入其他元素原子后,使原子层之间的相对滑动变得困难,导致合金的硬度变大
二、物质的量在化学方程式计算中的应用
活动一、物质的量与其他物理量之间的关系
任务一、请写出物质的量与质量、微粒数、气体体积、物质的量浓度等物理量之间的关系图,可得出
什么结论?
任务二、根据化学反应的实质,以金属钠与水反应为例,思考微观粒子与化学方程式有何关系?可得出什么结论?
任务三、分析完成教材P85页【例题】,思考物质的量在化学方程式计算中的步骤是什么?
【典例】250 mL 2 mol·L-1的硫酸与足量的铁屑完全反应。计算:
(1)参加反应的铁屑的物质的量;
(2)生成的H 的体积(标准状况)。(写出解题步骤)
2
【分析 】
【解析】
解题步骤:
第一步:
第二步:
第三步:
第四步:
第五步:
注意事项:
【对应训练】完全中和0.1 mol NaOH需HSO 的质量是多少?
2 4
解法一:解法二、
活动二、化学计算中的常用方法
任务一、以“一定量的铁粉和9 g硫粉混合加热,待其反应后再加入过量盐酸,将生成的气体完全燃
烧,共收集得9 g水,求加入的铁粉质量”为例,思考什么是关系式法?
任务二、以“为了检验某含有NaHCO 杂质的NaCO 样品的纯度,现将w g样品加热,其质量变为
3 2 3 1
w g,请列式计算该样品中NaCO 的质量分数”为例,思考什么是差量法?
2 2 3任务三、以“用1 mol·L-1的NaSO 溶液30 mL恰好将2×10-2 mol的XO — 还原,已知氧化产物为
2 3 4
SO 2- ,求元素X在还原产物中的化合价”为例,思考什么是守恒法?
4
【对应训练】1.Mg、Al组成的混合物与足量盐酸反应,产生标准状况下的氢气为4.48 L。下列推断
中不正确的是( )
A.参加反应的Mg、Al共0.2 mol B.参加反应的HCl为0.4 mol
C.Mg、Al在反应中共失去0.4 mol电子 D.若与足量的稀硫酸反应能产生0.2 mol H
2
2.在一定条件下,RO和F 可发生如下反应:RO+F +2OH-===RO+2F-+HO,从而可知在RO
2 2 2
中,元素R的化合价是( )
A.+4 B.+5 C.+6 D.+7
【课后巩固】1.教材P86页3、7、8、10、11
2.社会的进步与时代的发展充满了人类智慧的结晶。下列有关说法中错误的是( )
A.合金为纯净物,具有许多优良的物理、化学或机械性能
B.不锈钢是最常见的一种合金钢,不容易生锈。
C.商朝的“后母戊鼎”是我国较早使用的铜制品之一
D.近年来,人们又设计和合成了许多新型合金。如储氢合金、钛合金等
3.钛和钛的合金具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,尤其是钛合金与人
体器官具有很好的“生物相容性”。根据它们的主要性能,下列用途不切合实际的是( )
A.用来做保险丝 B.用于制造航天飞机
C.用来制造人造骨 D.用于家庭装修,做钛合金装饰门
4.合金品种多、应用广泛,很多高品质合金是大国重器的原材料。关于合金的下列叙述,不正确的
是( )
A.“合金材料”中只含金属元素,不含非金属元素
B.生活中大量使用铝合金是因为它的密度小、强度高、抗腐蚀能力强
C.Ti—Fe合金和La—Ni合金都是新型合金,特点是室温下吸、放氢的速率快D.焊锡(锡铅合金)熔点比金属锡低
5.将同体积同物质的量浓度的 AgNO 溶液中的 Ag+完全沉淀,则需同物质的量浓度的 NaCl、
3
MgCl 、AlCl 三种溶液的体积比为( )
2 3
A.1∶2∶3 B.3∶2∶1 C.1∶1∶1 D.6∶3∶2
6.镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。
反应中镁和铝的( )
A.物质的量之比为3∶2 B.质量之比为3∶2
C.摩尔质量之比为2∶3 D.生成气体的物质的量之比为2∶3
7.6 g Fe和Fe O 的混合物,加入150 mL足量的稀硫酸,在标准状况下 收
2 3
集到1.12 L H ,向反应后的溶液中滴加KSCN溶液不变红。为中和过量的稀硫酸,并使Fe元素全部转化
2
为Fe(OH) 沉淀,恰好消耗了200 mL 3 mol·L-1的NaOH溶液,则该稀HSO 的物质的量浓度为( )
2 2 4
A.2.25 mol·L-1 B.2 mol·L-1 C.3 mol·L-1 D.0.6 mol·L-1
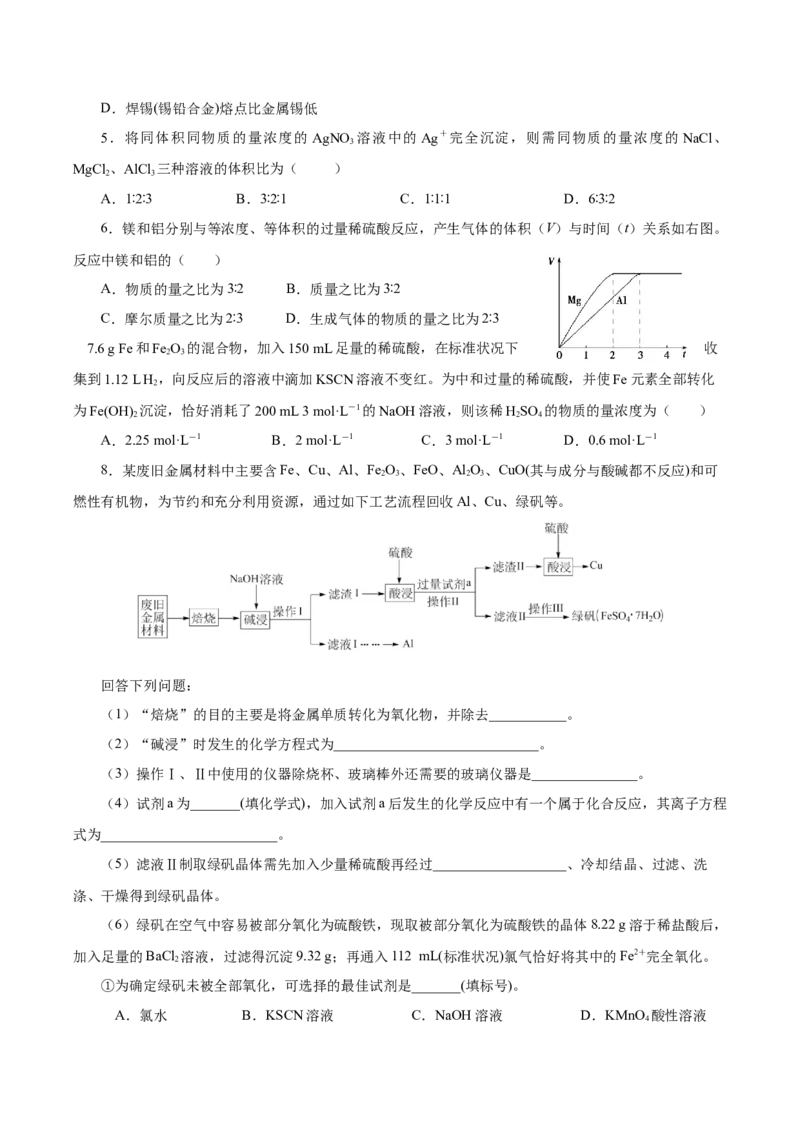
8.某废旧金属材料中主要含Fe、Cu、Al、Fe O、FeO、Al O、CuO(其与成分与酸碱都不反应)和可
2 3 2 3
燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
回答下列问题:
(1)“焙烧”的目的主要是将金属单质转化为氧化物,并除去___________。
(2)“碱浸”时发生的化学方程式为_____________________________。
(3)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是_______________。
(4)试剂a为_______(填化学式),加入试剂a后发生的化学反应中有一个属于化合反应,其离子方程
式为_________________________。
(5)滤液Ⅱ制取绿矾晶体需先加入少量稀硫酸再经过___________________、冷却结晶、过滤、洗
涤、干燥得到绿矾晶体。
(6)绿矾在空气中容易被部分氧化为硫酸铁,现取被部分氧化为硫酸铁的晶体8.22 g溶于稀盐酸后,
加入足量的BaCl 溶液,过滤得沉淀9.32 g;再通入112 mL(标准状况)氯气恰好将其中的Fe2+完全氧化。
2
①为确定绿矾未被全部氧化,可选择的最佳试剂是_______(填标号)。
A.氯水 B.KSCN溶液 C.NaOH溶液 D.KMnO 酸性溶液
4②推测晶体的化学式为_________________________________。