文档内容
第二节 金属材料
第3课时 物质的量在化学方程式中的应用
基础巩固
1.把一小块钠放入足量水中,会发生如下反应:2Na+2H O 2NaOH+H ↑。下列有关该反应的说法正确的
2 2
是 ( )
A.反应中Na与NaOH的质量相等
B.反应中HO和H 的质量相等
2 2
C.反应中HO和H 的质量之比为2∶1
2 2
D.反应中Na与NaOH的物质的量之比为1∶1
2.(2021·曲靖市第二中学高一期末)金属汞在加热条件下可以与氧气化合生成氧化汞,反应为2Hg +O
2
2HgO ,下列选项中,可以说明0.2 mol Hg与0.2mol O 充分反应后物质的种类及其数量的情况的是
2
( )
A.0.02 mol HgO + 0.2 mol Hg B.0.2 mol HgO + 0.1 mol O
2
C.0.2 mol HgO D.0.1 mol HgO + 0.1 mol Hg
3.用1 L 1.0 mol·L-1的氢氧化钠溶液吸收0.8 mol二氧化碳,所得溶液中碳酸根离子与碳酸氢根离子的物质
的量浓度之比是 ( )
A.1∶3 B.1∶2 C.2∶3 D.3∶2
4.将铁加入100 mL某浓度的盐酸中恰好完全反应,反应后生成的气体为V L(标准状况下),将铝加入
100 mL 2 mol·L-1 NaOH溶液中恰好完全反应,充分反应后生成的气体为3V L。下列说法正确的是( )
A.原铁和铝的物质的量相等
B.原盐酸的浓度为2 mol·L-1
C.铁加入盐酸中的离子方程式为2Fe+6H+===2Fe3++3H↑
2
D.盐酸与NaOH溶液的物质的量浓度之比为1∶3
5.将一定质量的锌片放入500 mL CuSO 溶液中,二者恰好完全反应,待充分反应后取出锌片,洗净后称
4
量,发现锌片比原来减轻了0.5 g,则该CuSO 溶液的物质的量浓度为( )
4
A.0.5 mol·L-1 B.1 mol·L-1
C.1.5 mol·L-1 D.2 mol·L-1
6.在500 mL NaOH溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体33.6 L。该NaOH溶液
的物质的量浓度为( )
A.1.0 mol·L-1 B.2.0 mol·L-1
C.1.5 mol·L-1 D.3.0 mol·L-1
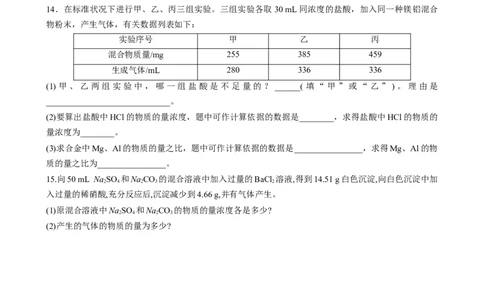
7.以太阳能为热源分解Fe O ,经热化学铁氧化合物循环分解水制 的过程如图所示。下列叙述不正确
3 4
的是( )
学科网(北京)股份有限公司A.过程Ⅰ中的能量转化形式是太阳能→化学能
B.过程Ⅱ的化学方程式为3FeO+H O Fe O +H ↑
2 3 4 2
C.过程Ⅰ中每消耗116 g Fe O 转移2 mol电子
3 4
D.铁氧化合物循环制H 具有节约能源、产物易分离等优点
2
8.将a g二氧化锰粉末加入b mol/L的浓盐酸c L中加热完全溶解,反应中转移电子d个,设N 为阿伏加
A
德罗常数的值,下列叙述正确的是( )
A.可以收集到氯气 B.N 可表示为: [来
A
C.反应后溶液中的Cl―数目为: D.反应后溶液中的H+数目为:bc-2d[来源:学
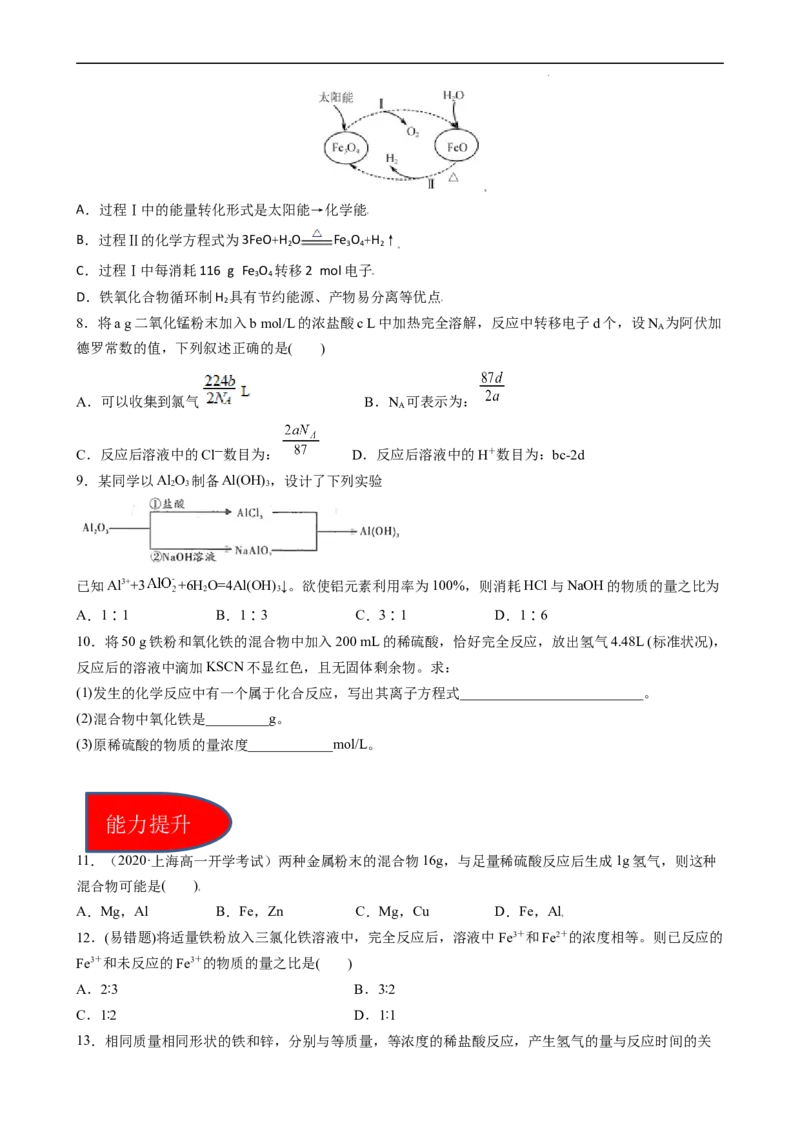
9.某同学以Al O 制备Al(OH) ,设计了下列实验
2 3 3
已知Al3++3 +6H O=4Al(OH) ↓。欲使铝元素利用率为100%,则消耗HCl与NaOH的物质的量之比为
2 3
A.1∶1 B.1∶3 C.3∶1 D.1∶6
10.将50 g铁粉和氧化铁的混合物中加入200 mL的稀硫酸,恰好完全反应,放出氢气4.48L (标准状况),
反应后的溶液中滴加KSCN不显红色,且无固体剩余物。求:
(1)发生的化学反应中有一个属于化合反应,写出其离子方程式__________________________。
(2)混合物中氧化铁是_________g。
(3)原稀硫酸的物质的量浓度____________mol/L。
能力提升
11.(2020·上海高一开学考试)两种金属粉末的混合物16g,与足量稀硫酸反应后生成1g氢气,则这种
混合物可能是( )
A.Mg,Al B.Fe,Zn C.Mg,Cu D.Fe,Al
12.(易错题)将适量铁粉放入三氯化铁溶液中,完全反应后,溶液中Fe3+和Fe2+的浓度相等。则已反应的
Fe3+和未反应的Fe3+的物质的量之比是( )
A.2∶3 B.3∶2
C.1∶2 D.1∶1
13.相同质量相同形状的铁和锌,分别与等质量,等浓度的稀盐酸反应,产生氢气的量与反应时间的关
学科网(北京)股份有限公司系如图所示,下列说法正确的是( )
A.乙表示锌与盐酸的反应
B.锌可能与盐酸恰好完全反应,而铁有剩余
C.两个反应消耗金属的质量相等
D.所得溶液的质量相等
14.在标准状况下进行甲、乙、丙三组实验。三组实验各取30 mL同浓度的盐酸,加入同一种镁铝混合
物粉末,产生气体,有关数据列表如下:
实验序号 甲 乙 丙
混合物质量/mg 255 385 459
生成气体/mL 280 336 336
(1)甲、乙两组实验中,哪一组盐酸是不足量的?______(填“甲”或“乙”)。理由是
_____________________________。
(2)要算出盐酸中HCl的物质的量浓度,题中可作计算依据的数据是________,求得盐酸中HCl的物质的
量浓度为________。
(3)求合金中Mg、Al的物质的量之比,题中可作计算依据的数据是________________,求得Mg、Al的物
质的量之比为________________。
15.向50 mL Na SO 和Na CO 的混合溶液中加入过量的BaCl 溶液,得到14.51 g白色沉淀,向白色沉淀中加
2 4 2 3 2
入过量的稀硝酸,充分反应后,沉淀减少到4.66 g,并有气体产生。
(1)原混合溶液中Na SO 和Na CO 的物质的量浓度各是多少?
2 4 2 3
(2)产生的气体的物质的量为多少?
学科网(北京)股份有限公司学科网(北京)股份有限公司