文档内容
第 16 讲 水的电离
知识导航
小杨老师 15521324728 侵权必究
课前引入
弱电解质包括哪些?
杨sir化学,侵权必究
弱电解质均存在电离平衡,那水的电离是怎样的?
知识精讲
小杨老师 15521324728 侵权必究
一、水的电离
1. 图示
2. 电离方程式:HO + HO ⇌ HO+ + OH-,简写为HO ⇌ H+ + OH-。
2 2 3 2
3. 任何水溶液中,都存在H+、OH-、HO三种微粒。
2 杨sir化学,侵权必究
二、水的离子积
1.表达式:K = c(H+)· c(OH-)
w
2.影响因素
T/℃ 0 10 20 25 40 50 100K /10-14 0.114 0.292 0.681 1.00 2.92 5.47 55.0
w
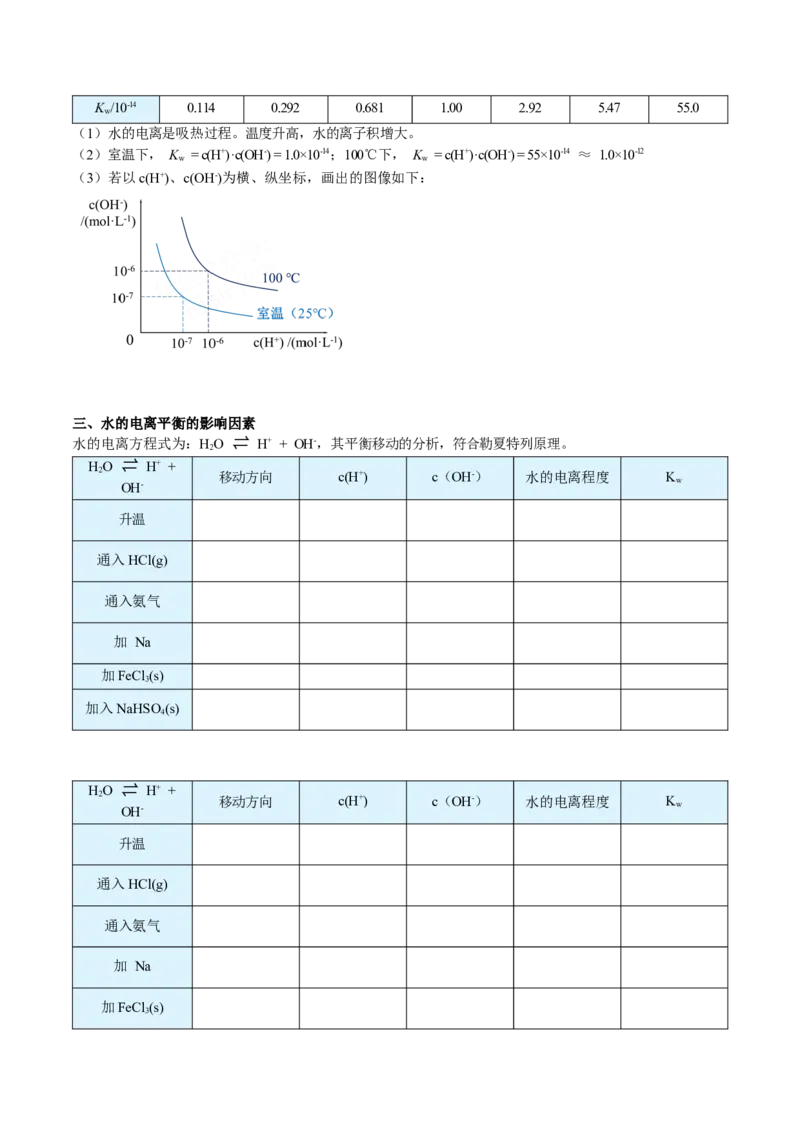
(1)水的电离是吸热过程。温度升高,水的离子积增大。
(2)室温下, K = c(H+)·c(OH-) = 1.0×10-14;100℃下, K = c(H+)·c(OH-) = 55×10-14 ≈ 1.0×10-12
w w
(3)若以c(H+)、c(OH-)为横、纵坐标,画出的图像如下:
杨sir化学,侵权必究
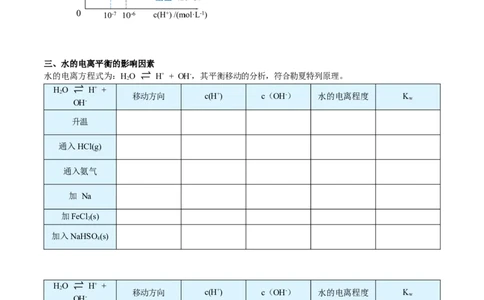
三、水的电离平衡的影响因素
水的电离方程式为:HO ⇌ H+ + OH-,其平衡移动的分析,符合勒夏特列原理。
2
HO ⇌ H+ +
2 移动方向 c(H+) c(OH-) 水的电离程度 K
OH- w
升温
通入HCl(g)
通入氨气
加 Na
加FeCl(s)
3
加入NaHSO(s)
4
HO ⇌ H+ +
2 移动方向 c(H+) c(OH-) 水的电离程度 K
OH- w
升温
通入HCl(g)
通入氨气
加 Na
加FeCl(s)
3加入NaHSO(s)
4
总结归纳——水的电离平衡的影响因素
1. 温度升高,促进水的电离,K 增大;
w
2. 酸、碱抑制水的电离,K 不变;
w 杨sir化学,侵权必究
3. 外加能与H+、OH- 反应的物质,会促进水的电离,K 不变。
w
对点训练
小杨老师 15521324728 侵权必究
题型一:水的电离
杨sir化学,侵权必究
【例1】下列有关“水”的说法正确的是
A.水是强电解质
B.氢氧两种元素只能组成水
C.水的电子式可表示为:
D.水的电离方程式可表示为:
题型二:水的离子积
杨sir化学,侵权必究
【变2-1】与纯水的电离相似,液氨中也存在着微弱的电离: , 的平衡浓度为
,下列说法正确的是( )
A.在此温度下液氨的离子积为
B.在液氨中放入金属钠,可生成
C.恒温下,在液氨中加入 ,可使液氨的离子积减小
D.降温可使液氨的电离平衡逆向移动,且
题型三:由水电离出的H+/OH-
杨sir化学,侵权必究【例3】常温下,0.1 mol·L-1的NaOH溶液中由水电离出的OH-的物质的量浓度为
A.0.1 mol·L-1 B.1.0×10-13 mol·L-1
C.1.0×10-7 mol·L-1 D.无法确定
【变4-1】室温下,在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是
①K+、Cl-、NO 、S2-
②K+、Fe2+、I-、SO
③Na+、Cl-、NO 、SO
④Na+、Ca2+、Cl-、HCO
⑤K+、Ba2+、Cl-、NO
A.③⑤ B.①③⑤ C.①③ D.②④⑤
杨sir化学,侵权必究
题型四:水的电离平衡
杨sir化学,侵权必究
【变5】水存在电离平衡:HO H++OH-,常温下,K 的数值为 1×10-14.下列说法不正确的是
2 w
A.常温下,水电离出的 c(H+)=c(OH-)=10-7mol·L-1
B.向水中加入NaCl,H+与 Cl-结合生成 HCl,使水的电离平衡向正反应方向移动
C.向水中加入HCl或者NaOH,水的电离平衡都向逆反应方向移动
D.改变温度,K 也会发生改变
w
【例6】25℃时,相同物质的量浓度的下列溶液:①NaCl溶液②NaOH溶液③ 溶液,其中水的电离
程度按由大到小顺序排列的一组是
A.③>②>① B.②>③>① C.①>②>③ D.③>①>②
杨sir化学,侵权必究
题型五:
杨sir化学,侵权必究
【变7】回答下列问题:
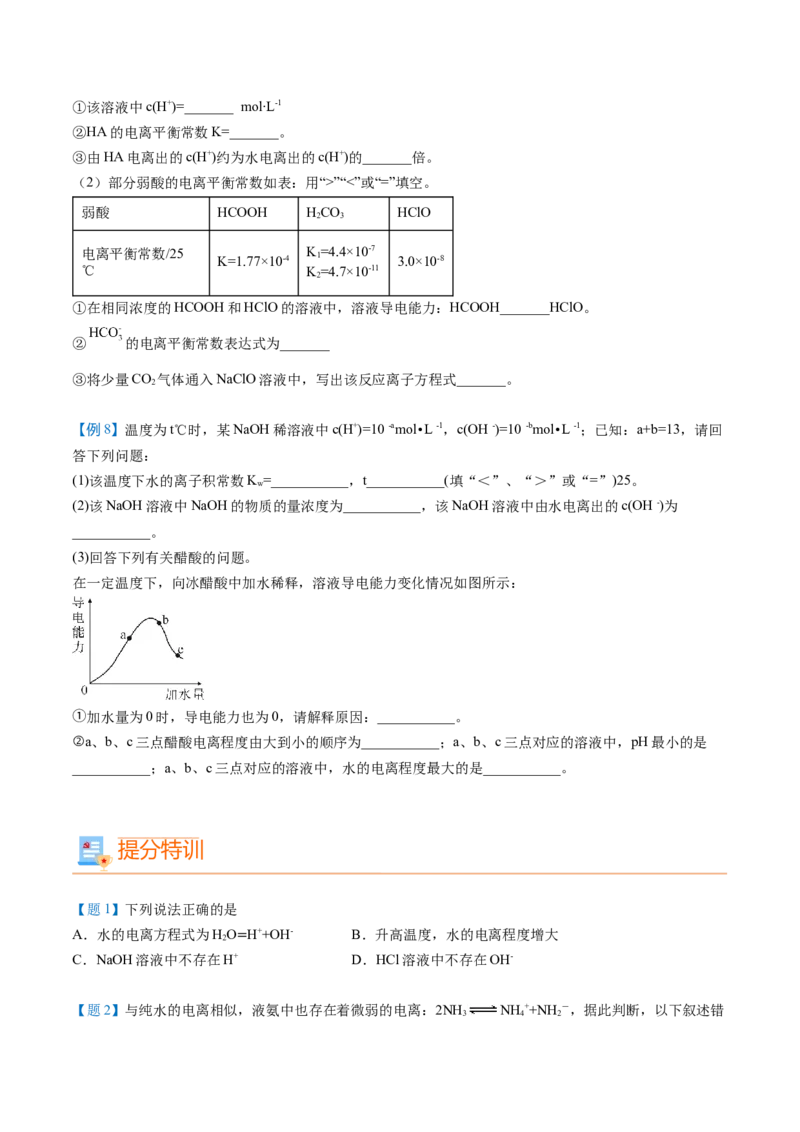
(1)已知室温时,0.1 mol∙L-1某一元酸HA在水中有0.1%发生电离,回答下列问题:①该溶液中c(H+)=_______ mol∙L-1
②HA的电离平衡常数K=_______。
③由HA电离出的c(H+)约为水电离出的c(H+)的_______倍。
(2)部分弱酸的电离平衡常数如表:用“>”“<”或“=”填空。
弱酸 HCOOH HCO HClO
2 3
电离平衡常数/25 K=1.77×10-4 K 1 =4.4×10-7 3.0×10-8
℃ K=4.7×10-11
2
①在相同浓度的HCOOH和HClO的溶液中,溶液导电能力:HCOOH_______HClO。
② 的电离平衡常数表达式为_______
③将少量CO 气体通入NaClO溶液中,写出该反应离子方程式_______。
2
【例8】温度为t℃时,某NaOH稀溶液中c(H+)=10 -amol•L -1,c(OH -)=10 -bmol•L -1;已知:a+b=13,请回
答下列问题:
(1)该温度下水的离子积常数K =___________,t___________(填“<”、“>”或“=”)25。
w
(2)该NaOH溶液中NaOH的物质的量浓度为___________,该NaOH溶液中由水电离出的c(OH -)为
___________。
(3)回答下列有关醋酸的问题。
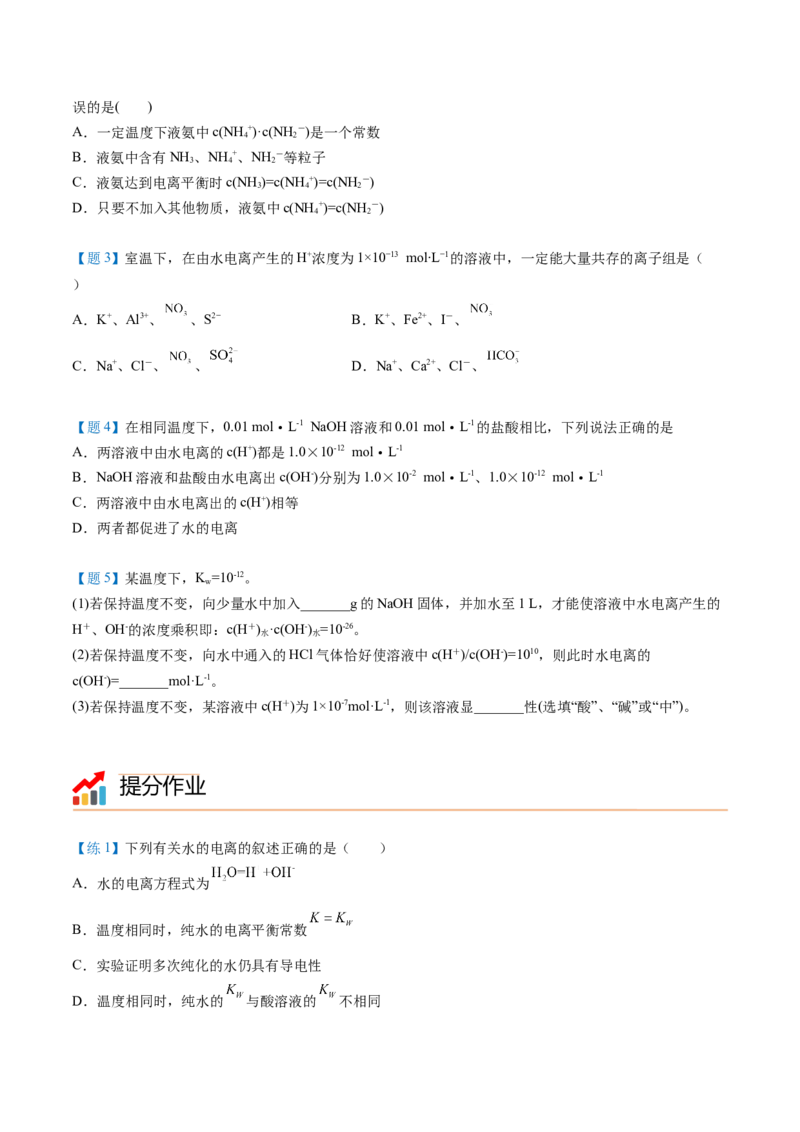
在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示:
杨sir化学,侵权必究
①加水量为0时,导电能力也为0,请解释原因:___________。
②a、b、c三点醋酸电离程度由大到小的顺序为___________;a、b、c三点对应的溶液中,pH最小的是
___________;a、b、c三点对应的溶液中,水的电离程度最大的是___________。
提分特训
小杨老师 15521324728 侵权必究
【题1】下列说法正确的是
A.水的电离方程式为HO H++OH- B.升高温度,水的电离程度增大
2
C.NaOH溶液中不存在H+ D.HCl溶液中不存在OH-
=
【题2】与纯水的电离相似,液氨中也存在着微弱的电离:2NH NH ++NH-,据此判断,以下叙述错
3 4 2误的是( )
A.一定温度下液氨中c(NH +)·c(NH -)是一个常数
4 2
B.液氨中含有NH 、NH +、NH -等粒子
3 4 2
C.液氨达到电离平衡时c(NH )=c(NH+)=c(NH-)
3 4 2
D.只要不加入其他物质,液氨中c(NH +)=c(NH-)
4 2 杨sir化学,侵权必究
【题3】室温下,在由水电离产生的H+浓度为1×10−13 mol∙L−1的溶液中,一定能大量共存的离子组是(
)
A.K+、Al3+、 、S2− B.K+、Fe2+、I-、
C.Na+、Cl-、 、 D.Na+、Ca2+、Cl-、
【题4】在相同温度下,0.01 mol·L-1 NaOH溶液和0.01 mol·L-1的盐酸相比,下列说法正确的是
A.两溶液中由水电离的c(H+)都是1.0×10-12 mol·L-1
B.NaOH溶液和盐酸由水电离出c(OH-)分别为1.0×10-2 mol·L-1、1.0×10-12 mol·L-1
C.两溶液中由水电离出的c(H+)相等
D.两者都促进了水的电离
【题5】某温度下,K =10-12。
w
(1)若保持温度不变,向少量水中加入_______g的NaOH固体,并加水至1 L,才能使溶液中水电离产生的
H+、OH-的浓度乘积即:c(H+) ·c(OH-) =10-26。
水 水
(2)若保持温度不变,向水中通入的HCl气体恰好使溶液中c(H+)/c(OH-)=1010,则此时水电离的
c(OH-)=_______mol·L-1。
杨sir化学,侵权必究
(3)若保持温度不变,某溶液中c(H+)为1×10-7mol·L-1,则该溶液显_______性(选填“酸”、“碱”或“中”)。
提分作业
小杨老师 15521324728 侵权必究
【练1】下列有关水的电离的叙述正确的是( )
A.水的电离方程式为
B.温度相同时,纯水的电离平衡常数
C.实验证明多次纯化的水仍具有导电性
D.温度相同时,纯水的 与酸溶液的 不相同【练2】室温下,某溶液中由水电离产生的c(H+)=10-10 mol·L-1,该溶液的溶质不可能是( )
A.HSO
2 4
B.NaCl
杨sir化学,侵权必究
C.HCl
D.Ba(OH)
2
【练3】室温下,若溶液中由水电离产生的c(OH−)=1×10—13mol·L—1,满足此条件的溶液中一定可以大量共
存的离子组是
A.Al3+、Na+、NO 、Cl— B.K+、Na+、Cl—、NO
C.K+、Na+、Cl—、AlO D.K+、NH 、SO 、NO
【练4】水的离子积常数
(1)水的电离平衡常数表达式为_______.
(2)水的离子积常数表达式为_______.
(3) 及影响因素
①25℃时, _______.
②水的电离是的可逆过程,故温度升高 _______.
③水的离子积常数只受_______的影响,与 、 的变化无关.
杨sir化学,侵权必究
【练5】某温度下,纯水的c(H+)为2×10-7mol•L-1,则此时c(OH-)为___mol•L-1,若温度不变,滴入稀
HSO 使c(H+)=5×10-4mol•L-1,则由水电离出的c(OH-)为___mol•L-1,此时温度___(填“高于”、“低
2 4
于”或“等于”)25℃。
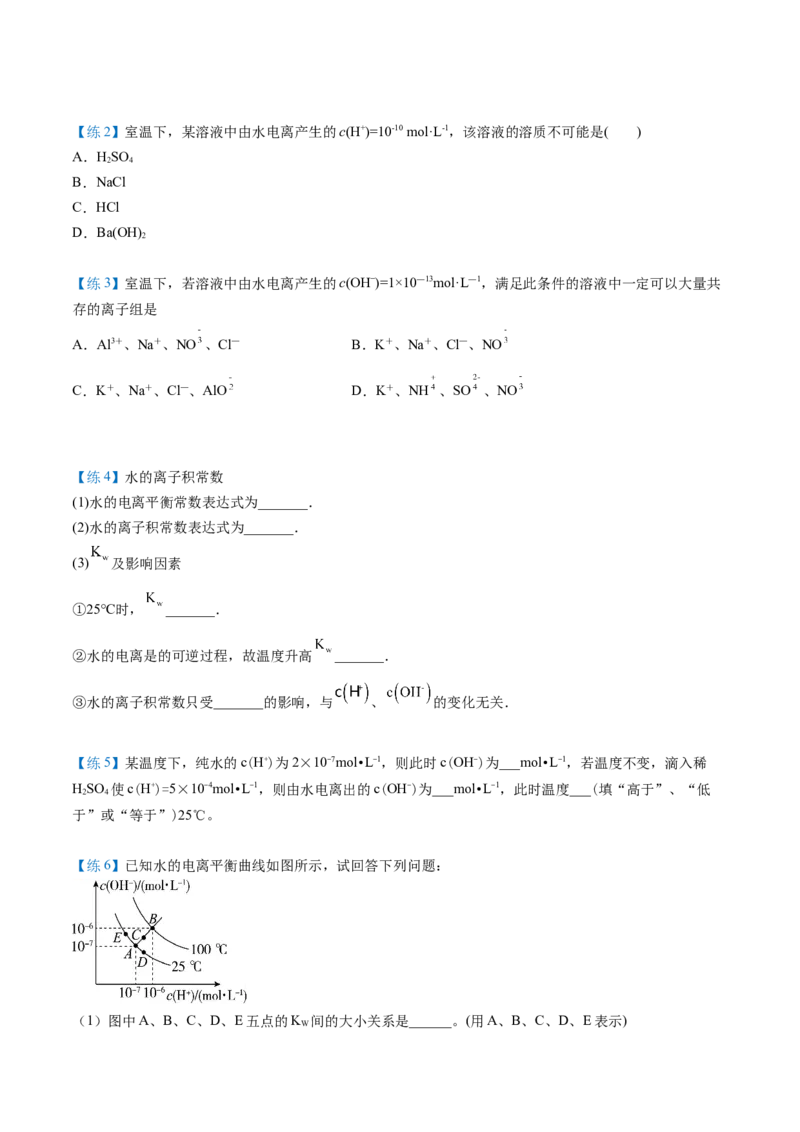
【练6】已知水的电离平衡曲线如图所示,试回答下列问题:
(1)图中A、B、C、D、E五点的K 间的大小关系是______。(用A、B、C、D、E表示)
W(2)若从A点到D点,可采用的措施是___________。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH固体
杨sir化学,侵权必究
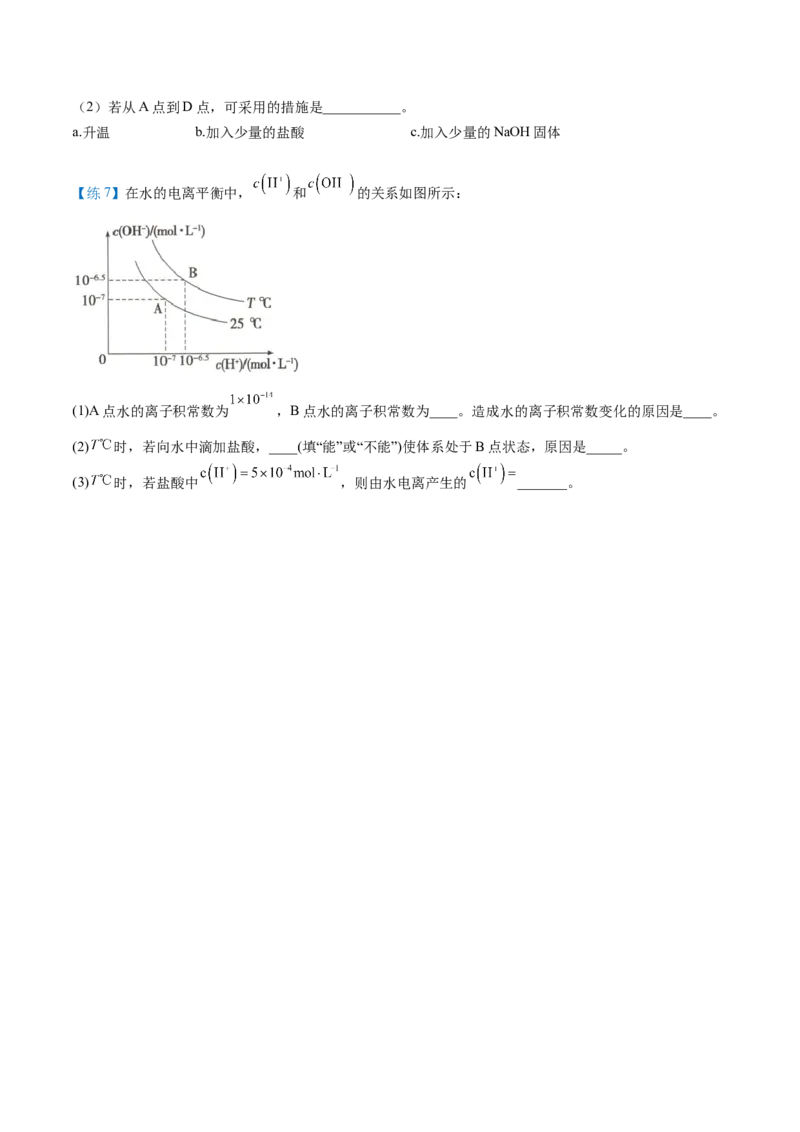
【练7】在水的电离平衡中, 和 的关系如图所示:
(1)A点水的离子积常数为 ,B点水的离子积常数为____。造成水的离子积常数变化的原因是____。
(2) 时,若向水中滴加盐酸,____(填“能”或“不能”)使体系处于B点状态,原因是_____。
杨sir化学,侵权必究
(3) 时,若盐酸中 ,则由水电离产生的 _______。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育