文档内容
单元检测卷
第九单元 溶液
(建议完成时间:50 分钟)
一、选择题
1.(2017•玉林)把下列物质分别放入水中,充分搅拌,可以得到溶液的是()
A.碘 B.面粉 C.蔗搪 D.花生油
2. (2017•绥化) 下列有关洗涤问题的说法中,不正确的是( )
A.汽油可溶解衣服上的油油渍 B.洗洁精可乳化餐具上的油污
C.醋酸能洗去暖水瓶内壁的水垢 D.酒精能洗涤瓷砖上的的水锈
3.(2017•郴州)下列关于溶液的说法正确的是( )
A.能溶解其他物质的物质叫做溶剂
B.凡是均一的、稳定的液体一定是溶液
C.溶液一定是无色透明的
D.饱和溶液一定是浓溶液
4.(2017•湘潭)往适量的水中加入下列物质,温度明显降低的是( )
A.浓硫酸 B.氢氧化钠 C. 氯化钠 D. 硝酸铵
5(2017•株洲)除质量分数以外,人们有时也用体积分数来表示溶液的浓度。例如,52%的饮
用白酒就是100体积的饮用白酒中含有52体积的乙醇。下列溶液的浓度属于用体积分
数来表示的是( )
A. 0.9%的生理盐水 B.5%的葡萄精注射液
C.10%的氢氧化钠溶液 D.75%的医用酒精
6.(2017•苏州)下列关于溶液的说法中,正确的是( )
A.泥土加入水中,振荡后可以形成溶液
B.蔗糖溶液上半部分溶液的甜度低于下半部分溶液的甜度
C.氢氧化钠溶液能导电,因为溶液中有较多自由移动的离子
D.氯化钠饱和溶液中不能再溶解少量硝酸钾晶体
7. (2017•宿迁)下列说法正确的是( )
A.均一稳定的液体一定是溶液 B.饱和济液一定是浓溶液
C.汽油洗涤油污属于乳化现象 D.将氢氧化钠溶于水,所得溶液温度升高
8.(2017•沈阳)13.按下列方法配制的溶液,其溶质质量分数为5%的是( )
A.称取5.0g氯化钾,溶解在95mL水中,充分搅拌
B.称取5.0g生石灰,放入95mL水中,充分搅拌C.量取5.OmL浓盐酸,倒入95mL水中,充分搅拌
D.称取5.0g二氧化锰,放入95mL水中,充分搅拌
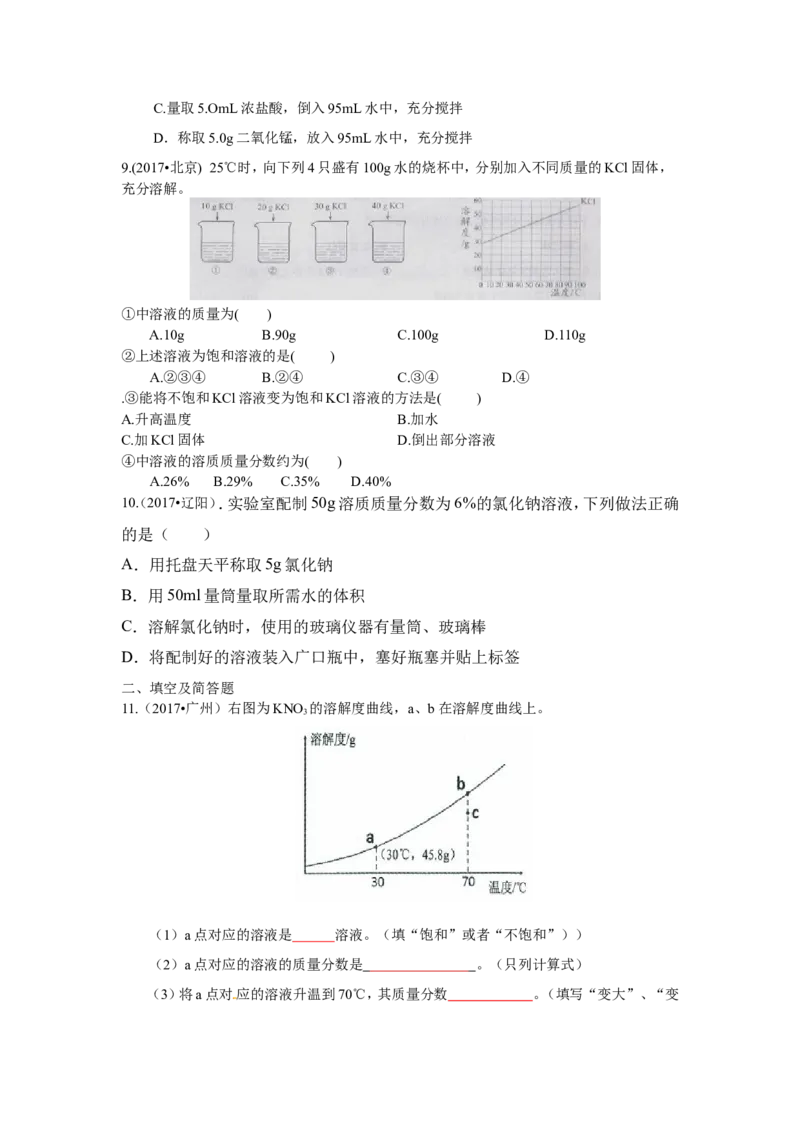
9.(2017•北京) 25℃时,向下列4只盛有100g水的烧杯中,分别加入不同质量的KCl固体,
充分溶解。
①中溶液的质量为( )
A.10g B.90g C.100g D.110g
②上述溶液为饱和溶液的是( )
A.②③④ B.②④ C.③④ D.④
.③能将不饱和KCl溶液变为饱和KCl溶液的方法是( )
A.升高温度 B.加水
C.加KCl固体 D.倒出部分溶液
④中溶液的溶质质量分数约为( )
A.26% B.29% C.35% D.40%
10(. 2017•辽阳).实验室配制50g溶质质量分数为6%的氯化钠溶液,下列做法正确
的是( )
A.用托盘天平称取5g氯化钠
B.用50ml量筒量取所需水的体积
C.溶解氯化钠时,使用的玻璃仪器有量筒、玻璃棒
D.将配制好的溶液装入广口瓶中,塞好瓶塞并贴上标签
二、填空及简答题
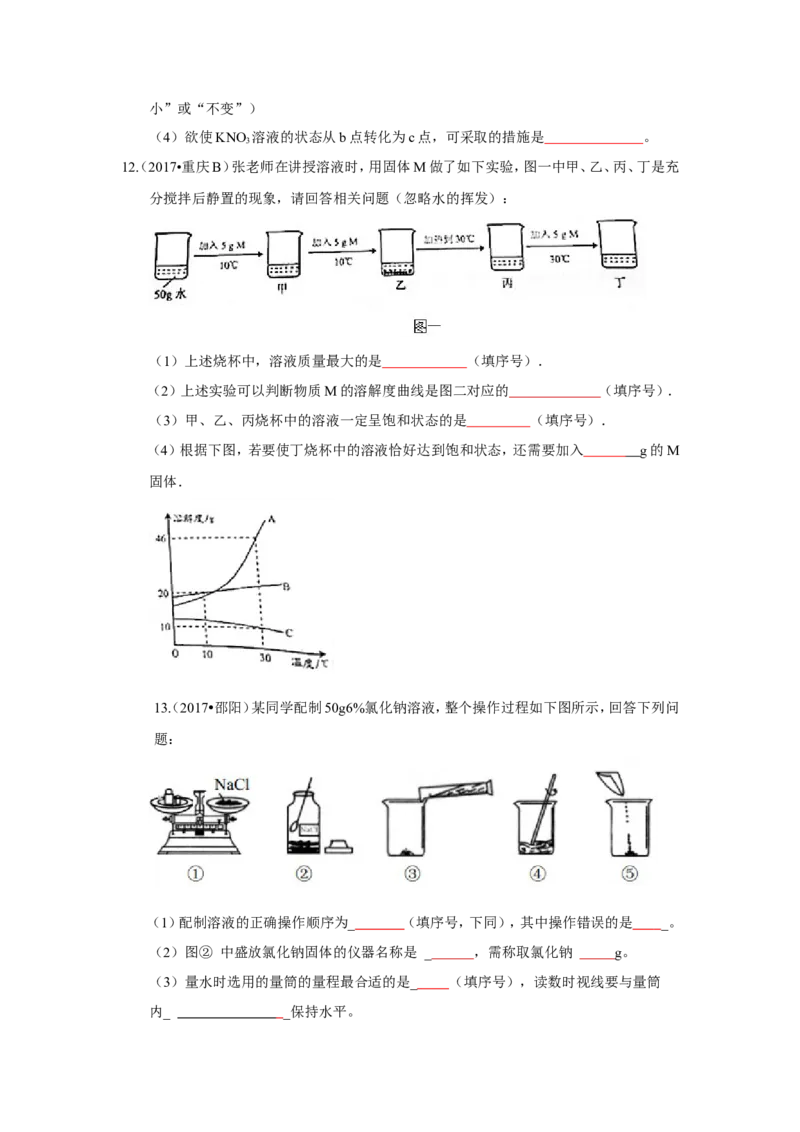
11.(2017•广州)右图为KNO 的溶解度曲线,a、b在溶解度曲线上。
3
(1)a点对应的溶液是 溶液。(填“饱和”或者“不饱和”))
(2)a点对应的溶液的质量分数是 。(只列计算式)
(3)将a点对应的溶液升温到70℃,其质量分数 。(填写“变大”、“变小”或“不变”)
(4)欲使KNO 溶液的状态从b点转化为c点,可采取的措施是 。
3
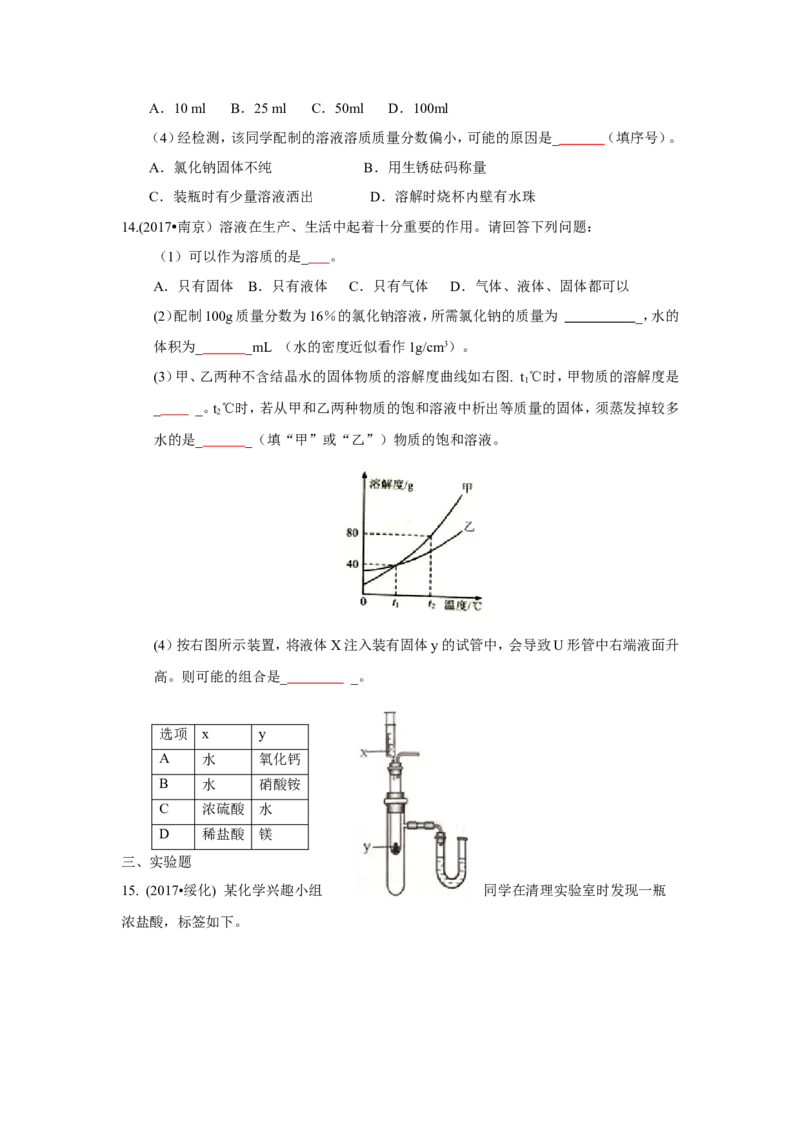
12(. 2017•重庆B)张老师在讲授溶液时,用固体M做了如下实验,图一中甲、乙、丙、丁是充
分搅拌后静置的现象,请回答相关问题(忽略水的挥发):
(1)上述烧杯中,溶液质量最大的是 (填序号).
(2)上述实验可以判断物质M的溶解度曲线是图二对应的 (填序号).
(3)甲、乙、丙烧杯中的溶液一定呈饱和状态的是 (填序号).
(4)根据下图,若要使丁烧杯中的溶液恰好达到饱和状态,还需要加入 g的M
固体.
13(. 2017•邵阳)某同学配制50g6%氯化钠溶液,整个操作过程如下图所示,回答下列问
题:
(1)配制溶液的正确操作顺序为_ (填序号,下同),其中操作错误的是 _。
(2)图② 中盛放氯化钠固体的仪器名称是 _ ,需称取氯化钠 g。
(3)量水时选用的量筒的量程最合适的是_ (填序号),读数时视线要与量筒
内_ _保持水平。A.10 ml B.25 ml C.50ml D.100ml
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是_ (填序号)。
A.氯化钠固体不纯 B.用生锈砝码称量
C.装瓶时有少量溶液洒出 D.溶解时烧杯内壁有水珠
14.(2017•南京)溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是_ 。
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为 _,水的
体积为_ _mL (水的密度近似看作1g/cm3)。
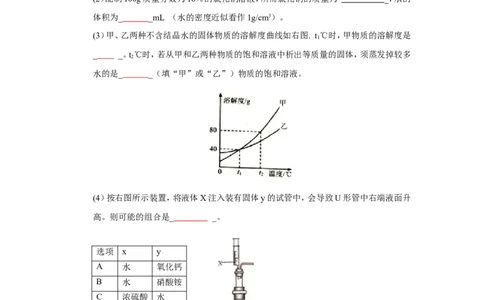
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如右图. t℃时,甲物质的溶解度是
1
_ _。t℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多
2
水的是_ _(填“甲”或“乙”)物质的饱和溶液。
(4)按右图所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升
高。则可能的组合是_ _。
选项 x y
A 水 氧化钙
B 水 硝酸铵
C 浓硫酸 水
D 稀盐酸 镁
三、实验题
15. (2017•绥化) 某化学兴趣小组 同学在清理实验室时发现一瓶
浓盐酸,标签如下。500ml
品名:盐酸 化学式:HC1
相对分子质量:36.5 密度:1.19g/ml
溶质质量分数:38%
报据标签计算。
(1) HCl中氢元素和氧元素的质量比为 (用最简整数比表示)。
(2)这瓶盐酸溶液的质量为 g。
(3)现要配制3800g溶质质量分数为10%的稀盐酸,需要溶质质量分数为38%的浓盐酸
的质量为 g,需要这种浓盐酸 瓶。
16.(2017•黑龙江龙东地区)在一定温度下,向20g Na CO 和NaCl的固体混合物中加入l0lg
2 3
水,溶解后,再向其中加入100gCaCl 溶液恰好完全反应,过滤,所得滤液的质量为211g,将
2
滤渣洗涤、 干燥,称其质量为m,试计算:
(l)m= g。
⑵当恰好完全反应时,所得溶液中溶质的质量分数为多少?
参考答案:
1. C 2. D 3. A 4. D 5. D 6. C 7. D 8. A 9.①D②D③C ④A10.B
11.(1)饱和(2) (3)不变。(4)增加溶剂。
12.(1)丁(2)A.(3)乙.(4)8
13.(1)②①⑤③④,①(2)广口瓶, 3(3) C,_凹液面最低处
(4)AD
14.(1)D。(2)16g, 84(3)40g,乙 (4)AD。
15.(1) 2:71 (2) 595。(3) 1000, 2
16.(l) 10
⑵设:原固体混合物中碳酸钠的质量为X,反应后生成氯化钠的质量为y。
NaCO+CaCl=CaCO↓+2NaCl
2 3 2 3
106 100 117
X 10g y
= x=10.6g
= y=11.7g所得溶液中溶质的质量分数: ×100%=10%
答:所得溶液中溶质的质量分数为10%。