文档内容
单元检测卷
第十一单元 盐 化肥
(建议完成时间:50 分钟)
一、选择题
1.(2017•盐城)“一带一路”赋予古丝绸之路崭新的时代内涵。古代染坊常用下列物质中的
一种盐来处理丝绸,这种盐是 ( )
A.熟石灰 B.碳酸钾 C.乙醇 D.烧碱
2.(2017•长沙)下列盐的用途中,错误的是( )
A.用含亚硝酸钠的工业盐制香肠 B.用碳酸钙做补钙剂
C.用氯化钠配制生理盐水 D.用碳酸氢钠做焙制糕点的发酵粉
3.(2017•广东)下图为xx泡打粉的标签如图所示,下列说法错误的是( )
A.碳酸氢钠俗称小苏打 B.泡打粉可以随意放置
C.加入泡打粉制作的蛋糕更松软 D.面粉是有机物,碳酸盐是无机物
4. (2017•来宾) 在粗盐难溶性杂质去除实验中,操作错误的是( )
A.称量时,在托盘天平左右两盘垫上相同质量的纸片
B.溶解时,用玻璃棒搅拌加快粗盐溶解
C.过滤时,用玻璃棒搅拌漏斗内的液体加快过滤
D.蒸发时,当蒸发皿中出现较多固体时停止加热
5. (2017•玉林)下列化学肥料中属于复合肥料的是( )
A.KSO B.CO(NH ) C.NHNO D.NH HPO
2 4 2 2 4 3 4 2 4
6.(2017•河南) 下列化肥分别与熟石灰混合研磨后。能闻到刺激性气味的是( )
A.NH Cl B.KNO C.NaNO D.Ca (PO )
4 3 3 3 4 2
7.(2017•鄂州) 化肥对提高农作无的产量有重要作用。下列有关化肥的说法不正确的是(
)
A.提倡农家肥与化肥综合利用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿D.常用作氮肥的化合物有尿素、碳酸氢铵等
8.(2017•重庆B)氯化铵(NH Cl)是“侯氏制碱法”的一种副产品。已知氯化铵的水溶液显酸
4
性,下列关于氯化铵的说法正确的是( )
A.氯化铵属于酸 B. 氯化铵是一种复合肥
C.氯化铵与熟石灰混合使用可提高肥效
D.氯化铵溶液与硝酸银溶液混合会产生白色沉淀
9.(2017•贵港) 下列各组物质的溶液,需要另加其他试剂才能区别的是( )
A.BaCl 、CuSO 、NaOH、NaCl B.Na SO 、BaCl 、KCO、NaNO
2 4 2 4 2 2 3 3
C.FeC1 、NaOH、HSO、Ba(NO ) D.MgCl 、NaOH、HCl、NaSO
3 2 4 3 2 2 2 4
10.(2017•安顺) 在溶液中能大量共存且呈无色的离子组是:( )
A. Na+、Fe3+、NO -、Cl- B.Ba2+、NH +、SO 2-、OH-
3 4 4
C. Ag+、H+、Cl-、NO - D.H+、Na+、NO -、SO 2-
3 3 4
二、简答与实验探究题
11. (2017•潍坊)实验室有一份氯化钠和氯化钡混合物样品。兴趣小组同学设计如下实验方
案,分离提纯氯化钠并测定样品中氯化钠的质量百分含量。请回答下列问题:
(1)用托盘天平称量样品前对天平进行的第一步操作是 。
(2)向溶液①中加入足量NaCO 溶液的目的是
2 3
该小组同学用右图所示装置进行操作II,请指出操作中存在的两处错
误: 。
(3)下列关于操作III的说法正确的是 (填序号)。
a. 该操作中用到的玻璃仪器有酒精灯、玻璃棒、蒸发皿
b. 该操作中用玻璃棒不断搅拌的目的是防止局部温度过高,造成液体
飞溅
c. 当蒸发皿中出现较多固体时,停止加热
d. 停止加热后,立即将蒸发皿直接放在实验台上
(4)样品中氯化钠质量百分含量为 。
12. (2017•六盘水)甲、乙两名同学分别做了碳酸钠溶液与氢氧化钡溶液反应的实验,
反.应后都进行过滤得到无色滤液,他们对自己得到的无色滤液中溶质的成分进行探究。
请你一同参与他们的探究活动
【提出猜想】他们各自所得滤液中溶质的成分有如下几种可能:
A.NaOH B.Na CO、Ba(OH) 、NaOH
2 3 2
C. _ D. NaCO 和NaOH
2 3【讨论交流】上述猜想中,肯定不成立的是 (填猜想序号),其理由是
。
【实验探究】甲、乙两同学为了验证各自所得滤液的成分,分别进行了如下实验:
实验操作 实验现象 实验结论
甲同 取少量滤液于试管中,加入足量的 _ _ 滤液中溶质的成分与
_
学 溶液 猜想C对应
乙同 取少量滤液于试管中,加入足量的 无明显实 滤液中溶质的成分与
学 NaCO 溶液 验现象 猜想A 对应
2 3
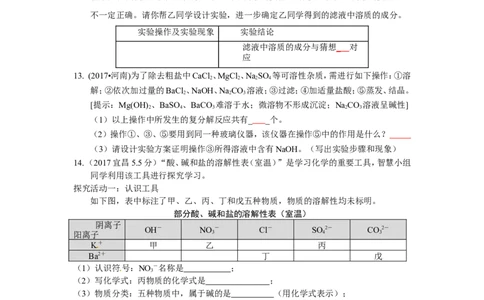
【反思与评价】经过讨论,大家一致认为甲同学的实验结论是正确的,乙同学的实验结论
不一定正确。请你帮乙同学设计实验,进一步确定乙同学得到的滤液中溶质的成分。
实验操作及实验现象 实验结论
滤液中溶质的成分与猜想 _ 对
应
13. (2017•河南)为了除去粗盐中CaCl 、MgCl 、NaSO 等可溶性杂质,需进行如下操作:①溶
2 2 2 4
解;②依次加过量的BaCl 、NaOH、NaCO 溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。
2 2 3
[提示:Mg(OH) 、BaSO、BaCO 难溶于水;微溶物不形成沉淀;NaCO 溶液呈碱性]
2 4 3 2 3
(1)以上操作中所发生的复分解反应共有_ _个。
(2)操作①、③、⑤要用到同一种玻璃仪器,该仪器在操作⑤中的作用是什么?
(3)请设计实验方案证明操作③所得溶液中含有NaOH。(写出实验步骤和现象)
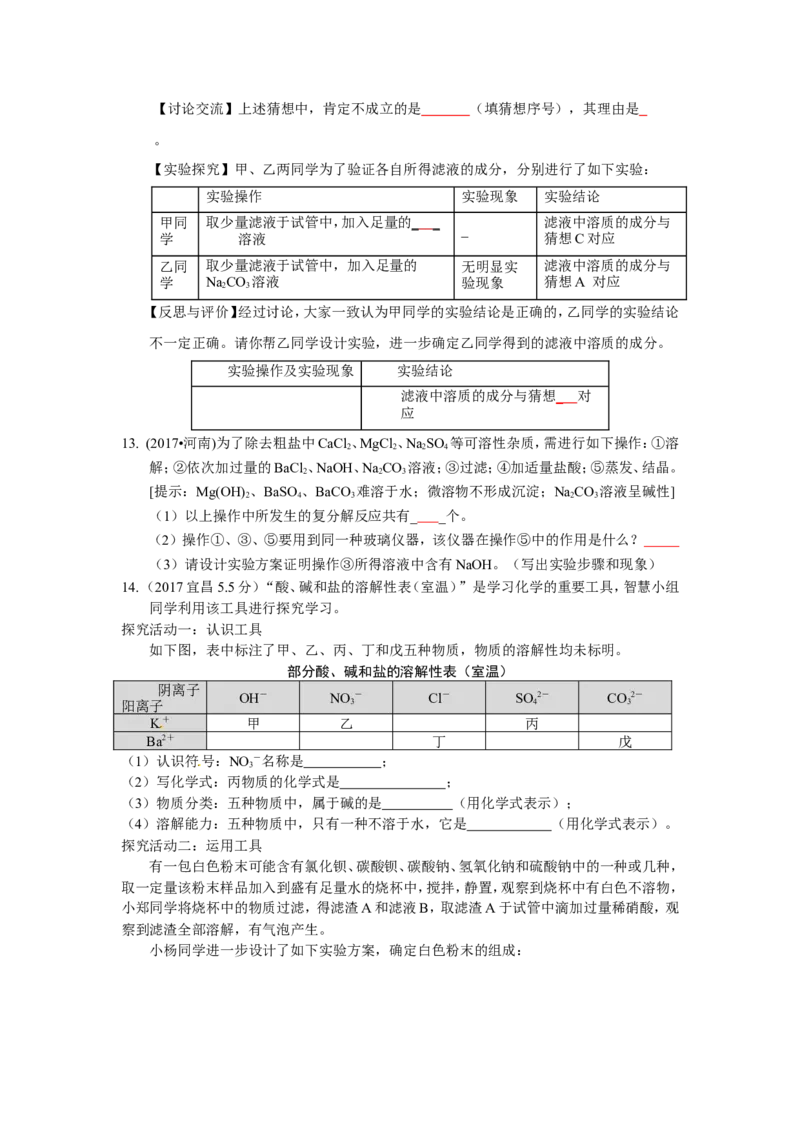
14. (2017宜昌5.5分)“酸、碱和盐的溶解性表(室温)”是学习化学的重要工具,智慧小组
同学利用该工具进行探究学习。
探究活动一:认识工具
如下图,表中标注了甲、乙、丙、丁和戊五种物质,物质的溶解性均未标明。
部分酸、碱和盐的溶解性表(室温)
阴离子
OH- NO - Cl- SO2- CO2-
阳离子 3 4 3
K+ 甲 乙 丙
Ba2+ 丁 戊
(1)认识符号:NO -名称是 ;
3
(2)写化学式:丙物质的化学式是 ;
(3)物质分类:五种物质中,属于碱的是 (用化学式表示);
(4)溶解能力:五种物质中,只有一种不溶于水,它是 (用化学式表示)。
探究活动二:运用工具
有一包白色粉末可能含有氯化钡、碳酸钡、碳酸钠、氢氧化钠和硫酸钠中的一种或几种,
取一定量该粉末样品加入到盛有足量水的烧杯中,搅拌,静置,观察到烧杯中有白色不溶物,
小郑同学将烧杯中的物质过滤,得滤渣A和滤液B,取滤渣A于试管中滴加过量稀硝酸,观
察到滤渣全部溶解,有气泡产生。
小杨同学进一步设计了如下实验方案,确定白色粉末的组成:滤液 步骤一 混合物 步骤二 混合物 步骤三 混合物
B C D E
加过量硝酸钡溶液 滴加少量酚酞溶液 滴加过量稀硝酸
针对上述实验方案中各步骤的现象,小杨同学提出下列三种不同的假设,依据每种假设
中各步骤不同的实验现象,可得出不同的实验结论。
步骤一 步骤二 步骤三
假设一 有白色沉淀生成
假设二 无白色沉淀生成 溶液变红 溶液变为无色
假设三 无白色沉淀生成 无明显现象 无明显现象
(1)依据假设一的现象,可确定原白色粉末中只含有碳酸钡、碳酸钠、氢氧化钠和硫酸钠四种
物质。则步骤二的现象是 ;步骤三的现象是 ;步骤三中发
生的任意一个化学反应的化学方程式是 。
(2)依据假设二的现象,原白色粉末可能的组成是 ;(任写一种可能的组成,
用化学式表示)
(3)依据假设三的现象,原白色粉末可能的组成有 种。
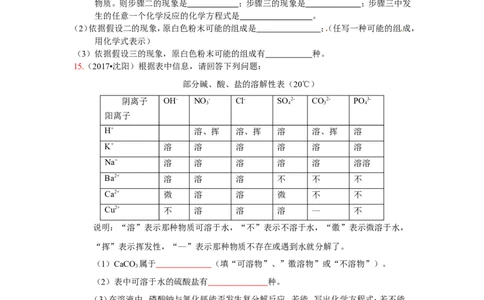
15.(2017•沈阳)根据表中信息,请回答下列问题:
部分碱、酸、盐的溶解性表(20℃)
阴离子 OH- NO - Cl- SO 2- CO2- PO 3-
3 4 3 4
阳离子
H+ 溶、挥 溶、挥 溶 溶、挥 溶
K+ 溶 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶 溶溶
Ba2+ 溶 溶 溶 不 不 不
Ca2+ 微 溶 溶 微 不 不
Cu2+ 不 溶 溶 溶 — 不
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“徽”表示微溶于水,
“挥”表示挥发性,“—”表示那种物质不存在或遇到水就分解了。
(1)CaCO 属于 (填“可溶物”、”徽溶物”或“不溶物”)。
3
(2)表中可溶于水的硫酸盐有 种。
(3)在溶液中,磷酸钠与氯化钙能否发生复分解反应。若能,写出化学方程式;若不能,
说明理由。_
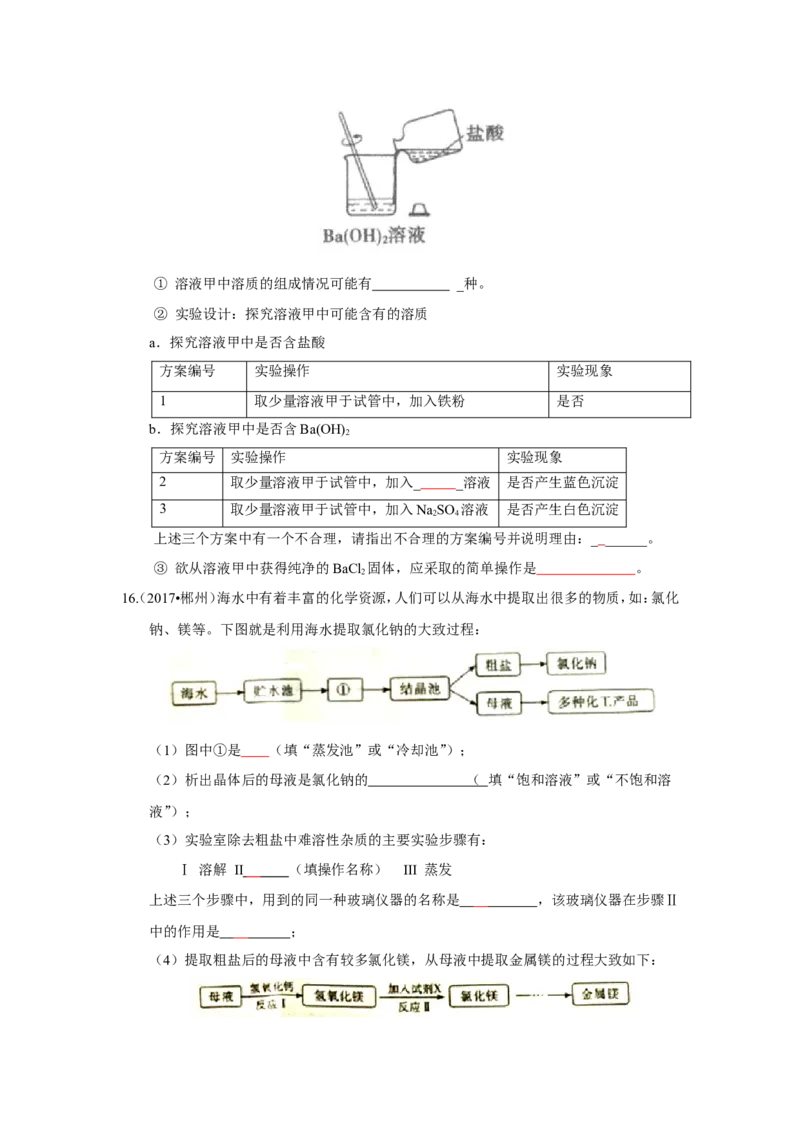
(4)某同学将盐酸倒入Ba(OH) 溶液中,得到溶液甲。
2① 溶液甲中溶质的组成情况可能有 _种。
② 实验设计:探究溶液甲中可能含有的溶质
a.探究溶液甲中是否含盐酸
方案编号 实验操作 实验现象
1 取少量溶液甲于试管中,加入铁粉 是否
b.探究溶液甲中是否含Ba(OH)
2
方案编号 实验操作 实验现象
2 取少量溶液甲于试管中,加入_ _溶液 是否产生蓝色沉淀
3 取少量溶液甲于试管中,加入NaSO 溶液 是否产生白色沉淀
2 4
上述三个方案中有一个不合理,请指出不合理的方案编号并说明理由:_ ______。
③ 欲从溶液甲中获得纯净的BaCl 固体,应采取的简单操作是 。
2
16(. 2017•郴州)海水中有着丰富的化学资源,人们可以从海水中提取出很多的物质,如:氯化
钠、镁等。下图就是利用海水提取氯化钠的大致过程:
(1)图中①是 (填“蒸发池”或“冷却池”);
(2)析出晶体后的母液是氯化钠的 ( 填“饱和溶液”或“不饱和溶
液”);
(3)实验室除去粗盐中难溶性杂质的主要实验步骤有:
Ⅰ 溶解 Ⅱ (填操作名称) Ⅲ 蒸发
上述三个步骤中,用到的同一种玻璃仪器的名称是 ,该玻璃仪器在步骤Ⅱ
中的作用是 ;
(4)提取粗盐后的母液中含有较多氯化镁,从母液中提取金属镁的过程大致如下:该过程中反应Ⅰ的基本反应类型是 ;
写出反应Ⅱ的化学方程式为 。
参考答案:
1. B 2. A 3. B 4. C 5. D6. A 7. C 8. D 9. A 10 D
11. (1) 调零。(2) 除尽样品中的BaCl ,未用玻璃棒引流 、 漏斗下端管口未紧贴烧杯
2
内壁。(3) abc(4) 58.4% 。
12. 【提出猜想】Ba(OH)、NaOH
2
【讨论交流】B, NaCO 和Ba(OH) 能发生反应/NaCO 和Ba(OH) 不能共存。
2 3 2 2 3 2
【实验探究】NaCO 溶液 , 产生白色沉淀
2 3
【反思与评价】加入Ba(OH) 溶液、A
2
13. (1)六(2)搅拌,使受热均匀
(3)取③所得溶液,加入足量的BaCl 溶液,静置,向上层清液中滴加无色酚酞溶液,若
2
溶液变红色,则溶质中含有NaOH。
14. 探究活动一:(1)硝酸根 (2)KSO (3)KOH (4)BaCO (5)BaCl 和KSO
2 4 3 2 2 4
探究活动二:
(1)步骤二:溶液由无色变成红色
步骤三:溶液由红色变成无色,有气泡产生,沉淀部分溶解
BaCO + 2HNO = Ba(NO) + HO + CO↑
3 3 3 2 2 2
或NaOH + HNO = NaNO + HO
3 3 2
(2)NaOH BaCO;NaOH BaCl NaCO;NaOH BaCl BaCO;
3 2 2 3 2 3
NaOH BaCO NaCO BaCl;(任写一种可能的组合)(3)4
3 2 3 2
15.(1)不溶物(2)3。(3)_2NaPO+3CaC1=Ca(PO)↓+6NaCl
3 4 2 3 4 2
(4)①3②a.有气泡产生 b. CuCl
2
3,溶液中含有BaCl,不论是否含有Ba(OH) 均会产生白色沉淀_。
2 2
③测溶液甲的pH,若pH ≤7,蒸发结晶;若pH > 7,向溶液甲中加入盐酸至溶液pH
≤7,再蒸发结晶。。
16.(1)蒸发池;(2)饱和溶液;(3)过滤;玻璃棒;引流;
(4)复分解反应;Mg(OH)+2HCl=MgCl+2HO 。
2 2 2