文档内容
化学人教九年级下第十一单元 盐 化肥单元检测
(时间:45分钟 满分:100分)
一、快乐点击(每小题3分,共30分)
1.下列各种变化,属于化学变化的是( )。
2.(2011·江西中考)下列购买的物质中不能作为氮肥使用的是( )。
A.硫酸铵[(NH )SO ] B.氨水(NH ·H O)
4 2 4 3 2
C.硝酸(HNO) D.尿素[CO(NH)]
3 2 2 [来源:学_科_网Z_X_X_K]
3.(2011·江苏徐州中考)盐在日常生活中是用途非常广泛的一类物质。下列说法中不正
确的是( )。
A.添加大量的亚硝酸钠来保鲜食品 B.硝酸钾在农业上可用作复合肥
C.农业上常用硫酸铜配制波尔多液 D.用纯碱除去面粉发酵生成的酸
4.下列物质的名称、俗名与化学式完全对应的是( )。
A.氯化钠 食盐 NaCl B.碳酸氢钠 纯碱 NaHCO
3
C.氢氧化钙 熟石灰 CaO D.氢氧化钠 火碱 NaOH
5.下列离子组能在pH=1的无色溶液中大量共存的是( )。
A. Fe3+ Na+ OH- B.K+ Na+
C.Cl- K+ Ba2+ D.Ca2+ Cl- Na+
6.下列化学方程式中属于复分解反应的是( )。
A.C+O 点燃,CO B.2HO通电,2H ↑+O↑
2 2 2 2 2
C.3CO+Fe O 高温,2Fe+3CO D.HCl+AgNO,AgCl↓+HNO
2 3 2 3 3
7.(2011·四川眉山中考)图表资料可以为我们提供许多信息。下列对图表资料的使用能
达到目的的是( )。
A.根据某元素的原子结构示意图推断该元素原子核内的中子数
B.根据酸、碱、盐的溶解性表可推知离子间能否在溶液中共存
C.根据元素的相对原子质量表查出某元素的质量
D.根据元素周期表查出某元素在地壳中的含量
8.根据复分解反应的发生条件,判断下列各组物质不能发生反应的一组是( )。
A.NaCO 溶液和CaCl 溶液 B.NaOH溶液和盐酸
2 3 2
C.CuSO 溶液和BaCl 溶液 D.KSO 溶液和NaCl溶液
4 2 2 4
9.硫酸厂的污水中含有硫酸,直接排放会导致河流水质酸化,加入下列物质不能解决问
题的是( )。
A.NaOH B.Ca(OH) C.BaCl D.CaO
2 2
10.某白色粉末可能含有NaOH、NaCO、NaSO 、NaCl中的一种或几种。为探究白色粉
2 3 2 4
末的性质,将该粉末放入足量水中,充分搅拌后,把所得溶液分为三份进行实验:
(1)第一份溶液中滴加酚酞溶液后,溶液呈红色
(2)第二份溶液中滴加稀盐酸后,开始无明显现象,随着盐酸的滴入逐渐有气泡产生
(3)第三份溶液中滴加BaCl 后有白色沉淀生成,过滤,所得沉淀全部溶于稀盐酸
2
分析实验得出的以下结论,合理的是( )。
A.一定含有NaCO,一定没有NaSO 、NaCl,可能含有NaOH
2 3 2 4 [来源:学科网]
B.一定含有NaCO,一定没有NaSO 、NaOH,可能含有NaCl
2 3 2 4
C.一定含有NaOH、NaCO,一定没有NaSO ,可能含有NaCl
2 3 2 4
D.一定含有NaCO、NaCl,一定没有NaSO ,可能含有NaOH
2 3 2 4
二、积累运用(本题包括4小题,共30分)
11.(4分)下列物质①熟石灰、②碳酸钠、③氯化钠、④碳酸钙、⑤碳酸氢钠、⑥氢氧化铝、
⑦稀盐酸等,在生产生活中有广泛用途,请按下列要求填空(填序号)。
(1)农业中用来降低土壤酸性,改良土壤结构的是____________;
(2)用于造纸、玻璃、印染、洗涤剂的是______;
(3)常用于面制品发酵的是____________;(4)天安门前的华表,其主要成分是________。
12.(8分)(1)按要求写出下列物质的化学式及类别(填单质、氧化物、酸、碱、盐)。
物质 铁 熟石灰 纯碱 小苏打 生石灰
化学式
类别
(2)选用上面物质写一个符合下列要求的化学方程式(每种物质只用一次)。
复分解反应_______________________________________________。
13.(8分)请根据酸、碱、盐的相关知识,回答下列问题:
(1)农业上常用于改良酸性土壤的一种碱是_______________________________。
(2)胃液中含有适量的盐酸。由于胃酸过多而引起的胃痛,可服用含有Mg(OH) 的药物来
2
中和过多的胃酸,发生反应的化学方程式为______________________________。
(3)用水鉴别NaOH、NaCl、CaCO 三种固体物质时,能够鉴别出NaOH固体所依据的现
3
象是__________________________________。
(4)探究稀盐酸、NaCO 溶液、Ca(OH) 溶液之间能否发生化学反应时,将所有溶液倒入
2 3 2
同一洁净烧杯中。除指示剂外,最终烧杯中一定含有的一种溶质是________。
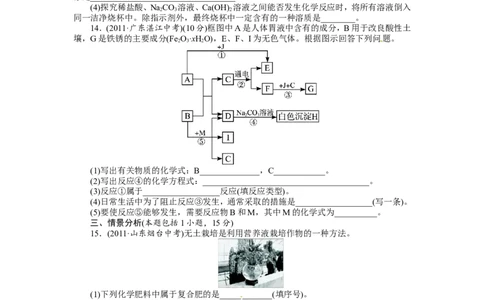
14.(2011·广东湛江中考)(10分)框图中A是人体胃液中含有的成分,B用于改良酸性土
壤,G是铁锈的主要成分(Fe O·xHO),E、F、I为无色气体。根据图示回答下列问题。
2 3 2
(1)写出有关物质的化学式:B______________,C____________。
(2)写出反应④的化学方程式:_______________________________________。
(3)反应①属于__________________反应(填反应类型)。
(4)日常生活中为了阻止反应③发生,通常采取的措施是__________________(写一条)。
(5)要使反应⑤能够发生,需要反应物B和M,其中M的化学式为__________。
三、情景分析(本题包括1小题,15分)
15.(2011·山东烟台中考)无土栽培是利用营养液栽培作物的一种方法。
[来源:学科网ZXXK]
(1)下列化学肥料中属于复合肥的是____________(填序号)。
①硝酸铵 ②磷酸二氢铵 ③硝酸钾 ④硫酸钾
(2)某同学要在实验室配制150 g溶质的质量分数为2%的硝酸钾溶液,需要硝酸钾的质
量为____g。
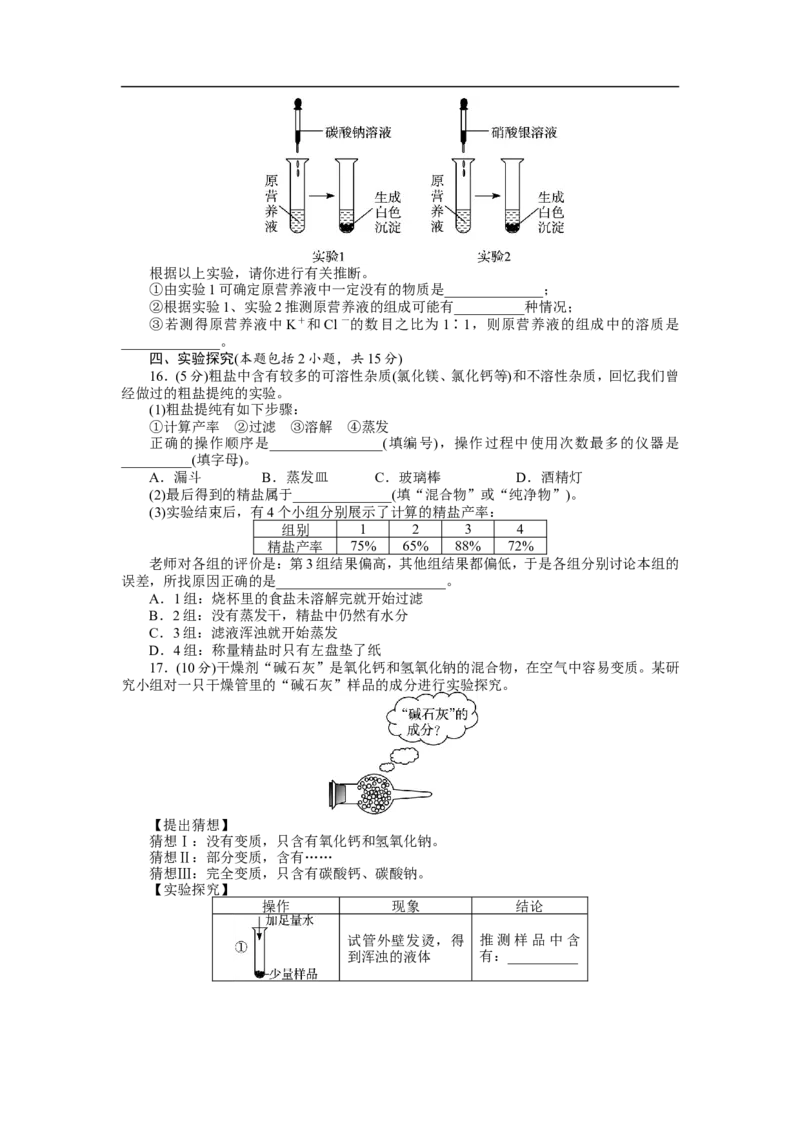
(3)现有一种无色的营养液,可能由KNO、Ca(NO )、KCO、KCl中的一种或几种物质组
3 3 2 2 3
成,为探究其成分,某同学设计并完成了如图所示的实验。根据以上实验,请你进行有关推断。
①由实验1可确定原营养液中一定没有的物质是______________;
②根据实验1、实验2推测原营养液的组成可能有__________种情况;
③若测得原营养液中K+和Cl一的数目之比为1∶1,则原营养液的组成中的溶质是
______________。
四、实验探究(本题包括2小题,共15分)
16.(5分)粗盐中含有较多的可溶性杂质(氯化镁、氯化钙等)和不溶性杂质,回忆我们曾
经做过的粗盐提纯的实验。
(1)粗盐提纯有如下步骤:
①计算产率 ②过滤 ③溶解 ④蒸发
正确的操作顺序是________________(填编号),操作过程中使用次数最多的仪器是
__________(填字母)。
A.漏斗 B.蒸发皿 C.玻璃棒 D.酒精灯
(2)最后得到的精盐属于______________(填“混合物”或“纯净物”)。
(3)实验结束后,有4个小组分别展示了计算的精盐产率:
组别 1 2 3 4
精盐产率 75% 65% 88% 72%
老师对各组的评价是:第3组结果偏高,其他组结果都偏低,于是各组分别讨论本组的
误差,所找原因正确的是________________________。
A.1组:烧杯里的食盐未溶解完就开始过滤
B.2组:没有蒸发干,精盐中仍然有水分
C.3组:滤液浑浊就开始蒸发
D.4组:称量精盐时只有左盘垫了纸
17.(10分)干燥剂“碱石灰”是氧化钙和氢氧化钠的混合物,在空气中容易变质。某研
究小组对一只干燥管里的“碱石灰”样品的成分进行实验探究。
[来源:Z,xx,k.Com]
【提出猜想】
猜想Ⅰ:没有变质,只含有氧化钙和氢氧化钠。
猜想Ⅱ:部分变质,含有……
猜想Ⅲ:完全变质,只含有碳酸钙、碳酸钠。
【实验探究】
操作 现象 结论
试管外壁发烫,得 推测样品中含
到浑浊的液体 有:__________写出产生大量气
滤渣溶解,产生大
泡的化学方程
量气泡
式:__________
写出产生白色沉
产生白色沉淀 淀的化学方程
式:__________
【小结与思考】
(1)从上述实验现象推断:猜想________成立。
(2)“碱石灰”样品里是否一定含有碳酸钙?请说明理由。
________________________________________________________________________。
五、计算应用(本题包括1小题,10分)
[来源:学.科.网Z.X.X.K]
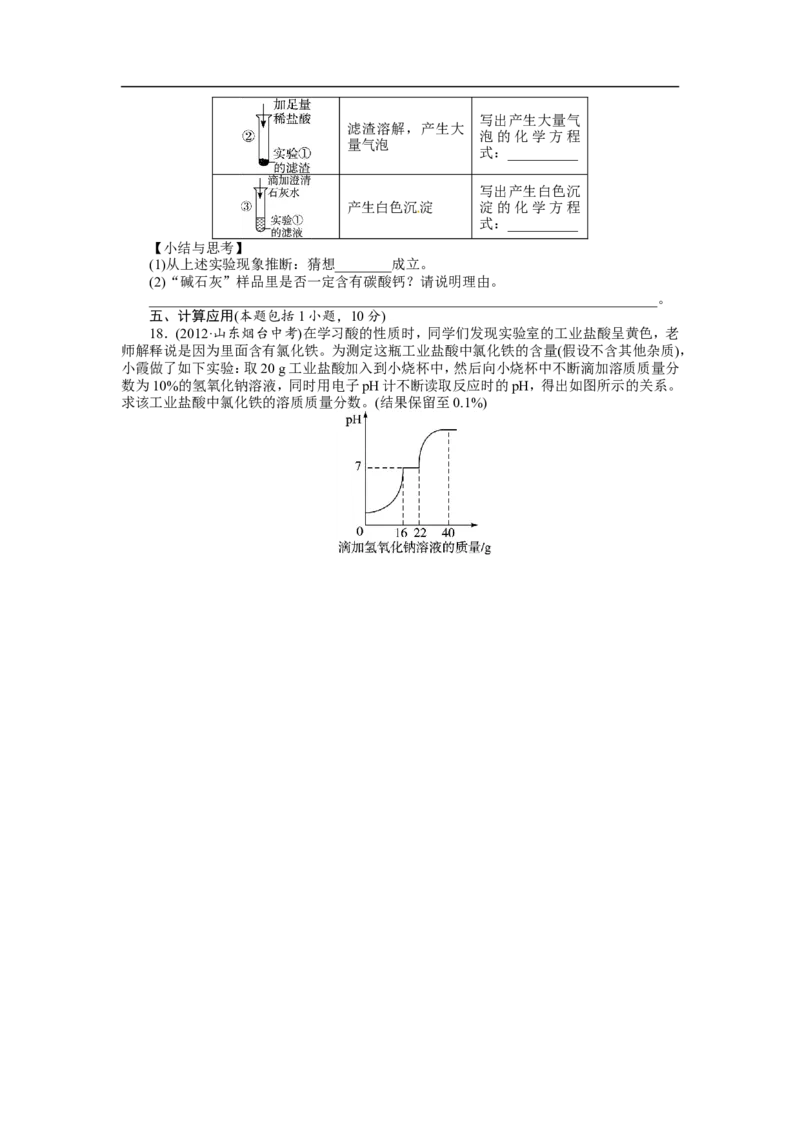
18.(2012·山东烟台中考)在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老
师解释说是因为里面含有氯化铁。为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),
小霞做了如下实验:取20 g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分
数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系。
求该工业盐酸中氯化铁的溶质质量分数。(结果保留至0.1%)参考答案
1. 答案:D
2. 答案:C
3. 答案:A
4. 答案:AD
5. 解析:pH=1的溶液为酸性溶液,A选项中的OH-,D选项中的 不能与H+共存,
故可排除;C选项中 、Ba2+能结合为BaSO 沉淀,故可排除。
4
答案:B
6. 解析:复分解反应是指两种化合物相互交换成分,生成另外两种化合物的反应。A属
于化合反应,B属于分解反应,C是氧化还原反应,不属于基本化学反应类型,D中HCl和
AgNO 相互交换成分,生成AgCl和HNO,属于复分解反应。
3 3
答案:D
7. 解析:元素的原子结构示意图中没有中子数的信息;根据酸、碱、盐的溶解性表可推
知离子间能否反应生成气体、沉淀或水,即能判断反应是否能发生;元素的相对原子质量表
中没有某元素的质量;元素周期表中没有元素在地壳中的含量。
答案:B
8. 解析:复分解反应发生的条件是有气体、沉淀或水生成。A选项中生成碳酸钙沉淀,B
选项中生成水,C选项中生成硫酸钡沉淀,它们都能发生复分解反应;D选项不具备复分解反
应发生的条件,不能发生反应。
答案:D
9. 解析:
A √ 2NaOH+HSO ===Na SO +2HO 酸性减弱
2 4 2 4 2
B √ Ca(OH) +HSO ===CaSO +2HO 酸性减弱
2 2 4 4 2
C × BaCl +HSO ===BaSO ↓+2HCl 酸性几乎不变
2 2 4 4
D √ CaO+HSO ===CaSO +HO 酸性减弱
2 4 4 2
答案:C
10. 解析:“第一份溶液中滴加酚酞溶液后,溶液呈红色”说明溶液呈碱性,则可能有
NaOH或NaCO。“第二份溶液中滴加稀盐酸后,开始无明显现象,随着盐酸的滴入逐滴有
2 3
气泡产生”说明NaOH和NaCO 同时存在,滴入稀盐酸后,盐酸先与NaOH反应,所以开始
2 3
无现象,然后再与NaCO 反应,产生气泡。“第三份溶液中滴加BaCl 后有白色沉淀生成”,
2 3 2
沉淀可能为:①BaCO ,②BaSO,③BaCO 和BaSO 混合物,根据“过滤,所得沉淀全部溶
3 4 4 4
于稀盐酸”,则确定沉淀有BaCO ,无BaSO,因此一定无NaSO 。
3 4 2 4
答案:C
11. 答案:(1)① (2)② (3)⑤ (4)④
12. 答案:(1)Fe 单质 Ca(OH) 碱 NaCO 盐 NaHCO 盐 CaO 氧化物
2 2 3 3
(2)Na CO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
13. 答案:(1)氢氧化钙〔或熟石灰或消石灰或Ca(OH) 〕
2
(2)Mg(OH) +2HCl===MgCl +2HO
2 2 2
(3)溶解放热(或放热或温度升高)
(4)氯化钠(或NaCl)
14. 解析:本题是一道推断题,解题的关键是根据文字和图像信息寻找有用的突破口。A
是人体胃液中含有的成分,可判断A为盐酸,B用于改良酸性土壤,可判断B为Ca(OH) ,依
2
此为突破口,可推断其他物质。A和B发生的反应为2HCl+Ca(OH) ===CaCl +2HO,C通
2 2 2
电能分解,说明C为HO,则D为CaCl ,④为CaCl 溶液与NaCO 溶液发生的反应:CaCl +
2 2 2 2 3 2
NaCO===CaCO ↓+2NaCl;反应③得到的是铁锈,可判断该反应为铁的生锈,则F为O,C
2 3 3 2
为HO,J为Fe,日常生活中为阻止铁生锈,主要方法是隔绝O 和HO,具体方法有刷油漆、
2 2 2
涂油等;通过以上分析可知,①为铁与稀盐酸发生的置换反应;在初中教材中,能与Ca(OH)
2
反应生成三种物质的反应只有一类,即Ca(OH) 与铵盐的反应,可判断该铵盐为NH Cl。
2 4
答案:(1)Ca(OH) HO
2 2
(2)CaCl +NaCO===CaCO ↓+2NaCl
2 2 3 3(3)置换 (4)刷油漆(或涂油等)
(5)NH Cl
4
15. 解析:(1)复合肥料是指含有两种或两种以上营养元素的化肥,磷酸二氢铵含有N、P
两种营养元素,硝酸钾中含有N、K两种元素,因此都属于复合肥。(2)硝酸钾的质量=150
g×2%=3 g。(3)①滴入NaCO 溶液后产生了白色沉淀说明营养液中有Ca(NO ) 无KCO,
2 3 3 2 2 3
因为Ca(NO ) 和KCO 同时存在会发生反应生成CaCO 沉淀。②实验2中滴入硝酸银溶液
3 2 2 3 3
产生白色沉淀说明该营养液肯定含KCl,由此推出原营养液的组成可能为Ca(NO )、KCl或
3 2
Ca(NO )、KCl、KNO 两种情况。③原营养液中K+和Cl-的数目之比为1∶1,则营养液的组
3 2 3
成不可能为Ca(NO )、KCl、KNO,因为此组成中K+的数目会多于Cl-的数目。
3 2 3
答案:(1)②③ (2)3 (3)①KCO ②2 ③KCl、Ca(NO )
2 3 3 2
16. 解析:(1)粗盐提纯的正确操作步骤为:溶解、过滤、蒸发、计算产率,在四步操作中都
需用到玻璃棒。(2)最后得到的精盐中还含有氯化镁、氯化钙等可溶性杂质,属于混合物。(3)
精盐产率偏低的原因包括:食盐未全部溶解就过滤,使部分食盐损失,A正确;若未蒸发干就
进行称量,会导致产率偏高,B错误;滤液仍浑浊就蒸发会导致精盐的质量偏高,使结果偏高,
C正确;若称量精盐时只在左盘中垫纸会导致精盐的质量高于理论值,使结果偏高,D错误。
答案:(1)③②④① C (2)混合物 (3)AC
17. 解析:在①中的少量样品中,加入足量水,结果试管壁发烫,并且得到了浑浊的液体,
说明样品与水反应放热或溶于水放热,因此样品中有氧化钙或氢氧化钠固体或者氧化钙和
氢氧化钠的混合物;在②中,实验①有剩余的滤渣,加入稀盐酸后,生成气体,说明该滤渣一
定是碳酸钙,因为①中加入了足量的水;在③中,滴加氢氧化钙溶液,产生白色沉淀,说明一
定存在碳酸钠。
答案:①氧化钙或氢氧化钠或氧化钙和氢氧化钠(答名称或化学式均可)
②CaCO +2HCl===CaCl +HO+CO↑
3 2 2 2
③NaCO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
(1)Ⅱ
(2)不一定有碳酸钙。因为样品中若有氢氧化钙(或氧化钙),也会在加水时与碳酸钠生成
碳酸钙
18. 解析:分析图像每一段所发生的反应。用氢氧化钠测定盐酸中氯化铁的质量分数,要
注意加入的氢氧化钠首先与盐酸反应,从图像可以看出加入16 g氢氧化钠溶液之前,pH是
不断增大的,这一段是氢氧化钠与盐酸反应;从16 g到22 g是氢氧化钠与氯化铁的反应,所
以在计算时,与氯化铁反应的氢氧化钠溶液的质量是6 g,再进行下面的计算就简单多了。
答案:解:根据图中信息可知:
与氯化铁反应的氢氧化钠溶液的质量为22 g-16 g=6 g
设:20 g该工业盐酸中氯化铁的质量为x
FeCl +3NaOH===Fe(OH) ↓+3NaCl
3 3
162.5 120
x 6 g×10%
= x=0.812 5 g
该工业盐酸中氯化铁的质量分数为 ×100%≈4.1%
答:该工业盐酸中氯化铁的质量分数为4.1%。