文档内容
第八单元 测试题
一、我会选(14分)
( )1.下列物质属于纯净物的是
A.生铁 B.钢 C.赤铁矿 D.金刚石
( )2.铁元素的化合价由低到高的排列正确的是
A.Fe(OH) Fe O Fe B.Fe(NO) Fe FeCl
2 2 3 3 2 3
C.Fe FeO Fe O D.Fe(OH) FeSO FeCl
2 3 3 4 3
( )3.下列有关铁生锈的叙述错误的是
A.铁生锈时一定伴随物理变化 B.铁生锈时,铁发生了缓慢氧化
C.铁生锈的实质是铁与空气中氧气反应,生成氧化铁
D.铁生锈时会有难以察觉的热量放出
( )4.要除去铜粉中混有的少量铁粉,下列物质不合适的是
A.稀硫酸 B.稀盐酸 C.CuSO 溶液 D.HO
4 2
( )5.把一根洁净的铁钉放入稀硫酸中,下列叙述正确的是
①在铁钉表面产生气泡 ②溶液由无色逐渐变为浅绿色 ③铁钉的质量增加 ④
溶液的质量减轻
A.②③ B.①②③ C.①②④ D.①②
( )6、下面物质中,能用金属和酸直接反应得到的是
A、MgCl B、Al (SO ) C、ZnCl D、Fe (SO )
2 2 4 3 2 2 4 3
( )7.被雨水淋湿的自行车,应
A.先用布擦干,再用带油的布擦拭 B.在自行车表面刷一层油漆
C.用布擦干即可 D.晾干后,用盐酸除去锈层
( )8.下列有关金属说法正确的是
A.铝在空气中能生成一层致密的氧化物保护膜
B.铜的化学性质不活泼,在潮湿的空气中也不生锈
C.钛具有耐腐蚀性,可用来制造海轮的外壳
D.镀锌的“白铁皮”不易生锈,说明锌没有铁活泼
( )9.不法分子常常用金光闪闪的“金元宝”(铜锌合金)来蒙骗人们,下列鉴别方法中
错误的是
A.加盐酸 B.测密度 C.用火烧 D.看颜色
( )10.下列反应方程式中正确的是 ( )
A.4Fe+3O2 2Fe2O3 B.2Fe+6HCl=2FeCl3+3H2↑
C.3CuSO4+2Fe=Fe2(SO4)3+3Cu D.Fe+H2SO4=FeSO4+H2↑
( )11.将X、Y、Z三种金属分别投入足量的稀硫酸中,只有X、Z能发生反应,
并放出氢气。将Z投入X的硝酸盐溶液中,有金属X产生。则X、Y、Z三种金属的活
动性由强到弱的顺序为
A、Z>Y>X B、Z>X>Y C、X>Z>Y D、T>Z>X
( )12.在下列溶液中分别放入锌粒,一段时间后把锌粒取出,溶液质量减少的是
A、MgCl 溶液 B、盐酸 C、稀硫酸 D、AgNO 溶液
2 3
( )13.将过量的铁粉放入含AgNO 和Zn(NO ) 的混合溶液里,搅拌,使其充分反应后
3 3 2
过滤,滤纸上留下的金属是
A、Ag B、Fe、Zn C、Fe、Ag D、Ag、Zn、Fe
( )14.有下列三组试剂①锌、银、硝酸铜溶液②银、硝酸锌溶液、硫酸铜溶液③铜、硫酸锌溶
1液、硝酸银溶液,能用来验证金属活动性:锌>铜>银的试剂组有
A、①和② B、①和③ C、②和③ D、只有③
二、我会填(每空0.5分,共8分)
15.铁生锈,实际上是 、
和 等物质相互作用,发生氧化的过程,因此铁锈中至少含
有 等元素。防止铁制品生锈,除了要保持铁制品表面
和 外,最常用的方法 。
16.炼铁的主要反应原理是在 的 条件下,用 从含铁
的矿石中将铁还原出来,常见的铁矿石有(填主要成分):赤铁矿 ,磁铁
矿 等。黄铁矿的主要成分是FeS,它不太适合炼铁,其原因是:
2
。
17.在日常生活中,我们有很多的做法都是在不自觉中运用了金属的某些性质,如:烧
菜用的铲勺是铁制的,但一般都要装木柄,是因为铁具有 性;铁块
可以制成铁丝,是利用它的 性;做电线时铝比铁好,说
明 ;用钛合金做轮船外壳而不选钢材,反映
出 。
三、我会设计(每空1分,共25分)
18、完成金属活动性顺序并填空:
K Ca Na Mg Zn Sn Pb (H) Hg Pt Au
(1)在金属活动性顺序中,金属越 化学性质越活泼;
(2)在金属活动性顺序中, 的金属可置换出酸中的氢元素;
(2)在金属活动性顺序中, 的金属能把 的金属从它们的
化合物溶液中置换出来。
19.我国西汉时期就开始冶炼铜,方法是先用硫酸与氧化铜作用生成水和硫酸铜,再用
铁置换出硫酸铜中的铜,称为“湿法炼铜”,写出上述两步反应的化学方程式:
;
。
20.铁的化合物在化学反应中,通常发生颜色变化,依照示例写出有关铁及化合物有颜
色变化的三例化学方程式。
示例:Fe+CuSO===FeSO+Cu,反应中,溶液由蓝色变为浅绿色,且铁表面有一层红色
4 4
物质生成。
①在 反应
中 。
21.经研究发现,长期使用我国铁锅炒菜做饭,可有效减少缺铁性贫血,原因是
;有经验的厨师在炒菜时还加入适量的食用醋,认为效果会更好,理由
。
22、判断下列反应能否发生,若能请写出化学方程式:
(1)铝与稀硫酸 ;(2)银与稀盐酸
(3)铁与硫酸锌 ;(4)铜与硝酸银
23、向含有ZnSO 和CuSO 的溶液中加入一定量的铁粉,充分反应后过滤,则滤纸上
4 4
的固体中一定含有的物质是 ,可能含有的是 .
24、除去下列物质中的杂质(括号内的物质为杂质)
化学方程式 操作步骤
铜粉(铁粉)
FeSO (CuSO )
4 4
225、铝桶不能用来盛放波尔多液(含有硫酸铜),原因是(用化学方程式表示)
_____________________________________________________
四、我会探究(5分)
26.下列是某种金属的部分性质。
颜色、状态 硬度 密度 熔点 延展性 导电、导热 耐腐蚀
银白色固体 较硬 4.5 g/cm3 高 好 好 好
该金属加入到稀盐酸中无气泡产生。
①试推断该金属的化学性质
。
②该金属可能有的几种用途是
。
③请自选化学试剂设计实验,探究该金属的化学活动性与铁比较的强弱。
你的猜想 验证方法 现象和结论
该金属的化
学活动性比铁
四、我会计算(4+4=8分) Fe-56 O-16 Zn-65 H-1
27.100 t含80%的赤铁矿石能冶炼出含杂质3%的生铁多少吨?
28.将10g黄铜(铜、锌合金)加入足量的稀盐酸中,充分反应后,共生成0.1g气体,则
该黄铜中铜的质量分数是多少?
附加题:
31.有关金属资源的叙述错误的是( )
A.地球上金属资源大多数以化合物形式存在 B.目前世界年产量最高的金属是铁
C.保护金属资源的惟一途径是防止金属的腐蚀 D.地球的金属资源是有限的,而
且不能再生
2.在地壳中,铁元素常以 形式存在,原因
是 ;在铁合金中,铁元素以 形式存在,铁元
素的化合价为 。
3.一工业废水中含有大量的硫酸亚铁、少量的硫酸铜及不溶性杂质,试设计一种经济
简便的分离方案,并说明每一步骤的目的。(不必写出化学方程式,其中少数步骤的目的已
写出,表中空格可不填满,也可增加)
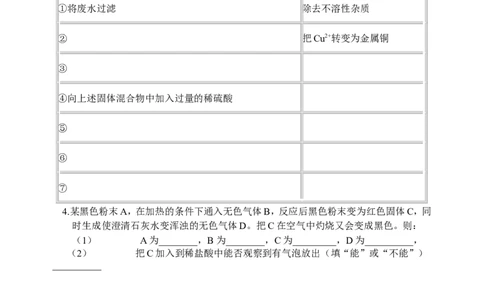
实验步骤 实验目的
①将废水过滤 除去不溶性杂质
② 把Cu2+转变为金属铜
③
④向上述固体混合物中加入过量的稀硫酸
⑤
⑥
⑦
4.某黑色粉末A,在加热的条件下通入无色气体B,反应后黑色粉末变为红色固体C,同
时生成使澄清石灰水变浑浊的无色气体D。把C在空气中灼烧又会变成黑色。则:
(1) A为________,B 为________,C为_________,D为__________,
(2) 把C加入到稀盐酸中能否观察到有气泡放出(填“能”或“不能”)
__________
4