文档内容
专项测试卷9
第九单元《溶液》
第一部分 溶液及溶液的溶质质量分数
1.(2016淄博)如图为实验室新购置的盐酸试剂瓶标签上的内容,用掉一部分盐酸后(忽
略盐酸的挥发),不能再表示试剂瓶中剩余盐酸信息的是( )
A.37% B.36.5 C.1.19g/cm3D.500mL
2.下列关于溶液的说法中正确的是( )
A.一杯糖水,下部分一定比上部分甜
B.溶液一定是无色的
C.均一、稳定的液体一定是溶液
D.食盐水是溶液,糖水也是溶液,将两者混合后仍然是溶液
3.关于溶液和乳化的下列说法 错误的是( )
A.溶液中可以含有多种溶质
B.溶液是均一、稳定的混合物
C.用汽油洗去衣服上的油污是乳化现象
D.溶液不一定是无色的
4. 衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如表所示:
溶质 碘
溶剂 水 酒精 汽油 苯(有毒)
溶解性 微溶 可溶 易溶 易溶
由表中提供的信息判断,洗净衣服上的碘污渍的最佳选择是( )
A. 水 B. 酒精 C. 汽油 D. 苯
5.下列关于溶液的说法中,正确的是( )
A. 溶液都是无色透明的液体 B. 洗洁精具有溶解作用,能去除餐具上的油污
C. 均一、稳定的物质都是溶液 D. 味精加入适量水后可以形成溶液
6.(2016常德)将100g 98%的浓硫酸注入900g水中,所得稀硫酸中溶质的质量分数为
( )
A.9.8% B.10.0%C.10.9%D.11.1%7..(2015福州)实验室用硝酸钾固体配制100.0 g溶质质量分数为3.0%的硝酸钾溶液,下列
说法正确的是 ( )
A. 用50mL量筒量水 B. 将固体放于托盘天平的右盘称取
C. 将固体直接投入量筒中溶解 D. 将配好的溶液装入贴有标签的试剂瓶中,塞好
瓶塞
8.实验室用蔗糖配制50.0g溶质的质量分数为10%的蔗糖溶液,下列说法错误的是( )
A.用托盘天平称取5.0g蔗糖
B.用量程为10mL的量筒量取所需的水
C.溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒
D.将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签[来源:学科网]
9.野外旅行时,根据季节可以带上“即热饭盒”或“化学冰箱”.“化学冰箱”即把一种化
学试剂放入容器中,加一定量的水,就可以形成低温小环境,这种试剂可以是下列物质中的(
)
A. 浓硫酸 B. 硝酸铵 C. 固体氢氧化钠 D. 食盐
10.溶液是自然界中常见的物质。下列有关溶液的说法正确的是( )
A.溶液的上层浓度小,下层浓度大
B.溶液蒸干后,均能得到固体溶质
C.溶液中只有一种溶质时,溶液为纯净物
D.物质在溶解得到溶液的过程中,通常有放热或吸热的现象出现
11.生活中的下列物质:(1)牛奶、(2)雪碧饮料、(3)矿泉水、(4)生理盐水、(5)豆浆、(6)蒸
馏水、(7)食醋、(8)蔗糖水、(9)链霉素粉末、(10)酒精、(11)碘酒、(12)60°的白酒、(13)
车用乙醇汽油、(14)10%的过氧乙酸、(15)医用酒精、(16)石灰浆、(17)清新洁净的空气。其
中不属于溶液的是 _;属于乳浊液的是_ _ ;属于纯净物的是 _
。
12. (2015盐城)盐城濒临黄海,海盐文化全国知名.某兴趣小组同学去盐场参观,带回了部
分粗盐样品,并对其进行了如下探究:
(1)操作①中必须用到的一种仪器是 (填序号)
A.研钵 B.量筒 C.烧杯 D.试管(2)操作③的名称是 ,操作④中用到玻璃棒,作用为 .
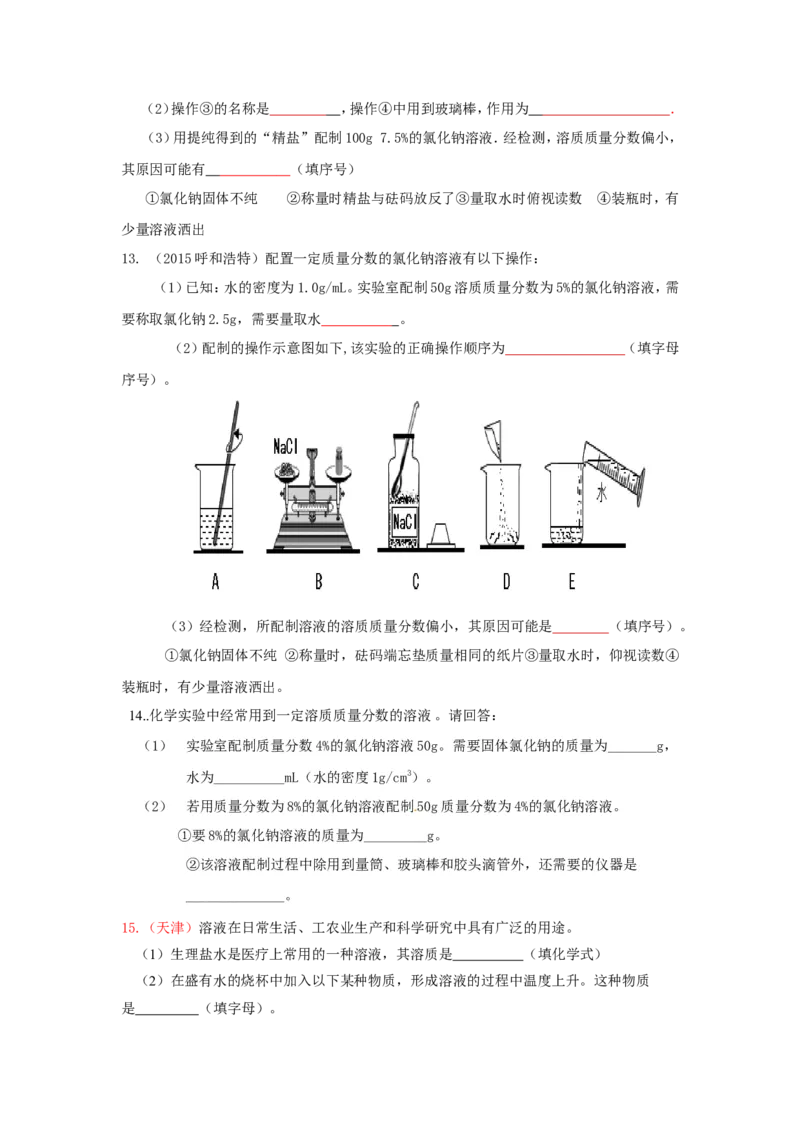
(3)用提纯得到的“精盐”配制100g 7.5%的氯化钠溶液.经检测,溶质质量分数偏小,
其原因可能有 (填序号)
①氯化钠固体不纯 ②称量时精盐与砝码放反了③量取水时俯视读数 ④装瓶时,有
少量溶液洒出
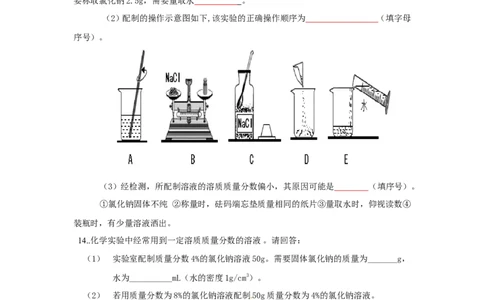
13. (2015呼和浩特)配置一定质量分数的氯化钠溶液有以下操作:
(1)已知:水的密度为1.0g/mL。实验室配制50g溶质质量分数为5%的氯化钠溶液,需
要称取氯化钠2.5g,需要量取水 。
(2)配制的操作示意图如下,该实验的正确操作顺序为 (填字母
序号)。
(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是 (填序号) 。
①氯化钠固体不纯 ②称量时,砝码端忘垫质量相同的纸片③量取水时,仰视读数④
装瓶时,有少量溶液洒出。
14..化学实验中经常用到一定溶质质量分数的溶液。请回答:
(1) 实验室配制质量分数4%的氯化钠溶液50g。需要固体氯化钠的质量为_______g,
水为__________mL(水的密度1g/cm3)。
(2) 若用质量分数为8%的氯化钠溶液配制50g质量分数为4%的氯化钠溶液。
①要8%的氯化钠溶液的质量为_________g。[来源:学。科。网]
②该溶液配制过程中除用到量筒、玻璃棒和胶头滴管外,还需要的仪器是
______________。
15.(天津)溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)生理盐水是医疗上常用的一种溶液,其溶质是 (填化学式)
(2)在盛有水的烧杯中加入以下某种物质,形成溶液的过程中温度上升。这种物质
是 (填字母)。A. 氯化钠 B. 硝酸铵 C. 氢氧化钠
(3)某同学在实验室用氯化钠固体和蒸馏水配制50g质量分数为6%的氯化钠溶液时,
涉及以下实验步骤:①溶解 ②称量和量取 ③计算 ④装入试剂瓶贴好标签。
配制上述溶液正确的实验步骤顺序是 (填序号)
(4)某注射用药液的配制方法如下:
①把1.0g药品溶于水配制成4.0mL溶液a;
②取0.1mL溶液a,加水稀释至1.0mL,得溶液b;
③取0.1mL溶液b,加水稀释至1.0mL,得溶液c;
④取0.4mL溶液c,加水稀释至1.0mL,得溶液d。
由于在整个配制过程中药液很稀,其密度都可近似看做1g/cm3。则最终得到的药液(溶液d)
中溶质的质量分数为 。
第二部分 饱和溶液与不饱和溶液及溶解度
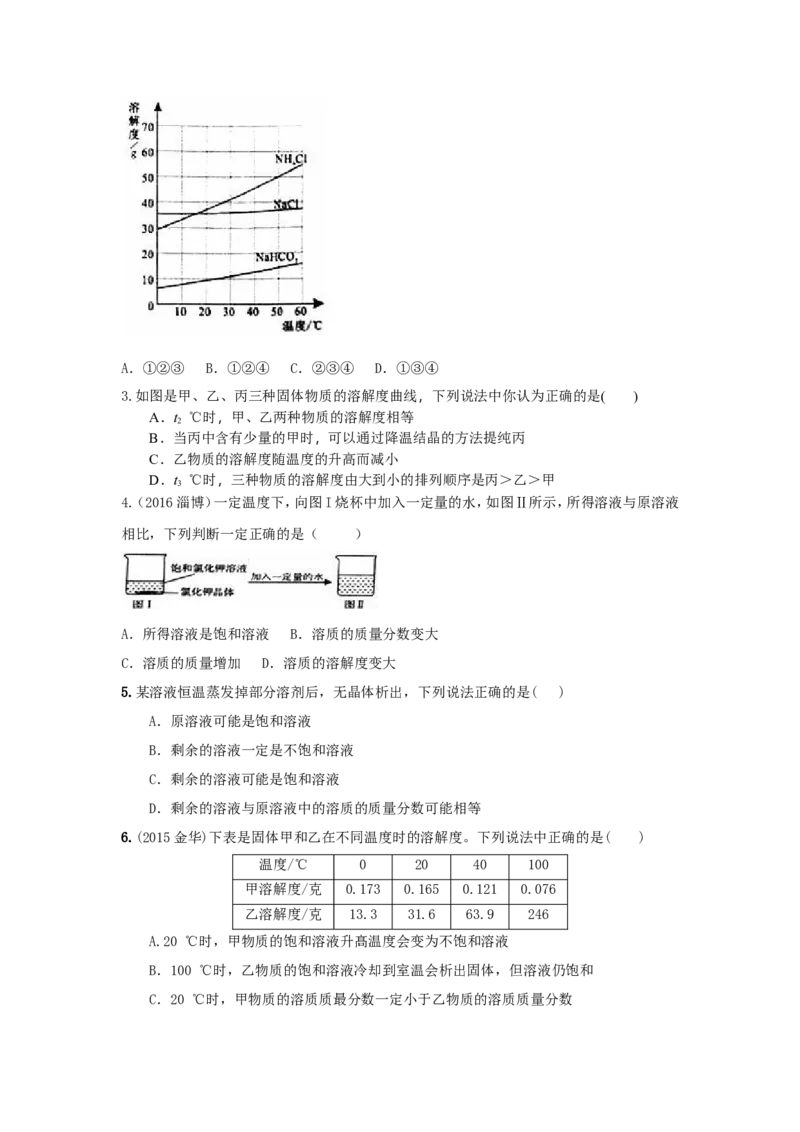
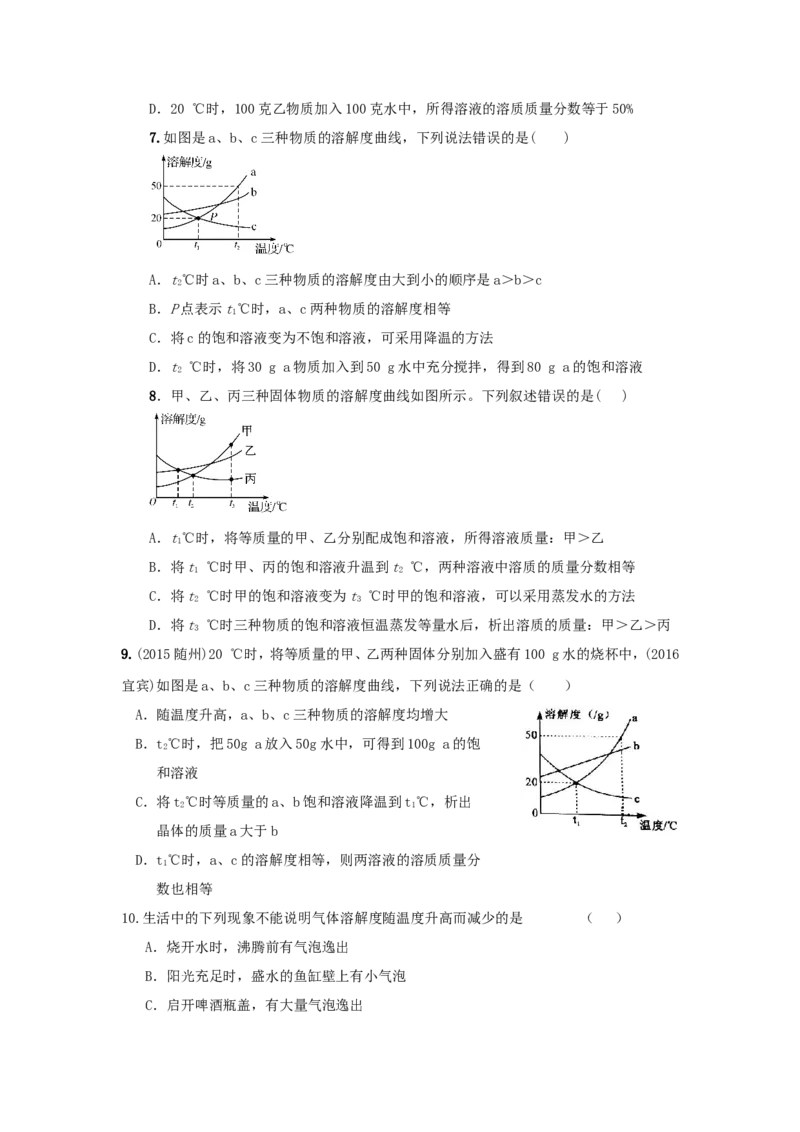
1.(2016德州)甲、乙两种固体物质的溶解度曲线如图所示.下列叙述中正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t℃时,甲、乙两物质饱和溶液的溶质质量分数一定相等
1
C.t℃时,将30g甲物质放入70g水中,所得饱和溶液的质量为100g
2
D.t℃时,甲、乙两物质的饱和溶液降温到t℃,析出晶体质量甲>乙
2 1
2.(2016济宁)如图是氯化钠、氯化铵和碳酸氢钠三种物质的溶解度曲线,分析曲线得到的以
下说法中,正确的是( )
①氯化钠和氯化铵是易溶物质,碳酸氢钠是可溶物质
②在20℃时,三种物质饱和溶液的溶质质量分数为NHCl>NaCl>NaHCO
4 3
③在30℃时,氯化钠和氯化铵固体各20g分别溶于50g水,所得溶液都是饱和溶液
④利用结晶法从氯化钠、氯化铵混合物中分离出氯化铵的最佳温度在10℃以下。A.①②③ B.①②④ C.②③④ D.①③④
3.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法中你认为正确的是( )
A.t ℃时,甲、乙两种物质的溶解度相等
2
B.当丙中含有少量的甲时,可以通过降温结晶的方法提纯丙
C.乙物质的溶解度随温度的升高而减小
D.t ℃时,三种物质的溶解度由大到小的排列顺序是丙>乙>甲
3
4.(2016淄博)一定温度下,向图I烧杯中加入一定量的水,如图Ⅱ所示,所得溶液与原溶液
相比,下列判断一定正确的是( )
A.所得溶液是饱和溶液 B.溶质的质量分数变大
C.溶质的质量增加 D.溶质的溶解度变大
5.某溶液恒温蒸发掉部分溶剂后,无晶体析出,下列说法正确的是( )
A.原溶液可能是饱和溶液
B.剩余的溶液一定是不饱和溶液
C.剩余的溶液可能是饱和溶液
D.剩余的溶液与原溶液中的溶质的质量分数可能相等
6.(2015金华)下表是固体甲和乙在不同温度时的溶解度。下列说法中正确的是( )
温度/℃ 0 20 40 100
甲溶解度/克 0.173 0.165 0.121 0.076
乙溶解度/克 13.3 31.6 63.9 246
A.20 ℃时,甲物质的饱和溶液升髙温度会变为不饱和溶液
B.100 ℃时,乙物质的饱和溶液冷却到室温会析出固体,但溶液仍饱和
C.20 ℃时,甲物质的溶质质最分数一定小于乙物质的溶质质量分数D.20 ℃时,100克乙物质加入100克水中,所得溶液的溶质质量分数等于50%
7.如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
A.t℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c
2
B.P点表示t℃时,a、c两种物质的溶解度相等
1
C.将c的饱和溶液变为不饱和溶液,可采用降温的方法
D.t ℃时,将30 g a物质加入到50 g水中充分搅拌,得到80 g a的饱和溶液
2
8.甲、乙、丙三种固体物质的溶解度曲线如图所示。下列叙述错误的是( )
A.t℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:甲>乙
1
B.将t ℃时甲、丙的饱和溶液升温到t ℃,两种溶液中溶质的质量分数相等
1 2
C.将t ℃时甲的饱和溶液变为t ℃时甲的饱和溶液,可以采用蒸发水的方法
2 3
D.将t ℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:甲>乙>丙
3
9.(2015随州)20 ℃时,将等质量的甲、乙两种固体分别加入盛有100 g水的烧杯中,(2016
宜宾)如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A.随温度升高,a、b、c三种物质的溶解度均增大
B.t℃时,把50g a放入50g水中,可得到100g a的饱
2
和溶液
C.将t℃时等质量的a、b饱和溶液降温到t℃,析出
2 1
晶体的质量a大于b
D.t℃时,a、c的溶解度相等,则两溶液的溶质质量分
1
数也相等
10.生活中的下列现象不能说明气体溶解度随温度升高而减少的是 ( )
A.烧开水时,沸腾前有气泡逸出
B.阳光充足时,盛水的鱼缸壁上有小气泡
C.启开啤酒瓶盖,有大量气泡逸出D.夏季黄昏时,池塘里的鱼浮出水面
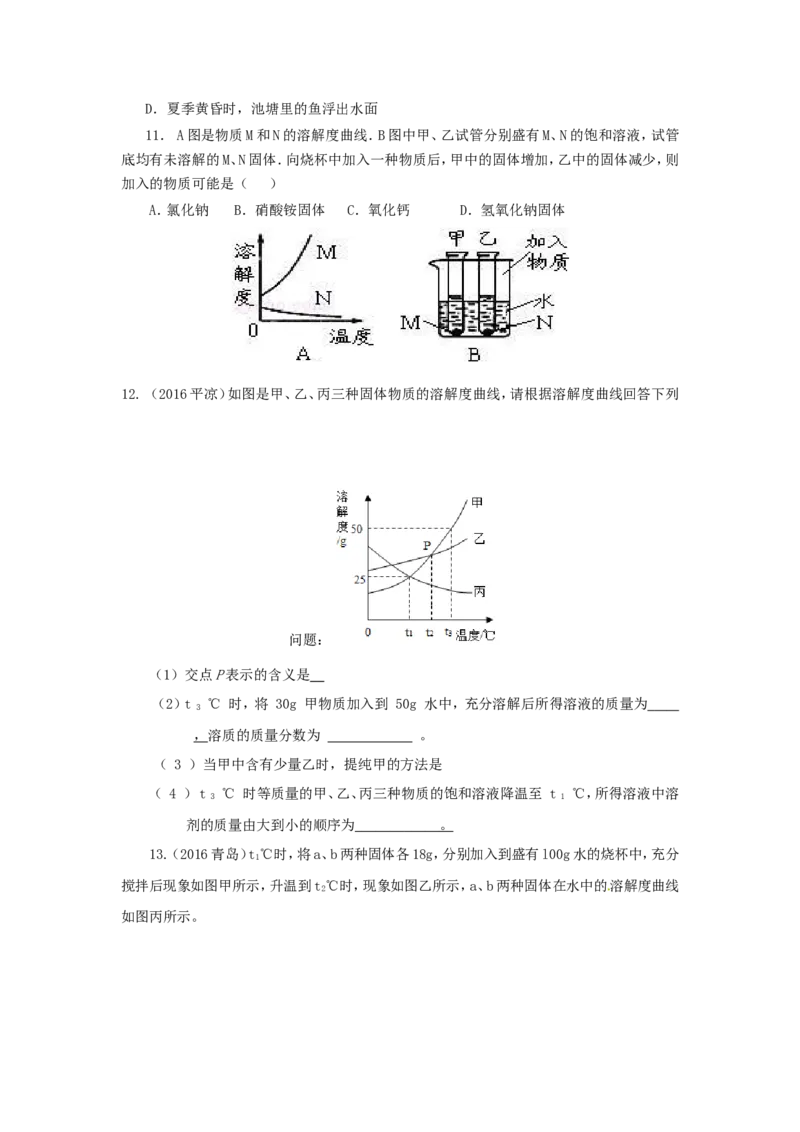
11. A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛有M、N的饱和溶液,试管
底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体增加,乙中的固体减少,则
加入的物质可能是( )
A.氯化钠 B.硝酸铵固体 C.氧化钙 D.氢氧化钠固体
12. (2016平凉)如图是甲、乙、丙三种固体物质的溶解度曲线,请根据溶解度曲线回答下列
问题:
(1)交点P表示的含义是__
(2)t ℃ 时,将 30g 甲物质加入到 50g 水中,充分溶解后所得溶液的质量为
3
,溶质的质量分数为 。
( 3 )当甲中含有少量乙时,提纯甲的方法是
( 4 ) t ℃ 时等质量的甲、乙、丙三种物质的饱和溶液降温至 t ℃,所得溶液中溶
3 1
剂的质量由大到小的顺序为 。
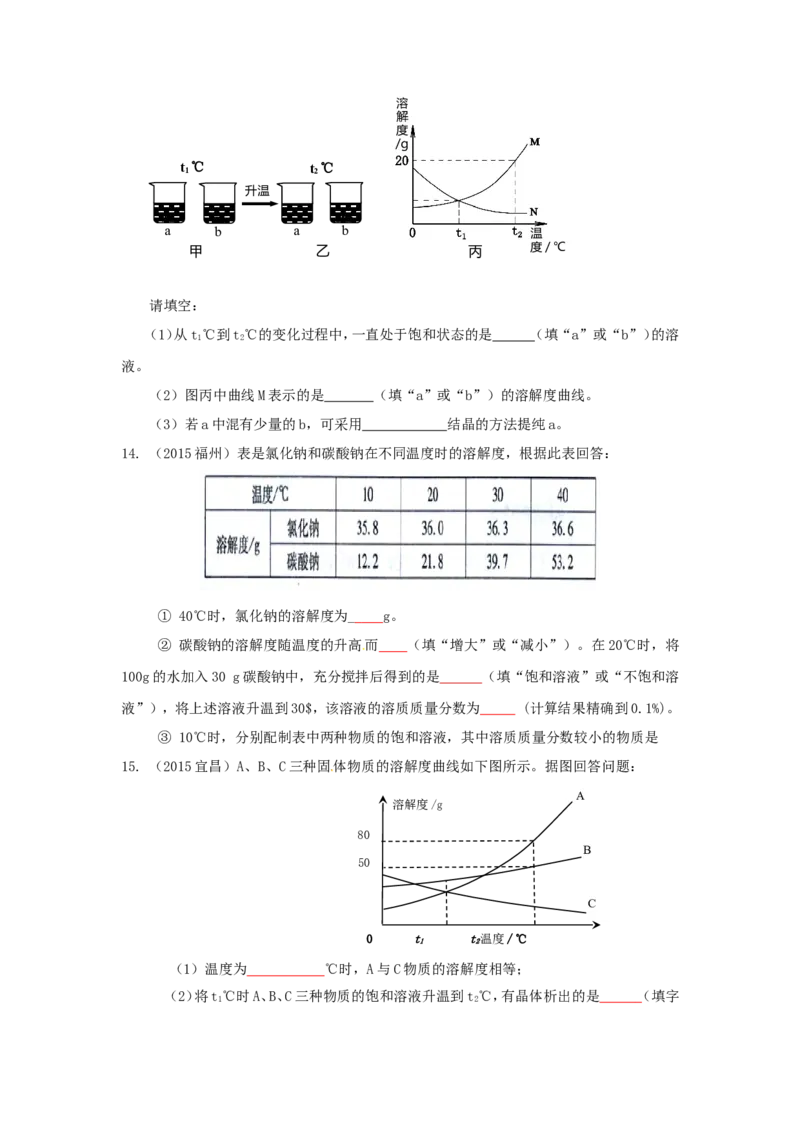
13.(2016青岛)t℃时,将a、b两种固体各18g,分别加入到盛有l00g水的烧杯中,充分
1
搅拌后现象如图甲所示,升温到t℃时,现象如图乙所示,a、b两种固体在水中的溶解度曲线
2
如图丙所示。溶
解
度
/g
t ℃ t ℃
1 2
升温
a b a b 温
甲 乙 丙 度/℃
请填空:
(1)从t℃到t℃的变化过程中,一直处于饱和状态的是 (填“a”或“b”)的溶
1 2
液。
(2)图丙中曲线M表示的是 (填“a”或“b”)的溶解度曲线。
(3)若a中混有少量的b,可采用 结晶的方法提纯a。
14. (2015福州)表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
① 40℃时,氯化钠的溶解度为_ g。
② 碳酸钠的溶解度随温度的升高而 (填“增大”或“减小”)。在20℃时,将
100g的水加入30 g碳酸钠中,充分搅拌后得到的是 (填“饱和溶液”或“不饱和溶
液”),将上述溶液升温到30$,该溶液的溶质质量分数为 (计算结果精确到0.1%)。
③ 10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是
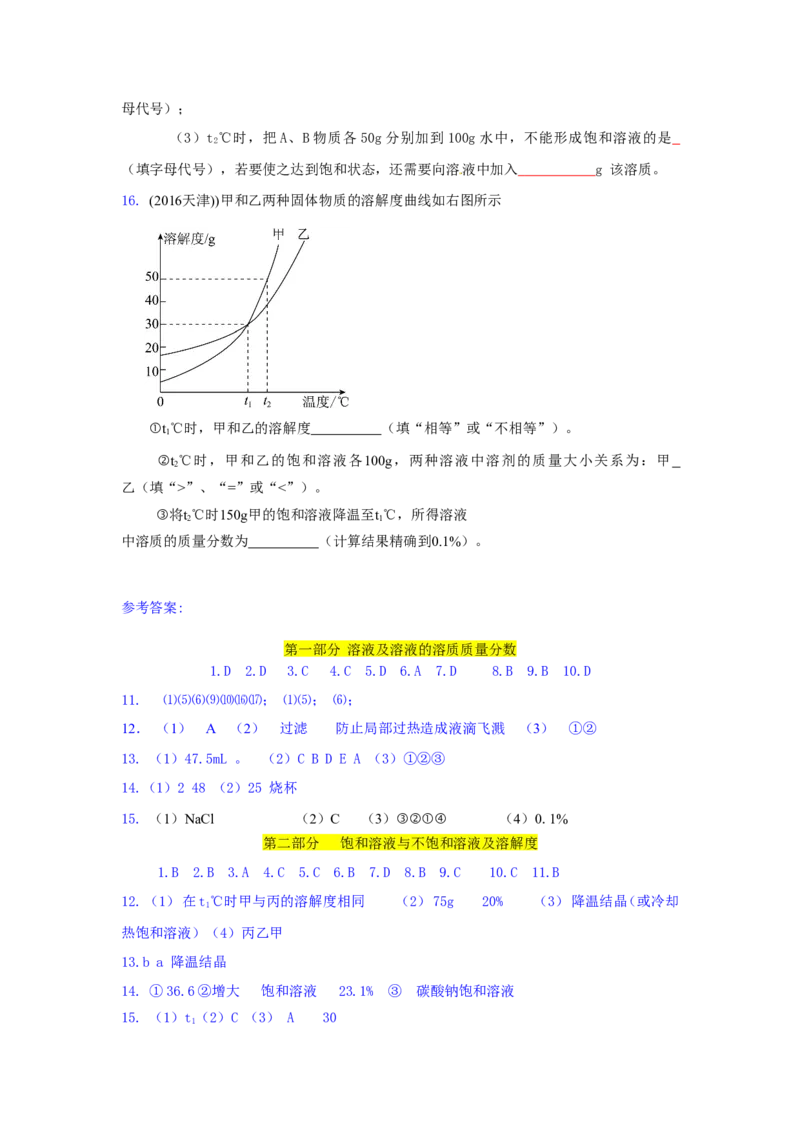
15. (2015宜昌)A、B、C三种固体物质的溶解度曲线如下图所示。据图回答问题:
A
溶解度/g
80
B
50
C
0 t t温度/℃
1 2
(1)温度为 ℃时,A与C物质的溶解度相等;
(2)将t℃时A、B、C三种物质的饱和溶液升温到t℃,有晶体析出的是 (填字
1 2母代号);
(3)t℃时,把A、B物质各50g分别加到100g水中,不能形成饱和溶液的是
2
(填字母代号),若要使之达到饱和状态,还需要向溶液中加入 g 该溶质。
16. (2016天津))甲和乙两种固体物质的溶解度曲线如右图所示
①t℃时,甲和乙的溶解度 (填“相等”或“不相等”)。
1
②t℃时,甲和乙的饱和溶液各100g,两种溶液中溶剂的质量大小关系为:甲
2
乙(填“>”、“=”或“<”)。
③将t℃时150g甲的饱和溶液降温至t℃,所得溶液
2 1
中溶质的质量分数为 (计算结果精确到0.1%)。
参考答案:
第一部分 溶液及溶液的溶质质量分数
1.D 2.D 3.C 4.C 5.D 6.A 7.D 8.B 9.B 10.D
11. ⑴⑸⑹⑼⑽⒃⒄; ⑴⑸; ⑹;
12. (1) A (2) 过滤 防止局部过热造成液滴飞溅 (3) ①②
13. (1)47.5mL 。 (2)C B D E A (3)①②③
14.(1)2 48 (2)25 烧杯
15. (1)NaCl (2)C (3)③②①④ (4)0.1%
第二部分 饱和溶液与不饱和溶液及溶解度
1.B 2.B 3.A 4.C 5.C 6.B 7.D 8.B 9.C 10.C 11.B
12. (1) 在t℃时甲与丙的溶解度相同 (2) 75g 20% (3) 降温结晶(或冷却
1
热饱和溶液)(4)丙乙甲
13.b a 降温结晶
14. ①36.6②增大 饱和溶液 23.1% ③ 碳酸钠饱和溶液
15. (1)t(2)C (3) A 30
116.① 相等 ② < ③ 23.1%