文档内容
第五单元测试卷
姓名______________班级_____________学号____________
一、选择题(每小题只有1个选项符合题意。)
1.下列是日常生活中常发生的一些变化,其中都属于化学变化的一组是( )
A.水受热沸腾、酒精挥发 B.汽油挥发、动物的呼吸作用
C.剩饭变馊、铁锅生锈 D.玻璃破碎、甘蔗榨成汁
2.化学反应遵循质量守恒定律的原因是化学反应前后( )
A.分子的种类没有改变 B.分子的数目没有改变
C.原子的种类、数目和质量都没有改变 D.物质的种类没有改变
3.根据化学方程式不能获得的信息是( )
A.反应中的反应物和生成物 B.各反应物、生成物之间的质量比
C.化学反应的快慢程度 D.反应发生所需要的条件
4.某物质在纯氧中燃烧生成了氮气和水蒸气,该物质一定含有( )
A.氮元素和氧元素 B.氢元素和氧元素
C.氮元素和碳元素 D.氮元素和氢元素
5.红磷在耐高温的密闭容器中(内含空气)加热,能正确表示容器里所盛物质总质量变化的
图象是( )
6.二甲醚(CH OCH )可由一氧化碳和物质X在一定的条件下制得。反应的化学方程式
3 3
为2CO+4X====== CH OCH +H O,则X的化学式为( )
3 3 2
A.C H OH B.H O C.C H D.H
2 5 2 2 2 4 2
7.碳在氧气中燃烧,下列说法符合质量守恒定律的是( )
A.2gC和9gO 生成11gCO B.3gC和8gO 生成11 gCO
2 2 2 2
C.4gC和7gO 生成11gCO D.5gC和6gO 生成11gCO
2 2 2 2
点燃
8.化学方程式3Fe + 2O ==== Fe O 可读作( )
2 3 4
A.铁加氧气等于四氧化三铁
1B.三个铁加两个氧气等于一个四氧化三铁
C.铁和氧气点燃后生成四氧化三铁
D.铁加氧气点燃等于四氧化三铁
9.某纯净物M微热就能分解生成NH 、H O和CO ,由此还不能得出的结论是( )
3 2 2
A.M不稳定 B.M是化合物
C.M中含有水 D.M由四种元素组成
10.氨基钠(NaNH )是合成维生素A的原料。工业上将金属钠于97~100℃熔融,向反应器
2
中缓慢通入无水液氨(NH ),再加热至350~360℃生成氨基钠(NaNH )和氢气。下列说法
3 2
中,不正确的是
A.钠可能与水反应 B.钠的熔点比铁的熔点低
C.维生素A中一定含有钠元素
△
D.反应的化学方程式为:2Na+2NH 2NaNH +H ↑
3 2 2
11.汽车尾气中的CO在四氧化三钴(Co O )纳米棒的催化作用下,低温即与O 反应生成
3 4 2
CO 。下列关于该反应的说法中,不正确的是( )
2
A.反应前后Co O 质量改变 B.可降低汽车尾气对大气的污染
3 4
C.反应类型为化合反应 D.反应前后碳元素的化合价改变
12.在化学反应A+2B===C+D中,5.6gA和7.3gB恰好完全反应,生成12.7gC,同时得到D
的质量是( )
A.0.2g B. 5.6g C.0.4g D.0.73g
13.下列说法错误的是( )
A.一切化学反应都是遵循质量守恒定律的。
B.镁在空气中燃烧,虽然生成氧化镁的质量比镁大,但这个反应也遵循质量守恒定律。
C.氯酸钾和二氧化锰加热后试管中残留物比反应物质量小,但这个反应也是遵循质量守恒
定律的。
D.水蒸发为水蒸气,质量没有改变,由此可说明化学变化是符合质量守恒定律的。
14.讨论某一化学方程式表示的意义,他们所描述的化学方程式是( )
A. C O 点 燃 CO
2 2
2B. 2COO 点 燃 2CO
2 2
C. 2H O 点 燃 2H O
2 2 2
D. CH 2O 点 燃 CO 2H O
4 2 2 2
15.有反应: 8A + 3B = C + 6D(其中A、D是化合物,B 、C 是单质)。若13.6g A与
2 2 2 2
21.3g B 恰好完全反应,生成32.1g D,已知C 的相对分子质量为28,则B的相对原子质量
2 2
为( )
A.14 B.16 C.32 D.35.5
二.选择题(每小题有1~2个选项符合题意。)
16.在下列各项中,化学反应前后肯定没有发生改变的是( )
①原子的数目 ②分子的数目 ③元素的种类
④物质的总质量 ⑤物质的种类 ⑥原子的种类
A.①③④⑤ B.①③④⑥ C.①④⑥ D.①③⑤
17.在化学反应A+B===C+D中,已知12gA和18gB恰好完成反应生成6gC,若实际反应
时生成了8gD,则参加反应的B的质量是( )
A.3g B.4g C.1g D.6g
18.已知在空气中完全燃烧1.6g某纯净物生成4.4gCO 和3.6 H O,则该纯净物的组成中
2 2
( )
A.只有C元素 B. 只有C、H元素 C. 只有C、H、O元素 D. 都不正确
19.下图为某反应的微观模拟示意图。从图中获得的有关信息不正确的是( )
反应前 反应后
( 和 分别表示不同元素的原子)
A.分子是化学变化中的最小粒子
B.化学反应前后原子的数目没有增减
C.该化学反应属于分解反应
3D.分子间存在一定的间隔
20.将一定量的丙醇(C H O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质
3 8
量如下表:
物质 丙醇 氧气 水 二氧化碳 X
反应前质量/g 6.0 12.8 0 0 0
反应后质量/g 0 0 7.2 8.8 a
下列判断正确的是( )
A.表中a的值为2.8
B.X一定是该反应的催化剂
C.X可能含有氢元素
D.若起始时氧气的质量是14.4g,则无X生成
三、填空题
21.某同学写了以下化学方程式:
点燃 MnO
2
A.Mg + O ==== MgO B.KClO ==== KCl + O ↑
2 2 3 2
通电 点燃
C.2H O ==== 2H O + O ↑ D.2H ↑+ O ↑=====2H O
2 2 2 2 2 2 2
E.3Fe + 2O ==== Fe O
2 3 4
根据化学方程式错误的不同,将其序号填入以下相应的空白处:
(1)未配平的是 ;(2)化学式写错的是 ;(3)“↑”使用不当的是 ;
(4)未注明反应条件的是 ;(5)反应条件写错的是 。
22.完成下列化学反应的化学方程式:
(1)电解水:__________________________________________________________
(2)硫在空气中的燃烧:____________________________________________
(3)高锰酸钾制氧气:
(4)有水生成的分解反应:______________________________________________
(5)有水生成的化合反应:______________________________________________
23.石英的主要成分为二氧化硅,它是玻璃工业和陶瓷工业的原料,冶金工业的助熔剂。
(1)二氧化硅的结构与金刚石相似,都是由 (填“分子”、“原子”或“离子”)
4构成的,二氧化硅 (填“属于”或“不属于”)氧化物。
(2)装有氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是在常温下,NaOH与玻璃塞中的SiO
2
缓慢地发生反应生成Na SiO 和H O,Na SiO 使瓶口与瓶塞粘合在一起,则该反应的化学
2 3 2 2 3
方程式为
。
(3)硅是太阳能电池和电脑芯片不可缺少的材料。生产高纯硅的流程示意图如下:
高温
①
制备粗硅的反应为:SiO + 2C=== Si + 2CO↑。
2
② 整个制备过程必须达到无水无氧,若在H 还原SiHCl 过程中混入O ,可能引起的后果
2 3 2
是
。
③ 为了达到绿色化学和节约资源的目的,物质 A需要循环使用,A的化学式是
。
24.硝酸可发生反应: 。据此回答:
(1)反应的基本类型属于 反应,硝酸(HNO )氮元素的化合价为 。
3
(2)X的化学式为 ,推断的依据为 。
(3)硝酸的保存应注意 、 。
25.质量守恒定律的定量研究对化学科学发展具有重大意义。
(1)已知m g镁条放在空气中完全燃烧,生成m g氧化镁(不考虑其它反应),该反应的化学
1 2
方程式 ,m m 。(填“大于”、“小于”或“等
1 2
于”)。
(2)小西在做该实验时,观察到耀眼的白光,冒出大量白烟,称量无误时,发现m >m ,其原
1 2
因是
。
5四、实验题
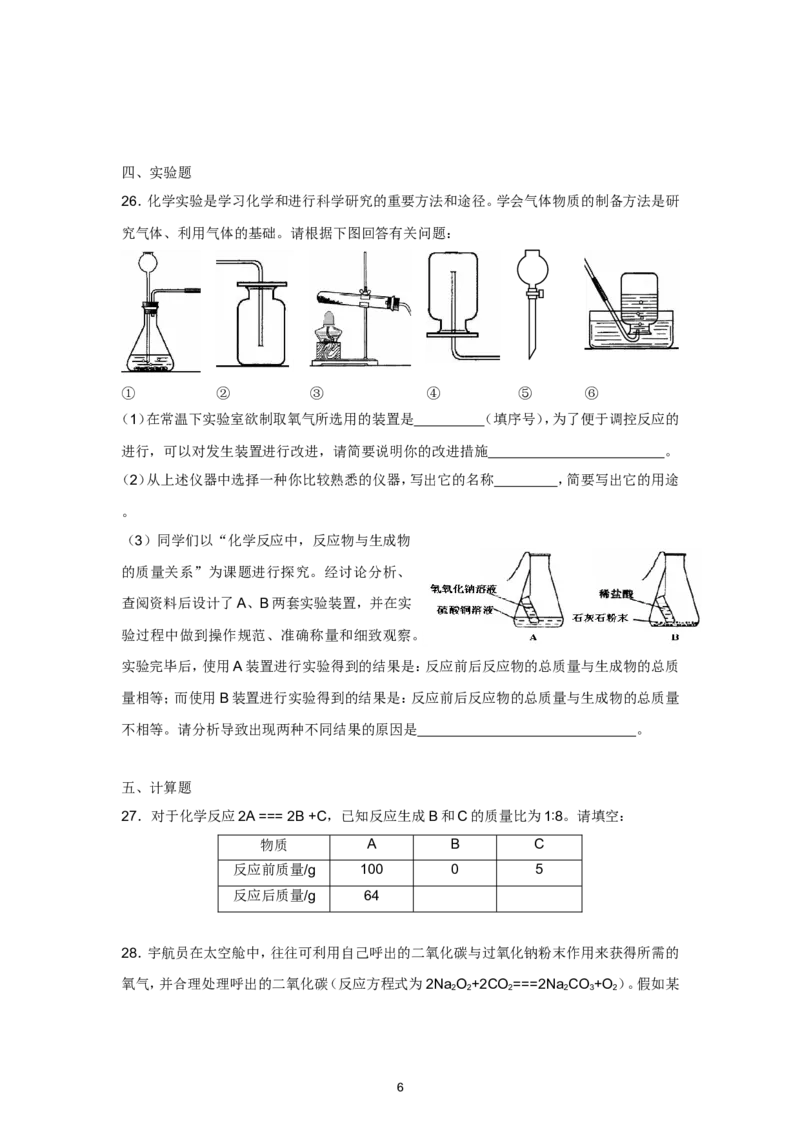
26.化学实验是学习化学和进行科学研究的重要方法和途径。学会气体物质的制备方法是研
究气体、利用气体的基础。请根据下图回答有关问题:
① ② ③ ④ ⑤ ⑥
(1)在常温下实验室欲制取氧气所选用的装置是 (填序号),为了便于调控反应的
进行,可以对发生装置进行改进,请简要说明你的改进措施 。
(2)从上述仪器中选择一种你比较熟悉的仪器,写出它的名称 ,简要写出它的用途
。
(3)同学们以“化学反应中,反应物与生成物
的质量关系”为课题进行探究。经讨论分析、
查阅资料后设计了A、B两套实验装置,并在实
验过程中做到操作规范、准确称量和细致观察。
实验完毕后,使用A装置进行实验得到的结果是:反应前后反应物的总质量与生成物的总质
量相等;而使用B装置进行实验得到的结果是:反应前后反应物的总质量与生成物的总质量
不相等。请分析导致出现两种不同结果的原因是 。
五、计算题
27.对于化学反应2A === 2B +C,已知反应生成B和C的质量比为1∶8。请填空:
物质 A B C
反应前质量/g 100 0 5
反应后质量/g 64
28.宇航员在太空舱中,往往可利用自己呼出的二氧化碳与过氧化钠粉末作用来获得所需的
氧气,并合理处理呼出的二氧化碳(反应方程式为2Na O +2CO ===2Na CO +O )。假如某
2 2 2 2 3 2
6宇航员在某次太空飞行中预计消耗氧气480Kg,请计算该宇航员在太空舱中至少应准备的
过氧化钠的质量。(请写出计算过程)
附加题(每空1分,共5分。)
29.比较、分析、归纳是学习化学的重要方法。通过比较可以发现相同的反应物在不同外界条
件下,会发生不同的反应。请参照示例归纳反应规律:
组别 化学方程式 规律
反应物相同时,反
示例 应物的量不同,生
成物不同
(1)
3Cu8HNO (稀) 3Cu(NO ) 2NO 4H O
3 3 2 2
(2)
Cu4HNO (浓) 3Cu(NO ) 2NO 2H O
3 3 2 2 2
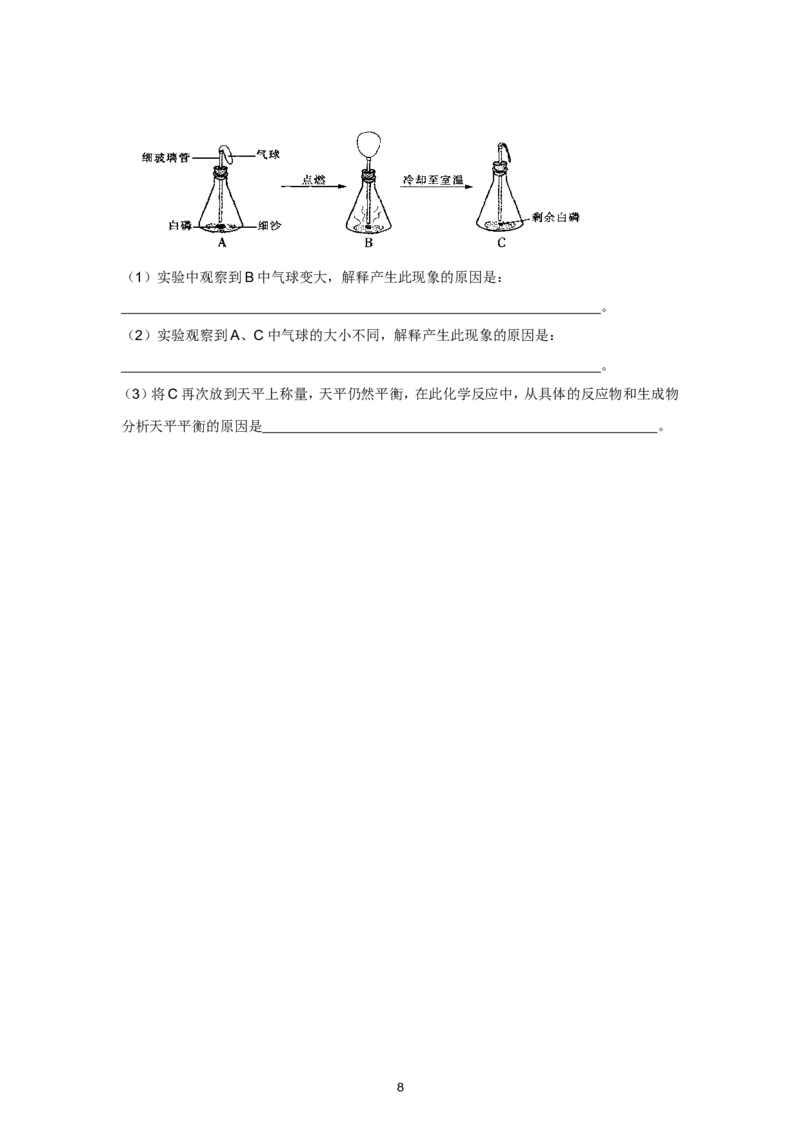
30.在用白磷(白磷与红磷组成相同,着火点为40℃)探究质量守恒定律的实验中,晓涵同学
将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,
并引燃白磷,实验过程如下图所示。请回答下列问题:
7(1)实验中观察到B中气球变大,解释产生此现象的原因是:
。
(2)实验观察到A、C中气球的大小不同,解释产生此现象的原因是:
。
(3)将C再次放到天平上称量,天平仍然平衡,在此化学反应中,从具体的反应物和生成物
分析天平平衡的原因是 。
8参考答案及评分标准
一、选择题(每小题2分,本题共30分。)
题 1 2 3 4 5 6 7 8 9 1
号 0
答 C C C D B D B C C C
案
11 12 13 14 15
A A D B D
二、选择题(每小题2分,本题共10分,2个选项选对一个且正确的给1分,错选多选不给
分。)
题 16 17 18 19 20
号
答 B D B AC AD
案
三、填空题(除特别说明外每空1分。)
21.(1)B (2)A (3)D (4)E (5)C
22.(若完成附加题,每空1分;若不完成附加题,每空2分。)
通电
(1)2H O ===== 2H ↑ + O ↑
2 2 2
点燃
(2)S + O ===== SO
2 2
(3)2KMnO =====K MnO + MnO + O ↑
4 2 4 2 2
MnO
2
(4)2H O ===== 2H O + O ↑
2 2 2 2
点燃
(5)2H + O =====2H O
2 2 2
23.(1)原子 属于
(2)2NaOH + SiO = Na SiO + H O
2 2 3 2
(3)硅被氧化得不到高纯硅,且发生爆炸 HCl
24.(1)分解 +4
(2)O 质量守恒定律(若答“化学反应前后各原子的种类和数目不变”或“化学反应前
2
9后各原子的数目不变”等合理答案均给分,若答“化学反应前后各原子的种类不变”或
“化学反应前后原子的总数不变”或“化学反应前后各元素的种类不变”或“化学反应前
后各元素的个数不变”等均不给分)
(3)避光(或“棕色瓶保存”等合理答案) 低温(或“防止受热”等合理答案)
25.(1)小于
(2)生成的MgO部分以白烟形式散逸到空气中
四、实验题(每空1分。)
26.(1)①②或①⑥ 用⑤分液漏斗代替长颈漏斗
(2)试管 作为少量物质的反应容器等(合理答案都给分)
(3)A中的两种物质反应产生了沉淀没有脱离体系,所以质量不变,而B中产生了CO 散失,
2
使剩余物质的质量比原物质质量减小。
五、计算题(27题每空1分,28题5分。)
27.4 37
28.解:设至少准备过氧化钠的质量为x
答:该宇航员应在太空舱中至少准备2340Kg过氧化钠。
附加题(共5分,若做,则22题每个方程式1分1个)
29.(1)反应物相同时,反应条件(或温度)不同,生成物不同
(2)反应物相同时,反应物的浓度不同,生成物不同
1030.(1)白磷燃烧放出热量使瓶内压强变大,大于外界大气压,从而气球变大
(2)白磷燃烧消耗氧气,生成固体五氧化二磷,使瓶中压强变小,小于外界大气压,在大气压
的作用下,C中气球变小,A内压强等于外界大气压,所以A、C中气球大小不同
(3)参加化学变化(或消耗;或反应掉)的白磷的质量和氧气的质量总和等于生成的五氧化二
磷的质量。
11