文档内容
一对一辅导教案
学生姓名 性别 年级 初三 学科 化学
第( )次课
授课教师 上课时间 年 月 日 课时:2课时
共( )次课
教学课题 人教版九年级化学第六章碳和碳的氧化物同步教案
知识目标:
1、了解金刚石和石墨的物理性质和用途,知道碳单质的化学性质。
2、了解二氧化碳和一氧化碳的性质,知道二氧化碳的用途。
3、了解实验室中制取二氧化碳所用的药品、反应原理,知道实验室制取二氧化碳所用的药品、发
生装置的选取、操作步骤、检验和收集方法。
教学目标 能力目标:
1、通过探究活动过程,体验化学实验方法的科学性,了解实验室制取气体的思路和方法;
2、探究实验室制取二氧化碳的装置、药品,并利用设计的装置制取二氧化碳。
情感态度价值观:
通过学习,保持和增强对生活和自然中化学现象的好奇心和探究欲,强化保护环境、解决环境
问题的意识
重点:碳单质和二氧化碳的化学性质,实验室制取二氧化碳原理、装置设计及制取方法。
教学重点
难点:对金刚石和石墨物性差异很大的原因的理解;实验室制取二氧化碳装置的设计思路;对二氧
与难点
化碳与水反应原理的探究。
教学过程
(一)金刚石、石墨和C
60
知识梳理
一、碳的单质
1、金属石:无色透明、正八面体形状,很硬,可用来切割玻璃;经琢磨后,可以成为璀璨夺目的装饰品——钻石。
2、石墨:深灰色、有金属光泽、不透明、细鳞片状固体很软、有良好的导电性,可制作铅笔芯。
3、木炭、活性炭有强吸附性。
4、C :由60个碳原子构成,分子形似足球,又名足球烯
60
二、碳的化学性质
1、碳与氧气反应: C+O CO(充分燃烧)
2 2
2C+O 2CO(不充分燃烧)
2
2、碳与某些氧化物反应:
2CuO+C 2Cu+CO↑
2
现象:澄清石灰水变浑浊,试管粉末中有红色物质。
焦炭在工业上可用来炼铁:2FeO+3C 4Fe+3CO↑
2 3 2
3、还原反应:含氧化合物里的氧被夺去的反应。
还原性:能夺走含氧化合物里氧的物质具有还原性。
例题精讲
1、 金刚石和石墨的物理性质有很大差异的原因是 ( )
A.金刚石和石墨是由不同种元素组成 B.金钢石石墨里碳原子排列 不同
C.金刚石是单质,石墨是化合物 D.金刚石是纯净物,石墨是混合 物
2、关于碳及碳的化合物的说法,正确的是( )
A. CO与CO 都可以将氧化铜还原成铜
2B.CO 的排放不是导致酸雨的原因
2
C.在室内放一盆澄清石灰水可以防止CO中毒
D.铅笔字迹易变模糊是因为常温下石墨的化学性质活泼
3、碳和碳的化合物都是非常重要的物质。
(1)碳原子的结构示意图为 ,碳原子的核电荷数为________。
(2)碳的单质有多种,具有下列结构的碳单质中,由分子构成的是________(填序号)。
(3)上面三种碳的单质在氧气中完全燃烧的产物都是________。
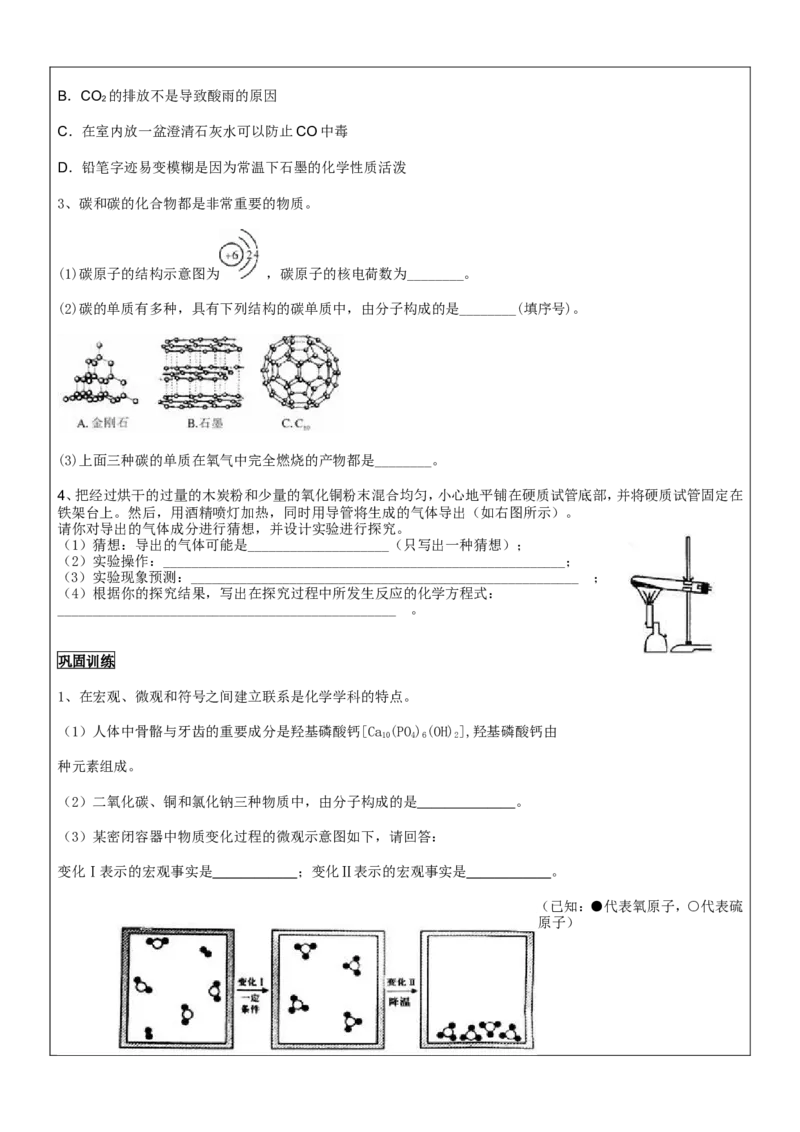
4、把经过烘干的过量的木炭粉和少量的氧化铜粉末混合均匀,小心地平铺在硬质试管底部,并将硬质试管固定在
铁架台上。然后,用酒精喷灯加热,同时用导管将生成的气体导出(如右图所示 )。
请你对导出的气体成分进行猜想,并设计实验进行探究。
(1)猜想:导出的气体可能是____________________(只写出一种猜想);
(2)实验操作:_________________________________________________________;
(3)实验现象预测:_______________________________________________________ ;
(4)根据你的探究结果,写出在探究过程中所发生反应的化学方程式:
________________________________________________ 。
巩固训练
1、在宏观、微观和符号之间建立联系是化学学科的特点。
(1)人体中骨骼与牙齿的重要成分是羟基磷酸钙[Ca (PO)(OH)],羟基磷酸钙由
10 4 6 2
种元素组成。
(2)二氧化碳、铜和氯化钠三种物质中,由分子构成的是 。
(3)某密闭容器中物质变化过程的微观示意图如下,请回答:
变化Ⅰ表示的宏观事实是 ;变化Ⅱ表示的宏观事实是 。
(已知:●代表氧原子,○代表硫
原子)2、芯片是所有电脑“智能家电”核心部件,它是以高纯度的单质硅(元素符号为Si)为材料制成的。用化学方法制得高纯硅的
反应原理为:①SiO
2
+C==Si+CO ②Si+2Cl
2
==SiCl
4
③SiCl
4
+H
2
==Si+HCl。根据以上信息请回答:
(1)上述反应中属于置换反应的是 (填编号)。
(2)SiCl 物质的名称为 ; 其中的Si的化合价是
4
(3)反应①中的C表现了 性(选填“氧化”或“还原性”)。
(4)反应①中生成的气体是 (填化学式),它是煤气的主要成分,容易使人发“煤气中毒”事故,煤气中毒实
际是由于 的原因。当你发现有人煤气中毒时应该
采取的措施有 (任写一点)。
3、生活离不开化学,化学与生活息息相关。
(1)右图的净水装置中,活性炭的主要作用是_______(填字母序号)。
A.沉淀B.过滤C.吸附D.消毒
(2)生活中,人们常常利用燃料燃烧产生的能量来做饭和取暖,煤、氢气、乙醇、汽油、柴油等燃料中,不属于化石燃料的是
________。随着全球能源使用量的增长,人类正在开发新能源,如潮汐能、核能、________(填一种)等。
4、2013年3月,浙江大学实验室里诞生了世界上最轻的材料——“碳海绵”。“碳海绵”具备高弹性和疏松多
孔的结构,主要成分是石墨烯和碳纳米管(两者都是碳单质)。下列关于“碳海绵”的说法中不正确的是
A. 常温下化学性质活泼 B. 具有吸附性
C. 在一定条件下可还原氧化铜 D. 在氧气中完全燃烧的产物是CO
2
5、芯片是所有电脑“智能家电”核心部件,它是以高纯度的单质硅(元素符号为Si)为材料制成的。用化学方法制得高纯硅的
反应原理为:①SiO
2
+C==Si+CO ②Si+2Cl
2
==SiCl
4
③SiCl
4
+H
2
==Si+HCl。根据以上信息请回答:
(1)上述反应中属于置换反应的是 (填编号)。
(2)SiCl 物质的名称为 ; 其中的Si的化合价是
4
(3)反应①中的C表现了 性(选填“氧化”或“还原性”)。
(4)反应①中生成的气体是 (填化学式),它是煤气的主要成分,容易使人发“煤气中毒”事故,煤气中毒实
际是由于 的原因。当你发现有人煤气中毒时应该
采取的措施有 (任写一点)。
(二)二氧化碳制取的研究
知识梳理
一、实验室制取CO
2
1. 药品:石灰石(或大理石)和稀盐酸2. 原理:
CaCO +2HCl=CaCl +HO+CO↑
3 2 2 2
注意:(1)不能用浓盐酸代替稀盐酸,因为浓盐酸易挥发,使制得的CO 不纯(混有氯化氢气体);
2
(2)不能用稀硫酸代替稀盐酸,因为稀硫酸与CaCO 反应生成微溶于水的硫酸钙覆盖在大理石(或石灰石)的
3
表面,阻止反应的进行;
(3)不能用NaCO 或CaCO 代替大理石(或石灰石),因为NaCO 与稀盐酸的反应速度太快,不便于收集。
2 3 3 2 3
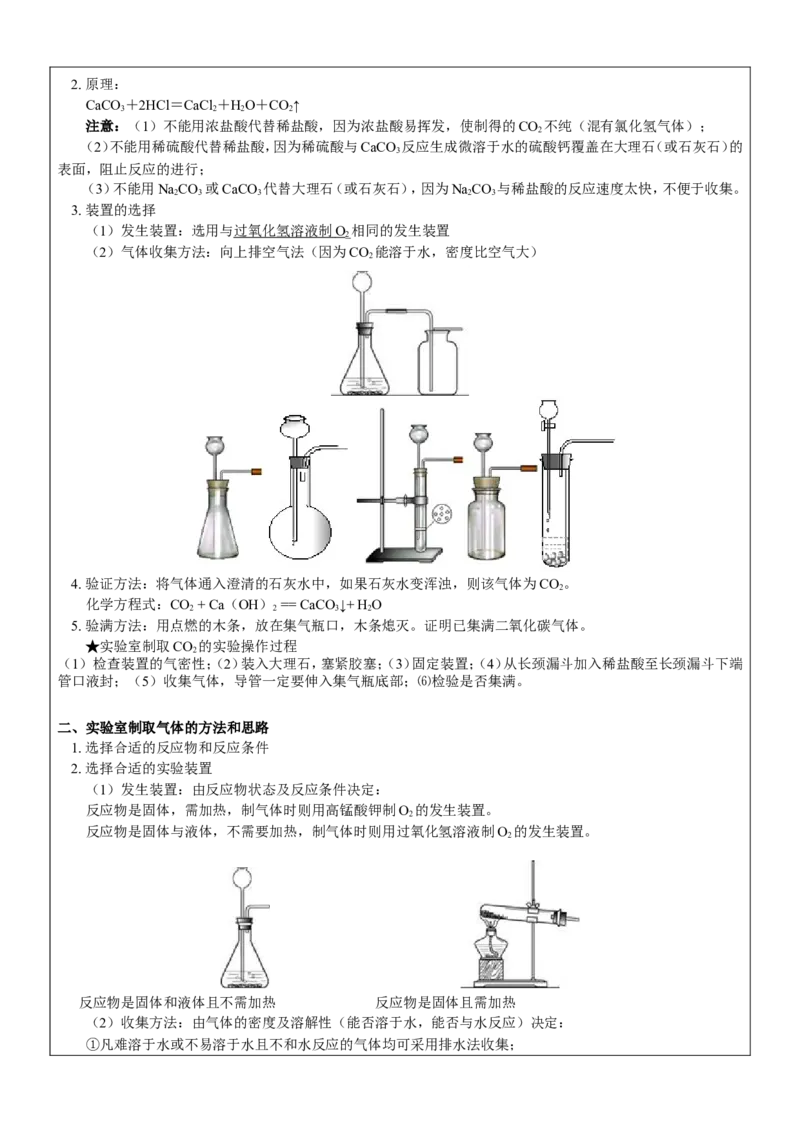
3. 装置的选择
(1)发生装置:选用与 过氧化氢溶液制 O 相同的发生装置
2
(2)气体收集方法:向上排空气法(因为CO 能溶于水,密度比空气大)
2
4. 验证方法:将气体通入澄清的石灰水中,如果石灰水变浑浊,则该气体为CO。
2
化学方程式:CO + Ca(OH) == CaCO↓+ H O
2 2 3 2
5. 验满方法:用点燃的木条,放在集气瓶口,木条熄灭。证明已集满二氧化碳气体。
★实验室制取CO 的实验操作过程
2
(1)检查装置的气密性;(2)装入大理石,塞紧胶塞;(3)固定装置;(4)从长颈漏斗加入稀盐酸至长颈漏斗下端
管口液封;(5)收集气体,导管一定要伸入集气瓶底部;⑹检验是否集满。
二、实验室制取气体的方法和思路
1. 选择合适的反应物和反应条件
2. 选择合适的实验装置
(1)发生装置:由反应物状态及反应条件决定:
反应物是固体,需加热,制气体时则用高锰酸钾制O 的发生装置。
2
反应物是固体与液体,不需要加热,制气体时则用过氧化氢溶液制O 的发生装置。
2
反应物是固体和液体且不需加热 反应物是固体且需加热
(2)收集方法:由气体的密度及溶解性(能否溶于水,能否与水反应)决定:
①凡难溶于水或不易溶于水且不和水反应的气体均可采用排水法收集;②凡密度比空气大的气体可采用瓶口向上排空气法收集;
③凡密度比空气小的气体可采用瓶口向下排空气法收集。
3. 验证所制得的气体
例题精讲
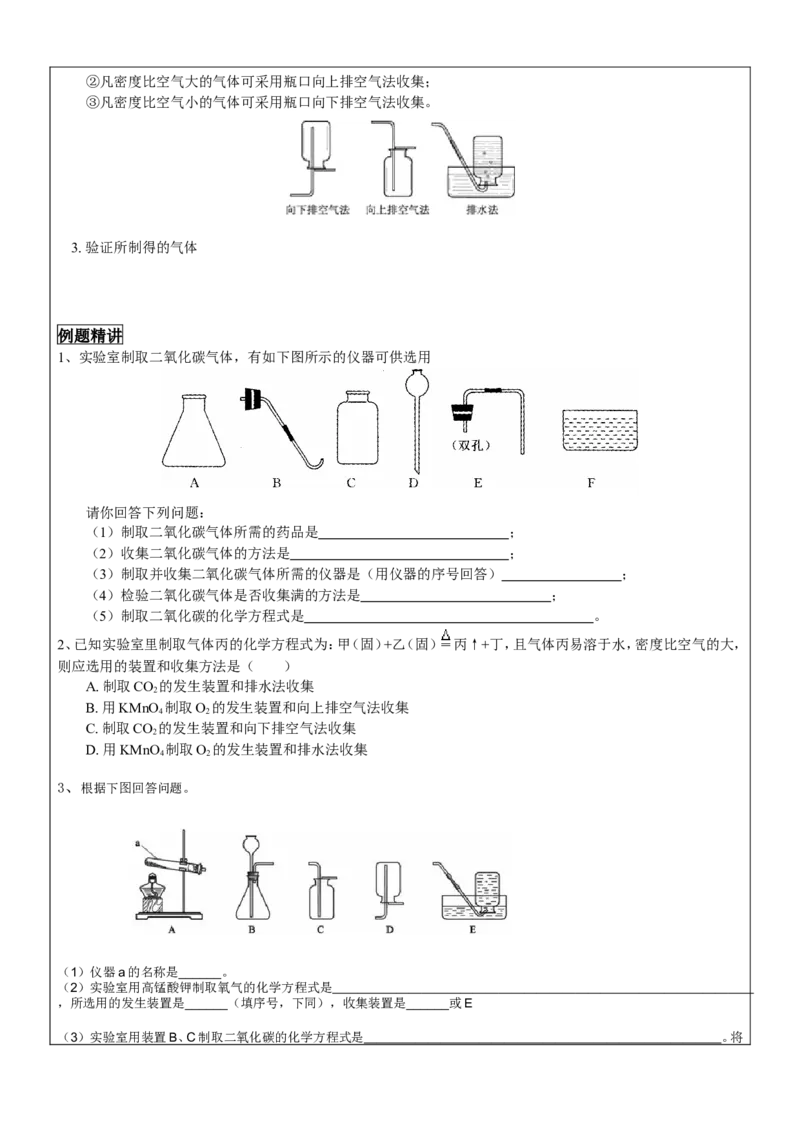
1、实验室制取二氧化碳气体,有如下图所示的仪器可供选用
请你回答下列问题:
(1)制取二氧化碳气体所需的药品是 ;
(2)收集二氧化碳气体的方法是 ;
(3)制取并收集二氧化碳气体所需的仪器是(用仪器的序号回答) ;
(4)检验二氧化碳气体是否收集满的方法是 ;
(5)制取二氧化碳的化学方程式是 。
2、已知实验室里制取气体丙的化学方程式为:甲(固)+乙(固) 丙↑+丁,且气体丙易溶于水,密度比空气的大,
则应选用的装置和收集方法是( )
A. 制取CO 的发生装置和排水法收集
2
B. 用KMnO 制取O 的发生装置和向上排空气法收集
4 2
C. 制取CO 的发生装置和向下排空气法收集
2
D. 用KMnO 制取O 的发生装置和排水法收集
4 2
3、根据下图回答问题。
(1)仪器a的名称是______。
(2)实验室用高锰酸钾制取氧气的化学方程式是
,所选用的发生装置是______(填序号,下同),收集装置是______或E
(3)实验室用装置B、C制取二氧化碳的化学方程式是 。将生成的气体通入紫色石蕊溶液,观察到的现象是 ,该反应的化学
方程式是 。
4、小强在做实验时,发现硬水在蒸发的过程中,产生了少量气体并得到一种难溶性的固体(水垢).提出猜想:产
生的气体可能是二氧化碳,难溶性的固体可能是碳酸盐.进行实验:
(1)将生成的气体通入 中,观察到 的现象,证明气体是二氧化碳,写出有关反应的化学表达式: .
(2)向这种难溶性的固体中滴入稀盐酸,观察到大量的气泡产生,则这种固体可能是碳酸盐;若这种固体是碳酸钙,写出该反
应的化学表达式: 。 反馈与应用:通过上述实验得到启发,在家可用 除去热水瓶胆内壁的水垢.
巩固训练
1、下列各组仪器中,不能用来组装实验室制取二氧化碳装置的是( )
A. 长颈漏斗、集气瓶、酒精灯 B. 长颈漏斗、集气瓶、试管
C. 长颈漏斗、锥形瓶、集气瓶 D. 平底烧瓶、长颈漏斗、集气瓶
2、小明和小红利用下图装置,以碳酸钙和稀盐酸为原料来制取二氧化碳气体,并进行比较分析.
(1)小明用图甲和图乙组合来制取二氧化碳气体,如何检验二氧化碳是否收集满?请写出具体操作:
。
(2)小红认为用甲丙收集二氧化碳气体的方法比图乙更好.你认为她的理由是: (写出一点)。
(3)实验过程中小红发现反应有快慢,请你列举一种判断反应快慢的方法
。
3、请结合下列常用的仪器和装置,回答有关问题:
(1)写出标号仪器的名称:d ;e 。
(2)选择上图中的 (填序号)可组合成实验室制取二氧化碳的发生装置,在不添加他仪器的情况下,检查该
发生装置气密性的方法为
;收集二氧化碳气体,可选择上图中的 (填序号)装置;若要检验二氧化碳气体,则需将 气体通过盛有
的i装置。
(3)在实验室除去水中的不溶性杂质时,除上图有关仪器外,必须添加的仪器含下列中的 (填序号)。A.玻璃棒 B. 铁架台(带铁圈) C.水槽 D.分液漏斗
4、阅读资料:
(1)氨气(NH )具有还原性,可以还原氧化铜,生成铜、氮气和水;
3
(2)实验室制氨气:2NH Cl + Ca(OH) CaCl + 2NH ↑ + 2H O
4 2 2 3 2
(3)白色的无水硫酸铜遇水会变成蓝色,可以用于检测微量水的存在;
(4)碱石灰可以吸收水分,可以干燥氨气;
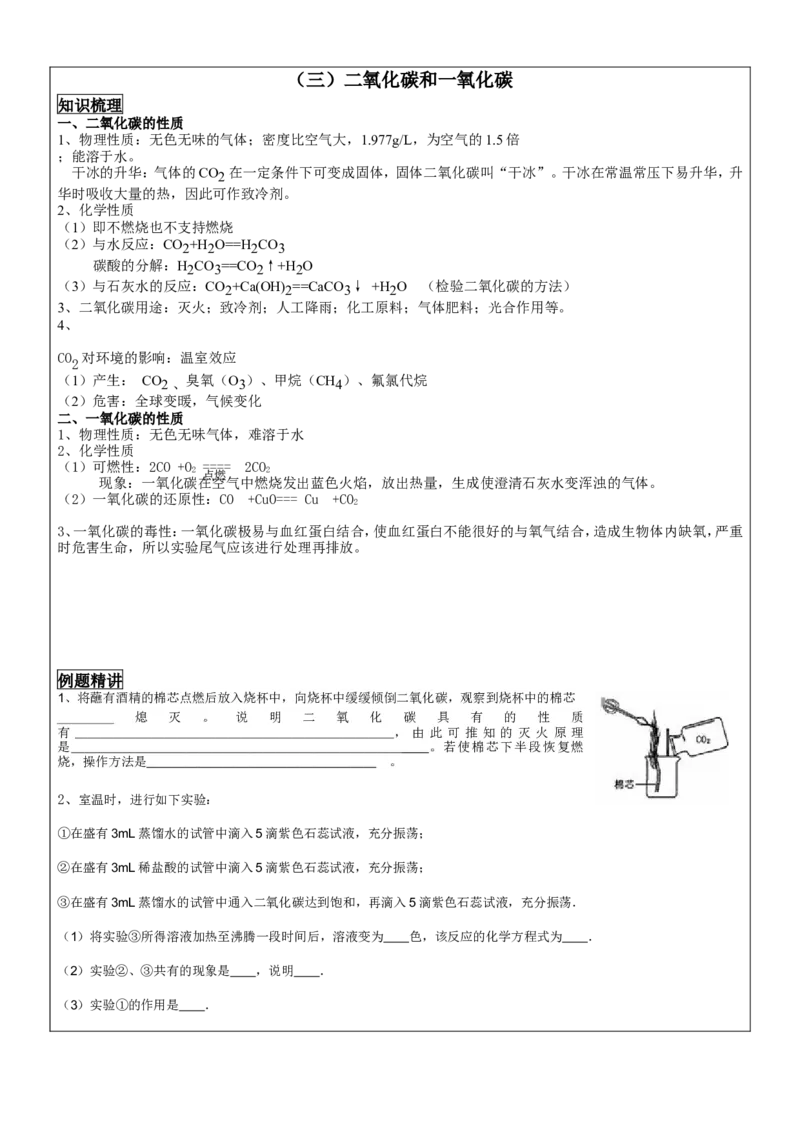
利用氨气还原氧化铜的反应,可设计测定铜元素相对原子质量近似值的实验。原理是先称量反应物氧化铜的质量,反应完全
后测定生成物水的质量,由此计算铜元素相对原子质量。为此设计了下列实验装置(图中部分夹持仪器省略,加入的NH C1
4
与Ca(OH) 的量足以产生使CuO完全还原的氨气):
2
图9
请回答下列问题
(1)写出氨气还原氧化铜的化学方程式
(2)B装置的作用是 D装置的作用是 __________
(3)为了确认没有水进入C装置中,需在整套装置中添加装置M于 (选填序号)。
a. A-B间 b. B-C间 c.C-D间
(4)在本实验中,若测得水的质量为a g,反应物氧化铜的质量为b g,则铜元素的相对原子质量是____。
(5)在本实验中,还可通过测定______和_____的质量,达到实验目的。(三)二氧化碳和一氧化碳
知识梳理
一、二氧化碳的性质
1、物理性质:无色无味的气体;密度比空气大,1.977g/L,为空气的1.5倍
;能溶于水。
干冰的升华:气体的CO2 在一定条件下可变成固体,固体二氧化碳叫“干冰”。干冰在常温常压下易升华,升
华时吸收大量的热,因此可作致冷剂。
2、化学性质
(1)即不燃烧也不支持燃烧
(2)与水反应:CO2+H2O==H2CO3
碳酸的分解:H2CO3==CO2 ↑+H2O
(3)与石灰水的反应:CO2+Ca(OH)2==CaCO3 ↓ +H2O (检验二氧化碳的方法)
3、二氧化碳用途:灭火;致冷剂;人工降雨;化工原料;气体肥料;光合作用等。
4、
CO 对环境的影响:温室效应
2
(1)产生: CO2 、臭氧(O3 )、甲烷(CH4 )、氟氯代烷
(2)危害:全球变暖,气候变化
二、一氧化碳的性质
1、物理性质:无色无味气体,难溶于水
2、化学性质
(1)可燃性:2CO +O ==== 2CO
2 点燃 2
现象:一氧化碳在空气中燃烧发出蓝色火焰,放出热量,生成使澄清石灰水变浑浊的气体。
(2)一氧化碳的还原性:CO +CuO=== Cu +CO
2
3、一氧化碳的毒性:一氧化碳极易与血红蛋白结合,使血红蛋白不能很好的与氧气结合,造成生物体内缺氧,严重
时危害生命,所以实验尾气应该进行处理再排放。
例题精讲
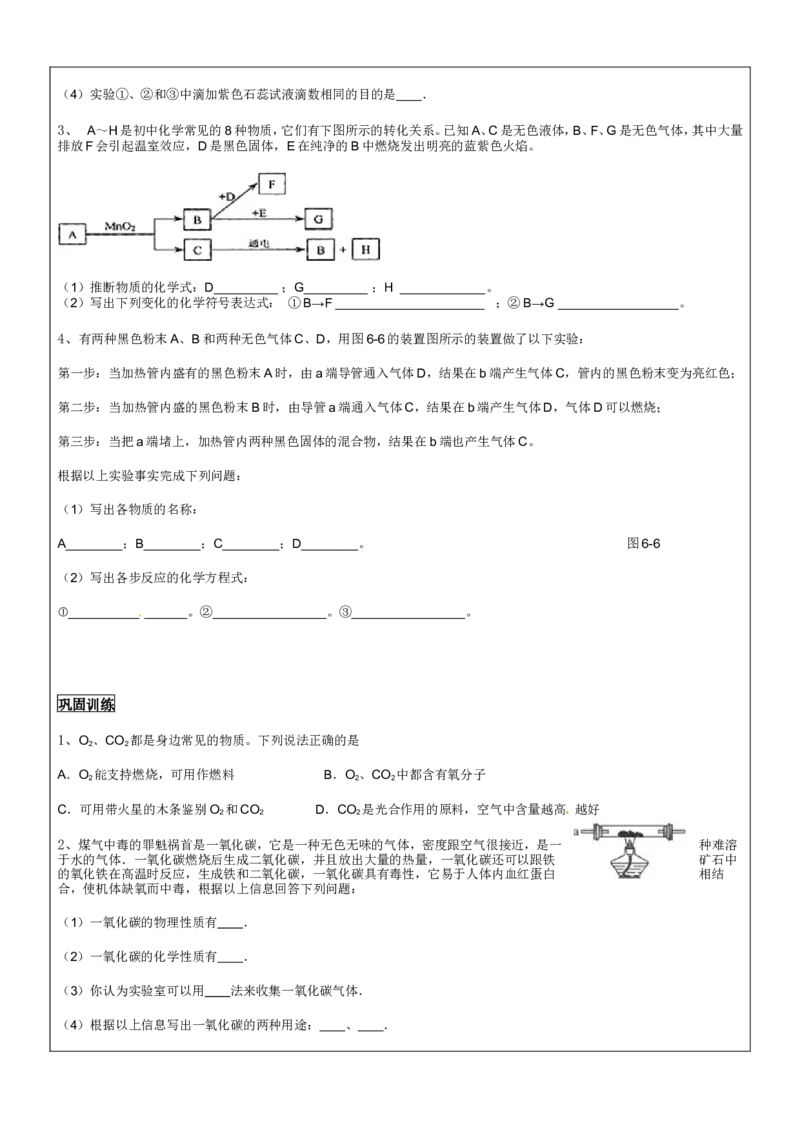
1、将蘸有酒精的棉芯点燃后放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到烧杯中的棉芯
________ 熄 灭 。 说 明 二 氧 化 碳 具 有 的 性 质
有 , 由 此 可 推 知 的 灭 火 原 理
是 。若使棉芯下半段恢复燃
烧,操作方法是 。
2、室温时,进行如下实验:
①在盛有3mL蒸馏水的试管中滴入5滴紫色石蕊试液,充分振荡;
②在盛有3mL稀盐酸的试管中滴入5滴紫色石蕊试液,充分振荡;
③在盛有3mL蒸馏水的试管中通入二氧化碳达到饱和,再滴入5滴紫色石蕊试液,充分振荡.
(1)将实验③所得溶液加热至沸腾一段时间后,溶液变为 色,该反应的化学方程式为 .
(2)实验②、③共有的现象是 ,说明 .
(3)实验①的作用是 .(4)实验①、②和③中滴加紫色石蕊试液滴数相同的目的是 .
3、 A~H是初中化学常见的8种物质,它们有下图所示的转化关系。已知A、C是无色液体,B、F、G是无色气体,其中大量
排放F会引起温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰。
(1)推断物质的化学式:D_________ ;G_________ ;H ____________。
(2)写出下列变化的化学符号表达式: ①B→F _____________________ ;②B→G _________________。
4、有两种黑色粉末A、B和两种无色气体C、D,用图6-6的装置图所示的装置做了以下实验:
第一步:当加热管内盛有的黑色粉末A时,由a端导管通入气体D,结果在b端产生气体C,管内的黑色粉末变为亮红色;
第二步:当加热管内盛的黑色粉末B时,由导管a端通入气体C,结果在b端产生气体D,气体D可以燃烧;
第三步:当把a端堵上,加热管内两种黑色固体的混合物,结果在b端也产生气体C。
根据以上实验事实完成下列问题:
(1)写出各物质的名称:
A________;B________;C________;D________。 图6-6
(2)写出各步反应的化学方程式:
①__________ ______。②________________。③________________。
巩固训练
1、O 、CO 都是身边常见的物质。下列说法正确的是
2 2
A.O 能支持燃烧,可用作燃料 B.O 、CO 中都含有氧分子
2 2 2
C.可用带火星的木条鉴别O 和CO D.CO 是光合作用的原料,空气中含量越高 越好
2 2 2
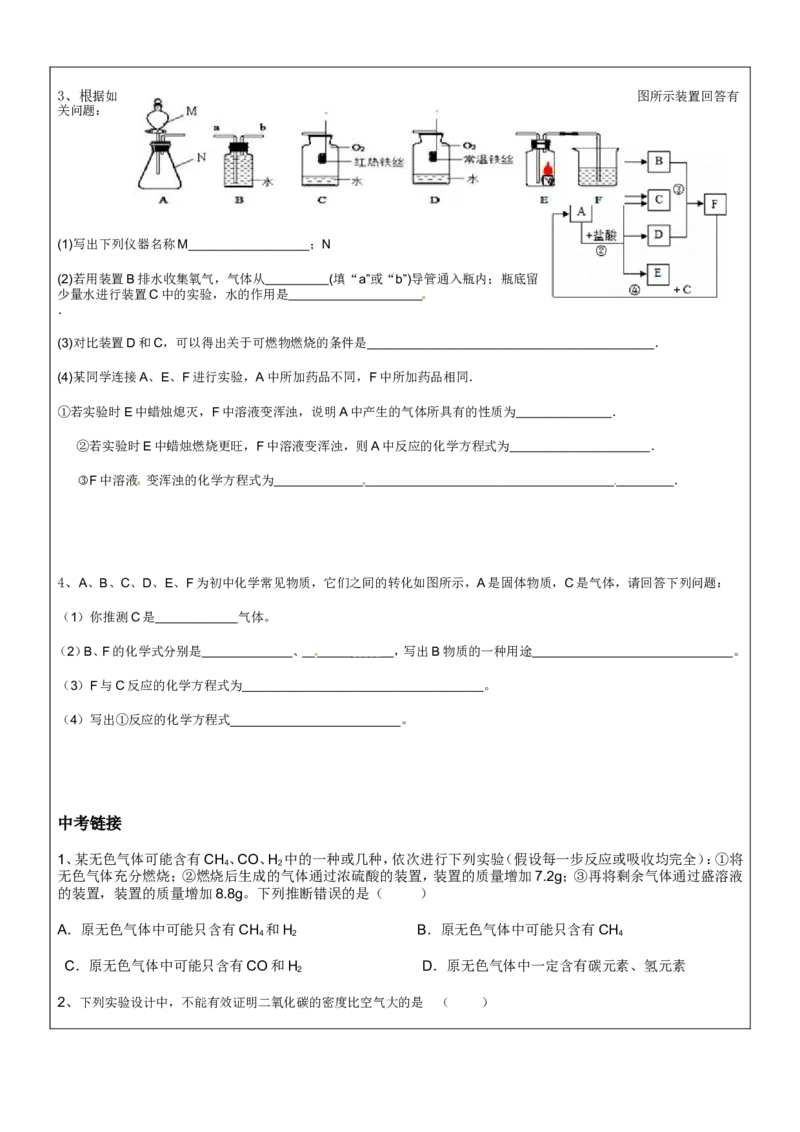
2、煤气中毒的罪魁祸首是一氧化碳,它是一种无色无味的气体,密度跟空气很接近,是一 种难溶
于水的气体.一氧化碳燃烧后生成二氧化碳,并且放出大量的热量,一氧化碳还可以跟铁 矿石中
的氧化铁在高温时反应,生成铁和二氧化碳,一氧化碳具有毒性,它易于人体内血红蛋白 相结
合,使机体缺氧而中毒,根据以上信息回答下列问题:
(1)一氧化碳的物理性质有 .
(2)一氧化碳的化学性质有 .
(3)你认为实验室可以用 法来收集一氧化碳气体.
(4)根据以上信息写出一氧化碳的两种用途: 、 .3、根据如 图所示装置回答有
关问题:
(1)写出下列仪器名称M ;N
(2)若用装置B排水收集氧气,气体从 (填“a”或“b”)导管通入瓶内;瓶底留
少量水进行装置C中的实验,水的作用是
.
(3)对比装置D和C,可以得出关于可燃物燃烧的条件是 .
(4)某同学连接A、E、F进行实验,A中所加药品不同,F中所加药品相同.
①若实验时E中蜡烛熄灭,F中溶液变浑浊,说明A中产生的气体所具有的性质为 .
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应的化学方程式为 .
③F中溶液 变浑浊的化学方程式为 .
4、A、B、C、D、E、F为初中化学常见物质,它们之间的转化如图所示,A是固体物质,C是气体,请回答下列问题:
(1)你推测C是 气体。
(2)B、F的化学式分别是 、 ,写出B物质的一种用途 。
(3)F与C反应的化学方程式为 。
(4)写出①反应的化学方程式________________________。
中考链接
1、某无色气体可能含有CH 、CO、H 中的一种或几种,依次进行下列实验(假设每一步反应或吸收均完全):①将
4 2
无色气体充分燃烧;②燃烧后生成的气体通过浓硫酸的装置,装置的质量增加7.2g;③再将剩余气体通过盛溶液
的装置,装置的质量增加8.8g。下列推断错误的是( )
A.原无色气体中可能只含有CH 和H B.原无色气体中可能只含有CH
4 2 4
C.原无色气体中可能只含有CO和H D.原无色气体中一定含有碳元素、氢元素
2
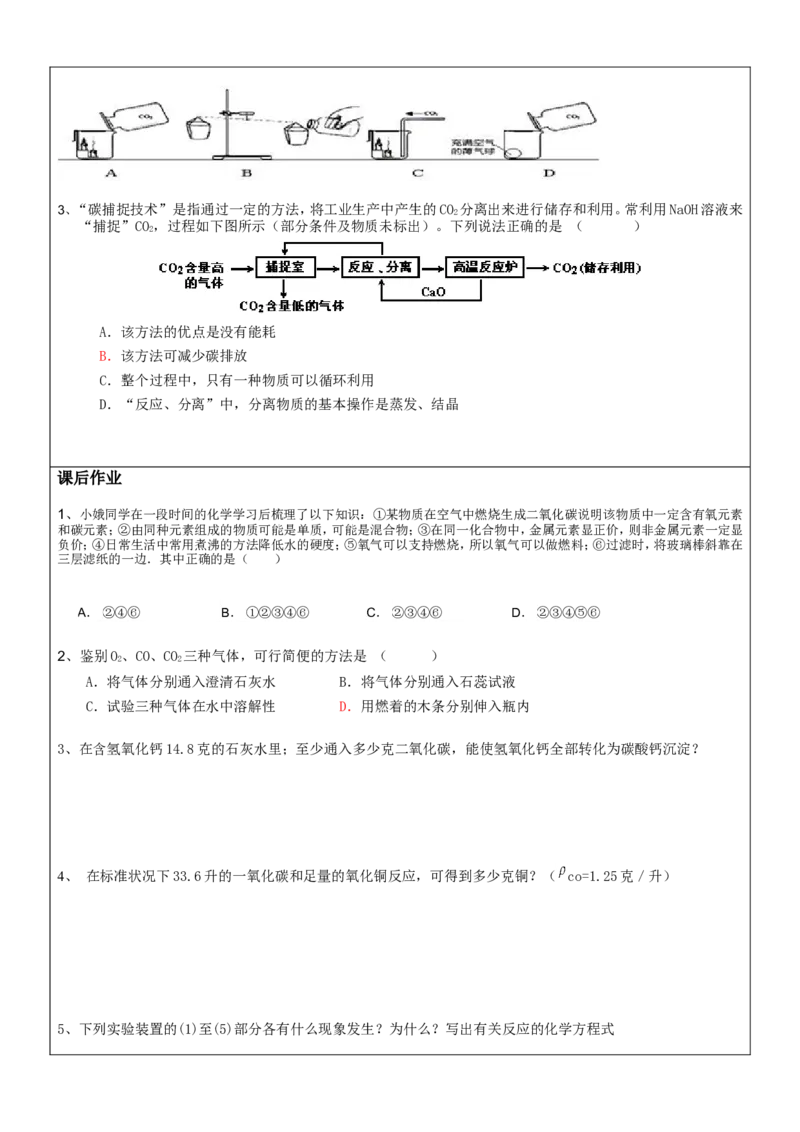
2、下列实验设计中,不能有效证明二氧化碳的密度比空气大的是 ( )3、“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO
2
分离出来进行储存和利用。常利用NaOH溶液来
“捕捉”CO,过程如下图所示(部分条件及物质未标出)。下列说法正确的是 ( )
2
A.该方法的优点是没有能耗
B.该方法可减少碳排放
C.整个过程中,只有一种物质可以循环利用
D.“反应、分离”中,分离物质的基本操作是蒸发、结晶
课后作业
1、小娥同学在一段时间的化学学习后梳理了以下知识:①某物质在空气中燃烧生成二氧化碳说明该物质中一定含有氧元素
和碳元素;②由同种元素组成的物质可能是单质,可能是混合物;③在同一化合物中,金属元素显正价,则非金属元素一定显
负价;④日常生活中常用煮沸的方法降低水的硬度;⑤氧气可以支持燃烧,所以氧气可以做燃料;⑥过滤时,将玻璃棒斜靠在
三层滤纸的一边.其中正确的是( )
A.②④⑥ B.①②③④⑥ C.②③④⑥ D.②③④⑤⑥
2、鉴别O、CO、CO 三种气体,可行简便的方法是 ( )
2 2
A.将气体分别通入澄清石灰水 B.将气体分别通入石蕊试液
C.试验三种气体在水中溶解性 D.用燃着的木条分别伸入瓶内
3、在含氢氧化钙14.8克的石灰水里;至少通入多少克二氧化碳,能使氢氧化钙全部转化为碳酸钙沉淀?
4、 在标准状况下33.6升的一氧化碳和足量的氧化铜反应,可得到多少克铜?( co=1.25克/升)
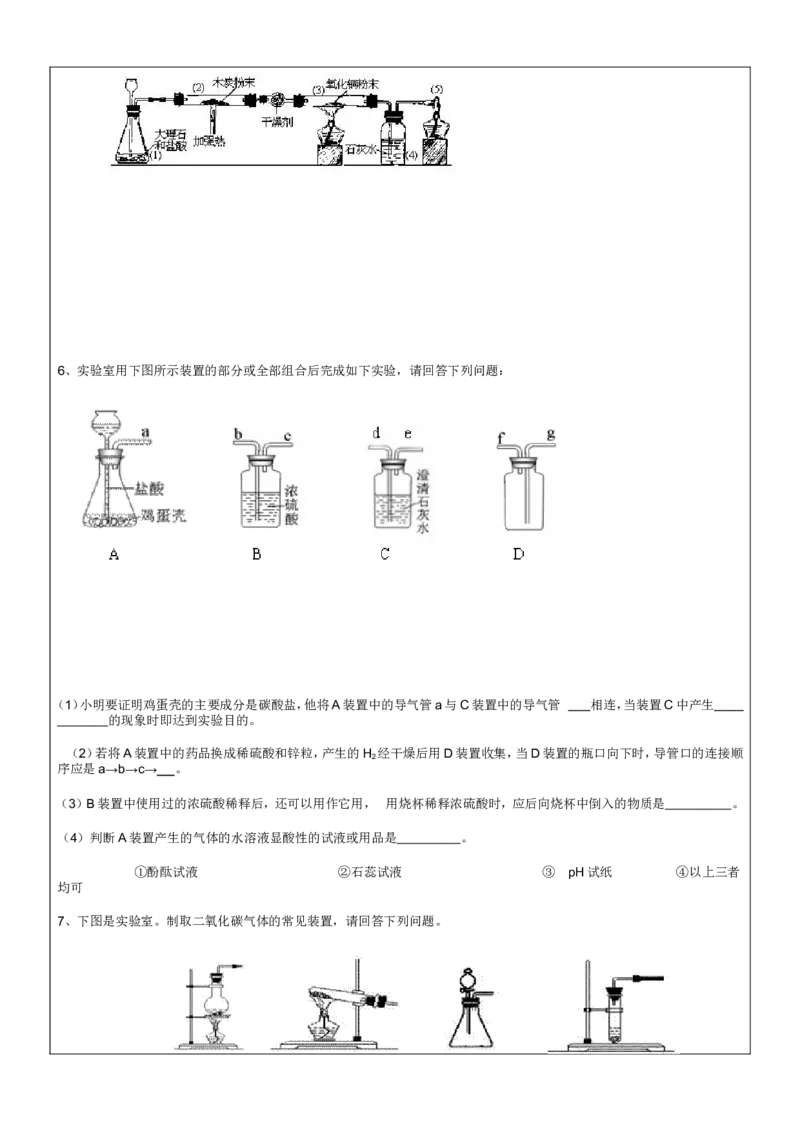
5、下列实验装置的(1)至(5)部分各有什么现象发生?为什么?写出有关反应的化学方程式6、实验室用下图所示装置的部分或全部组合后完成如下实验,请回答下列问题:
(1)小明要证明鸡蛋壳的主要成分是碳酸盐,他将A装置中的导气管a与C装置中的导气管 相连,当装置C中产生
的现象时即达到实验目的。
(2)若将A装置中的药品换成稀硫酸和锌粒,产生的H 经干燥后用D装置收集,当D装置的瓶口向下时,导管口的连接顺
2
序应是a→b→c→ 。
(3)B装置中使用过的浓硫酸稀释后,还可以用作它用, 用烧杯稀释浓硫酸时,应后向烧杯中倒入的物质是 。
(4)判断A装置产生的气体的水溶液显酸性的试液或用品是 。
①酚酞试液 ②石蕊试液 ③ pH试纸 ④以上三者
均可
7、下图是实验室。制取二氧化碳气体的常见装置,请回答下列问题。A B C D
(1)仪器a的名称是 。
(2)实验室不用浓盐酸和大理石制二氧化碳,因为 。
(3)若用稀硫酸和大理石制二氧化碳时,会生成微溶的硫酸钙,覆盖在大理石的表面,从而阻止反应的继续进行。如果对稀硫
酸和大理石加热,反应就能进行,原因是 若在上述溶液中加铵盐,则反应
速度进一步加快,请写出一种铵盐的名称或化学式 。据此判断,稀硫酸和大理石反应制取二氧化碳时最宜选用
上述装置中的( )来完成。
(4)写出检验二氧化碳的化学方程式