文档内容
第十一单元 盐 化肥 复习
(一) 重点、难点突破
Ⅰ生活中几种常见的盐
1.盐的概念:由金属离子和酸根离子构成的化合物(离子化合物);
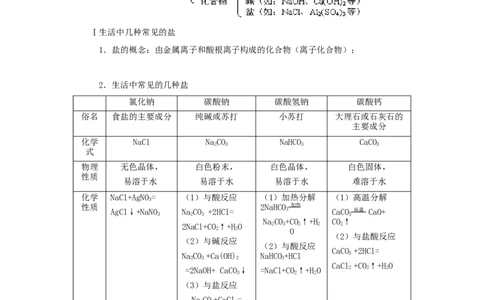
2.生活中常见的几种盐
氯化钠 碳酸钠 碳酸氢钠 碳酸钙
俗名 食盐的主要成分 纯碱或苏打 小苏打 大理石或石灰石的
主要成分
化学 NaCl NaCO NaHCO CaCO
2 3 3 3
式
物理 无色晶体, 白色粉末, 白色晶体, 白色固体,
性质
易溶于水 易溶于水 易溶于水 难溶于水
化学 NaCl+AgNO= (1)与酸反应 (1)加热分解 (1)高温分解
3
性质 2NaHCO 加热
AgCl↓+NaNO NaCO +2HCl= 3 CaCO 高温 CaO+
3 2 3 3
NaCO+CO↑+H CO↑
2NaCl+CO↑+HO 2 3 2 2 2
2 2 O
(2)与盐酸反应
(2)与碱反应
(2)与酸反应
CaCO +2HCl=
NaCO +Ca(OH) NaHCO+HCl 3
2 3 2 3
CaCl +CO↑+HO
=2NaOH+ CaCO↓ =NaCl+CO↑+HO 2 2 2
3 2 2
(3)与盐反应
NaCO+CaCl=
2 3 2
2NaCl+CaCO↓
3
用途 化工原料、调味 化工原料、洗涤剂 食品工业、医疗 建筑材料、制生石灰
3. 复分解反应及条件
(1)概念:两种化合物相互交换成分,生成另外两种化合物的反应叫复分解反应。
(2)发生的条件:生成物中有沉淀、或有气体或有水生成。
(3)掌握常见盐类溶解性表。4.盐的化学性质
(1)盐+金属 新金属+新盐,发生的条件是:盐可溶,而金属必须是金属活
动顺序表中相对靠前的金属(K、Ca、Na不能与盐溶液反应置换出其它金属)。
例:Cu+2AgNO = 2Ag+Cu(NO)
3 3 2
(2)盐+酸 新盐+新酸,发生的条件是:反应物都可溶,而生成物至少有一
种不溶(碳酸盐均可和酸反应)。
例:AgNO + HCl = AgCl↓+ HNO,CaCO +2HCl = CaCl +CO↑+HO
3 3 3 2 2 2
(3)盐+碱 新盐+新碱,发生的条件是:反应物都可溶,而生成物至少有一种
不溶。
例:CuSO + 2NaOH=NaSO + Cu(OH)↓
4 2 4 2
(4)盐+盐 新盐+新盐,发生的条件是:反应物都可溶,而生成物至少
有一种不溶。
例:NaCO+CaCl=2NaCl+CaCO↓
2 3 2 3
5.碳酸根离子或碳酸氢根离子的检验
(1)步骤:加入稀盐酸,并将产生的气体通入澄清石灰水中。
(2)现象:澄清石灰水变浑浊。
(3)结论:原物质中一定有碳酸根离子或碳酸氢根离子
说明:实验室制二氧化碳选用大理石或石灰石与稀盐酸反应,原材料易得且价格
便宜,一般不用纯碳酸钙、碳酸钠或碳酸氢钠的原因是相对成本较高,反应速率过快
不易控制。不用浓盐酸的原因是浓盐酸有挥发性,使制得的二氧化氧碳不纯。不用硫
酸的原因是反应会生成微溶的硫酸钙,覆盖在大理石或石灰石上面,阻止反应进一步
发生。
6.铵盐的检验:加碱微热产生刺激性气味气体。原理是:NH++OH- NH↑+HO
4 3 2
7.粗盐的提纯
(1)粗盐中由于含有氯化镁和氯化钙等杂质,易吸收空气中的水分而潮解。
(2)溶解 过滤 蒸发结晶 计算产率
实验步骤 实验仪器 其中玻璃棒的作用
溶解 烧杯、玻璃棒 加速溶解
过滤 铁架台(带铁圈)、漏斗、烧杯、玻璃棒 引流
使液体受热均匀,防止
蒸发 铁架台(带铁圈)、蒸发皿、玻璃棒
液体飞溅Ⅱ化学肥料
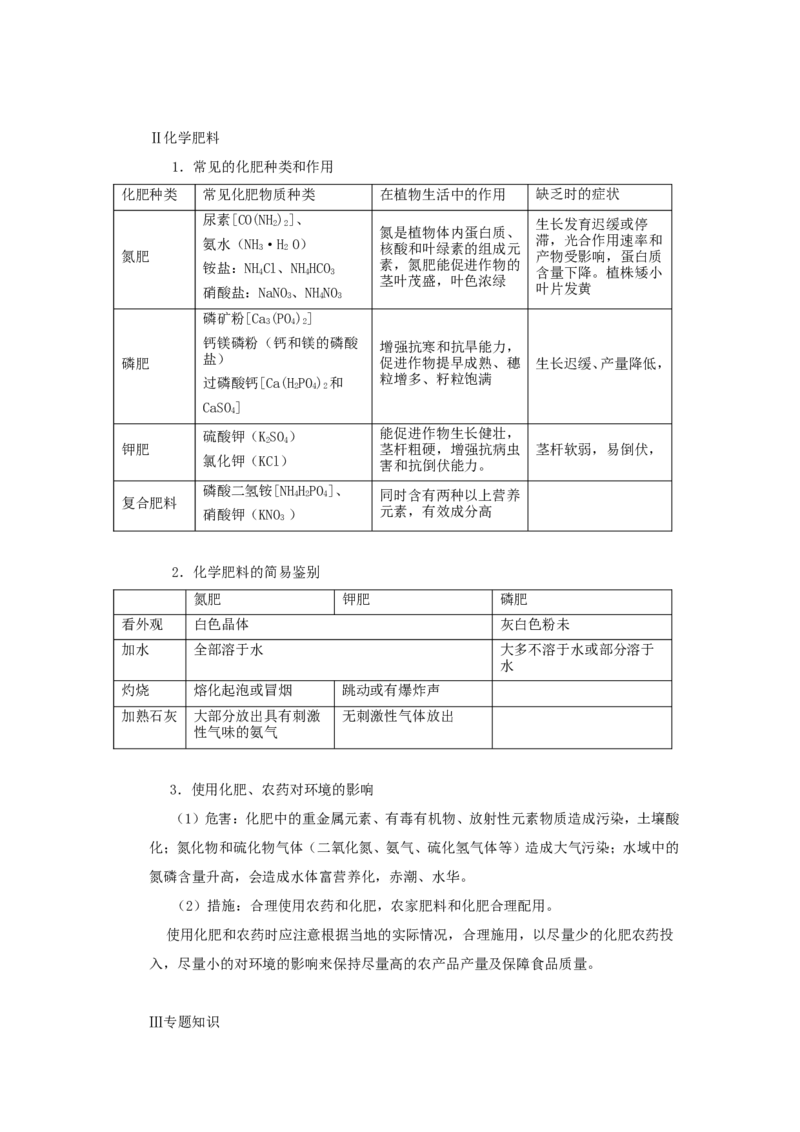
1.常见的化肥种类和作用
化肥种类 常见化肥物质种类 在植物生活中的作用 缺乏时的症状
尿素[CO(NH)]、
2 2 生长发育迟缓或停
氮是植物体内蛋白质、
氨水(NH·H O) 滞,光合作用速率和
3 2 核酸和叶绿素的组成元
氮肥 产物受影响,蛋白质
铵盐:NHCl、NHHCO 素,氮肥能促进作物的
4 4 3 含量下降。植株矮小
茎叶茂盛,叶色浓绿
硝酸盐:NaNO、NHNO 叶片发黄
3 4 3
磷矿粉[Ca(PO)]
3 4 2
钙镁磷粉(钙和镁的磷酸 增强抗寒和抗旱能力,
磷肥 盐) 促进作物提早成熟、穗 生长迟缓、产量降低,
过磷酸钙[Ca(HPO) 和 粒增多、籽粒饱满
2 4 2
CaSO]
4
硫酸钾(KSO) 能促进作物生长健壮,
2 4
钾肥 茎杆粗硬,增强抗病虫 茎杆软弱,易倒伏,
氯化钾(KCl)
害和抗倒伏能力。
磷酸二氢铵[NHHPO]、
4 2 4 同时含有两种以上营养
复合肥料
硝酸钾(KNO ) 元素,有效成分高
3
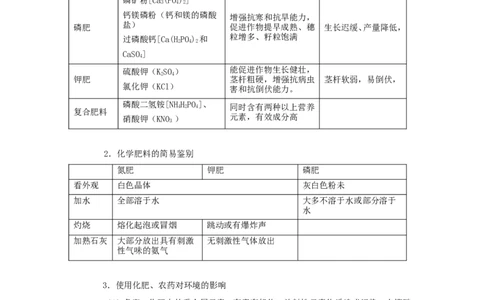
2.化学肥料的简易鉴别
氮肥 钾肥 磷肥
看外观 白色晶体 灰白色粉未
加水 全部溶于水 大多不溶于水或部分溶于
水
灼烧 熔化起泡或冒烟 跳动或有爆炸声
加熟石灰 大部分放出具有刺激 无刺激性气体放出
性气味的氨气
3.使用化肥、农药对环境的影响
(1)危害:化肥中的重金属元素、有毒有机物、放射性元素物质造成污染,土壤酸
化;氮化物和硫化物气体(二氧化氮、氨气、硫化氢气体等)造成大气污染;水域中的
氮磷含量升高,会造成水体富营养化,赤潮、水华。
(2)措施:合理使用农药和化肥,农家肥料和化肥合理配用 。
使用化肥和农药时应注意根据当地的实际情况,合理施用,以尽量少的化肥农药投
入,尽量小的对环境的影响来保持尽量高的农产品产量及保障食品质量。
Ⅲ专题知识1.几种重要离子的鉴别
(1)H+:若能使紫色石蕊试液变红的溶液则含有H+,或加入少量活泼金属,如果有
气体放出并证明是H,则含有H+;
2
(2)OH-:若能使紫色石蕊试液变蓝,或使无色酚酞试液变红,则含有OH-;
(3)NH+:用NaOH溶液检验,加热,若产生能使湿润红色石蕊试纸变蓝的气体,
4
则含有NH+。
4
2.物质的提纯
要注意的是,除杂(或提纯)应遵循以下几条原则:
(1)在除去原有杂质时,不要与要保留的物质发生反应;
(2)在除去原有杂质时,不能引入新的杂质;
(3)常用加入某种物质,使杂质转化为沉淀或气体而除去的方法来除杂(或提纯)。
3.物质的鉴别
在物质的鉴别过程中,不用或只用一种其它试剂鉴别一组物质的问题,是物
质鉴别题中的两种重要类型。这类问题的解题方法通常有两种:
(1) 从具有特征的物质入手,用看颜色、闻气味等方法先确定其中有特征的物
质,再用其鉴别其它的物质(初中化学常利用铜离子或铁离子的颜色与众
不同的特征来设计这类鉴别问题)。
(2) 如果被鉴别物质通过两两混合可产生不同的实验现象(如不同的沉淀与气
体等实验现象),也可以用来作为鉴别这些物质的方法。
4.物质的共存
物质能否共存是酸碱盐学习中的一个使初学者头痛的问题。对此,我们可简单
归纳如下:
(1) 碳酸根与酸和钙离子不能共存;
(2) 铜盐、铁盐等与碱不能共存;
(3)酸与碱、碱与酸性氧化物不能共存。
Fe3+ + 3OH- = Fe(OH) ↓ 红褐色沉淀
3
Cu2+ +2OH- = Cu(OH) ↓ 蓝色沉淀
2
H+ +OH- =HO
22H+ +CO2- = HO+CO↑ 无色气泡
3 2 2
Ca2+ +CO2- = CaCO ↓ 白色沉淀
3 3
(二)学习方法建议
1.弄清概念,对于化学概念是否达到准确的理解,主要有两个重要标志:一是能否准确
表达这个概念的内涵和外延;二是能否正确解答相应的基本问题,所以,我们在理解概念时,
要特别注意需较透彻的理解概念的内涵和外延,并学会正确的解答相应的基本问题。
本单元的概念较多,能否正确的理解概念,是学好酸,碱,盐的前提。比如能够理解有关
酸碱盐的定义,分清酸碱盐类物质是认识它们内在反应规律的前提。
2.重比较,区分易混淆概念和知识。比如盐的化学性质,与酸、碱的化学性质的区别与
联系等,通过对比,教师讲评,鼓励学生积极参与教学过程,激发学生参与、表现及成功的欲
望。同时由个别学生设计实验方案来引导全体学生,探究、创新、思考以新带旧、以旧促新知
识的学、质、疑,再次激发兴趣。
3.抓归纳,从整体上把握盐的相关知识。本单元的知识对历届学生来讲,都感到有难度。
无论是从它们的物理性质还是从化学性质上来讲都比较易混淆,更主要的是化学反应以及
化学方程式的书写不知遵循哪些规律。所掌握的都是零散的、不成系统的。通过复习课,应将
学生头脑中已有的知识系统化、网络化。通过本节课的学习,完善并提高学生对盐的性质及
反应规律的进一步掌握。
4.联系实际,注重应用,结合实验。盐的相关知识,从学习程序来说对学生并不陌生。如
学习物质从物质的物理性质、化学性质入手,到物质的用途学习。物理性质主要学习色、味、
态、溶解性、密度、熔沸点等内容。课本中介绍的几种盐是学生既熟悉又陌生的物质,教学中
应发挥学生的主体作用,利用其熟悉的知识激发学习兴趣、提高学习信心,挖掘学生的主动
性进行学习。教学中应充分利用化学实验对学生形成知识的重要作用。实验探究对激发学生
学习兴趣、提高学生学习能力有着相当重要的作用。
获取和掌握知识并不是教学的最终目的,我们的最终目的是要学生将学到的知识加以
应用。所以在教学最后应用知识环节,精心设计问题,培养学生的灵活应用能力,以达到使学
生学有所用的目的。