文档内容
第八单元 金属和金属材料
课题一 金属材料 第一课时
导学知识目标点:
1、了解常见金属的物理性质(通性和个性)
2、了解物质的性质与用途的关系
课时:1课时
导学方法:创设情境—联系实际—得出结论—解决实际问题
导学过程:
一、课前导学:
1、由金属材料制成家里的日常生活用品:
2、金属材料包括 和 。
3、Al、Fe、Cu发现朝代有早到晚排列顺序是: 、 、 。
二、课堂导学:
1、探究金属的物理性质:
①仪器和药品(在家中寻找一些废弃的金属用品,如:易拉罐、废电池皮、回形针、铜导线、罐头瓶盖等。)
②步骤
a把它们打磨后,观察颜色状态,并试试能否被弯曲折断。b用小刀在表面刻划,比较它们的硬度的大小。c
在火焰上方烧烤,试试它们能不能传热。d用铁锤锤击,看能否拉长压扁。e用电池、导线和小灯泡试试它
们能不能导电。
③交流讨论
金属的物理性质:
① ;② ;
③ ;④ 。
个性: 。
2、讨论:课本P3
3、金属的性质与用途之间的关系
用途主要由性质决定。还需考虑的因素:价格、资源、是否美观、使用是否便利、废物是否易于回收利
用和对环境的影响。
金属之最:
⑴地壳中含量最多的金属元素—铝⑵人体中含量最高的金属元素—钙⑶目前世界年产量最高的金
属—铁⑷导电、导热性最好的金属—银⑸硬度最高的金属—铬⑹熔点最高的金属—钨⑺熔点最低的金属
—汞⑻密度最大的金属—锇⑼密度最小的、最轻的金属—锂
课堂练习:
1、大多数金属都有一些共同的物理性质:一般有金属光泽,______ 和_ 较大, 较高,具有良好
和 、 性能。在室温下除 外,金属都是 ,但不同的金属还具有各自的一些特性,而且
各种金属的颜色、硬度、密度、熔点、导电性和导热性等物理性质差别也较大。
2、日常生活中使用的自来水管,你认为选用下面哪一种既经济又耐用( )
A.普通钢管 B.铜管 C.不锈钢管 D.塑料管
3、下列金属中导电性能最好的是 ( )
A.铜 B.铝 C.铁 D.银
课外练习:
1、用金属的化学式填空:
①白铁皮表面镀上的一层金属是 。②镀在保温瓶胆夹层的银白色的金属是_____。
③包装糖果、香烟的银白色金属材料是______。④体温表中的液体金属是___________。
⑤做干电池负极的材料是______。⑥广泛用于电线和电缆的金属是______、_______。
1⑦广泛用航空工业和造船工业的金属是___。⑧地壳中通常以单质形式存在的金属是___。
2、人类的生产和生活中离不开金属材料。通常所说的“金属材料”,既包括纯金属,也包括各种合金。下
列金属材料不属于合金的是( )
A.青铜 B.生铁 C.紫铜 D.焊锡
3、一种新兴的金属由于其密度小,延展性好,耐腐蚀性强,它和它的合金在航海、航空和化学工业中正逐
步取代铝和铝合金而被广泛应用。该金属是( )
A.锌 B.钛 C.镁 D.锰
4、用量最大的前三种金属是__________、__________、_________。地壳中含量最多的前两种金属是
____________、___________。熔点最高的金属是________,熔点最低的金属是_________。灯泡中发光灯
丝使用的金属是________。
5、某新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属线,当玻璃被击碎时,与金属线相连的警
报系统就会立刻报警。“防盗玻璃”能报警,这利用了金属的( )
A.延展性 B.导电性 C.弹性 D.导热性
6、人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。请回答:
(1)地壳中含量最多的金属元素是 。
(2)根据下图的应用实例,试说出金属具有的两点物理性质 、
(3)日常使用的金属材料多数属于合金,下表列出了一些常见合金的主要成分和性能。
合 合金的主要性能 主要成分及纯金属的性能
金
焊 熔点183℃ 锡:熔点232℃;铅:熔点327℃
锡
硬 强度和硬度好 铝、铜、镁等。硬度小,质软
铝
不锈钢 抗腐蚀性好 铁、铬、镍等。纯铁抗腐蚀性能不如不锈钢
由上表推断,与组成合金的纯金属相比,合金的优点一般有(填序号 )
①强度更低 ②硬度更高 ③熔点更高 ④抗腐蚀性更好
课后反思:
2第八单元 金属和金属材料
课题一 金属材料 第二课时
导学知识目标点:
合金及合金的性能、用途
课时:1课时
导学方法:创设情境—联系实际—得出结论—解决实际问题
导学过程:
一、课前导学:
1、合金:
2、铁的合金包括 和 。
二、课堂导学:
1、合金:
2、探究纯金属和合金的性质比较:
比较黄铜片和铜片、焊锡和锡的光泽和颜色;将它们相互刻划,比较它们的硬度。
现象
性质比较
黄铜 铜 焊锡 锡
光泽和颜色
硬 度
结 论
讨论:课本P5
纯金属 合金
铅 镉 铋 锡 焊锡 武德合金
熔点/℃ 327 321 271 232 183 70
结论
结论:
3 、铁的合金:包括 和
生铁 钢
含碳量 2~4.3% 0.03~2%
性 能 硬而脆,无韧性,可铸,不可锻轧 坚硬而有韧性,可铸,可锻轧,可延压
4、钛及钛合金
优良性能:
课堂练习:
1.人类的生产和生活中离不开金属材料。通常所说的“金属材料”,既包括纯金属,也包括各种合金。下
列金属材料不属于合金的是( )
A.青铜 B.生铁 C.紫铜 D.焊锡
2.下列关于合金的说法正确的是( )
A.合金都是不同的金属组成的 B.合金属于化合物
3C.合金不能导电、导热 D.合金的很多性能与组成它的纯金属不同
课外练习:
1、人类的生产和生活中离不开金属材料。通常所说的“金属材料”,既包括纯金属,也包括各种合金。下
列金属材料不属于合金的是( )
A.青铜 B.生铁 C.紫铜 D.焊锡
2、下列物质不属于合金的是()
A、钢B、不锈钢C、生铁D、四氧化三铁
3、对于合金的说法正确的是()
A、合金是纯净物B、合金是化合物C、合金是混合物D、以上说法均不对
4、被认为21世纪的重要金属材料的是()
A 黄金 B、白银 C、青铜 D、钛及其合金
5、连线:把合金与其用途用线连结。
做钢轨 硬铝
做医疗器械 焊锡
焊接金属 不锈钢
做飞机轮船 锰钢
6、2008年6月4日,第29届北京奥运会火炬接力传递活动在长沙市进行,长沙变成了欢乐的海洋,广大
师生参加了传递活动,目睹了“祥云”火炬的风采。美丽的“祥云”火炬是由金属合金材料制成的,合
金与纯金属比较,其优越的性能有(答现一条即可)
,原因是 。
7、钛和钛合金被认为是21世纪的重要金属材料.钛合金和人体有很好的"相容性",利用钛合金这一特性可
以( )
A.制造船舶 B.制保险丝 C.制人造骨 D.制造飞机
课后反思:
4第八单元 金属和金属材料
课题2 金属的化学性质
导学知识目标点:
1、金属的化学性质:(3条)
2、置换反应的概念。
3、金属与酸、盐性液反应现象。
4、金属活动顺序表及其应用(3条)
课时:1课时
导学方法:猜想与探究—观察与检验—分析与归纳—解释与结论
导学过程:
一、课前导学:
1、铁能在纯氧气中燃烧吗?若能,写出反应的化学方程式。
2、金属活动性顺序:
3、置换反应: 。
二、课堂导学:
1、金属与氧气反应
镁、铝常温下很容易反应,铜铁常温下反应很慢,金在高温下也不反应。
结 论:不同的金属与氧气反应的难易程度不同。
活动性:Mg、Al>Fe、Cu>Au
2、金属与酸的反应
实验探究1:
现象 反应的化学方程式
金属
稀盐酸 稀硫酸 稀盐酸 稀硫酸
镁 Mg+2HCl=MgCl+H↑ Mg+H SO =MgSO +H ↑
2 2 2 4 4 2
锌 Zn+2HCl=ZnCl+H ↑ Zn+H SO =ZnSO +H ↑
2 2 4 4 2
铁 Fe+2HCl=FeCl +H ↑ Fe+H SO =FeSO +H ↑
2 2 2 4 4 2
铜
结 论:不同的金属与酸反应的剧烈程度不同。
活动性: 。
3、置换反应:__________________________________ 用字母表示_____________________
4、金属与某些可溶性盐溶液的反应
实验 现象 化学方程式
铝丝浸入硫酸铜溶液中 溶液蓝色变浅,铝丝上附着一层红色固体 2Al+3CuSO=Al(SO)+3Cu
4 2 43
铜丝浸入硝酸银溶液中 铜丝上附有银白色固体,溶液由无色变为蓝色Cu+2AgNO=Cu(NO)+2Ag
3 32
铜丝浸入硫酸铝溶液中 无明显现象
结 论 :
。
5活动性: 。
5、金属活动性有强逐渐减弱
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Au Pt Au
金属活动性由强逐渐减弱
6、金属活动性顺序表的重要应用
①在金属活动性顺序中,金属的位置越靠前,它的活动性就越强。
K_____Ca Fe_____Zn Cu_______Ag
②在金属活动性顺序中,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
下列反应能否发生?为什么?
①Zn+HCl —— ②Mg+HSO —— ③Cu+HCl——
2 4
④Fe+ HSO —— ⑤Ag+ HSO ——
2 4 2 4
③在金属活动性顺序中,在金属活动顺序里,位于前面的金属能把位于后面的金属从它们盐溶液中置换
出来。
下列反应能否发生?为什么?
①Zn+CuSO —— ②Cu+AgNO —— ③Ag+ ZnSO—— ④Fe+CuSO——
4 3 4 4
课堂练习:
1、在金属活动性顺序表中,位于_____的金属能把位于_____的金属从它们化合物的_____里置换出来。
2、金属活动性大于铁,小于铝的是 ( )
A.Zn B.K C.Cu D.Mg
3、某同学为判断A、B、C三种金属的活动性大小,设计了下列四个实验:
(1)将金属B放入C的盐溶液中,看能否置换出C
(2)将金属B放入酸中,看能否置换出酸中的氢
(3)将金属A放入B的盐溶液,看能否置换出B
(4)将金属C放入A的盐溶液中,看能否置换出A
你认为上述可以不做的实验是( )
A、(1) B、(2) C、(3) D、(4)
4、我们常说的“真金不怕火炼”的原因是 ( )
A、金的熔点高 B、金的硬度大
C、金的密度大 D、金不活泼,高温时也不与氧气反应
课外练习:
1、将光亮的铁钉放入硫酸铜溶液中,能观察到的现象有:铁钉表面由___色变为____色;溶液由________
色逐渐变为_____色。写出其反应的化学方程式 。
2、设计除去杂质的实验方案,填写在下表(括号中为杂质)
混合物 除去杂质的化学方程式 主要操作步骤
铜粉(锌粉)
FeSO 溶液(CuSO)
4 4
4、新买的铝锅、铝壶用来烧开水时,凡是水浸到的地方都会变黑,说明水中有
A.钾的化合物 B.钠的化合物 C.钙的化合物 D.铁的化合物
5.将过量的铁粉放入含AgNO 和Zn(NO) 的混合溶液中,搅拌,使其充分反应后,过滤,滤液上留下的金属
3 3 2
是
A.Ag B.Fe、Ag C.Zn、Fe D.Zn、Fe 、Ag
6、将13g锌样品放入足量的硫酸中反应,放出的氢气是0.36g,则铁样品中含有的杂质可能是 ( )
A.Mg B.Al C.Cu D.Fe
7、市售紫葡萄的表面常附有一种浅绿色的斑点,它是为了防止霉菌而喷洒的农药“波尔多液”,“波尔
多液”是由硫酸铜溶液与石灰乳按一定比例混合而制成的;混合时发生的化学方程式是 ,
配制时不能用铁制容器是因为
8、有X、Y、Z三种金属,把Y投入到XCl2溶液中,Y表面有X析出;把X投入到Z(NO3)2溶液中,Z析出.
下列判断错误的是
A、金属活动性顺序是Y>X>Z B、金属活动性顺序是X>Z>Y
C、X、Y、Z可能是:铜、锌、汞 D、X、Y、Z可能是:铁、镁、铜
6课后反思:
第八单元 金属和金属材料
课题3 金属资源的利用和保护
导学知识目标点:
1、了解从常见铁矿石中提炼铁的原理。
2、冶炼铁的原理和含杂质等不纯量的化学方程式的计算。
课时:1课时
导学方法:联系实际—分析讨论—得出结论
导学过程:
一、课前导学:
1、常见的铁矿石 (主要成分 )、 (主要成分 )、 (主要成分
);
2、一氧化碳还原氧化铁的反应化学方程式:
二、课堂导学:
1、几种常见的金属矿物的名称和主要成分见下表。
金属矿物 赤铁矿 黄铁矿 菱铁矿 铝土矿 黄铜矿 辉铜矿
主要成分 FeO FeS FeCO AlO CuFeS CuS
2 3 2 3 2 3 2 2
2、铁的冶炼
原料 铁矿石、焦炭、石灰石等
在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
主要反
应原理 其主要反应原理为: Fe 2 O 3 +3CO 高温 3 CO 2 +2Fe
主要
高炉
设备
3、根据化学方程式对反应物或生成物中含有某些杂质进行有关计算
例如:某钢铁厂每天需消耗1000吨含氧化铁80%的赤铁矿,该场理论上日产含96%的生铁多少吨?
4、纯度与杂质质量分数的区别和联系
纯度=
杂质的质量分数=
纯度=
课堂练习:
71、地壳中含量最多的金属元素( )
A.铁 B.氧 C.硅 D.铝
2、用还原赤铁矿样品(主要成分为FeO,还有不与CO反应的杂质)18g,使反应中放出的CO 全部跟足量澄
2 3 2
清的石灰水反应,最后生成白色沉淀27g。则该样品中FeO 的质量分数为多少?
2 3
课外练习:
1、下列矿石的主要成分表达错误的是
A.黄铁矿(FeS) B.菱铁矿(FeCO) C.黄铜矿(CuFeS) D.辉铜矿(CuS)
2 3 2
2、还原铁的某氧化物2.16g,可以得到1.68g铁。则该种铁的氧化物的化学式为( )
A.FeO B.FeO C.FeO D.FeCO
2 3 3 4 3
3、用500t含氧化铁质量分数为70%的赤铁矿,可以炼出含杂质4%的生铁多少吨?
4、将150吨含杂质为10%的石灰石煅烧可得到含杂质质量分数为5%的生石灰多少吨?
课后反思:
89第八单元 金属和金属材料
课题3 金属资源的利用和保护
导学知识目标点:
1、了解金属锈蚀的条件以及防止金属锈蚀的方法。
2、认识回收利用废旧金属,资源保护的重要性。
课时:1课时
导学方法:联系实际—实验探究—得出结论—联系实际
导学过程:
一、课前导学:
1、铁制品锈蚀的条件是:
2、金属资源保护措施:
① ② ③
④ ⑤
二、课堂导学:
1、钢铁的锈蚀及其防护
(1)铁生锈条件的探究
现有洁净无锈的铁钉、试管、经煮沸迅速冷却的蒸馏水、植物油、棉花和干燥剂氯化钙。试设计实验
以证明铁制品锈蚀的条件。
现象 分析 结论
试管①
试管②
试管③
(2)铁制品的防护措施
①保持铁制品表面干燥和洁净。
②在铁制品表面涂一层保护膜(刷漆、涂油、电镀和烤蓝)。
③改变铁的组织结构,制成合金钢,如不锈钢。
2、金属资源保护
(1)防止金属腐蚀 (2)回收和利用废旧金属
(3)合理开采矿物(4)寻找金属代用品 (5)物尽其用
课堂练习:
1、铁生锈的主要条件是铁与 和 直接接触,防锈的方法有
许多例如: 、 。
2、金属资源有限,保护金属资源的有效途径有许多,举三种方法 、 、
。
3、铁生锈的过程是一个( )
A、剧烈的氧化反应 B、物理变化 C、缓慢氧化 D、快速的化学反应
4、车,船表面涂油漆的主要目的( )
A、防止撞坏 B、清洁美观 C、防止磨损 D、防止锈蚀
5.铁在一定条件下容易生锈,下列有关铁生锈的叙述错误的是( )
10A.铁生锈一定伴随着物理变化
B.铁生锈时,铁发生了缓慢氧化
C.铁生锈的本质就是铁与氧气反应生成氧化铁
D.铁生锈时,会有难以察觉的热量放出
6、下列各说法正确的是( )
A.在铁板表面镀上一层锌成为白铁,白铁是铁锌合金
B.铁是地壳中含量最多的金属元素
C.炼铁高炉炼出来的是生铁不是钢
D.从高炉排出来的废气,可以直接放空气
课外练习:
1、在面盆、痰盂等铁制品表面烧制搪瓷的目的是( )
A.增大硬度防止撞坏 B.增大厚度防止磨损
C.防止铁生锈且美观 D.美观和杀菌消毒作用
2、如图所示,大试管中是螺旋状光亮的铁丝,把试管倒插在水中放置一段时间,观察到铁丝表面有
___________生成,试管内水面将____ _____,产生这一现象的原因是
__________________________________________________________。
根据铁生锈的条件,填写出下列铁制品防锈的方法:
(1)钢锯条_____;(2)自行车车架______;(3)自行车车把____________;
(4)脸盆 ____ ;(5)不锈钢楼梯扶手_______;(6)铁制自来水管___________。
3、写出有关的化学反应方程式,并注明反应类型。
(1)铝很难从矿物中提取出来,因此利用电解氧化铝的方法得到金属铝。
___________________________________,反应类型____________________;
(2)古代湿法炼铜,“曾青的铁则化为铜”
___________________________________,反应类型____________________;
(3)法医常用锌和盐酸混合在一起,检验是否砒霜中毒,砒霜的主要成分为As O,若试样中有砒霜,则反
2 3
应生成砷化氢(AsH ),氯化锌和水。写出其反应的化学方程式:
3
__________________________________________________________;
(4)在潮湿的空气中,铜也能与空气中的二氧化碳、氧气、水等发生反应生成铜绿。
___________________________________,反应类型____________________;
(5)一氧化碳在高温下与铁矿石里的氧化铁(FeO)反应,生成铁和二氧化碳,化学反应方程式为是
2 3
______________________________,其中还原剂是____________________。
4、如果将一枚质量为12.8g的生锈的铁钉放入盛有87.2g稀硫酸的烧杯中,开始时铁钉表面的铁锈逐渐
溶解,溶液由无色变成_______,后来铁钉表面有_______产生,溶液又逐渐变成_________。如果等到铁
钉完全和稀硫酸反应,称量烧杯中所得溶质量为99.6g,请你计算生锈的铁钉中单质铁的质量分数。
课后反思:
11第九单元 溶液
课题 1 溶液的形成
导学目标知识点:
1.溶液,溶质,溶剂的概念及关系;
2.悬浊液和乳浊液的概念
3.溶解时的吸热和放热
课时:1课时
导学方法:创设情景→实验探究→归纳总结→联系实际→知识升华→激发兴趣
导学过程
一、课前导学:
溶液:
溶质: 溶剂:
乳浊液:
悬浊液:
二、课堂导学:
1.提问:海水是纯净的水吗?海水又苦有咸,这是为什么呢?
[学生讨论:海水的组成] 归纳得出结论:
2.[实验9-1]在20ml水中加入一匙蔗糖,用玻璃棒搅拌,还能看到蔗糖吗?
现象: 形成什么:
归纳总结: 叫做溶液
叫做溶质, 叫做溶剂
讨论:在蔗糖溶液和氯化钠溶液中,溶质是什么?溶剂是什么?
3.举出生活中一些常见溶液,并指出溶剂和溶质
课本P27讨论
4.[实验9-2]
溶剂 溶质 现象
水 碘
水 高锰酸钾
汽油 碘
汽油 高锰酸钾
[实验9-3]
溶剂 溶质 振荡前现象 振荡后现象 静置后现象 结论
水 乙醇
[实验9-4]
试管内加入的物 现象 把液体倒掉后的
质 试管是否干净
振荡前 振荡后 静置后
水和植物油
水和植物油及洗
涤剂
悬浊液:
乳浊液:
5.溶解时的吸热或放热现象
活动与探究:NaCl,NH NO ,NaOH分别放入水中溶解,并测量温度变化
4 3
水中加入的溶质 NaCl NH NO NaOH
4 3
加入溶质前水的温度
溶解现象
12溶质溶解后溶液的温度
结论
归纳总结:
教师引导,学生自我小结:
课堂练习:
1.下列物质与水混合,不能形成溶液的是( )
A.葡萄糖 B.硫酸铜 C.酒精 D.植物油
2.溶液的基本特征是( )
A.其组成中一定含有水 B.含有溶质和溶剂
C.具有均一性和稳定性 D.一定是无色透明的
3.将下列物质分别加到水中充分溶解,其中会使溶液的温度明显降低的物质是( )
A.NaOH固体 B.NH NO 固体 C.CaO固体 D.食盐固体
4 3
课后练习:
1.下列关于溶液的说法中正确的是( )
A.溶液一定是混合物 B.均一,稳定的液体都是溶液
C.凡是无色,透明的液体都是溶液 D.水和酒精混合形成的溶液,酒精是溶剂
2.下列溶液中,溶质是液体的为 ( )
A.医用葡萄糖溶液 B.20%的氢氧化钠溶 C.75%的消毒酒精 D.0.9%的生理盐水
3.下列清晰方法中利用乳化原理的是( )
A.用自来水洗手 B.用汽油清洗油污
C.用洗涤剂清洁餐具 D.用盐酸除水垢
4.写出下列溶液中溶质的化学式
(1)食盐水 (2)石灰水
(3)医用碘酒 (4)医用酒精 (5)浓盐酸
5.物质溶解的过程中发生两种变化,一种是溶质的分子(或离子)向水中扩散,这一过程要 热量,
另一种是溶质分子(或离子)和水作用,生成水合分子(或离子);这一过程要 热量,NaOH溶于水
时溶液温度升高,是因为
。
6.请你各举一个实例,说明下列有关溶液的叙述是错误的
(1)溶液一定是无色的。
实例: 溶液不是无色的;
(2)均一,稳定的液体都是溶液。
实例: 是液体,但是不是溶液;
(3)溶液中的溶质一定是固体
实例: 可做溶质,但不是固体;
(4)溶液中的溶剂一定是水。
实例: 溶液中的溶剂不是水。
课后反思:
课题2 溶解度
导学目标知识点:
131.饱和溶液与不饱和溶液的概念
2.饱和溶液与不饱和溶液相互转化方法
3.结晶的概念
4.判断溶液是饱和溶液的方法
课时:2课时
导学方法:学生阅读→教师总结→问题讨论→讲解总结→随堂练习→巩固提高
第一课时 N902
导学过程:
一、课前导学:
学生预习并完成相关概念:
饱和溶液:
不饱和溶液:
二、课堂导学:
1.提问:物质能不能无限制地溶解在一定量的水中呢?
2.课本P33 活动与探究
(1)取装有20ml水的烧杯
操作 加入5g氯化钠,搅拌 再加5g氯化钠,搅拌 再加5ml水,搅拌
现象
结论
(2)用硝酸钠代替氯化钠
操作 现象 结论
加入5g硝酸钾,搅拌
加入5g硝酸钾,搅拌
…………
加热
加入5g硝酸钾,搅拌
冷却
(学生根据实验现象进行讨论)
归纳总结:
叫做饱和溶液, 叫做不饱和溶液。
结晶:
3.判断某溶液是否饱和的方法:在一定条件下,溶质是否继续溶解
4.饱和溶液与不饱和溶液的相互转化
增加溶质或降低温度
不饱和溶液 饱和溶液
增加溶质或升高温度
[随堂练习]
1.如何判断某一蔗糖溶液是否饱和?
2.在一定温度下,向100g食盐饱和溶液中加入3g食盐,充分搅拌后,溶液的质量变为103g,此说法是否正
确,为什么?
3.“在一定量的氯化钠溶液中,加入少量硝酸钾固体,发现硝酸钾固体消失,则说明原氯化钠溶液不饱和”,
这句话是否正确?
教师引导,学生自我小结:
课堂练习:
1.要使一杯氯化铵不饱和溶液变为饱和溶液,可采取的方法是( )
14A.加水 B.不断搅拌
C.升高温度 D.加氯化铵晶体
2.在其他条件不变的情况下,将不饱和溶液变为饱和溶液,最简便且可靠的方法是( )
A.升高温度 B.降低温度
C.加入溶质 D.减少溶剂
课外练习:
1.在其他条件不变的情况下,向一定量的饱和溶液中加入少量硝酸钾晶体,则此饱和溶液的质量( )
A.增加 B.不变 C.减小 D.无法确定
2.下列有关溶液的说法错误的是( )
A.碘酒中的溶质是酒精
B.改变条件,饱和溶液与不饱和溶液可相互转化
C.氢氧化钙的饱和溶液一定是浓溶液
D.析出晶体后的溶液是该温度下的饱和溶液
3.天热的时候把半杯糖水(蔗糖已全部溶解)放进冰箱的冷藏室,过一段时间后发现杯底出现了部分蔗
糖晶体。对一这一现象的认识不正确的是( )
A.未放入冰箱前的糖水一定是饱和溶液
B.降低温度可从糖水中获得蔗糖晶体
C.放入冰箱前糖水中蔗糖的质量分数比放入冰箱后大
D.温度降低后蔗糖的溶解度随之变小
4.下列方法中:①加水②加硝酸钾③蒸发水④冷却⑤加热但保持溶液质量不变⑥加饱和硝酸钾溶液。能
使接近饱和硝酸钾溶液由不饱和变为饱和的是( )
A.①②⑤ B.①⑤⑥ C.②③④ D.②④⑥
5.在一定 下,向一定量的 里加入某种溶质,当溶质 时所得到的溶液叫做
饱和溶液。饱和溶液可以变成不饱和溶液,一般方法是通过 或 。因此,只有指明
和 时,溶液的“饱和”和“不饱和”才有确定的意义。
6.用“饱和”或“不饱和”填空:20℃时,盛有10g水的烧杯中加入3g某物质,充分溶解后还有1g剩余,
则所得溶液是该物质在20℃时的 溶液;若温度保持不变,继续向烧杯里加入10g水,充分溶解后所
得溶液是该物质的 溶液.
课后反思:
15课题2 溶解度
导学目标知识点:
1.溶解度的概念
2,溶解度曲线
课时:2课时
导学方法:学生阅读→教师总结→问题讨论→讲解总结→随堂练习→巩固提高
第二课时 N903
导学过程:
一、课前导学:
学生预习并完成相关概念:
溶解度: 、
溶解度曲线:
二、课堂导学:
[复习提问]在什么前提条件下讨论溶液的饱和与不饱和才有确定的意义?
[学生回答]
1.[活动与探究]
(1)向盛有20℃水的烧杯中加入氯化钠,向盛有40℃等量水的烧杯中加入硝酸钾,都至饱和状态。(比较
氯化钠与硝酸钾溶解的量,并讨论能否在该条件下地比较出二者的溶解能力)
(2)向40克20℃水中加入氯化钠,向100克20℃水中加入硝酸钾,都至饱和状态。
(比较氯化钠与硝酸钾溶解的量,讨论能否在该条件下定量地比较出二者的溶解能力)
(3)向100克20℃说中加入氯化钠直至饱和,向100克20℃水中加入硝酸钾配成不饱和溶液。
(比较二者溶解的量,讨论能否在该条件下定量地比较出二者的溶解能力)
[学生讨论,教师归纳总结]
2.固体的溶解度:
四大要素:① ② ③ ④
[提问]20℃时硝酸钾的溶解度是31.6g,这句话的含义是什么?
(阅读课本P36-37)
3.溶解度曲线:
①含义:
②作用:
③溶解度的变化规律:
4.[讨论]
(1)——打开汽水(或某些含有二氧化碳气体的饮料)盖时,汽水会自动喷出来。这活命气体在水中的溶
解度与什么有关?
(2)喝了汽水以后,常常会打嗝,这说明气体的溶解度还与什么有关?
(3)对于气体物质,研究它的质量方便,还是体积方便?
归纳总结:
① 气体的溶解度:
②五因素:
③影响因素:
升高温度, ;降低温度,
增大压强, ;减小压强,
教师引导,学生自我小结:
16课堂练习:
1.20℃时100g水中最多能溶解36g食盐,据此下列叙述正确的是( )
A.食盐的溶解度是36℃ B.20℃时食盐的溶解度是36℃
C.食盐的溶解度是100克 D.食盐的溶解度是36℃
2.影响同一固体物质溶解度大小的主要因素是( )
A.溶质的性质 B.水量的多少 C.温度 D.大气压
课外练习:
1.下列关于气体溶解度的说法正确的是( )
A.压强减小,气体溶解度增大
B.压强减小,气体溶解度减小
C.温度升高,气体溶解度减小
D.温度降低,气体溶解度减小
2.小华用凉开水养鱼,不久鱼全死了,下列解释合理的是( )
A.凉开水中几乎不含氧元素
B.凉开水中几乎不含氧原子
C.凉开水中几乎不含水分子
D.凉开水中几乎不含氧气
3.下列关于硝酸钾的溶解度的说法中正确的是( )
A.20℃时,20g硝酸钾溶解在100g水里,所以20℃时硝酸钾的溶解度为20g
B.20℃时,把20g硝酸钾溶解在水里制成饱和溶液,所以20℃硝酸钾的溶解度为20g
C.把31.6g硝酸钾溶解在100g水里,形成饱和溶液,所以硝酸钾的溶解度是31.6g
D.20℃时,31.6g硝酸钾溶解在100g水里,恰好形成饱和溶液,所以20℃时,硝酸钾的溶解度是31.6g
4.固体物质恶毒溶解度是指在一定温度下,固体物质在 g溶剂里达到 时所溶解的
。气体物质的溶解度是指压强为 和 时,气体溶解在1体积水里达到
时的 。20℃时,氯化钠的溶解度是36g,其含义是
。
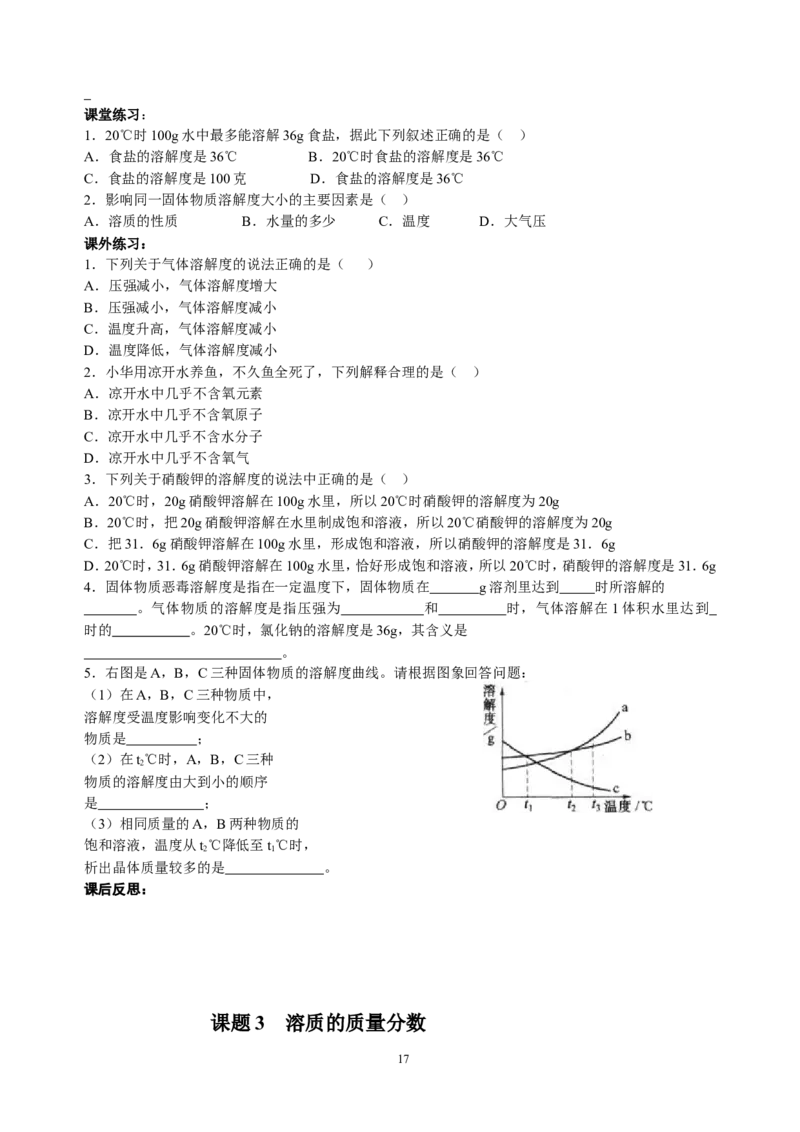
5.右图是A,B,C三种固体物质的溶解度曲线。请根据图象回答问题:
(1)在A,B,C三种物质中,
溶解度受温度影响变化不大的
物质是 ;
(2)在t℃时,A,B,C三种
2
物质的溶解度由大到小的顺序
是 ;
(3)相同质量的A,B两种物质的
饱和溶液,温度从t℃降低至t℃时,
2 1
析出晶体质量较多的是 。
课后反思:
课题3 溶质的质量分数
17导学目标知识点:
溶质的质量分数的概念及简单计算
课时:2课时
导学方法:学生阅读→教师总结→问题讨论→讲解总结→随堂练习→巩固提高
第一课时 N904
导学过程:
一、课前导学:
学生预习并完成相关概念:
1.溶质的质量分数定义:
2.溶质的质量分数公式:
二、课堂导学:
1.[活动与探究]在三支试管中各加入10ml水,然后分别加入约0.5g,1g,2g无水硫酸铜。比较三种硫酸铜
溶液的颜色,并对现象进行讨论。
(学生讨论,教师归纳总结)
(1)溶质的质量分数定义:
(2)溶质的质量分数公式:
计算:在上述活动与探究中,三种溶液中的溶质的质量分数各是多少?
①
②
③
2.溶液中溶质质量分数的计算
溶质质量= 溶液质量=
例题1在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。先要配制150kg这种溶液,需要氯
化钠和水的质量各是多少?
例题2化学实验室现有98%的浓硫酸,但在实验室中常需要用较稀的硫酸。要把50 g质量分数为98%
的浓硫酸稀释为质量分数为20%的硫酸,需要水的质量是多少?
教师引导,学生自我小结:
_______ _
课堂练习:
1.t℃时,在15g氯化钠中加入60g水,完全溶解后,溶液中氯化钠的质量分数为( )
A.15%
B.20%
18C.25%
D.33.3%
2.现有20%的氯化钠溶液100g,将它稀释为质量分数为10%的氯化钠溶液,需要水的质量是多少?
课外练习:
1.农业生产中通常用10%---15%的食盐溶液选种,现有配制好的15%的食盐水200kg,其中含水( )
A.30kg B.170kg C.140kg D.200kg
2.溶液中溶质的质量分数是 ,用数学公式可表示为
,现有溶质质量分数为20%的硫酸钾溶液,其20%表示的含义就是每 g硫酸钾溶液中
含有 g,将30g硫酸钾溶于70g水中,制取硫酸钾溶液 g,则硫酸钾溶液中溶质的质量分
数是 。
3.现需要30%的硝酸钾溶液1500g,需要硝酸钾和水的质量各是多少?
4.13g锌与100g稀硫酸恰好完全反应。求:
(1)生成氢气的多少克?在标准状况下体积为多少升?(标况下氢气密度为0.09g/L)
(2)原稀硫酸中溶质的质量分数是多少?
(3)反应后所得硫酸锌溶液中溶质的质量分数是多少?
课后反思:
课题3 溶质的质量分数
导学目标知识点:
19溶液的配制及计算
课时:2课时
导学方法:学生阅读→教师总结→问题讨论→讲解总结→随堂练习→巩固提高
第二课时 N905
导学过程:
一、课前导学:.
学生预习并完成相关内容:
溶液配制的步骤: ____________ _
_________ _
二、课堂导学:
[活动与探究]
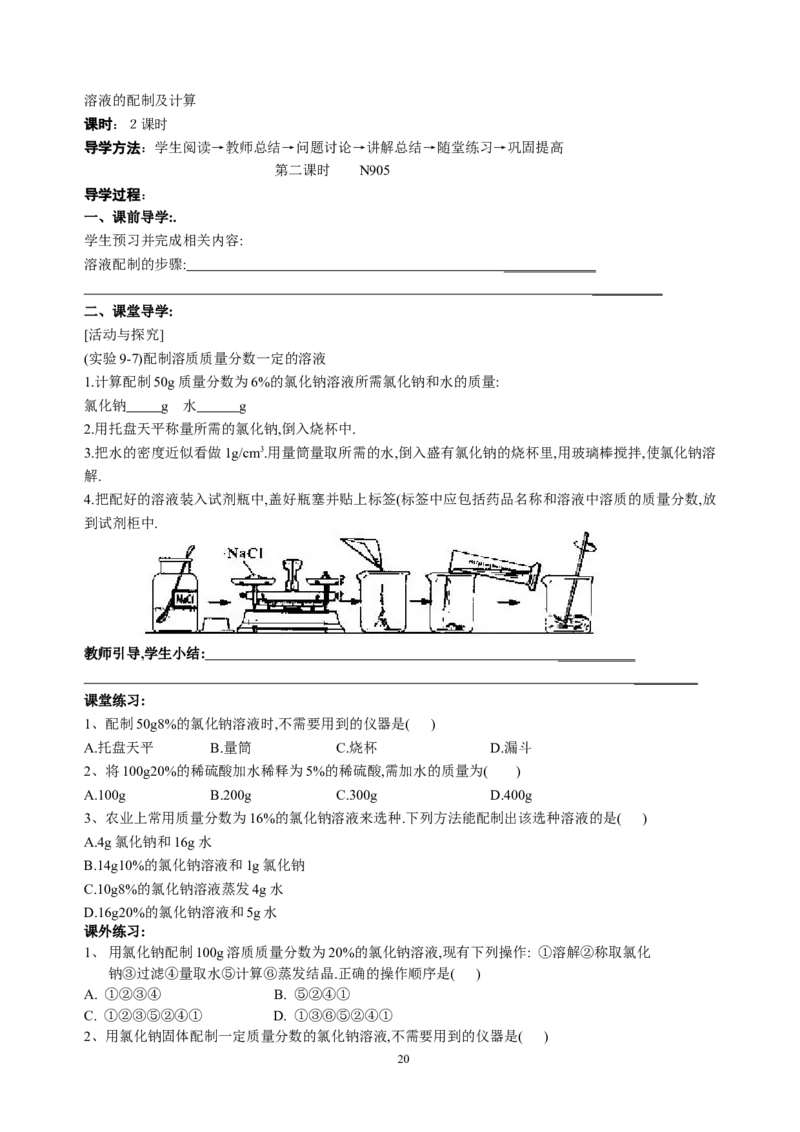
(实验9-7)配制溶质质量分数一定的溶液
1.计算配制50g质量分数为6%的氯化钠溶液所需氯化钠和水的质量:
氯化钠 g 水 g
2.用托盘天平称量所需的氯化钠,倒入烧杯中.
3.把水的密度近似看做1g/cm3.用量筒量取所需的水,倒入盛有氯化钠的烧杯里,用玻璃棒搅拌,使氯化钠溶
解.
4.把配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签(标签中应包括药品名称和溶液中溶质的质量分数,放
到试剂柜中.
教师引导,学生小结: __________ _
________ _
课堂练习:
1、配制50g8%的氯化钠溶液时,不需要用到的仪器是( )
A.托盘天平 B.量筒 C.烧杯 D.漏斗
2、将100g20%的稀硫酸加水稀释为5%的稀硫酸,需加水的质量为( )
A.100g B.200g C.300g D.400g
3、农业上常用质量分数为16%的氯化钠溶液来选种.下列方法能配制出该选种溶液的是( )
A.4g氯化钠和16g水
B.14g10%的氯化钠溶液和1g氯化钠
C.10g8%的氯化钠溶液蒸发4g水
D.16g20%的氯化钠溶液和5g水
课外练习:
1、用氯化钠配制100g溶质质量分数为20%的氯化钠溶液,现有下列操作: ①溶解②称取氯化
钠③过滤④量取水⑤计算⑥蒸发结晶.正确的操作顺序是( )
A. ①②③④ B. ⑤②④①
C. ①②③⑤②④① D. ①③⑥⑤②④①
2、用氯化钠固体配制一定质量分数的氯化钠溶液,不需要用到的仪器是( )
203、实验室里配制一定溶质质量分数的硫酸钠溶液时,有下列操作,其中错误的是( )
4、实验室为了配制50g5%的氯化钠溶液,需进行如下操作: ①计算②用 称取 g
氯化钠③用 (填“10ml”或“50ml”)量筒量取 ml水④将两者置于烧杯中,用
搅拌至溶解.
5、实验室欲配制1000g溶质质量分数为4%的氢氧化钠溶液.配制步骤为:
(1)计算,:需氢氧化钠固体 g,,水 ml(水的密度是1g/cm3)
(2)称量:用质量为23.1g的烧杯做称量容器,在托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应
放在 盘(填“左”或 “右”,在下表所列的砝码中,选出所需砝码(打“√”表示选用)
砝码/g 100 50 20 20 10 5
打“√”表示选用
并在下列标尺中选出能正确表示游码位置的选项
(3)溶解:将氢氧化钠固体溶于水,用 搅拌,使氢氧化钠全部溶解,冷却至室温
(4)把配好的溶液装入试剂瓶,盖好瓶盖并贴上标签,放入试剂柜中.
6、现有80g质量分数为10%的硝酸钠溶液,试回答下列问题:
(1)上述硝酸钠溶液中含溶质的质量为 g,溶剂的质量为 g.
(2)若向上述溶液中加入20g水,则所得溶液中溶质的质量分数为 ;
(3)若向上述溶液中加入20g硝酸钠,则所得溶液中溶质的质量分数为 ;
(4)若使上述溶液中溶质的质量分数变为20%,则应加入硝酸钠 g;
(5)若使上述溶液中溶质的质量分数变为20%,则应蒸发水 g;
(6)若使上述溶液中溶质的质量分数变为5%,则应加水 g.
课后反思:
21第十单元 酸和碱
课题1 常见的的酸和碱
第一课时
导学目标知识点:
1、酸碱指示剂的概念。
2、酸碱指示剂与酸溶液、碱溶液作用的现象。
3、盐酸、硫酸的物理性质。
4、浓硫酸的稀释。
课时:一课时
导学方法:实验法
导学过程:
一、课前导学:学生预习P ,并回答下列问题
48—49
1、酸碱指示剂(概念):_______________________________________________
2、初中所学的酸碱指示剂有两种,它们分别是__________、__________。
3、石蕊溶液遇酸变_______色,遇碱溶液变_________色。
酚酞溶液遇酸变_______色,遇碱溶液变_________色。
二、课堂导学:
提问、了解课前导学情况
(一)实验:向溶液中加入酸碱指示剂,师生共同实验,学生谈现象,完成下表
加入紫色石蕊溶液后的颜色变化 加入无色酚酞溶液后的颜色变化
食醋
石灰水
盐酸
氢氧化钠溶液
结论:1、上述 4 种物质中,可能是酸溶液的是____________________,可能是碱溶液的是
_______________。
2、酸碱指示剂是______________________________________________。
3、__________遇酸溶液变红色,___________遇酸不变色,
__________遇碱溶液变红色,___________遇碱溶液变蓝色。
活动与探究:P ,教师引导,学生看书
49
结论:花可以制备指示剂。
(二)几种常见的酸
1、探究盐酸的物理性质,探究硫酸的物理性质
实验10—2,学生填写P 表,归纳总结
50
结论:盐酸物理性质:__________________________________________________________________
硫酸物理性质:__________________________________________________________________
活动:学生自学盐酸和硫酸的用途:P 。
51
常见的酸:硝酸(填化学式)______________,醋酸(填化学式)___________。
2、浓硫酸的腐蚀性:
师生探究实验10—3,并完成P 表
51
①结论:___________________________________________________________________________
②浓硫酸稀释方法:_________________________________________________________________
③浓硫酸沾到皮肤或衣服上,应立即用___________冲洗,然后涂上________________。
课堂练习:
1、紫色的石蕊试液遇酸溶液变_________色,遇碱溶液变_________色。无色酚酞溶液遇酸溶液变
22__________色,遇碱溶液变_________色。
2、浓硫酸有强烈的腐蚀性、__________性。稀释浓HSO 时,一定要把_________________________
2 4
沿着___________注入_________里,并不断用玻璃棒搅拌,切不可把______________________________
__________________________。
3、保存或使用浓盐酸的合理方法是( )
A、密封保存在阴凉处 B、与碱类物质放在同一药品橱内
C、用广口瓶存放浓盐酸 D、把鼻孔凑到容器扣闻浓盐酸的气味
4、如图所示的选项中,实验室装有浓硫酸的试剂瓶上应贴有图标是( )
课外练习:
1、下列说法错误的是( )
A、浓盐酸敞口放置一段时间后,溶液的质量会减少
B、浓盐酸在空气中会白雾
C、氯化钠溶液敞口一段时间后,溶质的质量会增加
D、浓硫酸敞口一段时间后,溶质的质量分数减小
2、在实验室常用浓硫酸作某些气体的干燥剂,这是利用浓硫酸的( )
A、酸性 B、吸水性 C、脱水性 D、氧化性
3、白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列最不容易被蚁酸腐蚀的
是( )
A、镀锌水管 B、铜制塑像
C、大理石栏杆 D、铝合金门窗
4、化学实验过程中要规范操作,注意实验安全。下列有关做法中错误的是( )
A、洒在桌面上的酒精燃烧起来,立即用湿抹布或沙子扑灭
B、稀酸飞溅到皮肤上,立即用大量水冲洗再涂上3%—5%的小苏打溶液
C、点燃氢气前,一定要先检验氢气的纯度
D、稀释浓硫酸时,一定要把水注入浓硫酸中,并不断用玻璃棒搅拌
5、如图所示是稀释浓硫酸实验的示意图
(1)写出上图中,a、b两种仪器的名称:
a____________,b___________。
(2)b容器所盛的试剂是____________(填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生____________。
【联系与拓展】某媒体报道,2007年5月有一村民在家里误将装在酒瓶中的浓硫酸当成白酒喝下,造
成食道和胃严重损伤,这是因为浓硫酸具有___________。这一事件警示我们,家中存放或使用药物时应
注意:________________________________________________________________________________
________________________________________________________________________________________。
课后反思:
23课题 1 常见的酸和碱
第二课时
导学目标知识点:
酸的化学性质
课时:一课时
导学方法:学生预习,课堂实验
导学过程:
一、课前导学:
1、学生复习酸溶液、碱溶液与酸碱指示剂作用
酸溶液中滴加石蕊变_________色,酸溶液中滴加酚酞变_______色。
碱溶液中滴加石蕊变_________色,碱溶液中滴加酚酞变_______色。
2、复习Mg、Zn、Fe分别与盐酸、硫酸反应的现象,化学方程式
二、课堂导学:
1、学生探究酸与指示剂作用,并完成表格
加紫色石蕊溶液 加无色酚酞溶液
稀盐酸
稀硫酸
结论:______________________________________________
2、学生回忆金属与稀盐酸、稀硫酸反应完成化学方程式:
Mg + HCl —
Mg + HSO —
2 4
Zn + HCl —
Zn + HSO —
2 4
Fe + HCl —
Fe + HSO —
2 4
学生分析上述化学方程式,反应物之间,生成物之间的共同点有哪些
_____________________________________________________________________________________
结论:_______________________________________________________________________________
3、将一根生锈铁钉分别放入稀盐酸、稀硫酸中,学生观察现象,完成下列实验报告
现象 化学方程式
铁锈+盐酸 Fe O+6HCl=2FeCl +3H O
2 3 3 2
铁锈+硫酸 Fe O+3H SO =Fe (SO )+3H O
2 3 2 4 2 4 3 2
学生讨论:1、生成物共同之处是________________________________________________________。
2、该反应原理在生活中最显著用途是_________________________________________。
243、结论:___________________________________________________________________。
教师引导,学生自我小结:
1、酸具有的化学性质:
①酸溶液与指示剂作用:________________________________________________________________
②酸+活泼金属—__________+__________
该反应要求满足:____________________________________________________________________
③酸+金属氧化物—__________+__________
2、酸之所以具有通性,是因为___________________________________________________________
课堂作业:
1、用焊锡进行焊接前,常先用稀盐酸处理焊接处,其主要原理可表示为( )
A、Fe+2HCl=FeCl +H ↑ B、Fe O+6HCl=2FeCl +3H O
2 2 2 3 3 2
C、Fe O+3H =2Fe+3H O D、Fe(OH) +3HCl=FeCl +3H O
2 3 2 2 3 3 2
2、如图所示的实验中,小烧杯①盛的是紫色石蕊溶液,②盛的是浓盐酸。片刻后,可以观察到烧杯①
中液体的颜色是( )
A.紫色 B.红色 C.无色 D.蓝色
课外作业:
1、下列反应能进行的是( )
A、用稀盐酸除铁锈生成浅绿色的氯化亚铁
B、氧化铜溶解在稀硫酸中生成蓝色的硫酸铜
C、铜溶解在稀硫酸中生成蓝色的硫酸铜
D、铁溶解在稀盐酸中生成黄色的氯化铁
2、下列物质中,不能与稀硫酸反应的是( )
A、Cu B、CuO C、Fe D、Fe O
2 3
3、下列化学方程式正确的是( )
A、2Fe+6HCl=2FeCl +3H ↑
3 2
B、Fe O+4HCl=2FeCl +3H O
2 3 2 2
C、CuO+2HCl=CuCl +H O
2 2
D、Zn+2HNO=Zn(NO)+H ↑
3 3 2 2
4、用一种试剂一次能鉴别稀盐酸、氯化钠溶液和氢氧化钠溶液,这种试剂是( )
A、水 B、紫色石蕊试液 C、无色酚酞试液 D、氯化钠溶液
5、文文的家庭化学实验室有如下物品:①试管 ②烧杯 ③煤气和煤气炉 ④托盘天平⑤筷子 ⑥铁钉
⑦食盐 ⑧食醋 ⑨石灰水 ⑩牵牛花汁 ⑾水 ⑿饮料吸管 ⒀胶头滴管⒁小勺。只利用这些物品不能完成
的实验是( )
A、探究人体吸入的空气和呼出的气体中CO 含量的不同
2
B、探究牵牛花汁是否可作指示剂
C、探究加速食盐溶于水的有效方法
D、探究铁钉锈蚀的条件
6、某些植物的花汁可做酸碱指示剂。取三种花汁分别用酸溶液或稀碱溶液检验,颜色如下:
花种类 花汁在酒精(中性)中颜色 花汁在稀酸中颜色 花汁在稀碱中颜色
25玫瑰花 粉红 粉红 绿
万寿菊花 黄 黄 黄
大红花 粉红 橙 绿
试回答下列问题:
(1)检验生活中食盐水、肥皂水、汽水、石灰水四种物质的酸碱性,应选择
___________花汁,不选用其他花汁的原因是:______________________________
_____________________。
(2)取所选花汁少许分别滴入下列四种物质中,请将所显颜色填入下表中:
物质名称 食盐水 肥皂水 汽水 石灰水
所显颜色
7、浓硫酸具有强氧化性,常温下不会与铁、铝等金属反应,故盛放或运输浓硫酸时常用铁罐车。用水
冲洗装过浓硫酸的铁罐时,要避免火种接近,否则有爆炸的危险,写出两个有关反应的化学方程式。
①______________________________________________________________;
②______________________________________________________________。
8、实验室有两瓶标签破损的无色溶液甲、乙,推知它们只能是稀盐酸和硫酸钠
溶液。某校化学兴趣小组的同学设计用化学方法和物理方法区分它们。请回答有关问题:
(1) 化学方法:在不选用酸碱指示剂、pH试纸的情况下,选择不同物质类别的试剂进行区分(物质
类别是指单质、氧化物、酸、碱、盐等)。
所选试剂 实 验 现 象 及 结 论
方法一
方法二
(2)物理方法:小明同学仅使用了酒精灯和玻璃棒两种仪器,就把这两种无色溶液区分开来了。请你
猜测一下他的做法(简要叙述操作方法及判断方法)
。
课后反思:
26课题 1 常见酸和碱
第三课时
导学目标知识点:
1、掌握NaOH、Ca(OH) 的物理性质、化学性质。
2
2、NaOH、Ca(OH) 的俗名。
2
3、NaOH、Ca(OH) 的用途。
2
课时:1课时
导学方法:实验法、归纳法
导学过程:
一、课前导学:
1、氢氧化钠的俗名有__________、__________、____________。氢氧化钙的俗名有_________、
_________。
2、预习P 以及结合生活中看到Ca(OH) ,试着说出NaOH、Ca(OH) 的物理性质。
54 2 2
3、氢氧化钠用途有:____________________________________________________________________
4、Ca(OH) 用途有_____________________________________________________________________
2
二、课堂导学:
1、实验10-b P ,学生完成P 表
54 54
结论:1、氢氧化钠的物理性质:氢氧化钠是一种白色固体,极易溶于水,在空气中易潮解,溶解时放
热。用途:作某些气体干燥剂。
2、潮解:晶体吸收空气中的水分,表面溶解现象。(物理变化)
2、氢氧化钙
①制取:______________________________________
②氢氧化钙的物理性质:
氢氧化钙是一种白色固体,微溶于水
3、碱的化学性质
①碱与酸碱指示剂作用:
滴加酚酞 碱溶液滴加石蕊
②碱+某些非金属氧化物—__________+___________
Ca(OH) +CO — NaOH+CO —
2 2 2
结 论 : 氢 氧 化 钠 固 体 保 存 时 要 ____________ 。 原 因 有 2 个 :
①______________②________________________________。
拓展:SO +KOH—
3
碱溶液之所以具有相似的化学性质是因为________________________________________________。
学生自主归纳本节课内容
课堂练习:
1、氢氧化钠俗名叫___________、__________、____________,是一种_____色固体,__________溶于
水,有强烈的__________性,有_________性,可作某气体的干燥剂。
2、氢氧化钙俗名叫________、________,是一种_______色___________状固体,
__________溶于水。
3、碱具有相似化学性质的原因是________________________________________________________。
4、实验室干燥二氧化碳时应选用的干燥剂是( )
A、生石灰 B、NaOH固体 C、浓HSO D、稀HSO
2 4 2 4
5、下列各物质的俗名中,属于同种物质的是( )
A、烧碱、火碱、苛性钠 B、熟石灰、消石灰、生石灰
C、金刚石、大理石、石灰石 D、沼气、天然气、水煤气
6、工业上广泛用于石油精制、造纸、印染、制肥皂等,则该物质是( )
27A、硫酸 B、氯化钠 C、氢氧化钠 D、纯碱
课外练习:
1、下列物质中,不需密封保存的是( )
A、浓硫酸 B、氢氧化钠 C、大理石 D、澄清石灰水
2、氢氧化钠和氢氧化钙都是常见的碱,下列关于它们的说法中,正确的是( )
A、都能用作建筑材料 B、溶于水都能放出大量的热
C、它们的溶液都能用于检验二氧化碳气体
D、它们的溶液都能用于吸收二氧化碳气体
3、根据你所做过的家庭小实验,判断下列溶液能导电的是( )
①食盐溶液 ②酒精溶液 ③糖水 ④石灰水
A、①② B、②③ C、③④ D、①④
4、氢氧化钙放入水中,得到的上层清液即为石灰水,下层浑浊部分称为石灰浆和石灰乳。根据你所
学的化学知识回答:
(1)石灰水在实验室中的重要用途是:______________。
(2)生活中常用石灰浆来抹墙,其原因是:_______________________________________________
_________________________________。
(3)保存石灰水时需注意的问题是:____________________________________________________。
5、氢氧化钠是化学实验室中常用的试剂。
(1)氢氧化钠固体暴露在空气中,容易吸收水分而使表面覆盖一层溶液(这一现象又叫“潮解”);
它 还 能 ______________________________ , 这 一 变 化 的 化 学 方 程 式 可 表 示 为
_______________________________。所以氢氧化钠固体必须密封保存。
(2)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二
氧化硅缓慢地发生反应,产物使瓶口与瓶塞粘合在一起,反应的化学方程式为SiO+2NaOH=X+HO,试
2 2
推断X的化学式为_______________。
6、为了检验长期暴露在空气中的氢氧化钠固体是否变质,下列方法正确的是( )
A、放入水中,看是否全部溶解
B、滴加稀盐酸,看是否有气泡产生
C、滴加酚酞,看是否变色
D、用手接触,看是否有滑腻感
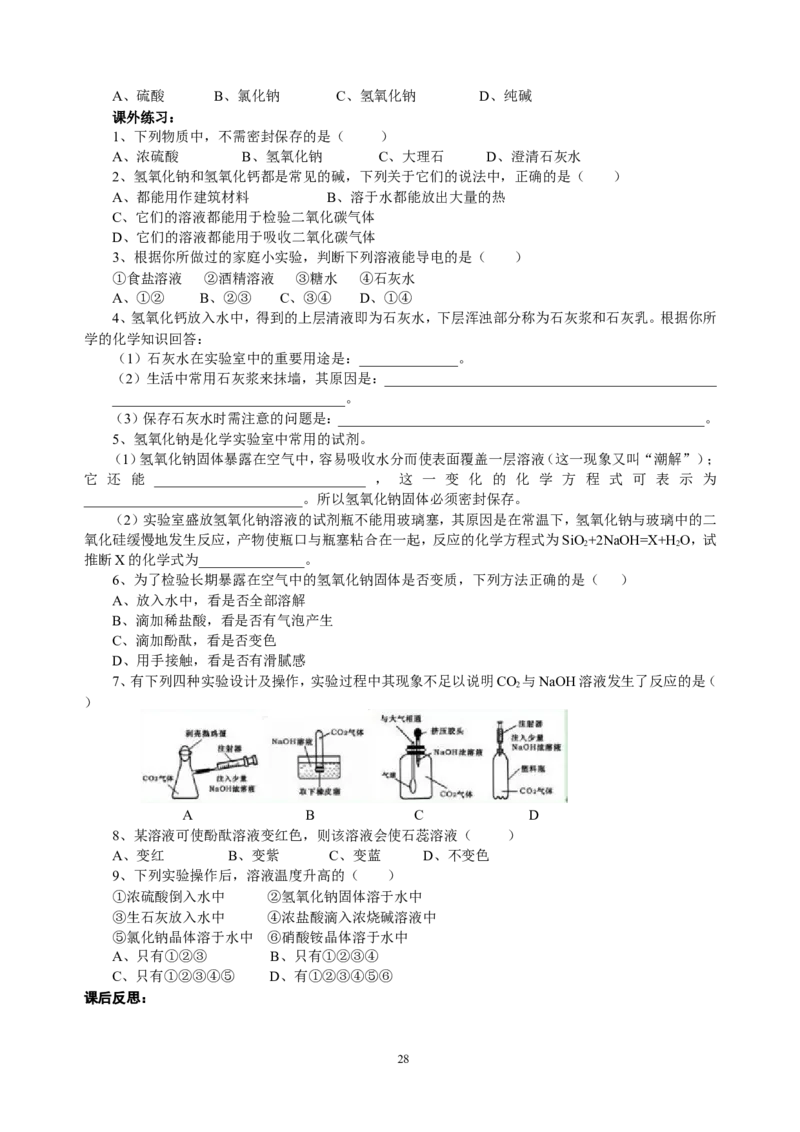
7、有下列四种实验设计及操作,实验过程中其现象不足以说明CO 与NaOH溶液发生了反应的是(
2
)
A B C D
8、某溶液可使酚酞溶液变红色,则该溶液会使石蕊溶液( )
A、变红 B、变紫 C、变蓝 D、不变色
9、下列实验操作后,溶液温度升高的( )
①浓硫酸倒入水中 ②氢氧化钠固体溶于水中
③生石灰放入水中 ④浓盐酸滴入浓烧碱溶液中
⑤氯化钠晶体溶于水中 ⑥硝酸铵晶体溶于水中
A、只有①②③ B、只有①②③④
C、只有①②③④⑤ D、有①②③④⑤⑥
课后反思:
28第十单元 酸和碱
课题2 酸和碱的中和反应
一、导学目标知识点:
1、中和反应在实际中的应用
2、中和反应的定义及其实验操作
3、溶液的酸碱度的表示法—pH
4、pH的测定方法
二、导学课时:1课时
三、导学方法:预习、阅读、实验
四、导学过程:
课前导学:
学生预习
1、中和反应概念
2、中和反应的应用
3、溶液酸碱度的意义
课堂导学:
一、中和反应
1、定义:_____________________________________________________________________________
2、实质:_____________________________________________________________________________
3、中和反应的实验操作:取少量氢氧化钠溶液,滴入几滴酚酞试液,再用滴管慢慢滴入稀盐酸,并不
停振荡,至红色刚刚变成无色,且30秒内不变色为止。
4、在NaOH溶液与盐酸反应时为什么要滴加酸碱指示剂?玻璃棒有什么作用?
__________________________________ ________________________________________________
5、化学方程式: 。
6、复分解反应与中和反应的关系?
_____________________________________________________________________________________
7、中和反应在实际中的反应。(学生阅读)
①改变土壤的酸碱性。
②处理工厂废水,解决环境污染问题。
③中和反应在医药方面的应用。
29二、溶液的酸碱度表示法—pH
1、酸碱度:
①定义。_____________________________________________________________________________
②酸碱度表示方法:
③pH的范围通常在
④溶液酸碱性的强弱与pH的关系
⑤酸碱性与酸碱度区别:_______________________________________________________________
2、pH的测定方法
①最简单方法:
②精确方法:
3、酸性或碱性溶液不一定是酸或碱。
三、了解溶液酸碱度的重要意义(P )(学生阅读)
62
1、化工生产中许多反应必须在一定pH溶液里才能进行;
2、在农业生产中,农作物一般适宜在pH为7或接近7的土壤中生长;
3、测定雨水的pH(因溶解有二氧化碳,正常雨水的pH约为5.6,酸雨的pH小于5.6),可以了解空气
的污染情况;
4、测定人体内或排出的液体的pH,可以了解人体的健康状况。
四、课堂练习:
1:溶液pH的概念及测定方法
溶液的酸碱度常用pH表示,范围为0~14。
pH<7,显 性,pH越小,酸性越 ;pH=7,显 性;pH>7,显 性,pH越大,碱
性越 。
测定方法:将一小片pH试纸放在玻璃片上,用玻璃棒蘸取待测液滴在试纸上,将试纸显示的颜色
与标准比色卡比较,得出溶液的pH。
2:小王测得生活中一些物质的pH如下表,下列说法不正确的是( )
物质 肥皂水 雨水 蔗糖水 食醋 纯碱水 柠檬汁
pH 10.2 5.8 7.0 3.3 8.1 2.0
A.蔗糖水是中性物质 B.肥皂水的碱性比纯碱水弱
C.柠檬汁的酸性比食醋强 D.雨水能使蓝色石蕊试纸变红
课外练习:
1:(武汉中考)小明同学对研究物质的酸碱性产生了浓厚的兴趣,他使用pH试纸测得家中某些物
30质近似的pH如下表:
物质 洁厕灵 苹果汁 护发素 玉米粥 洗发水 肥皂液 厨房清洁剂
pH 1 3 6 7~8 8 10 12
小明将自制的紫菜薹汁滴入上述7种物质中,发现紫菜薹汁与紫色石蕊试液的变化相似,将紫菜薹
汁滴入肥皂液中,液体变成绿色。
(1)若将紫菜汁滴入护发素中,你认为液体的颜色 (选填“不变”“变红色”或“变绿
色”)
(2)通过研究,小明同学懂得了洗发时先用洗发水再用护发素的科学道理。查阅资料:人体胃液pH
在0.5~1.5之间,小明同学懂得了患胃酸过多的病人不能空腹食用上述食物中的 。
(3)要洗去学校餐厅地面上的油垢,小明同学准备从家中选择带a“洁厕灵”、b“厨房清洁剂”两
种物质中的 (选“a”或“b”)
2:下列实际应用中,利用中和反应原理的是( )
①用生石灰作食品干燥剂
②用熟石灰和硫酸铜配制波尔多液
③施用熟石灰改良酸性土壤
④用氢氧化钠溶液处理泄漏的浓硫酸
A.①② B.③④ C.①④ D.②③
3:向盛有10mL稀盐酸(其中滴有少量紫色石蕊试剂)的烧杯中加入少量氢氧化钠溶液,用pH计(测
pH的仪器)测定溶液的pH,所得数据如下。请分析并回答下列问题:
加入NaOH溶液
0 2 4 6 8 10 12 14
的体积/ml
烧杯中溶液的pH 1.1 1.2 1.4 1.6 2.0 7.0 11.0 12.2
(1)当加入氢氧化钠溶液的体积为 ml时,稀盐酸和氢氧化钠溶液恰好完全反应。
(2)当加入氢氧化钠溶液的体积为13mL时,溶液显 色。
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?
。
课后反思:
31第十一单元 盐 化肥
课题1 生活中常见的盐
导学目标知识点:
1、氯化钠的性质及其用途。
2、过滤,蒸发等分离提纯物质的基本操作技能。
3、了解几种常见盐的化学式。
课时:1课时
导学方法:联系实际—归纳总结—实验探究
导学过程:
一、课前导学:
1、常见的盐(填化学式):
碳酸钠 : 碳酸氢钠: 硫酸铜: 氯化钠:
高锰酸钾: 大理石 : 硝酸银: 氯酸钾:
2、氯化钠的用途:
① ②
③ ④
⑤
3、过滤时“一贴二低三靠”的内容。
二、课堂导学:
(一)氯化钠
1、化学式: 俗名: 。
2、氯化钠的物理性质:食盐的主要成分,白色晶体,熔点801℃,沸点1413℃,味咸,中性,有杂质存
在时潮解。
(二)氯化钠在自然界里分布很广。
自然界中的 、 、 、 中蕴藏有大量的氯化钠。
(三)讨论:氯化钠有哪些用途?
1、医疗上: 2、农业上:
3、食品业: 4、工业上:
5、交通上:
四、活动与探究:粗盐的提纯(学生讨论P69的讨论(1)、(2))
粗盐初步提纯实验器材:
实验步骤:
1、溶解 用托盘天平称取5.0 g粗盐,用药匙将该粗盐逐渐加入盛有10 m L水的烧杯里,边加边用
玻璃棒搅拌,直到粗盐不再溶解为止。观察食盐水是否浑浊。称量剩下的粗盐,计算10m L水中约溶解了
多少克粗盐。
称取粗盐 / g 剩余粗盐 / g 溶解粗盐 / g
2、过滤 仔细观察滤纸上剩余物及滤液的颜色,如滤液浑浊,应再过滤一次,两次后仍浑浊,应查找
原因。
3、蒸发 把所得澄清滤液倒入蒸发皿,把蒸发皿铁架台的铁圈上,用酒精灯加热并用玻璃棒不断搅
拌,待蒸发皿中出现较多固体时,停止加热。利用蒸发皿的余热使滤液蒸干。
4、计算产率 用玻璃棒把固体转移到纸上,回收到指定的容器中,将提纯后的氯化钠与粗盐作比较,
并计算精盐的产率。
溶解粗盐 / g 精盐 / g 精盐产率 / g
〔交流与讨论〕:
321、在溶解、过滤、蒸发操作过程中,都用到玻璃棒,分别起什么作用?
溶解: 过滤: 蒸发:
2、过滤的注意事项:一贴二低三靠。(学生口述)
注意:盐与食盐的区别:食盐不等于盐,食盐是一种物质,而盐是一类物质,食盐是盐的一种。
学生归纳总结本节课内容。
课堂练习:
1、公路积雪会引起交通事故,撒食盐能使积雪很快融化。其主要原因是 ( )
A 食盐溶于水使水的凝固点降低 B 食盐溶于水放热使冰雪融化
C 食盐与水反应放热使冰雪融化 D食盐溶于水使水的沸点降低
2、小明同学在家做“粗盐提纯”实验,对其做法的认识中,错误的是 ( )
A 溶解时用筷子搅拌—加快溶解速度 B 将粗盐放入玻璃杯中加水溶解—粒子在不断运动
C 用自制净水器过滤粗盐水——可将粗盐水变为纯净物
D 实验时不使用一次性塑料杯——保护环境从身边做起
3、下表是某地市场上销售的一种“加碘盐”包装袋上的部分文字说明。请根据此表,结合学过的化学知
识,回答下列问题:
配料表 精制食盐,碘酸钾(KIO)
3
含碘量 20---40mg/kg
储藏方法 密封避光,防潮
食用方法 烹调时待食品熟后放入碘盐
(1)碘酸钾属于哪类化合物 (填“酸”,“碱”,“盐”或“氧化物”)
(2)根据含碘盐的食用方法,可推测碘酸钾的化学性质:碘酸钾在受热时
课外练习:
1、盐是指一类组成上含有______和_______的化合物。
2、氯化钠存在于______、_______、_______中,___色晶体,____溶于水,其溶解度受温度影响________。
其主要用途有①医疗上用氯化钠配制_________;②农业上可用氯化钠溶液_______;③工业上用氯化钠
作原料制取碳酸钠、氢氧化钠、氢气、盐酸等;④生活中的调味品,用来__________;⑤消除____________。
3、粗盐提纯的主要实验步骤是______、______、______、______。其中每一步都会使用的仪器是______,
其作用分别是___________、_________、__________、____________。
4、氯化钠是一种重要的化工原料。下列有关说法不正确的是 ( )
A.氯化钠俗称食盐 B.氯化钠中钠元素的化合价为+l价
C.氯化钠能和硝酸钾反应 D.生理盐水是0.9%的氯化钠溶液
5、公路积雪会引发交通事故,撒食盐能使积雪很快融化。其主要原因是 ( )
A.食盐溶于水使水的凝固点降低 B.食盐溶于水放热使冰雪融化
C.食盐与水反应放热使冰雪融化 D.食盐溶于水使水的沸点降低
6、请从一氧化碳、氮气、食盐、熟石灰四种物质中选择适当的物质用化学式填空:用
作粮食瓜果保护气的是 ;日常生活中用来调味和防腐的是 ;农业上用来配制农药波尔多
液的是 ;工业上用来冶炼金属的气体氧化物是 __ _ 。
7、右图为某同学进行粗盐提纯实验中过滤操作的示意图,试回答:
(1)写出标号的仪器名称①___________;②____________。
(2)漏斗中液面应该_____滤纸边缘;两次过滤后,滤液仍混浊的原因可能有___________________;
蒸发滤液时,用玻璃棒不断搅拌的目的是____________,等到蒸发皿中出现__________时停止加热,利用
蒸发皿的余热将滤液蒸干。
课后反思:
33第十一单元 盐 化肥
课题1 生活中常见的盐 第二课时
导学目标知识点:
1、了解碳酸钠,碳酸氢钠和碳酸钙的组成及其在生活中的主要用途。
2、掌握碳酸根离子或碳酸氢根离子检验的方法。
课时:1课时
导学方法:对比区别—归纳总结—实验探究
导学过程:
一、课前导学:
1、写出下列四种物质的化学式
氯化钠: 碳酸钠: 碳酸氢钠: 碳酸钙:
2、实验室制取二氧化碳的反应原理:
二、课堂导学:
(一)写出下列三种物质的化学式、俗称和用途
化学式 主要性质 用途
碳酸钠
碳酸氢钠
碳酸钙
(二)实验探究:
1、向盛有0.5克碳酸钠的试管里加入2毫升盐酸,迅速用带导管的胶塞塞紧试管口,并将导管另一端通入
盛有澄清石灰水的试管中,观察现象。用碳酸氢钠代替碳酸钠进行上述实验,并分析。
碳酸钠+盐酸 碳酸氢钠+盐酸
现 象
化学方程式
结论
讨论:如何对CO2-— 或者HCO -—进行检验?
3 3
2、向盛有少量碳酸钠的溶液的试管里滴入澄清的石灰水,观察现象。
现 象
化学方程式
结论
学生总结本节课的内容。
课堂练习:
341、蒸馒头时,在发酵的面团里加入些纯碱,其作用是 ( )
A、使馒头变白 B、 既除去生成的酸,又使馒头轻而体积大
C、加快面团的发酵速度 D、产生的二氧化碳使馒头质量变大
2.下列有关物质用途的叙述中,不正确的是 ( )
A 食盐做调味品 B 碳酸钙做补钙剂C 碳酸氢钠做发酵粉 D 用工业盐腌渍食品
3、鱼胆弄破后会使鱼肉粘上难溶于水的胆汁酸(一种酸)而变苦,要减少这种苦味,用来洗涤的最佳物质
是( )
A、水 B、纯碱 C、食盐 D、食醋
4、下面是某同学设计的鉴别石灰水和氢氧化钠溶液的几种方法,其中正确的选项是( )
①滴加酚酞试液 ②滴加碳酸钠溶液 ③滴加稀盐酸 ④通入二氧化碳气体
A、① ③ B、② ④ C、① ② D、② ③
课外练习:
1.下面是某同学设计的鉴别石灰水和氢氧化钠溶液的几种方法,其中正确的选项是( )
①滴加酚酞试液 ②滴加NaCO 溶液 ③通入CO 气体 ④除去热水瓶中的水垢
2 3 2
A ①③ B ②④ C ①② D ②③
2.下列说法错误的是
( )
A、干冰不是冰 B、金刚石不是金 C、食盐不是盐 D、铅笔芯中不含铅
3、工业生产,人类生活与化学有着密切的关系,请你用C、H 、O 、Na 、Cl、Ca六种元素中的一种或几种
(可重复使用)写出符合下列要求的物质的化学式:
(1)常用做建筑材料的盐 (2)一种有毒气体,可用于铁的冶炼
(3)少量存在于人体胃液中,可帮助消化的物质
(4)生活中常用于调味和腌渍蔬菜.鱼.肉等事物的盐
(5)在农业中常用来改良酸性土壤的一种碱
(6)常用来制糕点的是
4、学习碳酸钠知识时,老师做碳酸钠溶液和澄清石灰水反应演示实验,并对浑浊液过滤,得到澄清滤液。
课堂上老师的提问和同学们的回答如下图所示:
(1)假设你是丁同学,请你也提出一个与甲、乙、丙同学不同的合理猜想,把猜想写在上图丁
同学的对话框中。并对你自己的猜想设计一个简单的实验加以证明。
实验步骤 实验现象和结论
取样于试管中,
(2)你认为甲、乙、丙同学的猜想都合理吗?如有不合理的请说明理由。
课后反思:
35第十一单元 盐 化肥
课题1 生活中常见的盐 第三课时
导学目标知识点:
1、复分解反应的定义、条件。
2、部分的盐的溶解性。
3、盐的化学性质。
课时:1课时
导学方法:对比区别—归纳总结
导学过程:
一、课前导学:
常见的沉淀颜色和化学式。
氢氧化铜: 氢氧化铁: 氢氧化镁:
硫酸钡: 碳酸钡: 碳酸钙: 氯化银:
二、课堂导学:
(一)复分解反应
(学生活动:分析归纳P71的几个化学反应的生成物有什么特点)
复分解反应定义:
复分解反应条件:
(二)盐的化学性质:
1、盐跟某些金属的反应(举例: )
盐 + 金属= +
2、盐跟酸的反应 (举例: )
盐 + 酸= +
3、盐跟碱的反应 (举例: )
盐 + 碱= +
4、盐跟另种盐的反应 (举例: )
盐 + 盐= +
三、介绍部分酸、碱和盐的溶解性(教材P109的附录1)
1、钾钠铵盐易溶于水
2、硝酸盐易溶于水
3、碳酸盐、磷酸盐大多不溶于水
口诀:
钾钠铵盐皆可溶 硝酸盐入水影无踪 氯化物不溶氯化银
硫酸盐不溶硫酸钡 碳酸盐只溶钾钠铵
学生总结本节课的内容。
课堂练习:
1、在日常生活中常用做调味剂和防腐剂的是 ( )
A.纯碱 B.酒精 C.食盐 D.醋酸
2、在改进制碱法方面,曾做出杰出贡献的科学家是 ( )
A.侯德榜 B.拉瓦锡 C.道尔顿 D.汤姆生
3、HCl、NaOH、NaCl三种物质的溶液的pH值由大到小的顺序是_ _。
4、下列物质间中不能发生复分解反应的是( )
36A、碳酸钠和稀硫酸B、氢氧化钠溶液和氯化铜溶液
C、碳酸钾和硫酸钠D、硝酸钙溶液和碳酸钾溶液
课外练习:
1、若不用其他试剂,而用最简便的方法鉴别下列四种溶液:①硫酸镁溶液 ②氢氧化钾溶
液 ③硫酸铜溶液 ④氯化钠溶液。鉴别的正确顺序是( )
A. ③②①④ B.④③②① C.①②③④ D.③①④②
2、食盐、食醋、纯碱等均为家庭厨房中常用的物质,利用这些物质你能完成的实验是( )
①除去热水瓶中的水垢 ②鉴别食盐和纯碱 ③检验鸡蛋壳能否溶于酸
A. ①② B. ①③ C. ① D. ①②③
3、下列各组物质发生反应时,生成物中同时有“沉淀”、“气体”、或“水”中两种的是( )
A、NaCO 溶液和CaCl 溶液 B、Ba(OH) 溶液和CuSO 溶液
2 3 2 2 4
C、稀硫酸和Ba(OH) 溶液 D、FeO 粉末和稀盐酸
2 2 3
4、下列各组物质中,能相互反应且反应类型属于复分解反应的是( )
A、锌和稀盐酸 B、二氧化碳和水 C、氯化钠溶液和硝酸钾溶液 D、氢氧化钠和稀硫酸
5、下列物质间能否发生复分解反应?如能发生反应,写出有关反应的化学方程式。
①氯化镁溶液与硝酸银溶液反应
②硝酸钾溶液与氯化钠溶液
③硝酸溶液与氢氧化铜固体
④硫酸钾溶液与硝酸钡溶液
⑤碳酸氢钠溶液与稀硫酸溶液
课后反思:
37第十一单元 盐 化肥
课题1 生活中常见的盐 第四课时
导学目标知识点:
1、掌握酸、碱、盐等各类物质之间的反应规律。
2、运用复分解反应的条件,解决物质共存、除杂等问题。
课时:1课时
导学方法:对比区别—归纳总结
导学过程:
一、课前导学:
复分解反应的定义:
条件:
二、课堂导学:
1、酸、碱、盐等各类物质之间的反应规律
学生活动:根据复分解反应的条件,判断下列四种化合物的溶液两两之间是否能发生反应。
HSO Ba(NO ) NaOH KCO
2 4 3 2 2 3
HSO
2 4
Ba(NO )
3 2
NaOH
KCO
2 3
归纳总结:
①酸 + 碱 = (要求: )
②酸 + 盐 = (要求: )
③碱 + 盐 = (要求: )
④盐 + 盐 = (要求: )
2、共存
①离子之间可以发生反应产生难溶物或微溶物而不能大量共存。 如Ag+与Cl-;Ba2+与CO2-、SO2-;
3 4
Cu2+与OH-;Mg2+与OH-;Ca2+与CO2-;Fe3+ 与OH-。
3
②离子之间可以发生反应产生难电离的物质而不能大量共存。 如H+与OH-。
③离子之间可以发生反应产生气体而不能大量共存。如H+与CO 2-;H-与NH +等。
3 4
④其他情况,如题目要求无色溶液,则有颜色的离子不可能存在。
3、除杂 ( 物理方法; 化学方法)
物理方法:过滤、结晶、用磁铁吸引等
化学方法:解答除杂质一类的题目时,要注意三原则;三步骤;五种常用的方法。
三原则:①不增:提纯过程中不增加新的杂质;
②不变:被提纯的物质不能改变;
③易分:被提纯的物质与杂质易分离。
三步骤:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂
五种常用的方法:除杂质思路分析方法:
(1)沉淀法:加入一种试剂将被除去的杂质变为沉淀,再用过滤法除去。
(2)化气法:加热或加入一种试剂将杂质变为气体逸出。
(3)置换法:应用金属活动顺序通过置换反应除去杂质的方法。
(4)转纯法(转换法):将被除去的杂质变为提纯的物质。
(5)吸收法:利用混合物中某组分化学性质的差异,用试剂吸收其中一种,从而分离提纯物质的方法。
4、复分解反应的类型:
①酸 + 碱 = ②酸 + 盐 =
③碱 + 盐 = ④盐 + 盐 =
⑤酸 + 金属氧化物=
38学生总结本节课学习内容。
课堂练习:
1、某溶液能与镁反应生成氢气,则下列各组物质在该溶液中能大量存在的是(
A.KCl、NaCl、NaSO B.NaCl、NaNO、AgNO
2 4 3 3
C.NaCO、NaCl、NaSO D.HCl、NaCl、NaSO
2 3 2 4 2 4
2、下列各组物质在溶液中能大量共存的是( )
A.FeCl 、Na SO 、HCl B. NaOH、NaCl、HNO
2 2 4 3
C.MgSO 、NaNO 、KOH D. Na CO 、KNO 、HCl
4 3 2 3 3
课外练习:
1、下列各组物质在溶液中能够大量共存的是( )
A. BaCl NaCl H SO B. H SO NaCl Na CO
2 2 4 2 4 2
3
C. Na SO KNO NaOH D. NaOH H SO HCl
2 4 3 2 4
2、下列各组物质在某PH=14的无色溶液中,能大量共存的是( )
A.FeCl 、NaCl、KNO B.NaCl、NaOH、NaNO
3 3 3
C.CaCl 、NaNO 、Na CO D.KNO 、H SO 、NaCl
2 3 2 3 3 2 4
3、某固体可能由MgCl 、NaOH、BaCl 、Na SO 中的一种或多种组成。取少量该固体于烧杯中,
2 2 2 4
向烧杯中加入足量水搅拌后,观察到有白色不溶物存在;再向烧杯中滴加酸溶液。根据加酸过程中观察
到的现象绘制如下图像,结合图像判断下列说法合理的 是( )
A.加水后得到的液体中含有OH- B.白色不溶物可能为Mg(OH) 或BaSO
2 4
C.原固体中不可能含有三种物质 D.酸溶液一定不能为稀H SO
2 4
4、下列各组物质的溶液,不用其它试剂就可以将它们区别开的是
A. HCl NaOH Na CO Na SO B. HCl Cu(NO ) NaOH NaNO
2 3 2 4 3 2 3
C. NaOH MgSO Na CO H SO D. BaCl Na SO Ca(NO ) CaCl
4 2 3 2 4 2 2 4 3 2 2
5、有一包固体粉末,可能由CaCO、NaSO、KNO、CuSO、BaCl 的一种或几种组成,做实验得以下结果:
3 2 4 3 4 2
(1)将此固体粉末加到水中,得到白色沉淀上层清液为蓝色.
(2)该白色沉淀不溶于稀硝酸.从实验可判断出,该粉末中一定含有________,一定不含有________,
可能含有________.
课后反思:
39第十一单元 盐 化肥
课题2 化学肥料
导学目标知识点:
1、了解化学元素对植物生长的重要性及常见化肥的种类和作用。
2、了解化肥、农药对环境的影响。
课时:1课时
导学方法:自学—实验—分析—归纳
导学过程:
一、课前导学:
1、农作物生长需求量最大的营养元素是 、 、 。
2、常见的氮肥:
常见的磷肥:
常见的钾肥:
二、课堂导学:
1、氮、磷、钾肥的种类、作用及缺乏症状
化肥类别 种类 生理作用 缺乏症状
NHCI NHNO 氮是蛋白质、核酸、叶绿素的重要
4 4 3 植物生长迟缓,叶色
氮肥 NHHCO(NH)SO 成分,促进细胞分裂和生长,使枝
4 3 4 2 4 发黄,作物品质下降
NH.HO CO(NO) 叶茂盛浓绿
3 2 2
生长迟缓,植株矮小,
磷矿粉[Ca(PO)] 磷是蛋白质、核酸和酶等化合物
3 4 2 叶片暗绿,产量下降,
磷肥 钙镁磷肥 的组成元素,参与代谢活动,促进
磷过量造成晚熟贪
过磷镁钙 作物生长,增强抗旱抗寒能力
青,结实率下降
钾具有保证各种代谢顺利进行,
茎状软弱,易倒伏,老
促进植物生长,增强抗病虫害,抗
钾肥 KSO,KCI 叶及大部分叶边缘和
2 4 倒状的能力。促进淀粉的合成与
尖端枯黄,新叶正常
运输
2、复合肥料
(1)概念:化肥中同时含有两种或两种以上营养元素的肥料。如磷酸二氢铵:NH H PO 。磷酸
4 2 4
二氢钾:KH PO 等。
2 4
(2)特点:能同时均匀供给作物几种养分,充分发挥营养元素之间的相互作用,有效成分高。
注意:不合理使用化肥可能会形成:1、土壤污染2、水污染3、大气污染
3、[活动与探究]
探究初步区分氮肥、磷肥和钾肥的方法
(1)比较氮肥(氯化铵、碳酸铵)、磷肥(磷矿粉、过磷酸钙)和钾肥(硫酸钾、氯化钾)的外观、
气味和在水中的溶解性,归纳它们的性质。
氮肥 磷肥 钾肥
40碳酸氢铵 氯化铵 磷矿粉 过磷矿钙 硫酸钾 氯化钾
外观
气味
溶解性
(2)取研细的氮肥(硫酸铵、氯化铵)、钾肥(硫酸钾、氯化钾)各0.5g,分别放在铁片上灼烧
(如右图所示),观察现象。
再取上述化肥各少量,分别加入少量熟石灰粉末,混合、研磨,能否嗅到气味?
氮肥 钾肥
硫酸铵 氯化铵 硫酸钾 氯化钾
灼烧
加熟石灰研磨
(3)利用物理、化学性质的不同初步区分常见化肥的方法:(一看二加水三烧四加碱)
氮肥 钾肥 磷肥
看外观 白色晶体 灰白色粉末
大多不溶于水或部分溶
加水 全部溶于水
于水
不燃烧,跳动或有爆
灼烧 可燃烧,熔化起泡或冒烟
炸声
不具有刺激性气味的
加熟石灰 放出具有刺激性气味的氨
氨气放出
4、化肥的简易鉴别
一看:液态______;灰白色粉末为_____
二闻:碳酸氢铵(碳铵)有较强的氨气味
三溶:_____大多数不溶于水或部分溶于水
四反应 :___ _ _ _能与碱反应放出具刺激性气味的气体——氨气,可检验铵态氮肥。
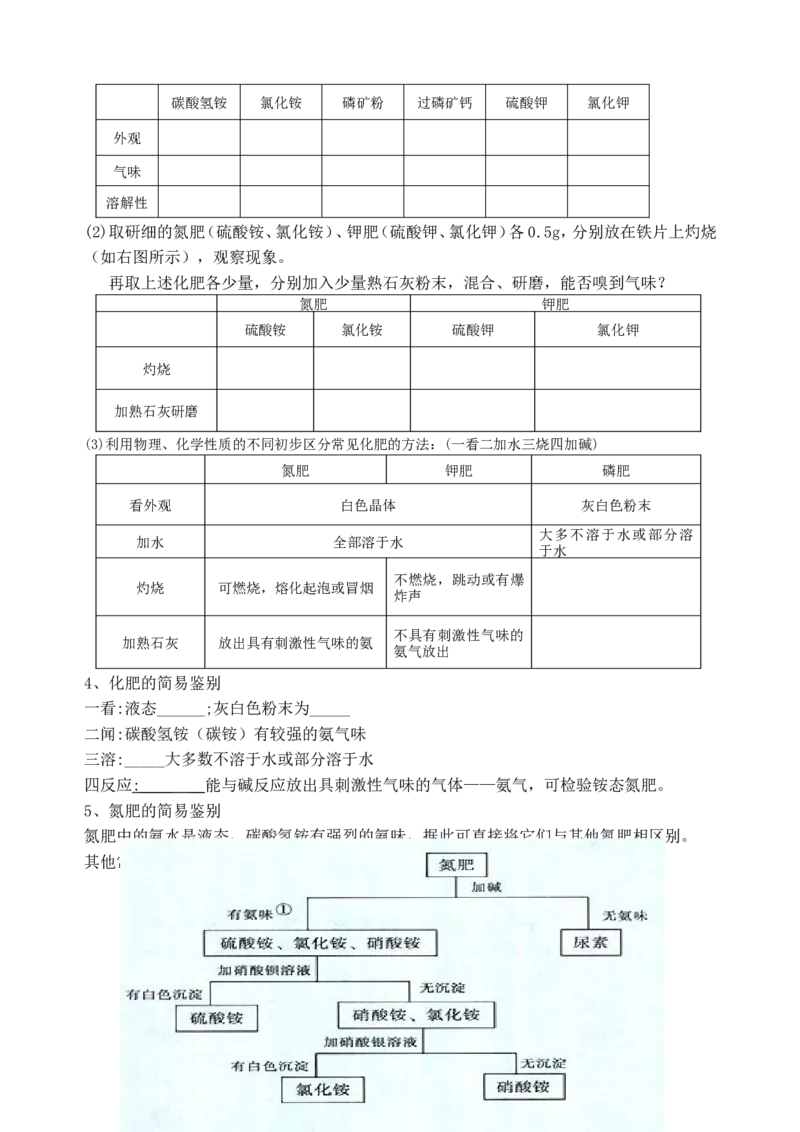
5、氮肥的简易鉴别
氮肥中的氨水是液态,碳酸氢铵有强烈的氨味,据此可直接将它们与其他氮肥相区别。
其他常见肥料可按下列步骤鉴别:
415、铵根离子的检验
取样,向样品中加入NaOH或Ca(OH) 微热,把湿润的红色石蕊试纸放在试管口,若试纸
2
变蓝,证明样品中含NH +。
4
学生归纳总结本节课内容。
课堂练习:
1、常用的含氮化肥有______,含磷化肥有______,含钾化肥有______。
2、下列化学肥料中属于钾肥的是( ),属于磷肥的是( ),属于复合肥料的是( )
A.K SO B.NH NO C.Ca(H PO ) D.NH H PO
2 4 4 3 2 4 2 4 2 4
3、下列化肥中,既能促进作物的茎、叶生长茂盛、叶色浓绿;又能促进作物生长健壮,茎杆粗
硬的是 ( )
A. (NH ) SO B. KNO C. CO(NH ) D. NH H PO
4 2 4 3 2 2 4 2 4
4、下列化肥中,从外观即可与其他化肥相区别的是 ( )
A.硫酸钾 B.磷矿粉 C.氯化钾 D.硝酸铵
5、下列物质中,属于碱类,又可作化学肥料的是 ( )
A.氨水 B.熟石灰 C.氯化铵 D.磷酸钙
课外练习:
1、下列物质可以直接做肥料施用的是( )
A. 磷酸钙 B. 氨水 C. 氢氧化钾 D. 硝酸
2、下列化肥不能与熟石灰混合施用的是( )
A. 氯化钾 B. 碳酸氢铵 C. 氨水 D. 硝酸钾
3、下列化肥属于复合肥料的是:( )
A. NH Cl B. NH NO C. KH PO D. KNO
4 4 3 2 4 3
4、某花圃所种的花卉缺乏氮和钾元素,如果只可施用一种化肥,应施的是( )
A.NH NO B.KNO C.KCl D.Ca(H PO )
4 3 3 2 4 2
5. 某同学家中种植的植物比正常的植株矮小瘦弱,叶片发黄,严重时叶脉呈淡棕色,你认为
应该施加下列哪一种化肥:( )
A. 氯化钾 B. 硝酸钾 C. 过磷酸钙 D. 尿素
6、某星期天,小明同学回家发现自家田里的小麦出现大面积倒伏现象,就向其父母提出了
42一条合理化建议:明年应在小麦生长期增施抗倒伏的化肥,你认为增施的化肥是( )
A.NH NO B.CO(NH ) C.Ca(H PO4) D.KCl
4 3 2 2 2 2
7、有三瓶失去标签的无色溶液:(NH ) SO 、Na CO 、KNO ,若只用一种试剂将它们一次性鉴别,
4 2 4 2 3 3
应选用的试剂为 ( )
A. HCl B. BaCl C. NaOH D. Ba(OH)
2 2
8、有4包失去标签的化肥,分别是氯化铵.氯化钾.碳酸钾.磷矿粉,某同学通过以下实验区
别(1)各取少许样品于试管中,按顺序编号为甲.乙.丙.丁;(2)观察颜色,甲.乙.丁为白色固
体,丙为灰色粉末;(3)在试管中分别加入水,甲.乙.丁全部溶解,丙不溶解;(4)再各取甲.乙.
丁少许加熟石灰研磨,乙有刺激性气味的气体产生,甲.丁没有;(5)取甲.丁少许各滴入盐酸,
甲有气体产生,丁没有.根据以上实验确定甲:_______乙:______丙:______丁:_____
9、某同学发现他家菜园中的蔬菜生长迟缓,便施用了一种氮肥,下图是氮肥包装标签的部
分文字。这种氮肥的相对分子质量是___________,其纯度(即化肥中硝酸铵的质量分数)是
_________。
课后反思:
第十二单元 化学与生活
43课题1 人类重要的营养物质
导学目标知识点:
1.了解营养物质是指蛋白质,糖类,油脂,维生素,无机盐和水等六类物质。
2.了解蛋白质,糖类,油脂,维生素与人体健康的关系。
课时:1课时
导学方法:学生阅读→教师总结→问题讨论
导学过程:
一、课前导学:
六大营养素为:
淀粉的化学式 葡萄糖的化学式
蔗糖的化学式
二、课堂导学:
阅读课本P86-91
(一)蛋白质
功能及作用:
课堂练习:一个女运动员可以在60S内跑完400m,她的最大氧气吸入量为4L/min,而肌肉在工作达到极
限时,每公斤体重每分钟需要氧气约0.2L,如果该运动员体重为50kg,她跑完400m将缺少多少氧气?
酶属于 ,是 , 。
讨论:有人用甲醛水溶液来浸泡水产品并出售,这样做有什么危害?
(二)糖类
糖类是 ,由 三种元素组成化合物。
淀粉的化学式为 ,葡萄糖的化学式为 。蔗糖的化学式
葡萄糖在人体组织里在酶的作用下经缓慢氧化转变为二氧化碳和水,同时放出能量,供机体活动和维持
恒定体温的需要,写出葡萄糖为人体提供能量的化学方程式:
在上述反应中,每克葡萄糖约放出 的能量,在人类食物所供给的总能量中,有
来自糖类。
(三)油脂
油脂是 ,常见的油脂有 ,
在常温下, 呈液态,称为油, 呈故态,称为脂肪,二者合称油脂。每克油脂在
人体内完全氧化放出 的能量,它供给人体日需能量的 。
四.维生素
维生素有 种,多数在人体内不能合成。它们可以起到 , ,
的作用。缺乏 ,会引起 ;缺乏 ,会引起 。
教师引导,学生自我小结:
课堂练习:
1.下列食物中,不能转化为人体活动所需能量的是( )
A.淀粉 B.葡萄糖 C.食盐 D.油脂
2.下列说法不正确的是( )
A.蔬菜,水果含有人体所需的维生素
44B.蛋,奶,鱼,肉富含的营养素是蛋白质
C.人体每天应摄取大量的油脂
D.谷类富含的营养素是糖类
课后练习:
1.在人体内需要量很小,但可以起到调节新陈代谢,预防疾病和维持身体健康作用的物质是( )
A.蛋白质 B.油脂 C.维生素 D.糖类
2.蛋白质是人体必需的重要营养成分之一。下列食物中,富含蛋白质的是( )
A.豆腐 B.馒头 C.西红柿 D.豆油
3.有关酶的说法不正确的是( )
A.酶是一种蛋白质B.酶是一种生物催化剂
C.酶具有高效催化作用D.酶的催化作用不具专一性
4.某同学到了傍晚就看不清东西,医生说他患了夜盲症,那他体内缺少的维生素可能是( )
A.维生素A B.维生素B C.维生素C D.维生素E
5.下列说法不正确的是( )
A.糖类食品能为人提提供能量
B.长期吸烟易患冠心病,肺气肿和肺癌等疾病
C.常食新鲜蔬菜,水果,可获得丰富的维生素C
D.食用甲醛浸泡的海产品,可提高免疫力
6.下列有关人体生理活动的叙述错误的是( )
A.代谢产生的CO 如不能及时排出,会使血液的PH增大
2
B.无机盐和水虽不能提供能量,却是人体必需的
C.胃液中少量的盐酸可以帮助消化
D.香烟烟气中的CO会使血红蛋白携氧能力降低
7.食物中的营养素主要包括 . . . .
和 六类物质。
8.蛋白质是构成 的基本物质,是 及 的主要原料,它是由
构成的复杂化合物。
9.医药商店销售的某种葡萄糖(化学式C H O)注射液部分说明如下图,测得该葡萄糖注射液中碳元素
6 12 6
质量分数为20%。请回答下列问题:
(1)葡萄糖中碳,氢,氧元素的质量比为 。
(2)该葡萄糖注射液中溶质的质量分数为 。
(3)某病人每天需要注射2支该注射液来补充能量,则他每天补充葡
萄糖的质量为 g。
(假设该葡萄糖注射液的密度为1g/cm3)
课后反思:
课题2 化学元素与人体健康
45导学目标知识点:
1.了解人体的元素组成,无机盐能够调节人体的新陈代谢,促进身体健康。
2.了解人体中元素的存在形式和某些元素(如钙,铁,薪等)对人体健康的重要作用。
课时:1课时
导学方法:学生阅读→教师总结→问题讨论
导学过程:
一、课前导学:
人体含量较多的元素有 种,它们约占人体质量的99.95%,在人体中含量超过
的元素,称为 ;含量在 以下饿元素,称为微量元素。
二、课堂导学:
1.我们周围世界的物质是由100多种元素组成的,而组成人体自身的元素约有 多种。
人体含量较多的元素有 种,它们约占人体质量的99.95%,在人体中含量超过
的元素,称为 ;含量在 以下饿元素,称为微量元素。
2.常见元素对人体的影响
(1)钙 成人提内约含钙 ,其中99%存在于 和 中,主要以
晶体的形式存在。青少年缺钙会得 ,老年人缺钙会
。
(2)钠和钾 人体内含钠 g,其中一半以 的形式存在于细胞外液中,成人每千克体重含钾
约 ,主要以 的形式存在于细胞内液中。它们各自保持一定的浓度,对于维持人体内的水
分和维持体液恒定的PH有重要作用。
(3)微量元素对人体的影响
元素 对人体作用 摄入量对人体的影响
铁
锌
硒
碘
氟
讨论:P95 人体缺少必需微量元素会得病,因此有人认为应尽可能多吃含有这些元素的营养补剂,你认
为这种想法对吗?为什么?
教师引导,学生自我小结:
课堂练习:
1.人体缺少某种元素会引起甲状腺肿大,该元素是( )
A.钙 B.碘 C.锌 D.铁
2.“绿色化学”的核心是在化学反应过程或化工生产中,尽量减少使用或彻底消除有害物质。下列做法
中,符合绿色化学的是( )
A.生产和使用剧毒农药 B.造纸厂用二氧化硫进行纸浆漂白
C.利用双氧水制氧气 D.化工厂产生的废气向高空排放
课后练习:
1.人体中有11种必需的常量元素,以下元素中属于常量元素的是( )
A.钙元素 B.铁元素 C.锌元素 D.碘元素
462.人们常喝牛奶是因为牛奶中富含人体所需的( )
A.铁元素 B.碘元素 C.锌元素 D.钙元素
3.食用下列食品,对人体健康有利的是( )
A.霉变的大米
B.用工业盐如亚硝酸钠腌制的鱼
C.用甲醛水溶液浸泡过的鱿鱼
D.用食醋凉拌的黄瓜
4.下列有关生活常识的说法中,正确的是( )
①小苏打是治疗胃酸过多症的一种药剂②香烟的过滤嘴可过除CO等有害物质,故吸烟对身体无害③摄
入过量重金属盐会使人中毒④使用霉变食品可使人引发肿瘤等恶性疾病
A.只有①② B.只有①②③
C.只有①③④ D.只有①④
5.下列广告用语从化学角度看,没有科学性错误的是( )
A.“K”牌咖啡,滴滴香浓,决不含任何化学物质
B.“雪山牌”矿泉水,真正的纯水
C.“大自然”牌蔬菜,天然种植,不含任何元素,真正的绿色食品
D.食用合格的“碘盐”,可预防某种甲状腺疾病
6.组成我们人体自身的元素约有 种。人体中含量较多的元素有 种,它们约占人体质量
的 。
7.无机盐对人体健康的影响很大,它们能够调节 ,促进 ,有的还是构成人体组织的重要
材料。
8.用化学方程式解释:
(1)市售麦片中含有微量极细的还原铁粉,饮用这种麦片后,铁在胃液中可转化为人体易于吸收的亚铁
盐
(2)可溶性的钡盐有毒,不溶性的钡盐无毒。透视肠胃时,常口服硫酸钡(俗称“钡餐)。某病人误服用碳
酸钡,结果引起中毒,原因是
医生赶快给病人服用泻药(主要成分是MgSO )来解毒
4
(3)碳酸钙是一种价廉高钙补钙剂,虽然碳酸钙难溶于水,但服用后可转化为可溶性钙盐被人体吸收,其
化学原理是 。因此碳酸钙在医疗上可以用来
自治疗 症。为了提高补钙效果,服用这种补钙剂时常需配合服用维生素D,据此可推知维生素D的
功能是 。
课后反思:
课题 3 有机合成材料
导学目标知识点:
471.知道三大有机合成材料——塑料,合成纤维,合成橡胶的性能和用途
2.了解有机化学物和有机高分子化合物的特点,初步区别有机化合物和无机化合物。
课时:1课时
导学方法:学生阅读→教师总结→问题讨论
导学过程:
一、课前导学:
三大有机合成材料: , , 。
有机高分子材料:
有机高分子材料可分为: 和
二、课堂导学:
1.有机化合物
(活动与探究)
化合物 化学式 组成元素 相对分子质量
甲烷
乙醇
葡萄糖
淀粉
蛋白质 ————————
硫酸
氢氧化钠
氯化钠
有机化合物的特点: ,如 ,有些含 的化合物,如
等具有 的特点,因为把它们看做 。
二.有机合成材料
有机高分子材料:
天然高分子材料包括
合成有机高分子材料包括
链状高分子材料具有 ,有些网状高分子材料具有
(1)塑料
人类使用最多的塑料是: 和 ,举出在生活中的用途
(2)纤维
天然纤维: ,合成纤维:
区分天然纤维和合成纤维最简单的方法:
(3)橡胶
人类常用的合成橡胶包括:
具有 等优良性能。
(4)白色污染
减少白色污染,可从以下几个方面着手:
1.
2.
3.
4.
学生讨论:使用塑料的利与弊
教师引导,学生自我小结:
课堂练习:
481.下列物质不属于有机合成材料的是( )
A.合金 B.塑料 C.合成橡胶 D.合成纤维
2.下列产品所用的塑料,具有热固性的是( )
A.放水塑料手套 B.雨衣 C.炒菜锅的手炳 D.浴帽
课后练习:
1.下列物质中属于有机高分子化合物的是( )
A.乙醇 B.淀粉 C.葡萄糖 D.蔗糖
2.解决“白色污染”问题,下列做法不宜提倡的是( )
A.使用新型可降解塑料 B.用布袋代替塑料袋
C.回收废弃塑料 D.焚烧废弃塑料
3.有机合成材料的出现是材料发展史上的一次重大突破,下列物质属于合成纤维的是( )
A.棉花 B.羊毛 C.蚕丝 D.尼龙
4.下列各组物质鉴别方法不正确的是( )
A.用肥皂水鉴别硬水和软水 B.用灼烧的方法鉴别羊毛和合成纤维
C.用碱鉴别铵盐和钾肥 D.跟和外观和是否溶于水鉴别食盐和亚硝酸钠
5.化合物主要有两大类: 和 。CH 属于 ,CO 属于
4 2
。 , 和 等是重要的有机合成材料。
6.特快电热壶由于快捷方便,被许多家庭,宾馆使用,
请根据下图回答
(1)制作材料中属于金属或合金是 ,
属于有机物的是 ;
(2)制作手炳的塑料属于 塑料
(填“热塑性”或“热固性”)
(3)用铜质材料制作电源插头的插脚是利
用铜具有 性;
(4)这种水壶具有水沸自动断电保护功能,
即水沸后因气压增大使电源开关自动断电。
从分子的角度解释水沸后气压增大的原因:
课后反思:
49