文档内容
湖南邵阳市郊区2017-2018学年九年级上学期化学期末考试试卷
一、单选题
1.下列成语与化学变化有关的是( )
A. 沙里淘金 B. 滴水成
冰 C. 木已成
舟 D. 钻木取火
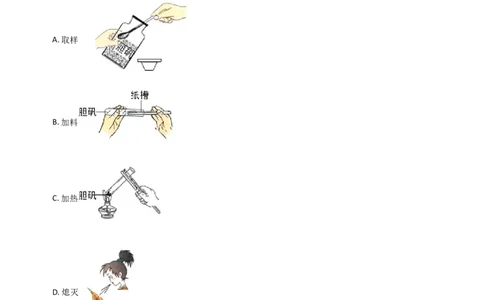
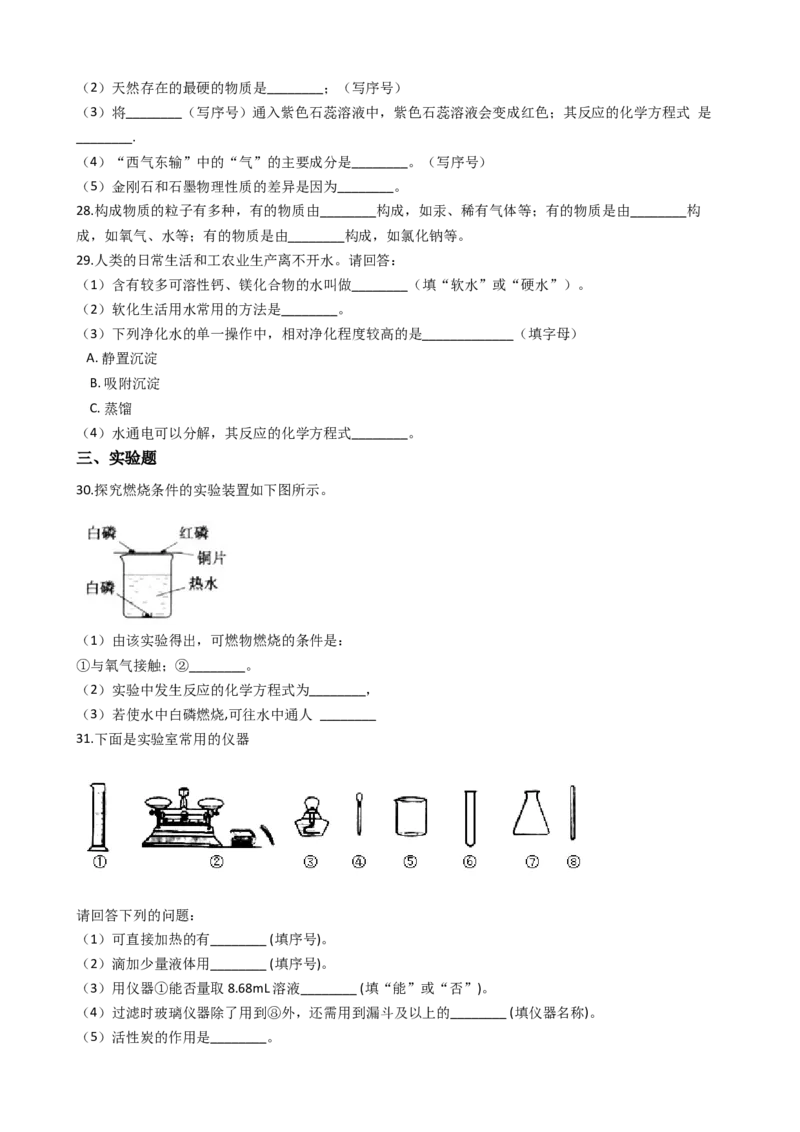
2.加热胆矾的实验过程中,相关实验操作正确的是( )
A. 取样
B. 加料
C. 加热
D. 熄灭
3.下列说法正确的是( )
A. 木炭燃烧后生成黑色固体
B. 铁丝伸入盛有氧气的集气瓶中剧烈燃烧
C. 红磷在空气中燃烧产生大量白雾 D. 氢气在
空气中燃烧发出淡蓝色火焰
4.下列各组物质,前者属于混合物,后者属于化合物的是( )A. 净化后的自来水 空气 B. 石灰水
水 C. 冰水混合物 液氧 D. 氮
气 煤
5.2013年6月12日,神舟十号航天员在太空中度过了中国传统节日﹣﹣端午节,并且吃到了粽子.粽子
采用真空包装是为了隔绝( )
A. 氮气 B. 水蒸
气 C. 氧
气 D. 稀有气体
6.有关催化剂的说法错误的是( )
A. 反应前后本身质量不变
B. 反应前后化学性质不变
C. 一定加快化学反应速率
D. 可能减慢化学反应速率
7.下列关于氧气的说法,错误的是( )
A. 实验室制取氧气时,不一定要加催化剂 B. 硫在氧气中燃烧,发出蓝
紫色火焰
C. 油锅着火,可用锅盖盖灭,原理是隔绝氧气 D. 氧气不溶于水
8.实验室用高锰酸钾制纯净氧气时,下列做法错误的是( )
A. 在试管口放一团棉花,防止高锰酸钾粉末进入导管 B. 把试管口略向下倾斜固
定在铁架台上
C. 导管口开始有气泡放出时就立即收集,防止生成的气体跑掉 D. 停止加热时,
先把导管移出水面,再熄灭酒精灯
9.造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
A. 分子很小 B. 分子在不断运
动 C. 分子之间有间隙
D. 分子由原子构成
10.与元素化学性质的关系最密切的是( )
A. 元素的相对原子质量
B. 原子核外的最外层电子数
C. 原子核内的中子数
D. 原子核内的质子数
11.根据右图提供的信息,下列说法正确的是( )
A. 钠原子最外层有11个电子
B. 钠的相对原子质量是22.99g
C. 钠的原子序数为11 D. 钠属于非金属元素12.在化学反应前后,下列各项中一定没有变化的( )
①原子的数目 ②分子的数目③元素的种类 ④物质的总质量 ⑤物质的种类 ⑥原子的种类
A. ①③④⑤ B. ①③⑤
C. ①③④⑥
D. ①④⑥
13.二甲醚(C H O)作为一种新能源,有关说法正确的是( )
2 6
A. 二甲醚中碳元素与氢元素的质量比为4︰1 B. 二甲醚的相对分子质量为48
C. 二甲醚由2个碳原子、6个氢原子和1个氧原子构成 D. 二甲醚属于氧化
物
14.不同元素间最本质的区别是 ( )
A. 中子数不同 B. 质子数不
同 C. 电子数不
同 D. 相对原子质量不同
15.下列观点,我不赞同的是( )
A. 肥皂水可以区别硬水和软水
B. 风力发电可以减少对环境的污染
C. 电线短路引起火灾最好用水灭火 D. 活性炭
可以吸附水中的色素和异味
16.下图表示治理汽车尾气所涉及反应的微观过程。下列说法正确的是( )
A. 该反应使有害气体转化为无害气体 B. 图中单质的化
学式为O
2
C. 该反应属于置换反应
D. 该反应分子个数发生了改变,不符合质量守恒定律
17.“低碳生活”已成为当今的热门话题。下列对“低碳生活”的理解不准确的是( )
A. 减少使用含碳的燃料
B. 其中“碳”指的是碳单质
C. 大力推广使用新能源和新燃料 D. 可
以有效防止温室效应
18.神舟七号飞船成功发射,发射神舟七号飞船的火箭用偏二甲肼(C H N )和四氧化二氮(N O )作常规推进
2 8 2 2 4
剂,反应的化学方程式为:C H N +2 N O =3X+2CO +4H O,则X的化学式为( )
2 8 2 2 4 2 2
A. O B. H C. N D. CO
2 2 2
19.下列二氧化碳的用途,既跟它的物理性质有关,又跟它的化学性质有关的是( )
A. 制纯碱 B. 制干
冰 C. 用来灭
火 D. 制化肥20.我们每时每刻都离不开空气,空气成分的微小变化都会直接影响人类的生存,你关注每天的空气质量
报告吗?在空气质量报告中一般不涉及( )
A. 二氧化碳 B. 二氧化硫 C. 氮氧化合
物(NO) D. 可吸入颗粒物(TSP)
x
21.1854年5月30日,英国战舰“欧罗巴”的船舱里装满了供战马吃的草料,航行途中突然草料着火,整
个战舰瞬间变为火海。则下列有关说法错误的是( )。
A. 草料舱没有氧气
B. 草料舱通风不好
C. 草料发生缓慢氧化积累了大量的热 D. 草料温度达到
了草料的着火点
22.下列方法能鉴别空气、氧气和二氧化碳三瓶气体的是( )
A. 将燃着的木条伸入集气瓶中 B. 将集气瓶倒扣在水
中 C. 观察颜色 D. 闻气味
23.某物质在空气中完全燃烧生成二氧化碳和水,则关于物质的组成描述正确的是( )
A. 该物质只含有碳元素和氢元素 B. 该
物质中碳元素与氢元素的质量比为12︰1
C. 该物质一定含有碳元素和氢元素,可能含有氧元素 D. 该物质的分子中碳原子
与氢原子的个数比为1︰2
24.在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关
数据如下表:
物质 W G H P
3
反应前质量/g18 1 2
2
1
反应后质量/g待测262
2
对该反应的认识正确的是( )
A. W待测值是13 B. 物质H是该反应的催化剂 C. P是生成
物 D. 该反应是分解反应
25.核电站可用硼酸(H BO )吸收中子,阻断核辐射。硼酸中硼元素的化合价是( )
3 3
A. +1 B. +3 C. +2 D. +4
二、填空题
26.26、用化学用语填空.
(1)2个氮原子________;
(2)镁离子________
(3)硫酸铜________;
(4)保持水的化学性质的最小粒子________;
(5)氧化铝中铝元素显+3价________。
27.下列物质中①二氧化碳 ②一氧化碳 ③金刚石 ④甲烷。
(1)有剧毒的是________;(写序号)(2)天然存在的最硬的物质是________;(写序号)
(3)将________(写序号)通入紫色石蕊溶液中,紫色石蕊溶液会变成红色;其反应的化学方程式 是
________.
(4)“西气东输”中的“气”的主要成分是________。(写序号)
(5)金刚石和石墨物理性质的差异是因为________。
28.构成物质的粒子有多种,有的物质由________构成,如汞、稀有气体等;有的物质是由________构
成,如氧气、水等;有的物质是由________构成,如氯化钠等。
29.人类的日常生活和工农业生产离不开水。请回答:
(1)含有较多可溶性钙、镁化合物的水叫做________(填“软水”或“硬水”)。
(2)软化生活用水常用的方法是________。
(3)下列净化水的单一操作中,相对净化程度较高的是_____________(填字母)
A. 静置沉淀
B. 吸附沉淀
C. 蒸馏
(4)水通电可以分解,其反应的化学方程式________。
三、实验题
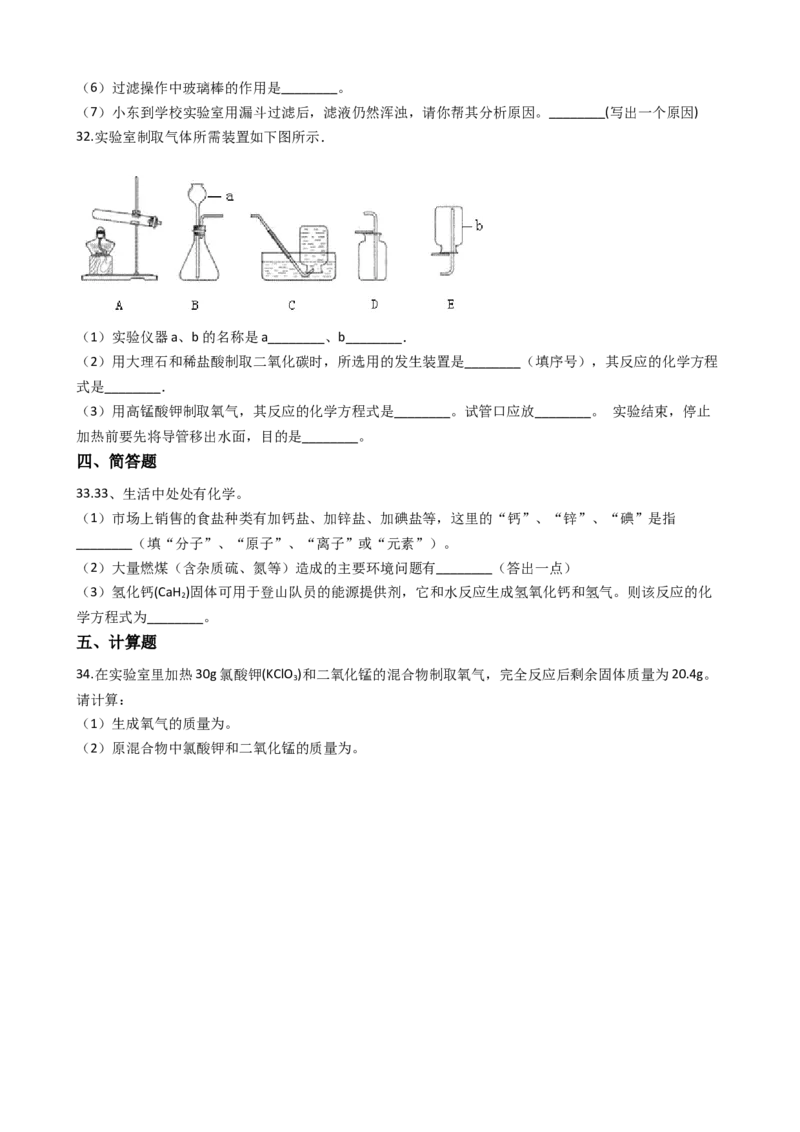
30.探究燃烧条件的实验装置如下图所示。
(1)由该实验得出,可燃物燃烧的条件是:
①与氧气接触;②________。
(2)实验中发生反应的化学方程式为________,
(3)若使水中白磷燃烧,可往水中通人 ________
31.下面是实验室常用的仪器
请回答下列的问题:
(1)可直接加热的有________ (填序号)。
(2)滴加少量液体用________ (填序号)。
(3)用仪器①能否量取8.68mL溶液________ (填“能”或“否”)。
(4)过滤时玻璃仪器除了用到⑧外,还需用到漏斗及以上的________ (填仪器名称)。
(5)活性炭的作用是________。(6)过滤操作中玻璃棒的作用是________。
(7)小东到学校实验室用漏斗过滤后,滤液仍然浑浊,请你帮其分析原因。________(写出一个原因)
32.实验室制取气体所需装置如下图所示.
(1)实验仪器a、b的名称是a________、b________.
(2)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是________(填序号),其反应的化学方程
式是________.
(3)用高锰酸钾制取氧气,其反应的化学方程式是________。试管口应放________。 实验结束,停止
加热前要先将导管移出水面,目的是________。
四、简答题
33.33、生活中处处有化学。
(1)市场上销售的食盐种类有加钙盐、加锌盐、加碘盐等,这里的“钙”、“锌”、“碘”是指
________(填“分子”、“原子”、“离子”或“元素”)。
(2)大量燃煤(含杂质硫、氮等)造成的主要环境问题有________(答出一点)
(3)氢化钙(CaH )固体可用于登山队员的能源提供剂,它和水反应生成氢氧化钙和氢气。则该反应的化
2
学方程式为________。
五、计算题
34.在实验室里加热30g氯酸钾(KClO )和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4g。
3
请计算:
(1)生成氧气的质量为。
(2)原混合物中氯酸钾和二氧化锰的质量为。答案解析部分
一、单选题
1.【答案】D
【考点】化学变化的基本特征,物理变化的特点,化学变化和物理变化的判别
【解析】【解答】A、沙里含有单质金,沙里淘金的过程中没有新物质生成,属于物理变化,不符合题
意;
B、滴水成冰的过程中没有新物质生成,属于物理变化,不符合题意;
C、用木材制造船的过程中没有新物质生成,属于物理变化,不符合题意;
D、钻木取火的过程中,木材燃烧起来,木材燃烧能生成水和二氧化碳,属于化学变化,符合题意。
故答案为:D。
【分析】A、沙里淘金没有新物质生成,属于物理变化;
B、滴水成冰没有新物质生成,属于物理变化;
C、木头制成木船过程中没有新物质生成,属于物理变化;
D、钻木取火的过程中,木材燃烧起来,此过程中有新物质生成,属于化学变化。
2.【答案】B
【考点】加热器皿-酒精灯,固体药品的取用,给试管里的固体加热
【解析】【解答】解:A、取用药品时,瓶塞不能正放在桌面上,故错误;
B、向试管中加入粉末状药品时,将试管横放,用纸槽将药品慢慢送到试管底部,然后将试管直立起来,
使药品落到试管底部,故正确;
C、给试管里的固体加热时,试管底部不能接触灯芯,试管口应略向下倾斜,以防试管炸裂,故错误;
D、熄灭酒精灯,应用灯帽盖灭,不能用嘴吹,故错误.
故选B.
【分析】A、根据取用药品时的注意事项分析,瓶塞不能正放在桌面上;
B、根据向试管中加入粉末状药品的方法分析,将试管横放,用纸槽将药品慢慢送到试管底部,然后将试
管直立起来,使药品落到试管底部;
C、根据给试管里的固体加热的注意事项分析,试管底部不能接触灯芯,试管口应略向下倾斜;
D、根据熄灭酒精灯的方法分析,用灯帽盖灭.
3.【答案】D
【考点】氧气与碳、磷、硫、铁等物质的反应现象,氢气、一氧化碳、甲烷等可燃气体的验纯
【解析】【解答】A、木炭燃烧放出热量,生成能使澄清石灰水变浑浊的气体,不符合题意;
B、铁丝伸入盛有氧气的集气瓶中,若不点燃不会剧烈燃烧,不符合题意;
C、红磷在空气中燃烧,产生大量的白烟,而不是白雾,不符合题意;
D、氢气在空气中燃烧,产生淡蓝色火焰,放出热量,符合题意。
故答案为:D。
【分析】A、木炭燃烧生成的是二氧化碳,是一种无色气体,描述为木炭燃烧放出热量,生成能使澄清石
灰水变浑浊的气体;B、铁丝必须点燃伸入高浓度氧气中,才能够燃烧;
C、烟是固体小颗粒在空气中形成的,雾是小液滴在空气中形成的,红磷燃烧生成的是固体,故应该产生
的是大量的白烟。
D、纯净的氢气可以在空气中安静的燃烧,发出淡蓝色火焰。
4.【答案】B
【考点】纯净物和混合物的概念,纯净物和混合物的判别,单质和化合物的概念,单质和化合物的判别
【解析】【解答】A、净化后的自来水中溶有可溶性物质,属于混合物;空气中含有氧气氮气等,属于混
合物,不符合题意;
B、石灰水中含有水和氢氧化钙,属于混合物;水是碳、氢两种元素组成的纯净物,属于化合物,符合题
意;
C、冰水混合物只有水一种物质,属于纯净物;液态氧是氧元素组成的纯净物,属于单质,不符合题意;
D、氮气是氮元素组成的纯净物,属于单质;煤炭的主要成分是碳,还含有硫等物质,属于混合物,不符
合题意。
故答案为:B。
【分析】A、净化后的自来水中还含有一些可溶性物质,属于混合物,空气有氮气、氧气等多种成分组
成,属于混合物
B、石灰水是氢氧化钙的水溶液,是混合物,水是由不同元素组成的纯净物,属于化合物;
C、冰水共存物中只有一种分子,属于纯净物,液态氧气中只有氧气这一种物质,属于纯净物;
D、氮气中只有一种分子,属于纯净物,煤是一种复杂的混合物。
5.【答案】C
【考点】空气对人类生活的重要作用,氧气的化学性质
【解析】【解答】粽子采用真空包装是为了隔绝氧气,这样可以防止粽子发生缓慢氧化,从而延长粽子
的保质期.故答案为:C.【分析】A、氮气化学性质稳定,可以做包装食品的防腐剂;
B、粽子不需要干燥,故真空包装的目的不是防水
C、氧气存在可以加速食品的腐败,主要是食品发生缓慢氧化提供氧气;
D、稀有气体化学性质稳定,可以做包装食品的防腐剂;
6.【答案】C
【考点】催化剂的特点与催化作用
【解析】【解答】A、催化剂反应前后本身质量不变,故A正确;A不符合题意;
B、催化剂反应前后化学性质不变,故B正确;B不符合题意;
C、催化剂是改变反应速率,而不一定是加快化学反应速率,有的催化剂还能减慢化学反应速率,故C错
误;C符合题意;
D、催化剂是改变反应速率,所以可能减慢化学反应速率,故D正确.D不符合题意.
故答案为:C.
【分析】催化剂反应前后本身质量不变、反应前后化学性质不变;不一定加快化学反应速率,可能减慢
化学反应速率.
7.【答案】D
【考点】氧气的物理性质,氧气与碳、磷、硫、铁等物质的反应现象,实验室制取氧气的反应原理,灭
火的原理和方法【解析】【解答】A、实验室用加热高锰酸钾制取氧气时,不用催化剂,不符合题意;
B、硫在氧气中燃烧,发出蓝紫色火焰,不符合题意;
C、油锅着火,盖上锅盖,使可燃物隔绝空气而熄灭,不符合题意;
D、氧气不易溶于水,而不是不溶于水,符合题意。
故答案为:D。
【分析】A、实验室制取氧气的方法分别是,加入硫酸钾和二氧化锰的混合物、加热高锰酸钾、分解过氧
化氢,其中加热高锰酸钾不需要催化剂;
B、硫在空气中燃烧发出淡蓝色火焰,在氧气中燃烧发出明亮蓝紫色火焰;
C、油锅着火可以放入切好的冷蔬菜,降温至着火点以下,也可以盖上锅盖,隔绝空气;
D、氧气不易溶于水或微溶于水,水中的鱼类就依靠微溶于水中的氧气而生存。
8.【答案】C
【考点】制取氧气的操作步骤和注意点
【解析】【解答】A、为了收集的氧气更纯净,应在试管口放一团棉花,防止高锰酸钾粉末进入导管,故
做法正确;A不符合题意;
B、为防止加热时试管内壁出现的小水珠流到试管底部将试管炸裂,因此试管口要略向下倾斜,故做法正
确;B不符合题意;
C、导管口的气泡连续、均匀的放出时开始收集,以防收集的氧气不纯,故做法错误;C符合题意;
D、为防止冷水倒吸入热的试管,则在实验完毕后,先将导管移出水面再熄灭酒精灯,故做法正确。D不
符合题意;
故答案为:C。
【分析】A、实验室用高锰酸钾制取氧气时,在试管口放一团棉花,防止高锰酸钾粉末进入导管或防止高
锰酸钾的粉末进入集气瓶;
B、为了防止冷凝水倒流,引起试管炸裂,把试管口略向下倾斜固定在铁架台上;
C、收集氧气时,试管口刚刚冒出的气泡是试管中排除的空气,要有连续不断的气泡冒出时再收集;
D、为了防止水槽中的水倒流入试管,实验结束时停止加热时,先把导管移出水面,再熄灭酒精灯。
9.【答案】B
【考点】利用分子与原子的性质分析和解决问题
【解析】【解答】由于烟草在燃烧的过程中会产生如CO、尼古丁、焦油等对人体有害的物质.构成这些
有害物质的微粒会不断运动,从而造成他人被动吸烟,也就是常说的“二手烟”.因此在公共场所应禁
止吸烟.
A、由分子的性质可知,吸食“二手烟”的主要原因与分子的大小无关,故A错误;
B、由于分子在不断运动,这是造成吸食“二手烟”的主要原因.故B正确;
C、由分子的性质可知,吸食“二手烟”的主要原因与分子之间有间隙无关.故C错误;
D、吸食“二手烟”的主要原因与分子的构成没有关系.故D错误.故选B.
【分析】准确理解分子的性质,会应用微粒的基本性质解释某些生活中的现象.
10.【答案】B
【考点】原子的定义与构成
【解析】【解答】由题意可知,最外层电子数与元素的化学性质关系最密切。因为物质参加化学反应时
发生作用(得失电子)的一般只是最外层电子,所以与元素化学性质的关系最密切的是原子核外的最外层电子数,与元素的相对原子质量、原子核内的中子数、原子核内的质子数无关。
故答案为:B。
【分析】A、相对原子质量是一个C--6原子质量的十二分之一为标准,其他原子质量跟他相比所得的值;
B、决定元素化学性质的是原子核外最外层电子数,主要看原子是否容易得失电子
C、中子数与元素的化学性质无关
D、原子核内的质子数决定原子和元素的种类。
11.【答案】C
【考点】元素的简单分类,元素周期表的特点及其应用
【解析】【解答】钠原子的最外层电子数为1个电子,故A不符合题意;
相对原子质量的单位是1,故B不符合题意;
元素名称的左上角的数字是原子序数,所以钠的原子序数为11,
故答案为:C;
金属元素有金字旁(除汞外),非金属没有金字傍,所以钠属于金属元素,故D不符合题意。
【分析】A、钠元素的原子序数为11,原子序数=质子数=核电荷数=核外电子数;
B、相对原子质量的单位为1;
C、钠元素通常说法为11号元素,即原子序数为11;
D、钠元素属于金属元素(带金字旁)
12.【答案】C
【考点】质量守恒定律及其应用
【解析】【解答】化学变化的实质就是分子分成原子,原子再重新组合成新分子,在反应前后,原子的
种类、数目、质量都不变;化学反应前后元素的种类不变;化学反应前后,有新分子生成,则分子的种
类一定发生改变;分子的数目可能发生改变,也可能不变。
故答案为:C。
【分析】A、化学反应有新物质生成,物质的种类一定发生改变;
B、化学反应有新物质生成,物质的种类一定发生改变;
C、根据质量守恒定律,在化学反应中,“六不变、两要变。一可能变”宏观看:物质的总质量、元素种
类、元素质量不变;微观看,原子种类、原子数目、原子质量不变。两个一定要改变的是物质种类和分
子种类,一个可能变的是分子数目;
D、在化学反应前后,元素的种类不会改变。
13.【答案】A
【考点】氧化物、酸、碱和盐的概念,分子、原子、离子、元素与物质之间的关系,相对分子质量的概
念及其计算,元素质量比的计算
【解析】【解答】A、二甲醚中碳元素与氢元素的质量比为(12×2):(1×6)=4:1,符合题意;
B、二甲醚的相对分子质量为12×2+1×6+16=46,不符合题意;
C、二甲醚是由二甲醚分子构成的,1个二甲醚分子是由2个碳原子、6个氢原子和1个氧原子构成的,不
符合题意;
D、二甲醚是由碳、氢、氧三种元素组成的化合物,不属于氧化物,不符合题意。
故答案为:A。
【分析】A、元素的质量比即原子个数乘以相对原子质量之比,故二甲醚中碳元素与氢元素的质量比为(12×2):(1×6)=4:1
B、相对分子质量即各元素原子个数乘以相对原子质量之和,故二甲醚的相对分子质量为
12×2+1×6+16=46;
C、二甲醚有二甲醚分子构成,它的一个原子由2个碳原子、6个氢原子和1个氧原子构成的;
D、氧化物是由两种元素组成,其中一种是氧化物的化合物,二甲醚组成元素是3种。
14.【答案】B
【考点】分子、原子、离子、元素与物质之间的关系,元素的概念
【解析】【解答】元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素的种类得是
核电荷数(即核内质子数),故不同种元素本质的区别是原子的核电荷数(即核内质子数)不同。
故答案为:B。
【分析】A、中子数决定元素的质量和原子的相对原子质量;
B、决定元素种类的是质子数或核电荷数,故不同种元素的根本区别即质子数或核电荷数不同
C、电子数尤其是最外层电子数决定元素的化学性质;
D、相对原子质量是为了原子质量的计算记忆方便而找的相对原子质量。
15.【答案】C
【考点】硬水与软水,常用燃料的使用与其对环境的影响,灭火的原理和方法,碳单质的物理性质及用
途
【解析】【解答】解:A、根据鉴别硬水和软水的方法用肥皂水,泡沫多、浮渣少的为软水,故A说法正
确;
B、根据风力发电可以减少对环境的污染,故B说法正确;
C、根据电线短路引起火灾不能用水直接灭火,因为水有一定的导电性,所以电线短路引起火灾最好用水
灭火说法错误;故C说法错误;
D、根据活性炭有很强的吸附能力,可以吸附水中的色素和异味,故D说法正确;
故选C.
【分析】A、根据鉴别硬水和软水的方法用肥皂水,泡沫多、浮渣少的为软水,进行解答;
B、根据风力发电可以减少对环境的污染,进行解答;
C、根据电线短路引起火灾不能用水直接灭火,因为水有一定的导电性,进行解答;
D、根据活性炭有很强的吸附能力,可以吸附水中的色素和异味,进行解答.
16.【答案】A
【考点】质量守恒定律及其应用,微粒观点及模型图的应用
【解析】【解答】A、因CO和NO都有毒,通过该反应生成无毒的二氧化碳和氮气,即将有害气体转化为
无害气体,符合题意;
B、因白球代表N原子,图中的单质应为N , 不符合题意;
2
C、因置换反应是单质与化合物反应生成单质和化合物,而该反应的反应物都是化合物,不符合题意;
D、一切化学变化都符合质量守恒定律,不符合题意。
故答案为:A。
【分析】A、该反应为一氧化碳和一氧化氮反应生成五毒的氮气和二氧化碳;
B、单质为氮气C、该反应的反应物是两种化合物,只有生成物中有一种单质,故不是置换反应;
D、所有化学反应都遵循质量守恒定律。
17.【答案】B
【考点】二氧化碳对环境的影响,低碳生活和低碳经济
【解析】【解答】A、减少使用含碳的燃料,可以减少二氧化碳的排放,符合的“低碳生活”,不符合题
意,不符合题意;
B、“低碳生活”中的“碳”指的是二氧化碳,而不是碳单质的“碳”,符合题意,符合题意;
C、大力推广使用新能源和新燃料,可以节省化石燃料的应用,减少有害气体的排放,属于“低碳生
活”,不符合题意,不符合题意;
D、造成温室效应的罪魁祸首是二氧化碳,“低碳生活”可以有效防止温室效应,不符合题意,不符合题
意。
故答案为:B。
【分析】A、减少使用含碳的燃料,即可减少二氧化碳的排放;
B、”碳“指二氧化碳
C、大力推广新能源和新燃料可以减少二氧化碳的排放
D、二氧化碳是引起温室效应的主要气体。
18.【答案】C
【考点】质量守恒定律及其应用
【解析】【解答】由质量守恒定律可得,在化学反应前后原子的种类和数目不变,在化学方程式
C H N +2N O =3X+2CO +4H O中,反应前所有物质中的碳原子共为2个,氢原子共为8个,氮原子共为6
2 8 2 2 4 2 2
个,氧原子数共为8个,反应后除X外,碳原子共为2个,氢原子共为8个,氮原子共为0个,氧原子数
共为8个,故每个X分子中含有氮原子共为2个,所以X为N 。
2
故答案为:C。
【分析】化学反应前后原子的种类和数目不变。
19.【答案】C
【考点】二氧化碳的用途,化学性质与物理性质的差别及应用
【解析】【解答】A、二氧化碳制纯碱有新物质生成,只利用了二氧化碳的化学性质,不符合题意;
B、制干冰是利用了二氧化碳易变成固体这一物理性质,不符合题意;
C、二氧化碳用来灭火是利用二氧化碳不燃烧,也不支持燃烧的化学性质和密度比空气大的物理性质,符
合题意;
D、二氧化碳制化肥有新物质生成,只利用了二氧化碳的化学性质,不符合题意。
故答案为:C。
【分析】A、制取纯碱是利用二氧化碳与氢氧化钠反应是化学性质;
B、制干冰是把气体二氧化碳加压降温变为二氧化碳的固体,是物理性质;
C、二氧化碳灭火利用其密度比空气大的物理性质,覆盖在可燃物的表面隔绝空气,也利用了其不燃烧不
支持燃烧的化学性质;
D、制话费利用的是二氧化碳的化学性质,即二氧化碳可以与氨气反正制取尿素。
20.【答案】A
【考点】空气的污染及其危害,防治空气污染的措施,目前环境污染问题【解析】【解答】A、二氧化碳不是污染物,无须报告,但空气中二氧化碳增多会带来温室效应,符合题
意;
B、二氧化硫,是空气主要污染物,要测量报告,不符合题意;
C、氮氧化合物(NO),是空气主要污染物,要测量报告,不符合题意;
x
D、可吸入颗粒物,是空气主要污染物,要测量报告,不符合题意。
故答案为:A。
【分析】A、二氧化碳不是大气污染物,含量过高会造成温室效应;
B、二氧化硫是大气污染物,含量过高会造成酸雨;
C、氮氧化合物中一氧化氮、二氧化氮等都是大气污染物;
D、可吸入颗粒属于污染物,空气中含量过高会造成雾霾。
21.【答案】A
【考点】燃烧与燃烧的条件
【解析】【解答】草料舱内有氧气的存在。【分析】根据燃烧条件和灭火原理分析,燃烧需要同时满足
可燃物、与氧气接触、温度达到着火点三个条件,缺一不可,若缺少一个则可灭火,所以灭火原理为撤
离可燃物或隔绝氧气或降温至着火点以下。
22.【答案】A
【考点】氧气的物理性质,氧气的化学性质,二氧化碳的物理性质
【解析】【解答】A、把燃着的木条分别伸入三个集气瓶中,若木条燃烧无明显变化,则是空气;若木条
熄灭,则是二氧化碳;若木条燃烧更旺,则是氧气;现象明显,能一次鉴别出这三瓶气体,符合题意;
B、空气、氧气都不易溶于水,无法鉴别,不符合题意;
C、空气、氧气和二氧化碳三种气体都是没有颜色的气体,用观察颜色的方法无法鉴别,不符合题意;
D、空气、氧气和二氧化碳三种气体都是没有气体的气体,用闻气体气味的方法无法鉴别,不符合题意。
故答案为:A。
【分析】鉴别物质必须根据物质不同的物理化学性质进行区分和鉴别。
A、燃着的木条在空气中正常燃烧,在氧气中燃得更加旺盛,在二氧化碳中熄灭。
B、气体倒扣在水中,只有二氧化碳能溶于水,没有十分明显的现象;
C、空气、氧气、二氧化碳都是无色气体;
D、空气、氧气、二氧化碳都是无味的气体。
23.【答案】C
【考点】质量守恒定律及其应用
【解析】【解答】生成物二氧化碳、水中含有C,H,O元素,根据质量守恒定律可知,则反应物中也一
定含有这三种元素,物质在空气中燃烧是和空气中的氧气反应,氧气由O元素组成,则C,H一定是从某
物质中来,而某物质中也可能含有O元素,故这种物质中一定含有含C和H,可能含O,碳元素与氢元素
的质量比、原子的个数比不能确定。
故答案为:C。
【分析】A、根据质量守恒定律,反应前后元素的种类和质量不变,所以某物质在空气中完全燃烧生成二
氧化碳和水,该物质中一定含有碳元素、氢元素,可能含有氧元素;
B、不知道该物质及生成物的质量,无法判断碳元素氢元素的质量比;
C、根据质量守恒定律,反应前后元素的种类和质量不变,所以某物质在空气中完全燃烧生成二氧化碳和水,该物质中一定含有碳元素、氢元素,可能含有氧元素;
D、不知道该物质及生成物的质量,不能确定该物质的分子中碳原子与氢原子的个数比为1︰2。
24.【答案】A
【考点】化合反应及其应用,质量守恒定律及其应用
【解析】【解答】A、由表中信息可知,P物质的质量减少为反应物,参加反应的质量是20g;G物质的质
量增加为生成物,生成的质量是25g;H物质的质量不变故H物质不参与反应。根据质量守恒定律可知,
W是反应物,参加反应的质量是5g,反应后物质W的质量为:18g-5g=13g,符合题意;
B、物质H的质量在反应前后不变,可能是该反应的催化剂,不符合题意;
C、P物质的质量减少,故为反应物,不符合题意;
D、反应物是两种,生成物是一种,属于化合反应,不符合题意。
故答案为:A。
【分析】A、分析表中的数据,可知20克P与5克W反应生成25克G,W原有18克,已经反应了5克,
剩余13克;
B、H的质量不变,可能是该反应的催化剂或不参与该反应;
C、P的质量减少,P为反应物;
D、该反应为P与W反应生成G,属于化合反应。
25.【答案】B
【考点】化合价规律和原则
【解析】【解答】根据在化合物中正负化合价代数和为零,可得硼酸中硼元素的化合价为:(+1)×3+
x+(-2)×3=0,则x=+3;
故答案为:B。
【分析】化合物中正负化合价的代数和为零,即(各元素的原子个数乘以化合)之和等于零。
二、填空题
26.【答案】(1)2N
(2)Mg2+
(3)CuSO
4
(4)H O
2
(5)
【考点】分子、原子、离子、元素与物质之间的关系,原子和离子的相互转化,化学式的书写及意义
【解析】【解答】(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素
符号前加上相应的数字,所以2个氮原子可表示为:2N;(2)根据离子的表示方法:在表示该离子的元
素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若
表示多个该离子,就在其元素符号前加上相应的数字,所以镁离子表示为Mg2+;(3)化学式书写的一般
规律是:正前负后,然后利用十字交叉法书写;硫酸铜中铜显+2价,硫酸根显-2价,表示为CuSO ;
4
(4)化学式书写的一般规律是:正前负后,然后利用十字交叉法书写,保持水的化学性质的最小粒子是
水分子,表示为H O;(5)元素正上方的数字表示元素的化合价,氧化铝中铝元素显+3价,表示
2
。【分析】(1)一个原子直接用元素符号表示,多个原子在元素符号前面添加系数;(2)离子是在元素符号的右上角先写数字,再写表示正负的符号;
(3)硫酸铜由铜离子和硫酸根离子构成,其中铜为正二价,硫酸根为负二价,则化学式为CuSO
4;
(4)保持物质化学性质的最小粒子是分子,则保持水的化学性质的微粒即为水分子;
(5)化合价是在元素符号的正上方,先写符号,再写数字。
27.【答案】(1)②
(2)③
(3)①;CO +H O=H CO
2 2 2 3
(4)④
(5)原子的排列方式不同
【考点】二氧化碳的化学性质,一氧化碳的毒性,化石燃料及其综合利用,碳单质的物理性质及用途
【解析】【解答】(1)一氧化碳极易与人体血液中的血红蛋白结合,从而使血红蛋白不能很好地与氧气
结合,失去了携氧能力,造成生物体内缺氧,而发生中毒现象;(2)天然存在的最硬的物质是金刚石;
(3)将二氧化碳通入紫色石蕊溶液中,二氧化碳与水反应生成碳酸,碳酸使紫色石蕊溶液变成红色;化
学方程式为:CO +H O=H CO ;(4)“西气东输”中的“气”的主要成分是甲烷;(5)由于金刚石和石
2 2 2 3
墨的碳原子排列方式不同,所以物理性质差异很大。【分析】(1)一氧化碳能与血液中的血红蛋白结
合,造成人体缺氧------中毒;
(2)天然最硬的物质为金刚石;
(3)二氧化碳与水反应生成的碳酸能够使石蕊有紫色变成红色,反应的方程式为:CO +H O=H CO ;
2 2 2 3
(4)西气东输是把我国西部丰富的天然气输送到我国东部地区,支持东部发展需要;天然气的主要成分
为甲烷;
(5)碳单质物理性质不同的原因是由于碳原子排列方式的不同。
28.【答案】原子;分子;离子
【考点】分子、原子、离子、元素与物质之间的关系
【解析】【解答】构成物质的基本粒子有分子、原子和离子,有的物质由分子构成,如氧气属于气态非
金属单质,是由氧分子构成的;水是由水分子构成的;有的物质是由原子构成,如汞属于金属单质,是
由汞原子直接构成的;稀有气体是由原子直接构成的;有的物质是由离子构成,如氯化钠是由钠离子和
氯离子构成的。【分析】一般说来,金属单质,稀有气体单质、非金属固体单质由原子直接构成;气体
和液体由分子构成;酸碱盐由离子构成。
29.【答案】(1)硬水
(2)煮沸水
(3)C
(4)2H O 2H ↑+ O ↑
2 2 2
【考点】电解水实验,水的净化,硬水与软水
【解析】【解答】(1)含有较多可溶性钙、镁化合物的水叫做硬水;(2)加热煮沸可以将硬水中的
钙、镁化合物转化为水垢,所以软化生活用水常用的方法是加热煮沸;(3)在吸附、沉淀、过滤、蒸馏
等净化水的方法中,蒸馏可以得到几乎纯净的水,净化程度较高;(4)水在通电的条件下能够分解成氧
气和氢气,该反应的化学方程式为:2H O 2H ↑+ O ↑。【分析】(1)硬水中含有较多可溶性钙
2 2 2镁化合物;
(2)生活中常常通过煮沸,让水中可溶性钙镁化合物转化成沉淀而除去;
(3)净化水中蒸馏所得到的水是纯净物,所以蒸馏是对水净化成都最高的方法
三、实验题
30.【答案】(1)温度达到着火点
(2)4P+5O 2P O
2 2 5
(3)氧气
【考点】燃烧的条件与灭火原理探究,燃烧与燃烧的条件
【解析】【解答】(1)图中铜片上的白磷在热水的温度下达到着火点,能够燃烧;水中的白磷不与空气
接触,不能燃烧;红磷由于着火点高,热水不能使其达到着火点,所以不能燃烧,就是说可燃物燃烧的
条件是①与氧气接触②温度达到着火点;(2)磷燃烧生成五氧化二磷,化学反应式是:4P+5O
2
2P O ;(3)若使水中白磷燃烧,需要与氧气接触,可往水中通人氧气。【分析】(1)燃烧必须满足三个条
2 5
件:可燃物,温度达到着火点,与氧气或空气接触
(2)白磷的着火点只有40℃,燃烧后生产五氧化二磷,
(3)水中的白磷达到了着火点,白磷是可燃物,所以还需要满足的条件是空气或氧气,则需要通入的是
空气或氧气
。
31.【答案】(1)⑥
(2)④
(3)否
(4)烧杯
(5)吸附
(6)引流
(7)滤纸破损或液面高于滤纸边缘等等
【考点】用于加热的仪器,液体药品的取用,过滤的原理、方法及其应用
【解析】【解答】(1)可以直接加热的仪器是试管;(2)用来吸取和滴加少量液体的仪器是胶头滴
管;(3)图中量筒的精确度到0.1mL,不能用来量取8.68mL溶液;(4)过滤时玻璃仪器除了用到⑧
外,还需用到漏斗和可作为滤液承接器的仪器是烧杯;(5)活性炭疏松多孔,具有很强的吸附性;
(6)过滤操作中玻璃棒的作用是引流;(7)过滤后,滤液仍然浑浊,原因可能是滤液面高于滤纸边
沿、滤纸破损、承接滤液的烧杯不干净等。【分析】(1)可直接加热的仪器有:试管、蒸发皿等
(2)滴加少量液体需要用滴管;
(3)量筒只能精确至0.1毫升;
(4)过滤的玻璃仪器有:玻璃棒,漏斗和烧杯;
(5)木炭和活性炭都具有吸附性,但活性炭的吸附性更强;
(6)过滤中玻璃棒的作用是引流;
(8)过滤后液体任然浑浊的原因是:滤液边缘高于滤纸边缘、滤纸破损、玻璃仪器不干净等。32.【答案】(1)长颈漏斗;集气瓶
(2)B;CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
(3)2KMnO K MnO +MnO +O ↑;棉花;防止水倒流引起试管炸裂
4 2 4 2 2
【考点】常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,制取氧气的操作步
骤和注意点,二氧化碳的实验室制法,制取二氧化碳的操作步骤和注意点
【解析】【解答】(1)仪器a是长颈漏斗,仪器b是集气瓶;(2)在常温下用大理石和稀盐酸来制取二
氧化碳,因此不需要加热,属于固+液常温型,
故答案为:B装置;碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,化学方程式为:
CaCO +2HCl═CaCl +H O+CO ↑;(3)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,化学方程式为
3 2 2 2
2KMnO K MnO + MnO + O ↑;为防止高锰酸钾的固体小颗粒随气流进入导管,所以试管口应放棉
4 2 4 2 2
团;实验结束,停止加热前要先将导管移出水面,再熄灭酒精灯,是为了防止水倒吸造成试管炸裂。
【分析】(2)制取二氧化碳是用碳酸钙和稀盐酸在常温下反应,故为固液不加热型的发生装置;
(3)高锰酸钾受热分解为锰酸钾、二氧化锰和氧气;实验结束时为了避免水槽中的水倒流入试管,需要
先撤离导管,在停止加热。
四、简答题
33.【答案】(1)元素
(2)产生SO 、NO 等气体污染空气
2 2
(3)CaH +2H O=Ca(OH) +2H ↑
2 2 2 2
【考点】书写化学方程式,常见污染物的来源、危害及治理
【解析】【解答】(1)加钙盐、加锌盐、加碘食盐中的“钙”、“锌”、“碘”不是以单质、分子、原
子等形式存在,这里强调存在的元素,与具体形态无关;(2)因煤中含有S、C等元素,燃烧后生成二氧
化硫、二氧化氮、二氧化碳等,二氧化硫、二氧化氮可造成空气污染,酸雨,二氧化碳造成温室效应;
(3)根据题意可知,反应物为CaH 和H O,生成物为Ca(OH) 和H , 方程式为:CaH +2H O=Ca
2 2 2 2 2 2
(OH) +2H ↑。【分析】(1)加钙盐、加锌盐、加碘食盐中的“钙”、“锌”、“碘”都是指元素;
2 2
(2)煤中含有硫磺,燃烧会生成二氧化硫,还会生成二氧化氮等,会形成酸雨;
(3)根据题意,反应物为氢化钙和水,生成物为氢氧化钙和氢气,再根据化学方程式的书写方法书写即
可。
五、计算题
34.【答案】(1)解:由于是完全反应,根据质量守恒,减少的质量就是生成的氧气的质量,即制得氧
气:30g-20.4g=9.6g;
(2)解:解:设生成氯化钾的质量为x
2KClO 2KCl + 3O
3 2
↑
245 96
x 9.6g
x =24.5g二氧化锰的质量为30g-24.5g=5.5g
答:原混合物中氯酸钾的质量为24.5g,二氧化锰的质量为5.5g。
【考点】质量守恒定律及其应用,根据化学反应方程式的计算
【解析】【分析】(1)根据质量守恒定律及催化剂在反应前后质量不变,可知氧气的质量为:30克-20.4
克=9.6克
(2)利用方程式克根据氧气的质量计算出氯酸钾的质量为24.5克、则二氧化锰的质量用30克氯酸钾和
二氧化锰的混合物减去氯酸钾的质量即可。