文档内容
第七单元 燃料及其利用
【知识网络】
【分析解读】
1. 本节考查内容主要为燃烧的条件和灭火的原理,主要形式为实验探究题,
也有选择题和填空题;燃烧条件的探究一般以选择题的形式出现,往往与灭火的
原理、反应的现象与本质的联系综合出题,但在中考题中主要以填空题的形式出
现。灭火的原理一般以选择题形式出现。中考中将会出现利用燃烧条件、灭火的
原理、安全常识、自救方法来设计灭火方案,或分析、解决生产、生活中的实际问
题的题目,这样既考查了知识,又联系生活实际,符合当今的教学理念及思想。
2. 反应的放吸热问题主要记清课本中碳和二氧化碳的反应为吸热反应,燃烧
反应及中和反应为放热反应,化石燃料中天然气为清洁能源。煤、石油、天然气都
属于不可再生能源。在反应的吸放热方面经常与物质溶于水时的吸放热相联系,
同时结合化石燃料的燃烧造成的环境问题与新能与新能源知识,以填空题的形式
进行考查。
3.熟记目前使用的新能源为氢气、乙醇等,正在推广或使用的新能源:太阳能
风能、地热能、核能、潮汐能,主要考查氢能的优缺点、及制备,在此基础上与环境
污染相联系,举例正在推广或使用的新能源的种类。
【知识梳理】
1 / 20考点一:燃烧的条件及灭火(高频考点)
1.燃烧的条件及灭火
____________
燃烧的条件 _________(或空气)
达到燃烧所需的_________
_________或使可燃物与其他物质隔离
灭火的原理 隔绝_________(或空气)
使__________________以下
方法总结:绝大多数燃烧都是可燃物与氧气在点燃或加热的条件下发生的。但有
些燃烧不一定需要氧气参加,如金属镁可以在氮气和二氧化碳中燃烧,钠可以在
氯气中燃烧等。
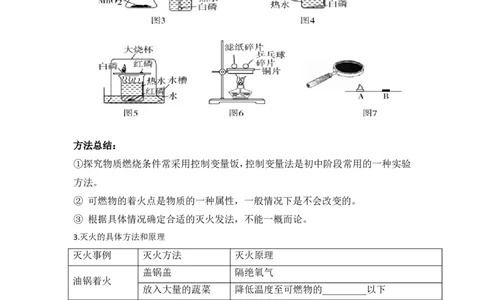
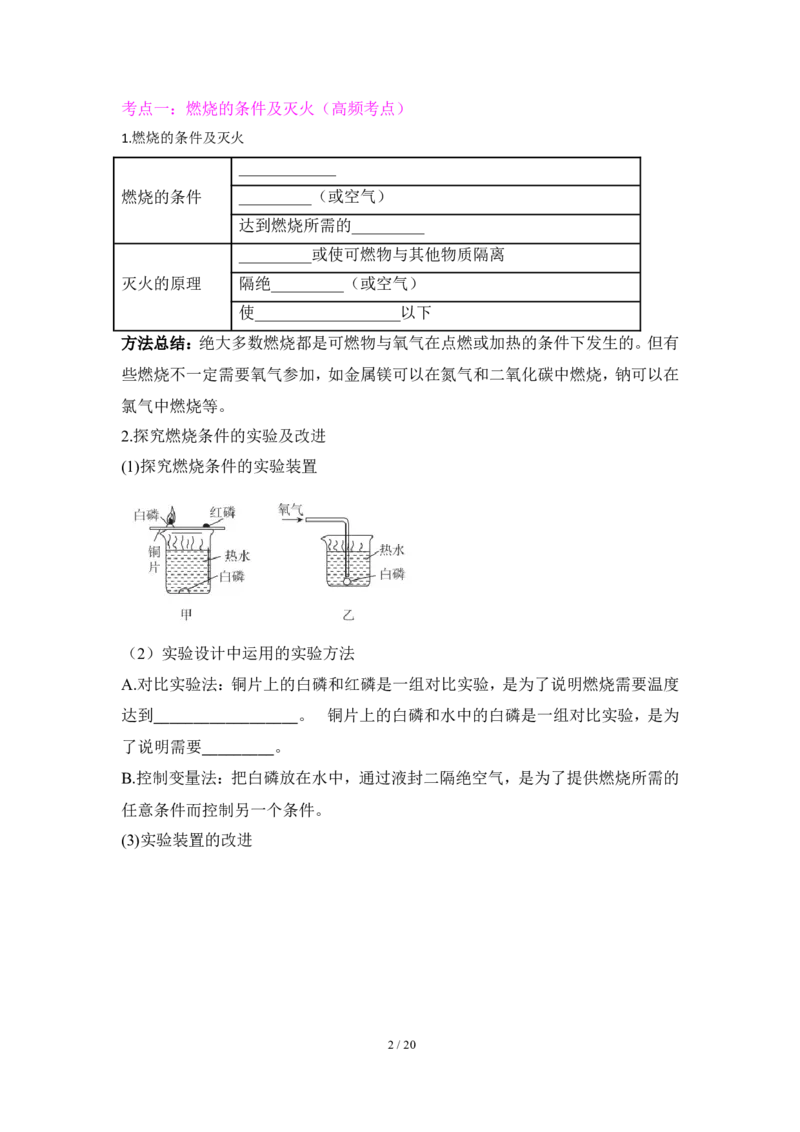
2.探究燃烧条件的实验及改进
(1)探究燃烧条件的实验装置
(2)实验设计中运用的实验方法
A.对比实验法:铜片上的白磷和红磷是一组对比实验,是为了说明燃烧需要温度
达到__________________。 铜片上的白磷和水中的白磷是一组对比实验,是为
了说明需要_________。
B.控制变量法:把白磷放在水中,通过液封二隔绝空气,是为了提供燃烧所需的
任意条件而控制另一个条件。
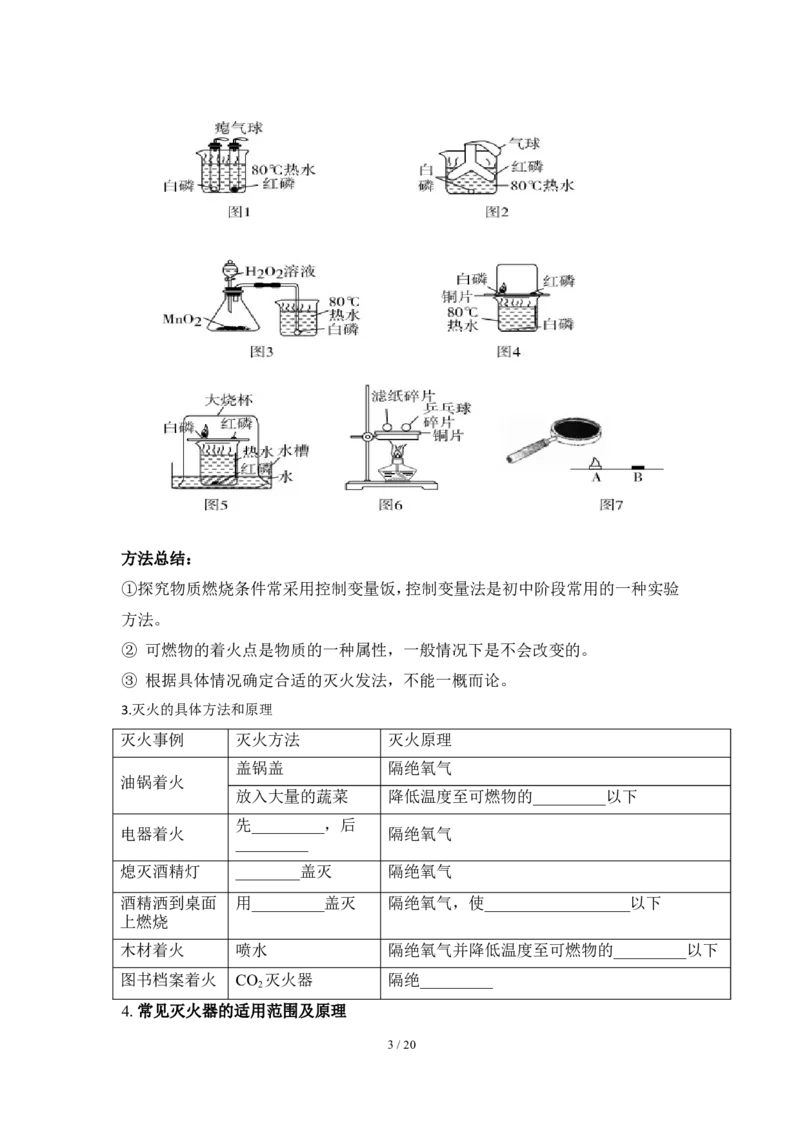
(3)实验装置的改进
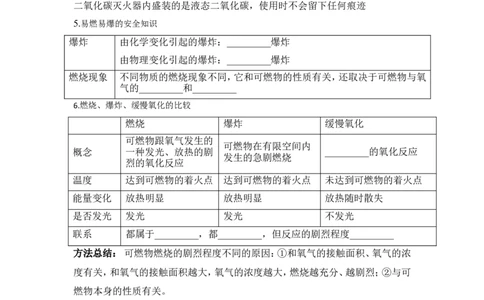
2 / 20方法总结:
①探究物质燃烧条件常采用控制变量饭,控制变量法是初中阶段常用的一种实验
方法。
② 可燃物的着火点是物质的一种属性,一般情况下是不会改变的。
③ 根据具体情况确定合适的灭火发法,不能一概而论。
3.灭火的具体方法和原理
灭火事例 灭火方法 灭火原理
盖锅盖 隔绝氧气
油锅着火
放入大量的蔬菜 降低温度至可燃物的_________以下
先_________,后
电器着火 隔绝氧气
_________
熄灭酒精灯 ________盖灭 隔绝氧气
酒精洒到桌面 用_________盖灭 隔绝氧气,使__________________以下
上燃烧
木材着火 喷水 隔绝氧气并降低温度至可燃物的_________以下
图书档案着火 CO 灭火器 隔绝_________
2
4. 常见灭火器的适用范围及原理
3 / 20灭火器 干粉灭火器 CO 灭火器 水基型灭火器
2
扑灭_________、_________、
扑灭油、气等燃烧引起的 扑灭汽油、柴油、木材、
适用范围 _________、精密仪器等物的
一般失火 棉布等引起的失火
失火
泡沫灭火器的反应原理:____________________________________。
干粉灭火器的反应原理:____________________________________。
二氧化碳灭火器内盛装的是液态二氧化碳,使用时不会留下任何痕迹
5.易燃易爆的安全知识
爆炸 由化学变化引起的爆炸:_________爆炸
由物理变化引起的爆炸:_________爆炸
燃烧现象 不同物质的燃烧现象不同,它和可燃物的性质有关,还取决于可燃物与氧
气的_________和_________
6.燃烧、爆炸、缓慢氧化的比较
燃烧 爆炸 缓慢氧化
可燃物跟氧气发生的
可燃物在有限空间内
概念 一种发光、放热的剧 _________的氧化反应
发生的急剧燃烧
烈的氧化反应
温度 达到可燃物的着火点 达到可燃物的着火点 未达到可燃物的着火点
能量变化 放热明显 放热明显 放热随时散失
是否发光 发光 发光 不发光
联系 都属于_________,都_________,但反应的剧烈程度_________
方法总结: 可燃物燃烧的剧烈程度不同的原因:①和氧气的接触面积、氧气的浓
度有关,和氧气的接触面积越大,氧气的浓度越大,燃烧越充分、越剧烈;②与可
燃物本身的性质有关。
7. 燃料充分燃烧和不充分燃烧
(1)充分燃烧的意义: ___________________________(放热多、节省能源);
___________________________。
(2)不充分燃烧的后果: 使燃料燃烧产生的_________减少,浪费资源;② 产生
大量的_________等物质,污染空气。
(3)如何做到使燃料充分燃烧:燃烧时要有足够多的_________;料要与空气要有
足够大的_________。
4 / 208.认识与燃烧和爆炸有关的图标
考点二:化学反应的能量变化与化石燃料(必考考点)
1.化学反应中的能量变化
(1)放热现象:物质的燃烧,金属与酸的反应等过程中都伴随着_______的现象。
(2)吸热现象:高锰酸钾分解,碳和二氧化碳的反应等过程中都伴随着_________
的现象。
2.人类生活对化学能的利用:
(1)生活燃料的利用:如_________、做饭等。
(2)利用燃料燃烧产生的能量:如火力发电、烧制陶瓷、冶金、发射火箭等。
(3)利用爆炸产生的能量:如开山炸石、拆除违章建筑等。
(4)利用食物在体内发生化学反应放出的能量,可维持体温和日常活动所需的能
量。
3.燃料充分燃烧的条件:一是___________________________;二是
___________________________。
4.化石燃料
(1)化石燃料包括_________、_________和_________,它们是_________ (填“可
再生”或“不可再生”)能源,属于_________ (填“纯净物”或“混合物”)。
(2)煤和石油
煤 石油
古代植物的遗骸经过一系列 古代动植物的遗骸在地壳中经过复杂
形成
复杂的变化形成的 变化形成的
元素组成 主要含__,少量H、N、O、S 主要含_________,少量S、O、N
类型 _________ _________
5 / 20黏稠液体,黑色或棕色,不溶于水,密
状态 黑色固体,有光泽
度比水小,无固定的熔点、沸点
方法总结:为了使煤得到充分利用,将煤隔绝空气加热,可以使煤分解成很多有
用的物质,如焦炭、煤焦油、煤气等,此过程是化学变化。石油的炼制是根据石油
各成分的沸点不同,通过分馏使之分离,此过程是物理变化。
(3)煤和石油的综合利用
(4)天然气
①天然气是由碳和氢组成的气态碳氢化合物,主要成分是_________,是一种最
简单的_________。有石油的地方就有天然气。甲烷也叫沼气、坑气,化学式为
_________。
②甲烷的性质
物理
纯净的甲烷是_________、_________ 的气体,密度比空气_________,
性质 _________溶于水,可用_________收集
化学 具有可燃性,燃烧时产生_________火焰,_________大量的热,生成的气体能
使_________变浑浊。其燃烧的化学方程式为__________________。
性质
方法总结:瓦斯气体是甲烷与空气的混合气体,点燃(或遇明火)时可能发生爆炸,
这种爆炸就是瓦斯爆炸,所以使用天然气之前,一定要检验气体的纯度。
考点三:新能源的开发和利用(高频考点)
1.化石燃料是人类生产、生活的主要能源。随着全球能源使用的增长,化石燃料等
6 / 20不可再生能源将日趋枯竭。世界各国人民的节能意识日趋增强,科学家也在开发
新能源,例如:___________________________等,这些能源也称为“绿色能源”
2.乙醇,俗名为酒精,化学式为_________。
(1)物理性质:无色透明、______溶于水、有特殊气味的液体,能与水以任意比互
溶,并能溶解多种有机物。
(2)化学性质:酒精易燃烧,其化学方程式为___________________________。
(3)制法:把小麦、玉米等含淀粉的粮食发酵,再经过蒸馏就得到酒精。
(4)用途:作有机溶剂、化工原料、消毒剂等。
方法总结:①工业酒精因含有甲醇(有毒),严禁兑酒饮用。②医用消毒酒精是体积
分数为70%~80%的乙醇水溶液。
3.氢气
(1)性质:无毒,极易燃烧,燃烧放出大量的热,其化学方程式为
___________________________。
(2)是_________的燃料。
(3)氢气作为燃料的三大优点:①__________________;②__________________;
③__________________。
(4)氢气的性质及制法
A.物理性质:在通常状况下,氢气是一种_________、_________、________溶于水
的气体。
B.氢气的实验室制取:a.反应原理:___________________________。
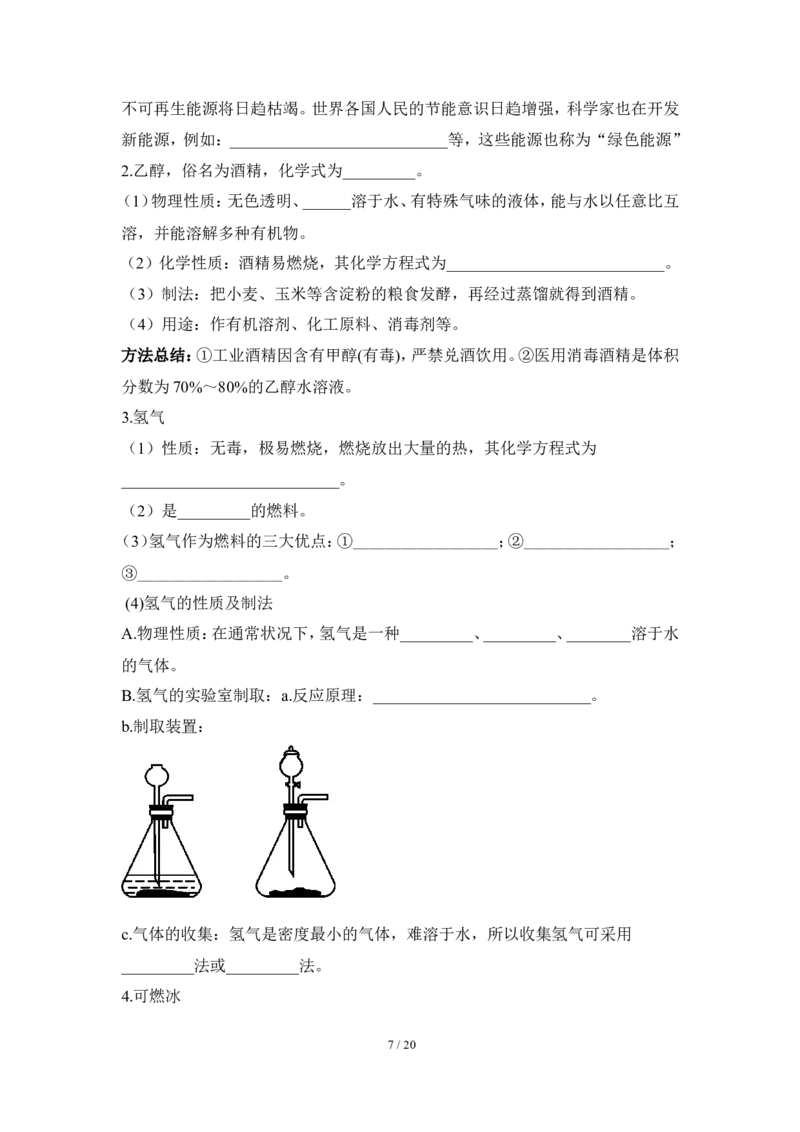
b.制取装置:
c.气体的收集:氢气是密度最小的气体,难溶于水,所以收集氢气可采用
_________法或_________法。
4.可燃冰
7 / 20可燃冰是透明无色、外形似冰的晶体,学名叫做“天然气水合物”,是天然气被
水分子包裹,在海底低温与高压作用下形成的。“可燃冰”作为燃料的优点突出
1 m3的“可燃冰”燃烧释放出的能量相当于164 m3的天然气燃烧放出的热量。
5.车用乙醇汽油是将变性燃料_________和_________以一定的比例混合而形成
的一种汽车燃料。使用车用乙醇汽油的好处:① __________________;②
__________________;③ __________________。
6.其他新能源 _________、_________、_________、_________、生物质能和核能
等。
方法总结:新能源就是除化石燃料之外的比较近期发现的能源,它们的使用过程
中一般对环境的影响比较小。
7.可再生能源与不可再生能源
定义 举例
可再生能源 不随其本身的转化或人类的利 太阳能、核能、水能、风能、氢
用而减少的能源 能等
不可再生能源 随本身的转化或人类的利用而 _________、_________、
减少的能源 _________
8.使用燃料对环境的影响
(1)煤燃烧产生的主要污染物
煤中主要含有_______元素,另外含有少量的硫元素和氮元素等,所以煤燃烧生
成_________、二氧化硫、二氧化氮以及烟尘等污染物,_________和_________溶
于雨水时可能会形成酸雨.
(2)汽车尾气造成的污染
A. 多数汽车使用的燃料是_________和_________。它们燃烧时产生的一些物质,
如一氧化碳、未燃烧的碳氢化合物、氮的氧化物、含铅化合物和烟尘等,会随尾气
直接排放到空气中,会对空气造成污染。
B.为了减少尾气对空气的污染,主要采取以下措施:
a.改进发动机的燃烧方式,使汽油能_________燃烧;
b.使用催化净化装置,使有害气体转化为无害物质;
c.使用无铅汽油,禁止含铅物质排放;
d.加大尾气的监测力度,禁止尾气超标的汽车上路。
e.使用清洁车用燃料,如压缩天然气(CNG)、液化石油气(LPG)、车用乙醇汽油等
8 / 209.酸雨
A.形成:煤燃烧时排放出_________、 _________等污染物。这些气体或气体在空
气中发生反应后的生成物溶于雨水,会形成酸雨。
B.危害:使土壤_________;破坏森林、植被及农作物;腐蚀_________、金属制品、
大理石雕像、名胜古迹等。
C.防治措施:防治措施:大力推广使用脱硫煤;天然气代替煤;开发_______等。
知识梳理参考答案
考场练兵
中考回顾
1.(2017呼和浩特中考)化学与我们的生活息息相关。以下说法正确的是( )
③天然气泄漏应立即打开排气扇换气 ④用聚氯乙烯塑料包装食品
⑤减少燃煤发电,增加太阳能发电,有利于治理雾霾
A.②⑤ B.②③⑤ C.④⑤ D.①③④
2.(2017广州中考)下列说法不正确的是( )
A.燃烧都放出热量
B.红磷常温下在空气中能自燃
C.炒菜油锅着火用锅盖盖灭
D.木材燃烧必须达到木材着火点
3.(2017四川内江中考,改编)据统计中国每年有上千家庭发生火灾,酿成悲剧。如
9 / 20果掌握一些灭火措施和安全知识,可以减少悲剧的发生。下列说法你认为正确的
是( )
A.电视机等电器着火用水扑灭
B.夜晚打开厨房中的电灯检查液化气罐是否漏气
C.煤矿矿井、大米加工厂、加油站等场所应禁止烟火
D.高楼住宅发生火灾,可使用楼内电梯逃生
4.(2017湖南邵阳中考)如图是某同学探究燃烧条件的改装装置,往烧杯中加入下
列物质,能引起白磷燃烧的是( )
A.硝酸铵 B.氢氧化钠 C.蔗糖 D.食盐
5.(2017成都中考)下列物质能发生燃烧的是( )
A.棉花 B.黄金 C.食盐 D.大理石
6.(2017山东德州中考)用白色瓷片接近酒精灯外焰时,瓷片没有明显变化;接近
焰心时,在瓷片上出现黑色粉末状固体,这是酒精没有完全燃烧时生成的炭黑。
用水壶烧水,开始时会发现:与火焰接触的壶底出现水珠和黑色的炭黑,下列说
法不正确的是( )
A.燃料中一定含有碳、氢、氧三种元素
B.燃料本身也可能含有水分子
C.加大空气的流量可以减少炭黑的生成
D.提高水壶的高度可以减少炭黑的生成
7.(2016天津中考)从环境保护的角度考虑,下列燃料中最理想的是( )
A.酒精 B.汽油 C.氢气 D.天然气
8.(2017湖南邵阳中考)2017年5月18日,中国又创下一项世界第一,在我国海域
试开采可燃冰获得成功。预计在2030年以前可燃冰资源会得到商业性开发利用,
将在一定程度上缓解化石能源面临被耗尽的危险。可燃冰中的主要可燃成分是甲
烷。
(1)目前使用的主要化石燃料有煤、 和天然气等。
(2)甲烷燃烧的化学方程式是 。
10 / 20(3)可燃冰属于未来的新能源,下列不属于新能源的是 (填序号)。
A.汽油 B.太阳能
C.氢能 D.核能
9.(2017天津中考)能源利用和环境保护是人类共同关注的问题。
(1)下列说法中正确的是 (填字母)。
A.煤、石油和天然气都属于可再生能源
B.从环境保护角度考虑,最理想的燃料是汽油
C.可燃冰将成为未来新能源,其中主要含有甲烷水合物
(2)煤燃烧时排放出的二氧化硫等污染物,有可能会导致降雨的酸性增强。我们把
pH 5.6(填“>”“=”或“<”)的降雨称为酸雨。某电厂为防止环境污染,用石灰石
浆来吸收二氧化硫,其反应的化学方程式为2CaCO +2SO +O =2CaSO +2X,则X
3 2 2 4
的化学式为 。
(3)研究发现,二氧化碳和氢气在催化剂作用下转化为甲醇(CH OH)和水。该反应
3
的化学方程式为 。
(4)将一定质量的甲醇与4.4 g氧气混合于密闭容器中,在一定条件下,发生如下
反应:8CH OH+xO mCO +nCO+16H O。当反应物完全耗尽且全部转化为
3 2 2 2
生成物时,有3.6 g水生成,同时生成二氧化碳的质量为 g。
模拟预测
1.为了提高燃料的燃烧利用率,可采用的方法是( )
A.添加足够多的燃料
B.只需使燃料与空气有足够大的接触面积
C.只需通入足够多的空气
D.既通入足够多的空气,又增大燃料与空气的接触面积
2.将燃着的镁条伸入盛有二氧化碳的集气瓶中,镁条继续燃烧,反应的化学方程
式为2Mg+CO 2MgO+C,下列有关叙述错误的是( )
2
A.该反应中Mg发生了氧化反应
B.镁条着火不能用CO 扑灭
2
C.该反应的实验现象是生成白色的氧化镁和黑色的碳
11 / 20D.燃烧并不一定需要氧气
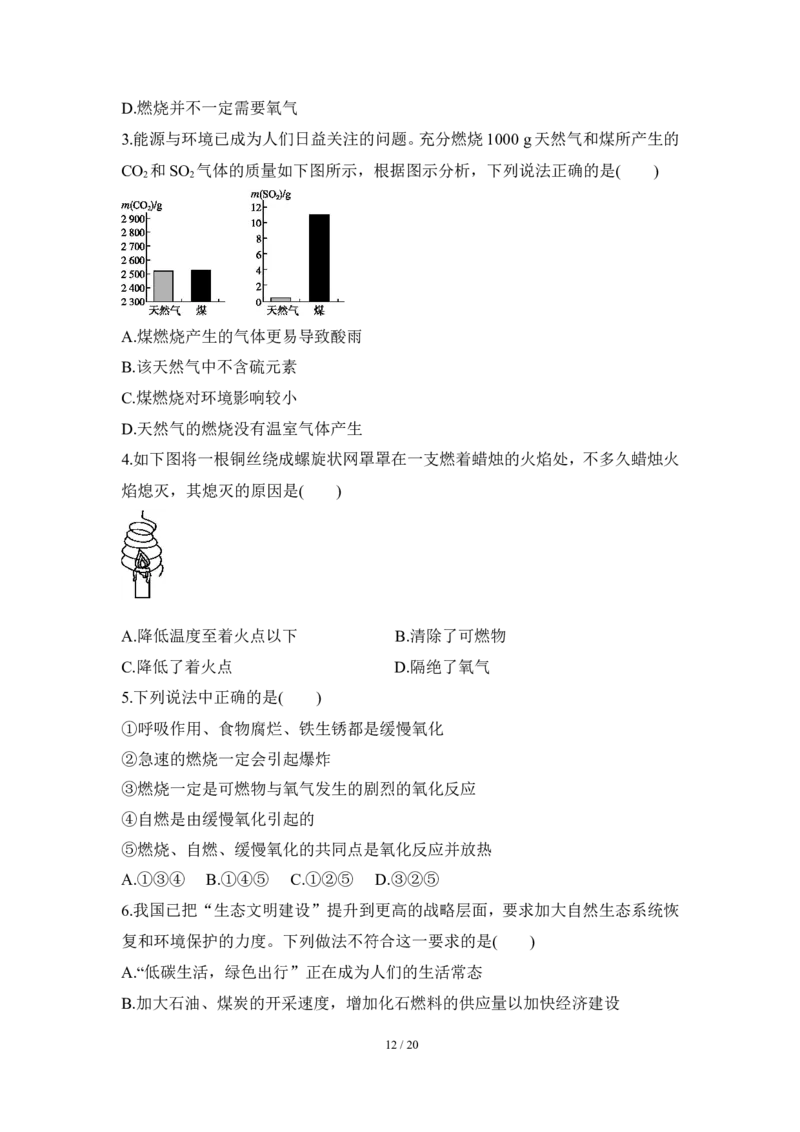
3.能源与环境已成为人们日益关注的问题。充分燃烧1000 g天然气和煤所产生的
CO 和SO 气体的质量如下图所示,根据图示分析,下列说法正确的是( )
2 2
A.煤燃烧产生的气体更易导致酸雨
B.该天然气中不含硫元素
C.煤燃烧对环境影响较小
D.天然气的燃烧没有温室气体产生
4.如下图将一根铜丝绕成螺旋状网罩罩在一支燃着蜡烛的火焰处,不多久蜡烛火
焰熄灭,其熄灭的原因是( )
A.降低温度至着火点以下 B.清除了可燃物
C.降低了着火点 D.隔绝了氧气
5.下列说法中正确的是( )
①呼吸作用、食物腐烂、铁生锈都是缓慢氧化
②急速的燃烧一定会引起爆炸
③燃烧一定是可燃物与氧气发生的剧烈的氧化反应
④自燃是由缓慢氧化引起的
⑤燃烧、自燃、缓慢氧化的共同点是氧化反应并放热
A.①③④ B.①④⑤ C.①②⑤ D.③②⑤
6.我国已把“生态文明建设”提升到更高的战略层面,要求加大自然生态系统恢
复和环境保护的力度。下列做法不符合这一要求的是( )
A.“低碳生活,绿色出行”正在成为人们的生活常态
B.加大石油、煤炭的开采速度,增加化石燃料的供应量以加快经济建设
12 / 20C.全面关停能耗大、污染严重的企业,以减少资源浪费,恢复自然生态
D.合理施用化肥和农药,减少对环境的影响,保障农产品产量及食品质量安全
7.下面与消防安全无关的公共标志是( )
8.能源和环境已经成为人们日益关注的问题。
(1)目前人们利用最多的能源是煤、 和天然气等化石燃料,煤燃烧会产生
大量的二氧化碳、二氧化硫和一氧化碳等气体,这些气体中,溶于水会导致酸雨
的主要是 。
(2)氢气作为一种清洁燃料没有大规模使用的原因是 (填字母)。
A.氢气的储存和运输 B.获得氢气的成本
C.制备氢气的原料 D.氢气燃烧的热值不高
9.能源紧缺、环境污染等是人类面临的重大问题。
(1)比较清洁的化石燃料的主要成分是 (填化学式)。
(2)燃煤会产生二氧化硫,大量二氧化硫释放到空气中,会导致雨水的 pH
(填“高于”或“低于”)正常值,形成酸雨。可以用碱液吸收二氧化硫,若用氢氧
化钠吸收二氧化硫会生成亚硫酸钠(Na SO ),请写出反应的化学方程式:
2 3
。
(3)在实验室里,可以用高锰酸钾溶液检验二氧化硫,反应的化学方程式为
2KMnO +2X+5SO =2MnSO +K SO +2H SO 。其中X的化学式为 。
4 2 4 2 4 2 4
(4)雾霾是一种灾害性天气,主要是由于人类生产生活向大气排放大量的细颗粒
物所致。请分析下列污染物中,会导致雾霾的是 (填序号)。
A.SO B.NO C.PM D.CO
2 2 2.5
10.H 、CO、CO 和CH 都是初中化学学习阶段常见的气体。
2 2 4
(1)可燃性气体与空气混合点燃可能会爆炸,所以可燃性气体点燃前应先
,CH 完全燃烧的化学方程式是 。
4
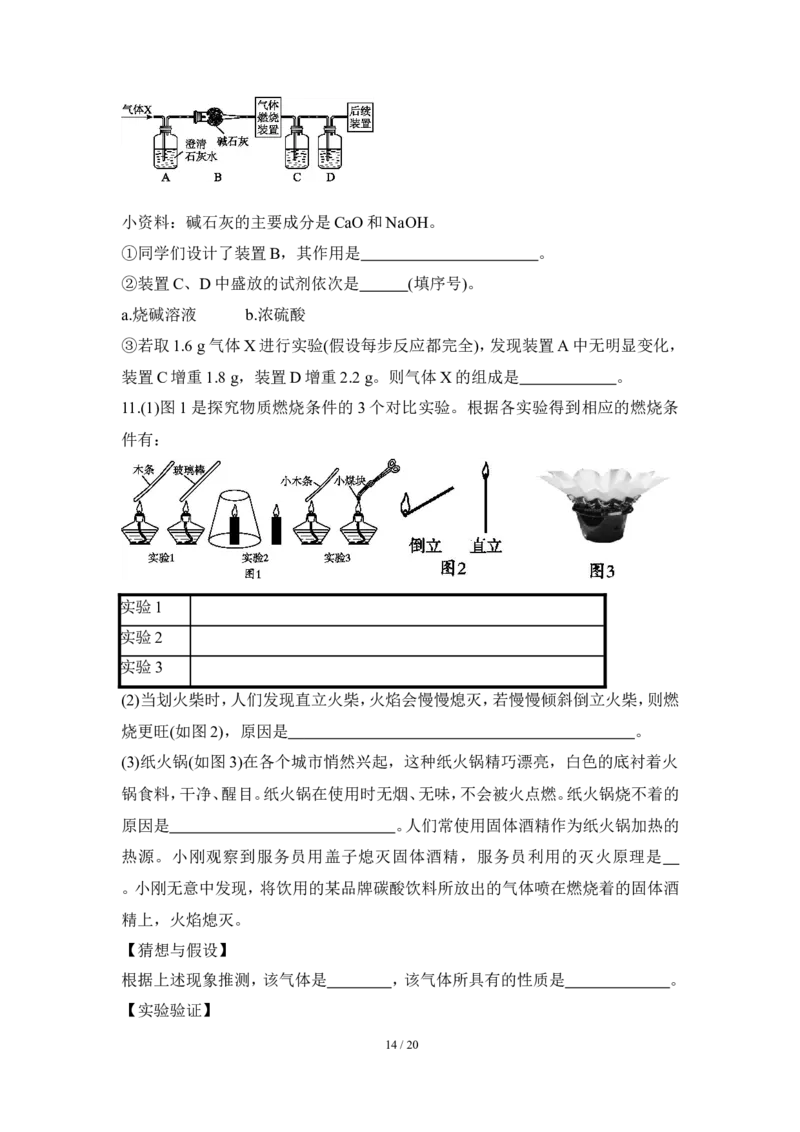
(2)某无色气体X可能含有上述4种气体中的一种或两种。为了确认气体X的组
成,同学们按如下图装置进行实验。
13 / 20小资料:碱石灰的主要成分是CaO和NaOH。
①同学们设计了装置B,其作用是 。
②装置C、D中盛放的试剂依次是 (填序号)。
a.烧碱溶液 b.浓硫酸
③若取1.6 g气体X进行实验(假设每步反应都完全),发现装置A中无明显变化,
装置C增重1.8 g,装置D增重2.2 g。则气体X的组成是 。
11.(1)图1是探究物质燃烧条件的3个对比实验。根据各实验得到相应的燃烧条
件有:
实验1
实验2
实验3
(2)当划火柴时,人们发现直立火柴,火焰会慢慢熄灭,若慢慢倾斜倒立火柴,则燃
烧更旺(如图2),原因是 。
(3)纸火锅(如图3)在各个城市悄然兴起,这种纸火锅精巧漂亮,白色的底衬着火
锅食料,干净、醒目。纸火锅在使用时无烟、无味,不会被火点燃。纸火锅烧不着的
原因是 。人们常使用固体酒精作为纸火锅加热的
热源。小刚观察到服务员用盖子熄灭固体酒精,服务员利用的灭火原理是
。小刚无意中发现,将饮用的某品牌碳酸饮料所放出的气体喷在燃烧着的固体酒
精上,火焰熄灭。
【猜想与假设】
根据上述现象推测,该气体是 ,该气体所具有的性质是 。
【实验验证】
14 / 20将该气体通入澄清石灰水,石灰水变浑浊,该反应的化学方程式是 。
15 / 20参考答案
知识梳理
考点一:燃烧的条件及灭火(高频考点)
1. 可燃物 氧气 最低温度 清除可燃物 氧气 降到着火点
2.(2)可燃物的着火点 与氧气接触
3. 着火点 切断电源 盖灭 灯帽 湿抹布 温度降低到着火点 着火点 氧气
4. 图书 档案 贵重金属
Na CO +2HCl=2NaCl+H O+CO ↑
2 3 2 2
2NaHCO Na CO +H O+CO ↑
3 2 3 2 2
5.炸药 轮胎 接触面积 氧气的浓度
6. 缓慢进行 氧化反应 放热 不同
7. (1)使有限的能源发挥最大的作用 降低环境污染的程度
(2)热量 CO
(3)空气 接触面
考点二:化学反应的能量变化与化石燃料(必考考点)
1. (1)放热 (2)吸热
2.(1)取暖
3.燃烧时要有足够的空气或氧气_ 燃料与空气(或氧气)要有足够大的接触面积
4. (1)煤 石油 天然气 不可再生 混合物
(2)C C、H 混合物 混合物
(4)①甲烷 有机物 CH
4
②无色 无味 小 难 排水法 蓝色 放出 澄清石灰水 CH +
4
2O =====CO +2H O
2 2 2
考点三:新能源的开发和利用(高频考点)
1.太阳能、风能、地热能、氢能
2. C H OH
2 5
(1)易
(2)C H OH+3O =====2CO +3H O
2 5 2 2 2
3.(1)2H +O =====2H O
2 2 2
16 / 20(2)最清洁
(3)来源广泛 放出的热量多 燃烧的产物无任何污染
(4)A.无色 无味 难 B. a. Zn+H SO ══ZnSO +H ↑ c.向下排空气 排水
2 4 4 2
5.乙醇 汽油 节省石油资源 减少汽车尾气的污染 促进农业生产
6.太阳能 风能 地热能 潮汐能
7. 煤 石油 天然气
8. (1)碳 一氧化碳 二氧化硫 二氧化氮
(2)A汽油 柴油 B. a. 充分
9.A.二氧化硫 二氧化氮
B. 酸化 建筑物
C.新能源
中考回顾
1.A 2.B 3.C 4.B 5.A 6.A 7.C
8.(1)石油 (2)CH +2O CO +2H O (3)A
4 2 2 2
9. (1)C (2)< CO (3)CO +3H CH OH+H O (4)3.3
2 2 2 3 2
模拟预测
1.解析:
提高燃料的燃烧利用率,既要增大燃料与氧气的接触面积,又要增大氧气的浓度
答案:D
2. 解析:
该反应中镁与氧结合生成了氧化镁,发生了氧化反应,故A正确;由于镁能在二
氧化碳中燃烧,所以,镁条着火不能用CO 扑灭,故B正确;该反应的实验现象是
2
生成白色的固体和黑色颗粒,不能将结论当成现象来叙述,故C错误;由于镁能
在二氧化碳中燃烧,说明了燃烧并不一定需要氧气,故D正确。
答案:C
3. 解析:
根据图示可知,天然气和煤燃烧后都会产生二氧化碳气体,等质量的天然气完全
燃烧产生的二氧化硫比等质量的煤完全燃烧产生的二氧化硫少很多,因此煤燃烧
17 / 20更容易导致酸雨,对环境影响比较大;二者燃烧都会产生导致温室效应的二氧化
碳气体;因为天然气燃烧后会产生二氧化硫,说明天然气中含有硫元素。
答案:A
4. 解析:
将一根铜丝绕成螺旋状网罩罩在一支燃着蜡烛的火焰处,铜丝会吸收热量,导致
温度降到蜡烛的着火点以下,从而使蜡烛熄灭,故选A。
答案:A
5. 解析:
急速的燃烧不一定发生爆炸,当燃烧发生在有限的空间内才会发生爆炸,故②错
误;燃烧不一定是可燃物与氧气发生的剧烈的氧化反应,例如氢气可以在氯气中
燃烧,故③错误。
答案:B
6. 解析:
石油、煤炭的含量是有限并且不可再生的,若加大它们的开采速度会导致资源的
匮乏,化石燃料的大量使用会导致环境污染,因此要合理开发,加大绿色能源的
开发利用,故B错误。
答案:B
7. 解析:
图A所示标志是禁止吸烟标志,与消防安全有关,错误;图B所示标志是当心火
灾——易燃物质标志,与消防安全有关,错误;图C所示标志是国家节水标志,与
消防安全无关,正确;图D所示标志是禁止烟火标志,与消防安全有关,错误。
答案:C
8. 解析:
(1)目前人们利用最多的能源是煤、石油和天然气等化石燃料;二氧化硫溶于水会
导致酸雨;
(2)由于氢气的储存和运输不方便,且获得氢气的成本高,因此氢气作为一种清洁
燃料没有大规模使用。
答案:(1)石油 二氧化硫 (2)AB
9. 解析:
(1)在化石燃料中天然气是比较清洁的能源,天然气的主要成分是甲烷,其化学式
18 / 20为CH ;
4
(2)酸雨的pH<5.6,即小于正常雨水的pH,氢氧化钠溶液吸收二氧化硫生成亚硫
酸钠(Na SO )和水,反应的方程式为SO +2NaOH=Na SO +H O;
2 3 2 2 3 2
(3)据反应的化学方程式:2KMnO +2X+5SO =2MnSO +K SO +2H SO 反应前含
4 2 4 2 4 2 4
有5个硫原子,2个钾原子,2个锰原子,10个氧原子,反应后已有2个钾原子,2
个锰原子,5个硫原子,12个氧原子,4个氢原子, 故2X中含有4个氢原子,2个
氧原子,故X为H O;
2
(4)雾霾是由可吸入颗粒物(PM )引起的,故C正确。
2.5
答案:(1)CH (2)低于 SO +2NaOH=Na SO +H O (3)H O (4)C
4 2 2 3 2 2
10. 解析:
(1)可燃性气体与氧气混合达到一定程度时遇明火会发生爆炸,所以可燃性气体
点燃前必须检验气体的纯度,否则可能发生爆炸,甲烷燃烧生成二氧化碳和水,
反应的化学方程式为CH +2O CO +2H O。
4 2 2 2
(2)①装置B中药品是碱石灰,碱石灰的主要成分是CaO和NaOH,可作干燥剂,
能吸收气体中的水分和二氧化碳,防止气体中水蒸气和二氧化碳干扰实验;
②装置C盛放的试剂应为浓硫酸,目的是通过装置 C是否增重测定H元素的有
无,装置D中盛放的试剂是烧碱溶液,目的是通过装置D是否增重测定C元素的
有无,如果先经过NaOH溶液时会带出水蒸气到浓硫酸中,影响水的测定结果,
因此要将气体燃烧后的产物依次通过浓硫酸和氢氧化钠溶液;
③装置A中无明显变化,说明气体中不含CO ;装置C增重1.8 g,说明气体燃烧
2
后生成1.8 g水,则含H元素的质量为1.8 g× ×100%=0.2 g;装置D增重2.2 g,
说明气体燃烧后生成2.2 g二氧化碳,同理可知含C元素0.6 g,故1.6 g气体X中
含H元素0.2 g、含C元素0.6 g,含O元素的质量=1.6 g-0.2 g-0.6 g=0.8 g,由于碳
元素与氧元素的质量比=0.6 g∶0.8 g=3∶4,因此1.6 g X气体中含有1.4 g CO,由
此可知气体X中没有CH ,剩下0.2 g气体为H 。
4 2
答案:(1)验纯 CH +2O CO +2H O
4 2 2 2
19 / 20(2)①除去CO 、H O ②b、a ③H 和CO
2 2 2
11. 解析:
(1)实验1:通过实验可知,木条能燃烧,玻璃棒不燃烧,因此可以得出燃烧时物质
必须具有可燃性;
实验2:扣在玻璃杯中的蜡烛燃烧一会儿后熄灭,而空气中的蜡烛不会熄灭,由此
可以得出可燃物要燃烧必须与氧气接触;
实验3:木条很快燃烧,小煤块需要加热一段时间后才能燃烧,因此可以得出可燃
物要燃烧温度必须达到着火点。
(2)当划火柴时,如果直立火柴,则火柴梗的温度达不到其着火点,容易熄灭;如果
火焰在火柴梗的下方,燃烧产生的热量充分的给火柴梗加热,很容易使温度达到
火柴梗的着火点,则燃烧更旺。
(3)由于火锅内的水蒸发吸收热量,因此纸火锅的温度达不到其着火点,故纸火锅
在使用时不会被火点燃;用盖子熄灭固体酒精,可使固体酒精与空气隔绝;由于
二氧化碳不能燃烧,也不支持燃烧,因此喷在燃烧着的固体酒精上,火焰会熄灭;
二氧化碳与澄清石灰水反应,生成碳酸钙(白色沉淀)和水,反应的化学方程式是
CO +Ca(OH) =CaCO ↓+H O。
2 2 3 2
答案:(1)实验1:物质具有可燃性
实验2:可燃物与氧气接触
实验3:温度达到可燃物的着火点
(2)如果直立火柴,则火柴梗的温度达不到其着火点,容易熄灭;如果火焰在火柴
梗的下方,燃烧产生的热量充分地给火柴梗加热,很容易使温度达到火柴梗的着
火点。
(3)温度未达到纸的着火点 使可燃物与空气隔绝二氧化碳 不能燃烧,也不支
持燃烧 CO +Ca(OH) =CaCO ↓+H O
2 2 3 2
20 / 20