文档内容
第三单元 物质构成的奥秘
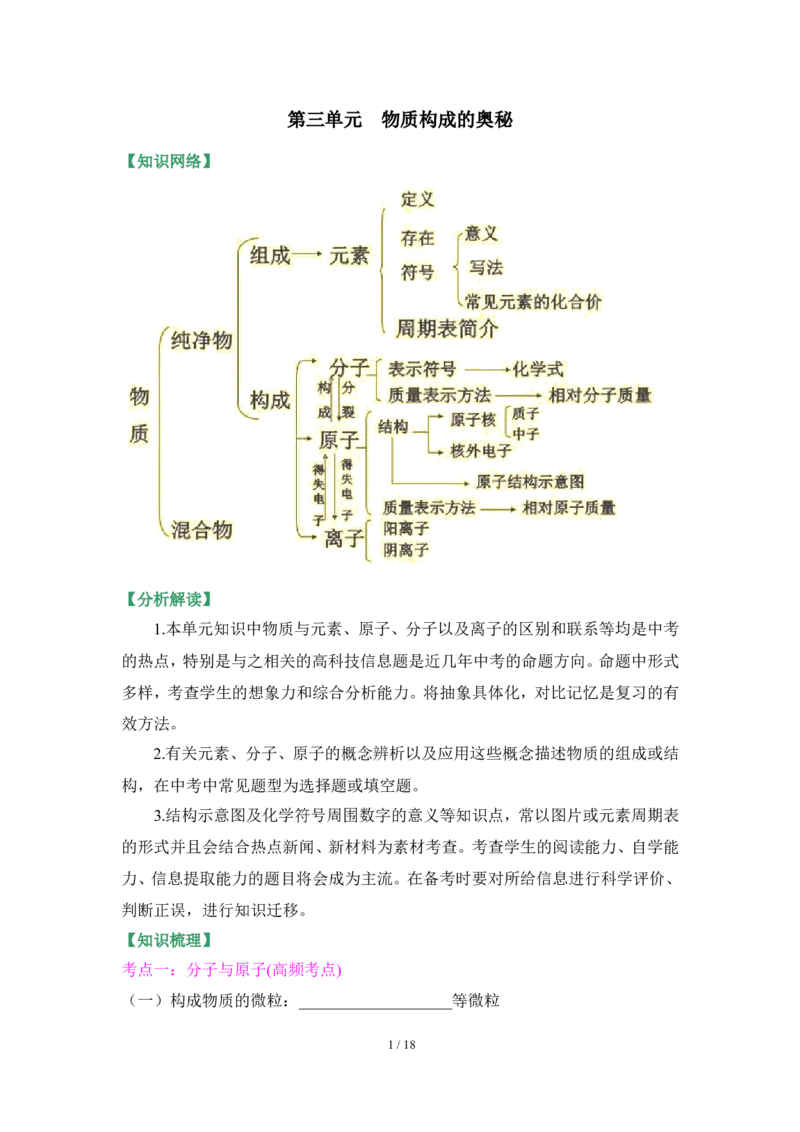
【知识网络】
【分析解读】
1.本单元知识中物质与元素、原子、分子以及离子的区别和联系等均是中考
的热点,特别是与之相关的高科技信息题是近几年中考的命题方向。命题中形式
多样,考查学生的想象力和综合分析能力。将抽象具体化,对比记忆是复习的有
效方法。
2.有关元素、分子、原子的概念辨析以及应用这些概念描述物质的组成或结
构,在中考中常见题型为选择题或填空题。
3.结构示意图及化学符号周围数字的意义等知识点,常以图片或元素周期表
的形式并且会结合热点新闻、新材料为素材考查。考查学生的阅读能力、自学能
力、信息提取能力的题目将会成为主流。在备考时要对所给信息进行科学评价、
判断正误,进行知识迁移。
【知识梳理】
考点一:分子与原子(高频考点)
(一)构成物质的微粒:___________________等微粒
1 / 181.由分子构成的物质:例如___________________等物质;
2.由原子构成的物质:___________________等物质;
3.由离子构成的物质:___________________等物质。
方法总结:物质构成的描述:物质由××分子(或原子)构成。例如:铁由铁原子构
成;氧气由氧分子构成。
(二)分子与原子的区别和联系
分子 原子
都是构成物质的一种粒子;_________、_________都非常小,彼此之间有间隔,
相同点 总是在不停地_________,同种分子(或原子)性质_________,不同种分子(或原
子)性质_________。
在_________中,分子可以再分 在化学反应中,原子不可以再分为,是
不同点
为_________ _________中最小的粒子。
分子由原子构成的,在_________中,分子可以再分为原子,原子可以_________
相互关系
为新分子
①物理变化只是构成物质的__________________发生了变化;
②化学变化是生成了__________________;
应用
③混合物是___________________________构成的;
④纯净物是__________________构成的
方法总结:①分子是保持物质化学性质的“最小粒子”,不是“唯一粒子”;
② “保持”的含义是指构成该物质的每一个分子与该物质的化学性质是一致的;
③分子只能保持物质的化学性质,而物质的物理性质需要大量的集合体一起来共
同体现,单个分子无法体现物质的物理性质。
④ “最小”不是绝对意义上的最小,而是“保持物质化学性质的最小”。
(三)用微粒的性质解释常见现象
分子的性质 解释 举例(以水为例)
分子的 常用来解释质量或体积很小的物质中所含1个水分子的质量约是3×10-26 kg,
_________和 分子的数目巨大或一个分子的质量或体积1滴水中大约有1.67×1021个水分
_________都 非常小等 子
很小
无规则 指速度大小、运动方向等物理量水分子都在_________,但分子运
不同且无规律 动的速率并不一样
分子在永不
停息地做无
运动 a.温度升高,分子运动的速率加 水蒸发成水蒸气,水分子运动速率
规则
快; _________;
________
b.温度降低,分子运动的速率减水冷凝成冰,水分子运动________
2 / 18慢,但不可能停止运动
a.物质膨胀,分子间的间隔增大; 水蒸发成水蒸气,水分子间的间隔
_________;
分子之间有 b.物质压缩或冷凝,分子间的间隔减小,
_________ 但不可能没有间隔 水冷凝成冰,水分子间的间隔
_________
a.分子相同的物质是同种物质,且化学性 水与冰的化学式都是H O,属于
2
质_________; _______物质,化学性质________;
分子的种类
决定其化学 b.分子不同的物质是不同物质,且性质 水与双氧水化学式分别为H O和
2
性质 _________ H O ,不是同种物质,_________不
2 2
同
方法总结:通过化学变化生成的物质是与反应物性质不同的新物质,分子不同,
化学性质不同;通过物理变化形成的物质是与反应物的大小、状态等不同的同种
物质,分子相同、化学性质相同。
(四)分子运动现象的实验
实验装置图:
实验现象:过一段时间,B烧杯中溶液_________,A烧杯中溶液_________;
原因分析:A中浓氨水有_________,氨气分子运动到B中与水反应生成氨水,氨
水显_________,能使酚酞溶液变红。
考点二:原子的构成(常见考点)
1.原子的构成
由于原子核内质子所带电荷和核外电子的电荷_________相等、且_________相反
因此,整个原子_________电性。
方法总结:①原子核位于原子中心,绝大多数由质子和中子构成(有一种氢原子
的原子核内只含1个质子,无中子),体积极小,密度极大,几乎集中了原子的全
部质量,核外电子的质量很小,可以忽略不计。②每个原子只有一个原子核,核电
3 / 18荷数(核内质子数)的多少,决定了原子的种类。 ③在原子中:核电荷数=质子
数=核外电子数。④原子核内的质子数不一定等于中子数,如钠原子中,质子数为
11,中子数为12。⑤并不是所有的原子中都有中子,如有一种氢原子中就没有中
子。
2. 相对原子质量
(1)定义:国际上以一种___________________________作为标准,其他原子的质
量跟它相比所得的数值,就是这种原子的相对原子质量。
(2)计算公式:某原子的相对原子质量=该原子的实际质量/ (碳—12原子质量的
1/12)
(3)相对原子质量=_________+_________
3.核外电子的排布
(1)核外电子排布的初步知识
①通常用_________表明运动着的电子离核远近的不同。
②元素原子核外电子最少的有1层,最多的有7层,最外层电子最多不超过
_________个(只有第1层的不超过_________个)。
(2)原子结构示意图
①原子结构示意图的含义
说明:圆圈表示原子核,里面的数字表示_________;弧线表示_________,上面的数字表
示每一个电子层上的_________
②原子结构与元素性质的关系
元素种类 最外层电子数 元素的性质 结论
金属元素 _________个 原子易_________电子
_________决定了
非金属元素 _________个 原子易_________电子
元素的化学性质
稀有气体元素 _________个(氦2个) 不易得、失电子,稳定
考点三:离子(高频考点)
1.概念:离子是带电的_________或_________,带正电的离子叫_________,带负
电的离子叫_________。
4 / 182. 表示方法:在元素符号右上角标明_________和_________,数字在_________,
符号在_________。若数字为1时,可省略不写。
3.分类及形成:阳离子(由于原子_________电子而形成)带_________电
阴离子(由于原子_________电子而形成)带_________电
方法总结:原子变为离子时,质子数、元素种类没有改变;电子数、最外层电子数
发生了改变。
4.离子符号表示的意义:表示一个某种离子;表示带n个单位某种电荷的离子。
5.离子中质子数与电子数的关系:
阳离子:质子数_________电子数 阴离子:质子数_________电子数
方法总结:①判断是否为稳定结构:最外层电子数为8(一个电子层时为2)个电
子的是相对稳定结构;②判断化学性质是否相似:最外层电子数(只有一个电子
层的除外)相同的粒子,化学性质相似。
考点四:元素及元素周期表(高频考点)
1.元素
定义 具有相同_________(_________)的一类原子的总称
在地壳中排前四位的元素_____、_____、_____、_____,其中含量最多的金属
分布
元素为_____。
决定元素种类:__________(__________)
三个
决定元素化学性质:_______________
决定
决定原子的质量:__________
分类 金属元素、非金属元素和稀有气体元素
方法总结:物质、元素、微粒之间的关系
5 / 182.元素和原子的区别与联系
项目 元 素 原 子
定义 具有相同核电荷数的一类原子的总称 化学变化中的最小粒子
①宏观概念,只表示种类不表示个数 ①微观概念,既表示种类又表示个数
②表示物质的________组成 ②表示物质的________构成
区别
③可以组成单质或化合物 ③可以构成分子,也可以直接构成物质。
④根据质子数和中子数分类 ④根据质子数(核电荷数)分类
①元素是具有相同核电荷数(即质子数)的一类原子的总称
②原子核内的________决定元素的种类,即同种元素的原子核电荷数(即质子数)
联系
一定相同
③若原子的最外层电子数相同,则它们的化学性质________ (H、He除外)
方法总结:①元素属于宏观概念,只讲种类,不讲个数。 ②同种元素的原子,核电
核数一定相同;而核电核数相同的粒子不一定属于同种元素,如Na+和NH +; ③
4
同种元素的离子因所带的电荷数不同,性质也不同,如Fe2+、Fe3+。 ④同种原子和
其所形成的离子一定是同种元素,如Na和Na+。
3.元素符号
(1)元素符号书写原则:国际上统一采用元素的________名称的第一个大写字母
来表示元素,若第一个字母相同,就再加一个小写字母来区别。
(2)元素符号表示的意义:
宏观:表示一种________,如O表示氧元素。
微观:表示该元素的一个________,如O表示一个氧原子。
方法总结:①由原子直接构成的物质(金属、某些固态非金属和稀有气体),它们的
元素符号还可以表示该物质。如Fe表示:铁元素,一个铁原子,铁(这种单质)。②
元素符号前面的数字不是1时,只表示原子的个数。如:2H只表示2个氢原子。
4.元素周期表
①定义:根据元素的原子结构和性质,将已知的100多种元素按原子序数科学有
序地排列起来所得的表叫元素周期表。为了便于查找,元素周期表按元素原子核
电荷数递增的顺序给元素编了号,叫原子序数。
原子序数=________数=________数=________数
周期数=________数
②分区:在周期表中对金属、非金属元素用不同的颜色做了分区,并标出了元素
6 / 18的相对原子质量。
③元素周期表的结构
A.每一格
B.每一横行(周期):周期表每一________行叫一个周期,共有_____个横行,有
_____个周期。
C.每一纵行(族):周期表中共有18个_____行,每一纵行叫做一个族(8、9、10三
个纵行共同组成一个族),共有_____个族。
练兵训练
中考回顾
1.(2017山东枣庄中考)下列关于“酒精温度计遇热读数上升”的微观解释正确的
是( )
A.分子质量增大 B.分子体积扩大 C.分子间距变大 D.分子个数增多
2.(2017广州中考)下图是元素X的一种粒子结构示意图,下列说法正确的是(
)
A.X是非金属元素 B.X的最外层电子数为8
C.该粒子最外层电子层已达到相对稳定结构 D.该粒子可表示为X-
3.(2017山东青岛中考)下列关于宏观事实的微观解释中,错误的是( )
A.自然界中水的天然循环——水分子不断运动
7 / 18B.天然气经压缩储存在钢瓶中——压强增大,分子之间的间隔变大
C.电解水生成氢气和氧气——在化学反应中分子发生改变
D.通过气味辨别酒精和水——分子不断运动,不同分子的性质不同
4.(2017湖南邵阳中考)下图中“ ”和“ ”分别表示氢原子和氮原子,能保持氨
气化学性质的微粒是( )
5.(2017江苏连云港中考)下图是元素周期表的一部分。下列说法正确的是( )
5 B 6 C
硼 碳
10.81 12.01
13 Al
铝
26.98
A.硼为金属元素
B.碳的原子序数是12.01
C.铝是地壳中含量最高的元素
D.三种原子中质量最大的是铝
6.(2017四川内江中考)下列有关说法错误的是( )
A.水的三态变化说明分子间具有间隙
B.原子不显电性是因为原子中质子数与中子数相等
C.五个二氧化硫分子可表示为5SO
2
D.Al3+可表示一个铝离子带三个单位的正电荷
7.(2017山东潍坊中考)下列说法正确的是( )
A.同种元素可能组成性质不同的几种单质
B.物质都是由分子或原子构成的
C.核电荷数:S2->S
D.在原子中质子数一定等于中子数
8.(2017成都中考)下图是X、Y两种微粒的结构示意图。下列说法正确的是( )
8 / 18A.X为原子,Y为离子
B.X、Y均属于非金属元素
C.X在反应中可失去6个电子
D.X与Y形成化合物的化学式为YX
9.(2017重庆中考B卷)下图是某品牌矿泉水的标签,回答下列问题。
(1)钙、镁和钾等指的是 (填序号)。
A.分子 B.原子 C.元素
(2)已知镁原子的结构示意图为 ,则Mg2+的质子数为 。
(3)已知偏硅酸的化学式为H SiO ,则偏硅酸钙的化学式为 。
2 3
10.(2017天津中考)根据下列粒子结构示意图,回答问题。
(1)A、B、C、D所示粒子共表示 种元素(填数字)。
(2)D所示粒子在化学反应中容易 电子(填“得到”或“失去”)。
(3)若E中x=10时,则该粒子属于 (填“原子”或“离子”)。
模拟预测
1.“见著知微”是化学学科的重要特点之一。它是指通过对实验现象的观察、思考
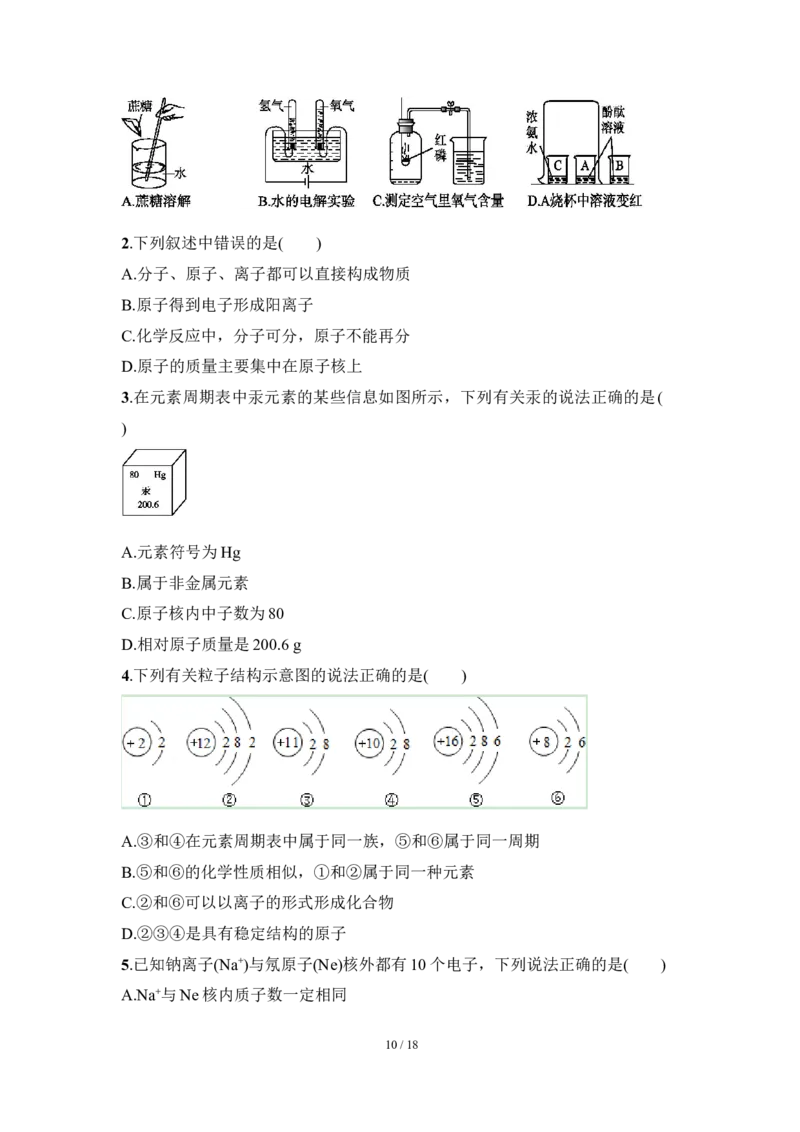
和推论,建立起对微小的原子、分子的认识。下列不符合这一特点的是( )
9 / 182.下列叙述中错误的是( )
A.分子、原子、离子都可以直接构成物质
B.原子得到电子形成阳离子
C.化学反应中,分子可分,原子不能再分
D.原子的质量主要集中在原子核上
3.在元素周期表中汞元素的某些信息如图所示,下列有关汞的说法正确的是(
)
A.元素符号为Hg
B.属于非金属元素
C.原子核内中子数为80
D.相对原子质量是200.6 g
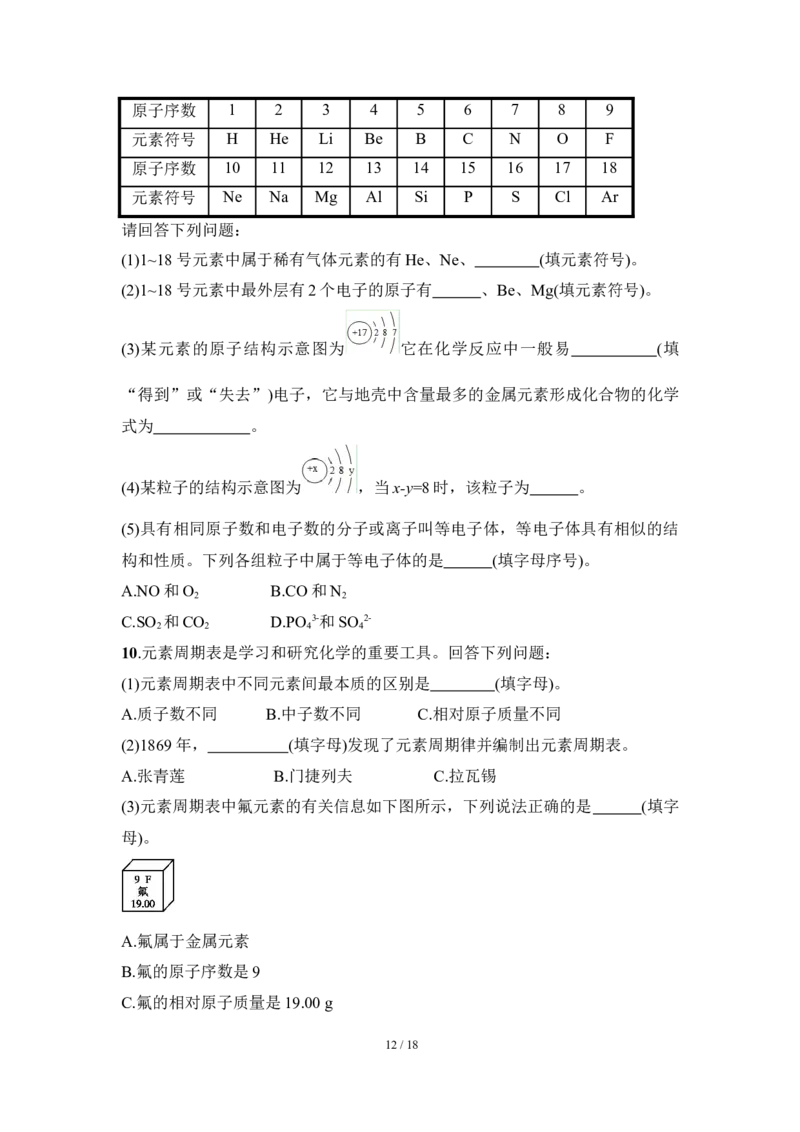
4.下列有关粒子结构示意图的说法正确的是( )
A.③和④在元素周期表中属于同一族,⑤和⑥属于同一周期
B.⑤和⑥的化学性质相似,①和②属于同一种元素
C.②和⑥可以以离子的形式形成化合物
D.②③④是具有稳定结构的原子
5.已知钠离子(Na+)与氖原子(Ne)核外都有10个电子,下列说法正确的是( )
A.Na+与Ne核内质子数一定相同
10 / 18B.Na+与Ne核内中子数一定相同
C.Na+与Ne一定属于同种元素
D.Na+与Ne核电荷数一定不同
6.下列有关符号中的数字“2”的意义,叙述正确的是( )
A.O 中的“2”表示2个氧原子
2
B.2Fe中的“2”表示2个铁原子
C.3H O中的“2”表示一个氢分子中含有2个氢原子
2
D.2N中的“2”表示2个氮分子
7.化学用语是学习化学的主要工具,是国际通用的化学语言。
(1)请你用化学用语填空。
①氩气 。
②某气体在空气中占 78%(体积百分含量),保持它的化学性质的最小粒子是
。
③地壳中含量最多的金属元素形成的离子 。
④标出氧化铁中铁元素的化合价 。
(2)请你试着写出两种带有数字“2”的粒子符号并指出其含义:
① ; ;
② ; 。
8.下图中A、B、C、D是四种粒子的结构示意图,E是银元素在元素周期表中的信
息。
请回答下列问题:
(1)图中A、B、C、D粒子共表示 种元素。
(2)D中x= 。
(3)E中银元素原子的质子数为 ,一个银原子质量是一个碳12原子质量
的 倍。
9.下表列出了1~18号元素的原子序数和元素符号:
11 / 18原子序数 1 2 3 4 5 6 7 8 9
元素符号 H He Li Be B C N O F
原子序数 10 11 12 13 14 15 16 17 18
元素符号 Ne Na Mg Al Si P S Cl Ar
请回答下列问题:
(1)1~18号元素中属于稀有气体元素的有He、Ne、 (填元素符号)。
(2)1~18号元素中最外层有2个电子的原子有 、Be、Mg(填元素符号)。
(3)某元素的原子结构示意图为 它在化学反应中一般易 (填
“得到”或“失去”)电子,它与地壳中含量最多的金属元素形成化合物的化学
式为 。
(4)某粒子的结构示意图为 ,当x-y=8时,该粒子为 。
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结
构和性质。下列各组粒子中属于等电子体的是 (填字母序号)。
A.NO和O B.CO和N
2 2
C.SO 和CO D.PO 3-和SO 2-
2 2 4 4
10.元素周期表是学习和研究化学的重要工具。回答下列问题:
(1)元素周期表中不同元素间最本质的区别是 (填字母)。
A.质子数不同 B.中子数不同 C.相对原子质量不同
(2)1869年, (填字母)发现了元素周期律并编制出元素周期表。
A.张青莲 B.门捷列夫 C.拉瓦锡
(3)元素周期表中氟元素的有关信息如下图所示,下列说法正确的是 (填字
母)。
A.氟属于金属元素
B.氟的原子序数是9
C.氟的相对原子质量是19.00 g
12 / 18(4)氟原子结构示意图为 ,氟原子在化学反应中易 (填“得到”或
“失去”)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为
。
13 / 18参考答案
知识梳理
考点一: 分子与原子(高频考点)
(一)
1.水、二氧化碳、氢气、氧气
2.金属、稀有气体、金刚石、石墨
3.氯化钠、氢氧化钠、高锰酸钾
(二)质量 体积 运动 相同 不同 化学反应 原子 化学变化
化学变化 重新组合 分子(或原子)间隔 新的分子(或原子)
不同分子(或不同原子或不同分子与原子) 同种分子(或原子)
(三)质量 体积 运动 运动 加快 减慢 间隔 增大 减少 相同 不相
同 相同
(四)变红 不变色 挥发性 碱性
考点二:原子的构成(常见考点)
1. 电量 电性 不显
2. (1)碳原子(碳—12)质量的1/12
(3)质子数 中子数
3. (1)①电子层 ②8 2
(2)①核电荷数 电子层 电子数
②<4 失 ≥4 得 8 最外层电子数
考点三:离子(高频考点)
1.原子 原子团 阳离子 阴离子。
2.电性 电荷数 前 后
3.失去 正 得到 负
4.
5.> <
14 / 18考点四:元素及元素周期表(高频考点)
1. 核电荷数 质子数 氧 硅 铝 铁 铝 质子数 核电荷数 最外层电子
数 原子核
2.宏观 微观 质子数 相似
3.元素符号
(1)拉丁文
(2)元素 原子
4.元素周期表
①质子 核电荷 核外电子 电子层
③B横 7 7 C.纵 16
中考回顾
1.C 2.C 3.B 4.A 5.D 6.B 7.A 8.D
9. (1)C (2)12 (3)CaSiO
3
10. (1)3 (2)得到 (3)原子
模拟预测
1. 解析:
蔗糖溶解说明分子是不断运动的,故A正确;水的电解实验说明分子在化学变化
中可以再分,而原子不能再分,故B正确;浓氨水能使烧杯内的酚酞溶液变红,说
明分子是不断运动的,故D正确。
答案:C
2. 解析:
原子得到电子形成阴离子,B项错误。
答案:B
3. 解析:
在周期表中的每个单元格中左上角表示的是质子数,右上角表示的是元素符号,
中间是元素名称,下面表示的是相对原子质量;汞是唯一不带“钅”字旁的金属
元素。
答案:A
4. 解析:
15 / 18③的原子最外层电子数为1,④的原子最外层电子数为8,因此它们在元素周期表
中不属于同一族,⑤和⑥的电子层数不同,因此不属于同一周期,A项错误;核内
质子数决定元素的种类,①和②核内质子数不同,因此它们不属于同一种元素,B
项错误;③中核内质子数多于核外电子数,是阳离子不是原子,D项错误。
答案:C
5. 解析:
Na+带一个单位的正电荷,核外有10个电子,说明钠原子的核外有11个电子;又
知,在原子中,核电荷数=质子数=核外电子数,则钠原子的核内质子数与核电荷
数均为11,则Na+的核内质子数与核电荷数也均为11。而氖原子为原子,其核电
荷数等于核内质子数等于核外电子数,均为10。故A、C选项错,D选项对。由于
核外电子数与核内中子数没有必然相等的联系,故B选项错。
答案:D
6. 解析:
A选项中的“2”,在化学式中元素符号的右下角,表示一个O 分子中含有两个氧
2
原子,故选项A错;B选项中的“2”在元素符号的前面,表示原子的个数,故选项
B正确;C选项中的“2”表示一个水分子中含两个氢原子,故选项C错;D中的
“2”在元素符号的前面,应表示原子的个数,而不是分子的个数,故选项D错。
答案:B
7. 解析:
(1)空气中占78%的气体为氮气,保持其化学性质的最小粒子为氮气分子(N );地
2
壳中含量最多的金属是Al,它易失去电子形成Al3+;在三氧化二铁中设铁的化合
价为x,则有2x+(-2)×3=0,x=+3。
答案:(1)①Ar ②N ③Al3+ ④ O
2 3
(2) 2NH 2个氨气分子
3
H O 1个水分子中含有2个氢原子(凡合理答案均可)
2
8. 解析:
(1)具有相同核内质子数的原子属于同种元素,图中A、B、C、D分别表示核内质
子数为13、17、18的三种元素。
(2)D是18号元素氩,核内质子数等于核外电子数,故x=8。
16 / 18(3)从图中看出,银的核内质子数为47,相对原子质量为108,根据相对原子质量
的含义,一个银原子的质量是一个碳12原子质量的 =9倍。
答案:(1)3 (2)8 (3)47 9
9. 解析:
(3)17 号元素为 Cl,地壳中含量最多的金属元素是 Al,二者形成的化合物为
AlCl 。
3
(4)从结构示意图可知,电子数=10+y;从“x-y=8”可知,质子数x=8+y,质子数≠
电子数,因此该粒子为离子。离子最外层一般为8电子的稳定结构,所以y=8,
x=16。
(5)判断等电子体,注意把握题目的信息“具有相同原子数和电子数的分子或离
子叫等电子体”。以上各选项中的两种分子或离子所含的原子数都相同,所含电
子数是分子中原子所含电子数的和,离子所带电子数还要考虑所带电荷数,即得
失电子数。A中NO分子含7+8=15个电子,而O 分子中含电子数为8×2=16个;B
2
中,CO分子含电子数为6+8=14,N 分子含电子数为7×2=14;C中,SO 分子所含
2 2
电子数为16+8×2=32,CO 分子所含电子数为12+8×2=28;D中, PO 3-所含电子
2 4
数为15+8×4+3=50, SO 2-所含电子数为16+8×4+2=50。故只有B、D正确。
4
答案:(1)Ar (2)He (3)得到 AlCl (4)S2- (5)BD
3
10. 解析:
(1)元素的种类是由质子数决定的,因此不同元素间最本质的区别是质子数不同;
(2)1869年,门捷列夫发现了元素周期律并编制出元素周期表;
(3)氟字中含有“气”字头,因此它属于非金属元素,故A错误;由元素周期表中
氟元素的有关信息可知,氟的原子序数是9,故B正确;相对原子质量的单位是
“1”,常省略不写,故C错误;
(4)氟原子最外层电子数为7,大于4,故在化学反应中易得到1个电子,显-1价,
钠元素为+1价,根据化合物中各元素的化合价的代数和为零可知,钠元素和氟元
素组成的化合物氟化钠的化学式为NaF。
答案:(1)A (2)B (3)B (4)得到 NaF
17 / 1818 / 18