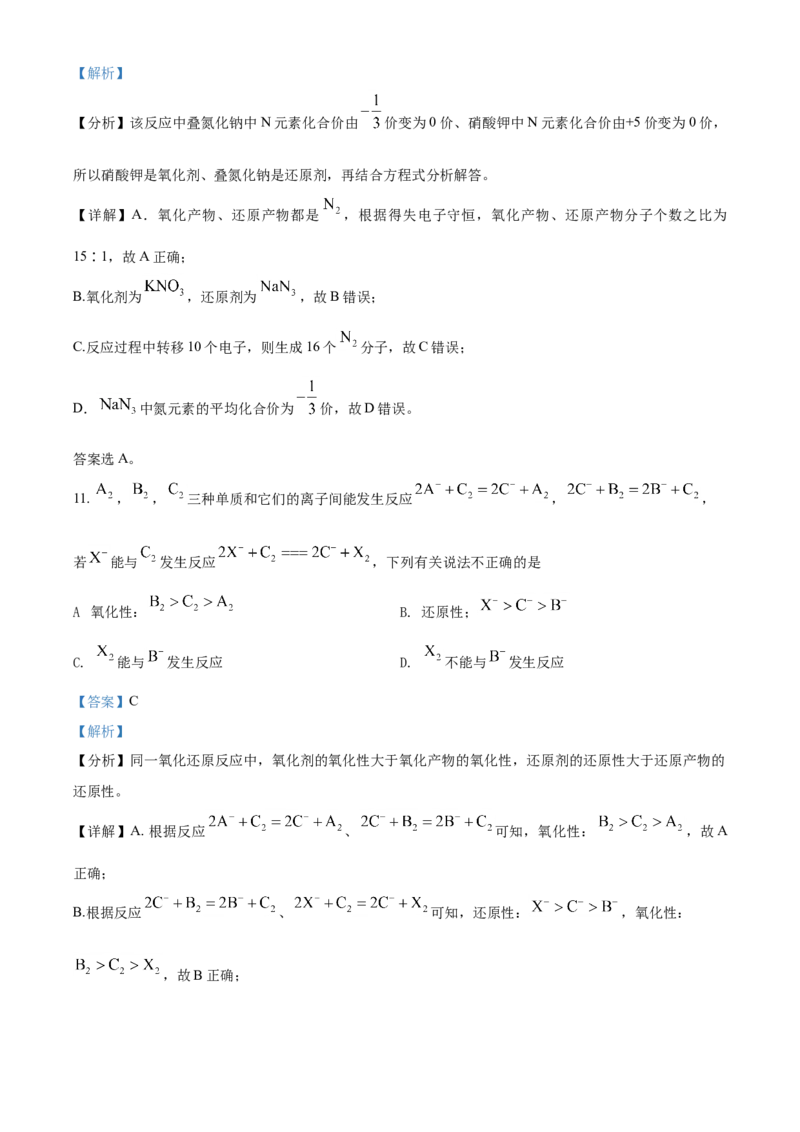文档内容
高一第三次月考化学试卷
考试范围:必修一前两章+第三章第一节;考试时间:90分钟
可能用到的原子量有:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Fe 56
第I卷(选择题,共54分)
一、单选题(本大题有18个小题,每小题3分,共54分)
1. 能够用来鉴别BaCl 、NaCl、NaCO 三种物质的试剂是 ( )
2 2 3
A. AgNO B. HSO C. HCl D. HNO
3 2 4 3
【答案】B
【解析】
【详解】A.硝酸银与三种物质均生成白色沉淀,无法鉴别,故A不符合题意;
B.硫酸与氯化钡反应生成白色沉淀,与碳酸钠反应生成气体,与氯化钠不反应无明显现象,三者现象不
同,故可以鉴别,故B符合题意;
C.HCl与氯化钡和氯化钠均不反应,无法鉴别,故C不符合题意;
D.硝酸与氯化钡和氯化钠均不反应,无法鉴别,故D不符合题意;
综上所述答案为B。
2. 下列关于0.5molNa SO 的说法正确的是( )
2 4
A. 含有3.01×1023个SO B. 含有0.5个NaSO
2 4
C. 含有0.5molNa+ D. 含有1mol氧原子
【答案】A
【解析】
【详解】A.0.5mol Na SO 含有0.5mol ,即 个 ,故A正确;
2 4
B.0.5mol Na SO 含有0.5mol ,1mol Na+,而不是0.5个NaSO ,故B错误;
2 4 2 4
C.含有Na+物质的量为0.5mol×2=1mol,故C错误;
D.0.5mol Na SO 含有氧原子物质的的量为0.5mol×4=2mol,故D错误。
2 4
综上所述,答案为A。
3. 下列关于氯水的说法正确的( )
A. 新制氯水呈浅黄绿色,是因为氯水中含有HClO
B. 新制氯水在光照的条件下,可以产生气体,该气体是氯气
C. 新制氯水中滴加硝酸银溶液,没有任何现象
D. 新制氯水中滴加石蕊试液,变红后褪色【答案】D
【解析】
【详解】A选项,新制氯水呈浅黄绿色,是因为氯水中含有氯气分子而显浅黄绿色,故A错误;
B选项,新制氯水在光照的条件下,可以产生气体,该气体是氧气,故B错误;
C选项,新制氯水中滴加硝酸银溶液,生成氯化银沉淀,故C错误;
D选项,新制氯水中滴加石蕊试液,氢离子使石蕊先变红,次氯酸使红色又褪色,故D正确;
综上所述,答案为D。
4. 已知12.3 g A与4.6 g B恰好完全反应生成了3.2 g C、4.5 g D和0.2 mol E,则E的摩尔质量是( )
A. 46 B. 46 g·mol-1
C. 64 g·mol-1 D. 64
【答案】B
【解析】
【详解】由于A与B恰好完全反应生成了C、D和E,则根据质量守恒定律可知 m(E)=(12.3 g+4.6 g)-(3.2
g+4.5 g)=9.2 g,则E的摩尔质量M(E)= =46 g·mol-1。故选B。
5. 下列溶液中Cl-浓度最大的是( )
A. 100mL3mol/LMgCl 溶液
2
B. 1000mL4mol/LNaCl溶液
C. 300mL7mol/LNaClO溶液
D. 250mL1.5mol/LAlCl 溶液
3
【答案】A
【解析】
【详解】A. 100mL3mol/LMgCl 溶液中Cl-浓度3mol/L 2=6mol/L;
2
B. 1000mL4mol/LNaCl溶液中Cl-浓度是4mol/L; ×
C. 300mL7mol/LNaClO溶液中没有氯离子,氯离子的浓度是0;
D. 250mL1.5mol/LAlCl 溶液中Cl-浓度是1.5mol/L 3=4.5mol/L;
3
则氯离子浓度最大 的是6mol/L, ×
故选:A。
6. 同温同压下,相同质量的SO 气体和CO 气体,下列叙述中正确的是
2 2
①分子数之比为11∶16 ②体积之比为16∶11
③密度之比为16∶11 ④原子个数之比为1∶1
A. ①③ B. ②④ C. ②③ D. ①④【答案】A
【解析】
【详解】相等质量的SO 气体和CO 气体,假设质量都为1g,其物质的量分别为 mol和 mol,物质
2 2
的量之比等于11:16;
①同温同压下,分子数之比为等于物质的量之比 : =11:16;故①符合题意;
②同温同压下,气体的体积比等于物质的量之比为11:16;故②不符合题意;
③同温同压下,气体的密度比等于摩尔质量之比:64:44=16:11;故③符合题意;
④一个SO 和一个CO 都含有3个原子,原子个数之比等于物质的量之比11:16;故④不符合题意;①③
2 2
正确;
答案选A。
7. 在标准状况下,将V L A气体(摩尔质量为M g·mol-1)溶于0.1L水中,所得溶液的密度为dg·cm-3,则溶
液的物质的量浓度为
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
【答案】B
【解析】
【详解】标准状况下,V L 气体的物质的量为 mol,则质量为 g,0.1L水的质量为100g,所以
溶液的质量为( +100)g,则溶液的体积为 mL= L,所以溶液的物质的量浓度为
= mol/L,故答案为B。
8. 如图是一种试验某气体化学性质的实验装置,图中B为弹簧夹。在A处通入干燥的氯气,当打开弹簧夹B时,C中红色布条颜色无变化;当关闭弹簧夹B时,C中红色布条颜色褪去。则D瓶所盛的溶液是
A. 浓硫酸 B. 饱和NaCl溶液 C. 水 D. NaOH溶液
【答案】B
【解析】
【详解】干燥的氯气不具有漂白性,湿润的氯气具有漂白性,在A处通入干燥的氯气,当打开弹簧夹B时,
C中红色布条颜色无变化,说明此时氯气未润湿,当关闭弹簧夹 B时,C中红色布条颜色褪去,说明装置
D中的液体可以湿润氯气,浓硫酸为干燥剂,氯气溶于水和NaOH溶液,难溶于饱和氯化钠溶液,所以装
置D中应为饱和氯化钠溶液,故答案为B。
9. 下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),化学反应的本质并不改变的
是
A. Na和O B. NaOH和CO C. NaO 和CO D. 木炭(C)和O
2 2 2 2 2 2
【答案】C
【解析】
【分析】
【详解】A.Na与O 常温下反应生成NaO,Na与O 加热时反应生成NaO,不符合题意;
2 2 2 2 2
B.CO 过量时与NaOH反应生成碳酸氢钠,CO 少量时与NaOH反应生成碳酸钠和水,不符合题意;
2 2
C.过氧化钠和二氧化碳反应只能生成碳酸钠和氧气,符合题意;
D.氧气过量时与木炭反应生成CO,氧气不足时与木炭反应生成CO,不符合题意;
2
答案选C。
10. 汽车剧烈碰撞时,安全气囊中发生反应 。对于该反应,下
列判断正确的是
A. 氧化产物与还原产物分子个数之比为15∶1
B. 氧化剂和还原剂是同一物质
.
C 反应过程中转移10个电子,则产生10个 分子
D. 中氮元素的化合价为 价
【答案】A【解析】
【分析】该反应中叠氮化钠中N元素化合价由 价变为0价、硝酸钾中N元素化合价由+5价变为0价,
所以硝酸钾是氧化剂、叠氮化钠是还原剂,再结合方程式分析解答。
【详解】A.氧化产物、还原产物都是 ,根据得失电子守恒,氧化产物、还原产物分子个数之比为
15∶1,故A正确;
B.氧化剂为 ,还原剂为 ,故B错误;
C.反应过程中转移10个电子,则生成16个 分子,故C错误;
D. 中氮元素的平均化合价为 价,故D错误。
答案选A。
11. , , 三种单质和它们的离子间能发生反应 , ,
若 能与 发生反应 ,下列有关说法不正确的是
.
A 氧化性: B. 还原性;
C. 能与 发生反应 D. 不能与 发生反应
【答案】C
【解析】
【分析】同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的
还原性。
【详解】A. 根据反应 、 可知,氧化性: ,故A
正确;
B.根据反应 、 可知,还原性: ,氧化性:
,故B正确;C. 由氧化性 可知,故 不能与 发生反应,故C错误;
D. 由氧化性 可知,故 不能与 发生反应,故D正确。
答案选C。
12. 在无色透明溶液中,能大量共存的离子组是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】B
【解析】
【详解】A. 题给附加条件是无色溶液,含 的溶液一般呈蓝色,A项不符合题意;
B. 、 、 、 离子间不反应,能大量共存,B项符合题意;
C. 是弱酸的酸式酸根离子,既能与酸反应也能与碱反应,故 和 不能大量共存,C项不
符合题意;
D. 与 能发生反应生成 沉淀,不能大量共存,D项不符合题意。
答案选B。
13. 下列化学反应中,不属于四种基本反应类型但属于氧化还原反应的是
A.
B.
C.
D.
【答案】C
【解析】
【详解】A.A为无单质参与的分解反应,不属于氧化还原反应,A不满足题意;
B.B为复分解反应,复分解反应不属于氧化还原反应,B不满足题意;
C.C不属于四大反应类型,但Cu元素、Fe元素化合价发生变化,属于氧化还原反应,C满足题意;D.D为有单质参加的化合反应,属于氧化还原反应,D不满足题意。
答案选C。
14. 下列各组中的两个反应,可用同一离子方程式表示的是
A. 和 , 和
B. 和 , 和
C. 和 , 和
D. 和 , 和
【答案】D
【解析】
【详解】A.在离子方程式中, 不可拆成离子形式而 可拆成离子形式,二者离子方程式不
相同,A项错误;
B. 和 反应,生成 沉淀和 , 和 反应,生成 沉淀和
,二者离子方程式不相同,B项错误;
C. 可电离出 和 ,面 可电离出 和 ,二者离子方程式不相同,C项
错误;
D.二者反应的离子方程式相同,均可表示为H++OH-=H O,D正确。
2
答案选D。
15. 古诗词是我们宝贵的精神财富。下列诗句中不涉及氧化还原反应的是( )
A. 野火烧不尽,春风吹又生
B. 春蚕到死丝方尽,蜡炬成灰泪始干
C. 泉眼无声惜细流,树阴照水爱晴柔
D. 爆竹声中一岁除,春风送暖人屠苏
【答案】C
【解析】
【详解】A.野火烧不尽,春风吹又生;燃烧是氧化还原反应,A不符合题意;
B.春蚕到死丝方尽,蜡炬成灰泪始干;蜡烛燃烧是氧化还原反应,B不符合题意;
C.泉眼无声惜细流,树阴照水爱晴柔;流水和光照不涉及化学变化,C符合题意;D.爆竹声中一岁除,春风送暖入屠苏;火药爆炸,为氧化还原反应,D不符合题意;
故选C。
16. 下列说法正确的是( )
A. 在氧化还原反应中,元素化合价降低被氧化
B. 能在水溶液或熔融状态下导电的物质是电解质
C. 在一个氧化还原反应中,有一种元素被氧化,必有另一种元素被还原
D. 清晨的阳光穿过茂密的树木枝叶所产生的美丽景象(美丽的光线)是由于胶体粒子对光线的散射形成的
【答案】D
【解析】
【详解】A.在氧化还原反应中,元素化合价降低,得电子,被还原,故A错误;
B.能在水溶液里或熔融状态下自身能导电的化合物是电解质,能导电的物质不一定是电解质,如金属单
质等,故B错误;
C.在一个氧化还原反应中,被氧化和被还原的元素可能是同一种,如反应Cl+H O=HCl+HClO中,被氧
2 2
化和被还原的元素均为Cl元素,故C错误;
D.胶体具有丁达尔效应,是因为胶体粒子对光线的散射形成的,故D正确;
答案选D。
17. 下列反应中需加入还原剂能进行的是
A. Fe2+ → Fe3+ B. MnO → Mn2+ C. SO → SO D. NH → NH
3
【答案】B
【解析】
【详解】A. Fe2+ → Fe3+,Fe元素的化合价升高,需要加入氧化剂才能实现,故A不选;
B. MnO → Mn2+,Mn元素的化合价降低,需要加入还原剂才能实现,故B选;
C. SO → SO ,S元素的化合价升高,需要加入氧化剂才能实现,故C不选;
D. NH → NH ,无元素化合价的变化,不需要加入还原剂即可实现,故D不选;
3
答案选B。
18. 下列粒子在化学反应中既能表现氧化性又能表现还原性的是
A. Fe3+ B. Cl- C. Fe D. Fe2+
【答案】D
【解析】
【详解】A.Fe元素常见化合价为+2、+3价,则Fe3+一般只有氧化性,故A错误;B.Cl-中化合价为-1价,最低价,只表现还原性,故B错误;
C.Fe化合价只能升高,只表面氧化性,故C错误;
D.Fe2+化合价只能既能升高为+3价,又能降为0价,在化学反应中既能表现氧化性又能表现还原性,故D
正确;
故答案为D。
第II卷(非选择题,共46分)
二、填空题(每空2分,共38分)
19. 作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一、
某中学的化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋
等生活用品,进行了如下探究。
I.甲同学老家在山西,对儿时在家乡品尝到的山西老陈醋的滋味记忆犹新,而今总是觉得超市买到的醋不
如儿时的味道,查阅相关资料后,得知以下信息:
①醋分两种,酿造醋和配制醋。正宗的老陈醋必须经长久时间酿造才得此美味,市场上多充斥着工业醋酸
加水勾兑的配制醋。
②酿造醋国家标准为醋酸含量必须大于3.50g/100mL,而配制醋国家标准仅为1.50g~3.50g/100mL。
③在老师的帮助下,测定了超市购买的食醋中,醋酸的物质的量浓度为0.75mol/L。
(1)请帮助甲同学计算从超市购买的食醋中醋酸含量为___________g/100mL,属于___________醋(填“酿造”
或“配制”,醋酸的化学式为CHCOOH)。
3
(2)请写出醋酸与鸡蛋壳(主要成分为CaCO )反应的离子方程式___________。
3
Ⅱ.如图是该学校化学实验室浓盐酸试剂标签上的部分内容。乙同学现用该浓盐酸配制100mL 1mol•L﹣1的
稀盐酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。
请回答下列问题:
(1)配制稀盐酸时,还缺少的仪器有___________。
(2)经计算,配制100mL1mol•L﹣1的稀盐酸需要用量筒量取上述浓盐酸的体积为___________mL。
(3)对所配制的稀盐酸进行测定,发现其浓度小于1mol•L﹣1,引起误差的原因可能是___________。
A.定容时俯视容量瓶刻度线B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
Ⅲ.丙同学对课堂上学到的胶体的相关知识产生了浓厚兴趣。他利用买来的鸡蛋的蛋清配制成溶液,用激
光笔照射溶液,在垂直于光束的方向上观察到鸡蛋清溶液中有一条光亮的通路,此现象称为___________。
【答案】 ①. 4.50 ②. 酿造 ③. 2CHCOOH+CaCO =2CH COO﹣+CO ↑+H O+Ca2+ ④. 100mL容量
3 3 3 2 2
瓶 ⑤. 8.5 ⑥. CD ⑦. 丁达尔效应
【解析】
【分析】食醋的物质的量浓度为0.7mol•L-1,总酸量为0.75mol•L-1×60g/mol=45g/L,醋酸与碳酸钙反应生成
醋酸钙、水和二氧化碳,据此分析解答;根据配制一定物质的量浓度的溶液的步骤:计算、量取、稀释、
移液、洗涤、定容、摇匀,结合c= 和稀释定律,c V =c V 分析解答。
浓 浓 稀 稀
的
【详解】I.(1)食醋 物质的量浓度为0.75mol•L-1,总酸量为0.75mol•L-1×60g/mol=45g/L,即4.5g/100mL,
为酿造醋,故答案为:4.5;酿造;
(2)醋酸与碳酸钙反应生成醋酸钙、水和二氧化碳,反应的离子方程式为2CHCOOH+CaCO =2CH COO-
3 3 3
+CO ↑+H O+Ca2+,故答案为:2CHCOOH+CaCO =2CH COO-+CO ↑+H O+Ca2+;
2 2 3 3 3 2 2
Ⅱ.(1)配制100mL 1mol•L﹣1的稀盐酸的步骤有:计算、量取、稀释、移液、洗涤、定容、摇匀,需要的
仪器有:量筒、烧杯、玻璃棒、100mL容量瓶和胶头滴管,还缺少的仪器有100mL容量瓶,故答案为:
100mL容量瓶;
(2)浓盐酸的物质的量浓度c= = =11.8mol/L,设需要的浓盐酸的体积为
VmL,根据稀释定律,c V =c V 可知:11.8mol/L×VmL=100mL×1mol•L-1,解得V=8.5mL,故答案为:
浓 浓 稀 稀
8.5;
(3)A.定容时俯视容量瓶刻度线,会导致溶液体积偏小,浓度偏高,故A不选;B.容量瓶在使用前未干
燥,里面有少量蒸馏水,不影响溶质的物质的量和溶液的体积,对浓度无影响,故B不选;C.转移溶液
后,未洗涤烧杯和玻璃棒,会导致溶质的损失,浓度偏低,故C选;D.定容摇匀后发现液面低于容量瓶
的刻度线是正常的,再加水至刻度线,会导致浓度偏低,故D选,故答案为:CD;
III.鸡蛋清溶液是胶体,用激光笔照射溶液,在垂直于光束的方向上观察到鸡蛋清溶液中有一条光亮的通
路,此现象称为丁达尔效应,故答案为:丁达尔效应。
20. 以物质的量为中心的相关计算,已知阿伏伽德罗常数为N .
A(1)质量相同的H、NH 、SO 、O 四种气体中,含有分子数目最少的是___________,在相同温度和相
2 3 2 3
同压强条件下,体积最大的是___________。
(2)73.0g HCl气体中含有_______个分子,标况下体积约为_______L
(3)23.75 g某+2价金属的氯化物(MCl )中含有3.01×1023个Cl-,则M的摩尔质量为___g/mol。
2
(4)将0.5L 1mol/L FeCl 溶液加水稀释至1L,所得溶液中氯离子的物质的量浓度是____mol/L。
3
【答案】 ①. SO ②. H ③. 2N ④. 44.8 ⑤. 24 ⑥. 1.5
2 2 A
【解析】
【详解】(1)由n=m/M=V/V =N/N 可知,质量相同时,气体的摩尔质量越大,物质的量越小、分子数越
m A
小、体积越小。质量相同的H、NH 、SO 、O 五种气体中,SO 的摩尔质量最大,则其物质的量最小、分
2 3 2 3 2
子数最小;氢气的摩尔质量最小,则其物质的量最大、体积最大;
故答案为SO ,H;
2 2
(2)73.0gHCl气体的物质的量为:n(HCl)=73.0g/36.5g/mol =2mol,2molHCl中含有2N 个HCl分子,
A
含有原子数为:2N ×2=4N ,标准状况下2molHCl的体积为:22.4L/mol×2mol=44.8L,
A A
故答案为4N ,44.8;
A
(3)3.01×10 23个Cl -的物质的量是0.5mol,所以氯化物的物质的量是0.25mol。则根据M=m/n可知,MCl
的摩尔质量=23.75g÷0.25mol=95g/mol;MCl 的相对分子质量为95,氯原子的相对原子质量是35.5,所
2 2
以M的相对原子质量为95-35.5×2=24,M的摩尔质量为24g/mol,故答案为24;
(4)0.5L1mol/LFeCl 溶液中氯离子的浓度为3mol/L,根据稀释定律C V =C V ,稀释前后氯离子的
3 浓 浓 稀 稀
物质的量不变,令稀释后所得溶液中氯离子的浓度为c,则0.5L×3mol/L=1L×c,解得c=1.5mol/L,故答案
为1.5。
【点睛】本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏加德罗常数、气体
摩尔体积之间的关系为解答关键,试题有利于提高学生的分析能力及化学计算能力。
21. 已知乙醇( )能与 和 的混合溶液在一定条件下发生反应:
。 和 和在
溶液中分别显橙色和绿色,回答下列问题:
(1)该反应_________(填“是”或“不是”)离子反应。
(2)写出 的电离方程式:___________。
(3)该反应(填“是”或“不是”)氧化还原反应,判断的依据是____________。
(4)你认为能否用这一反应来检测司机是否酒后驾_______(填“能”或“不能”),简述其原理:_________。
【答案】 ①. 是 ②. ③. 是Cr元素在反应前后化合价降低了,C元素
在反应前后化合价升高了 ④. 能 ⑤. 该反应前后有颜色变化, 在酸性条件下遇乙醇发生反
应,颜色由橙色变为绿色
【解析】
【详解】(1)该反应2KCr O+3C HOH+8H SO =2K SO +2Cr (SO )+3CH COOH+11H O过程中有离子参与
2 2 7 2 5 2 4 2 4 2 4 3 3 2
和生成,故是离子反应,故答案为:是;
(2) 是可溶性盐属于强电解质,故其电离方程式: ,故答案为:
;
的
(3)反应中Cr元素 化合价降低,C元素的化合价升高,则该反应是氧化还原反应,故答案为:是;
(4) 和 在溶液中分别显橙色和绿色,乙醇具有还原性,可以被KCrO 氧化,可利用颜色的变化
2 2 7
检验乙醇,故答案为:能;该反应前后有颜色变化, 在酸性条件下遇乙醇发生反应,颜色由橙色
变为绿色。
三、化学推断题(每空2分,共8分)
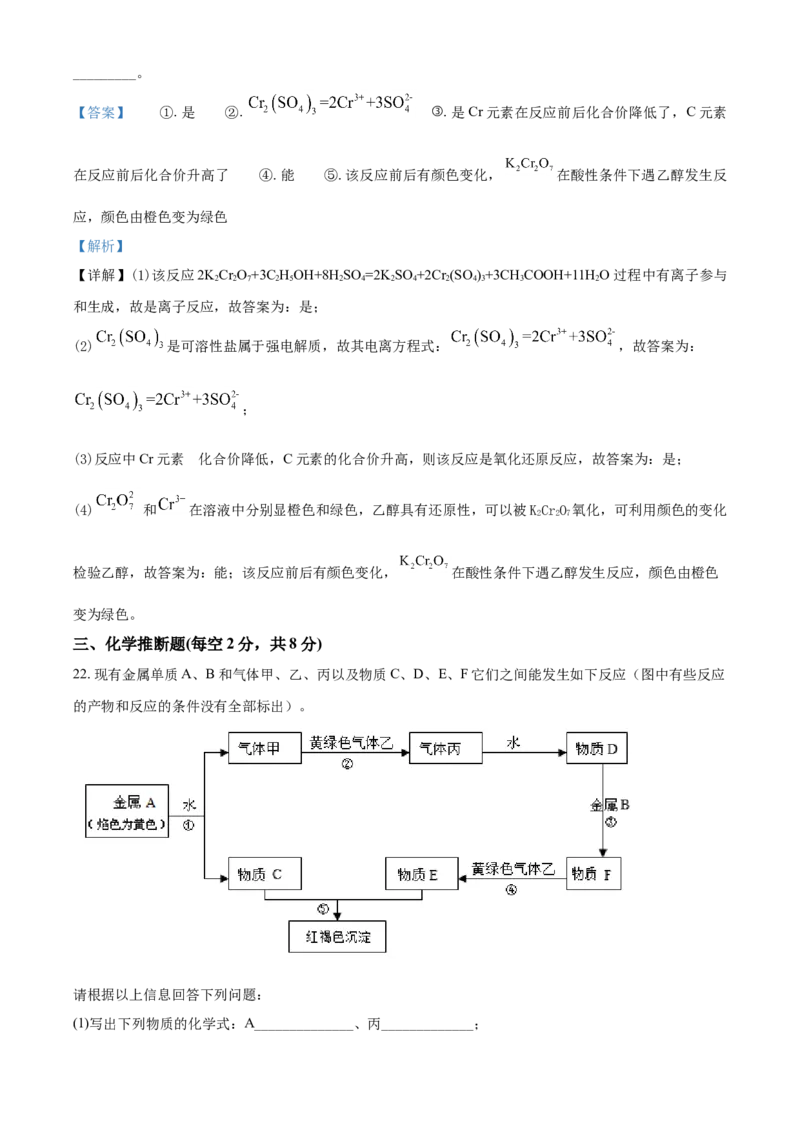
22. 现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F它们之间能发生如下反应(图中有些反应
的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A______________、丙_____________;(2)写出反应①化学方程式:______________________________________;
(3)写出反应④离子方程式________________________________________。
【答案】 ①. Na ②. HCl ③. 2Na+2HO=2NaOH+H↑ ④. 2Fe2++Cl=2Fe3++2Cl-
2 2 2
【解析】
【分析】金属A焰色反应为黄色,故A为Na,由反应①Na+水→气体甲+C,则甲为H ,C为NaOH,黄
2
绿色气体乙为Cl,与氢气反应生成丙为HCl,HCl溶于水得物质D为盐酸,氢氧化钠与物质E反应生成红
2
褐色沉淀是Fe(OH) ,故物质E中含有Fe3+,盐酸与金属B反应得到F,F与氯气反应得到E,可知金属B
3
为Fe,物质F为FeCl ,物质E为FeCl ,结合物质的性质解答该题。
2 3
【详解】(1)由上述分析可知,A为Na,丙为HCl;
(2)反应①为钠与水反应生成氢氧化钠和氢气,化学方程式为:2Na+2HO═2NaOH+H↑;
2 2
(3)反应④为氯化亚铁与氯气反应生成氯化铁,离子方程式2Fe2++Cl=2Fe3++2Cl-。
2