文档内容
山东省滨州市 2019-2020 学年高一上学期期末考试
化学试题
1.化学与生产生活息息相关。下列说法不正确的是
A. 城市空气质量报告中,PM2.5、PM10指的是悬浮颗粒物,会影响人体健康
B. “静电除尘”、“燃煤固硫”、“汽车尾气催化净化”能提高空气质量
C. 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质
D. 氧化亚铁可以用作色素,如应用于瓷器制作中使釉呈绿色
2.下列物质属于电解质且在该状态下能导电的是
A. Cu B. 熔融 NaCl C. KOH 溶液 D. BaSO 固体
4
3.下列物质属于碱性氧化物的是
A. NaO B. NaO C. SO D. NO
2 2 2 2 2
4.美国科学家用某有机分子和球形笼状分子C 制成了“纳米车”(如图所示,整辆“纳米车”的对角线的长度
60
仅为3至4纳米),每 辆“纳米车”是由一个有机分子和四个C 分子构成。“纳米车”可以用来运输单个的有
60
机分子。下列说法不正确的是
A. 人们用肉眼看不到“纳米车”的运动
B. “纳米车”的诞生说明人类操纵分子的技术进入了一个新阶段
C. C 是一种新型的化合物
60
D. C 的摩尔质量为720g•mol-1
60
5.如图表示质量相同的气体X和N 在相同容积的密闭容器中压强(P)和温度(T)的关系,则气体X可能是
2
.
A CO B. NH C. CH D. CO
3 4 26.下列事实中,与胶体有关的是
A. 人将植物油倒入水中,用力搅拌形成油水混合物
B. 可以用过滤的方法除去粗食盐水中的难溶杂质
C. 黑暗的电影院中,放映口发出的光会在影院中形成光柱
D. 利用活性炭净水
7.下列各组离子在指定的溶液中能大量共存的是
.
A 无色溶液中:K+、Cu2+、Na+、SO 2-
4
B. 强碱性的溶液中:K+、Na+、Cl-、CO2-
3
C. 强酸性的溶液中:Cl-、Fe2+、NO -、NH +
3 4
D. 使紫色石蕊试液呈红色的溶液中:Fe3+、Ba2+、SCN-、Cl-
8.为除去括号内的杂质,所选用的方法正确的是
A. FeCl 溶液(CuCl ),加入Fe粉,过滤
3 2
B. CO(SO ),通入饱和NaCO 溶液中
2 2 2 3
C. NO(NO ),通入水中
2
D. NaCO 溶液(Na SO ),加入过量Ba(OH) 溶液,过滤
2 3 2 4 2
9.下列说法不正确的是
A. 2 mol Na O 与足量水发生反应转移4 mole-
2 2
B. 少量的金属钠保存在煤油中
C. 现代化学已经成为实验与理论并重的科学
D. 高炉炼铁中实际起还原作用的是一氧化碳
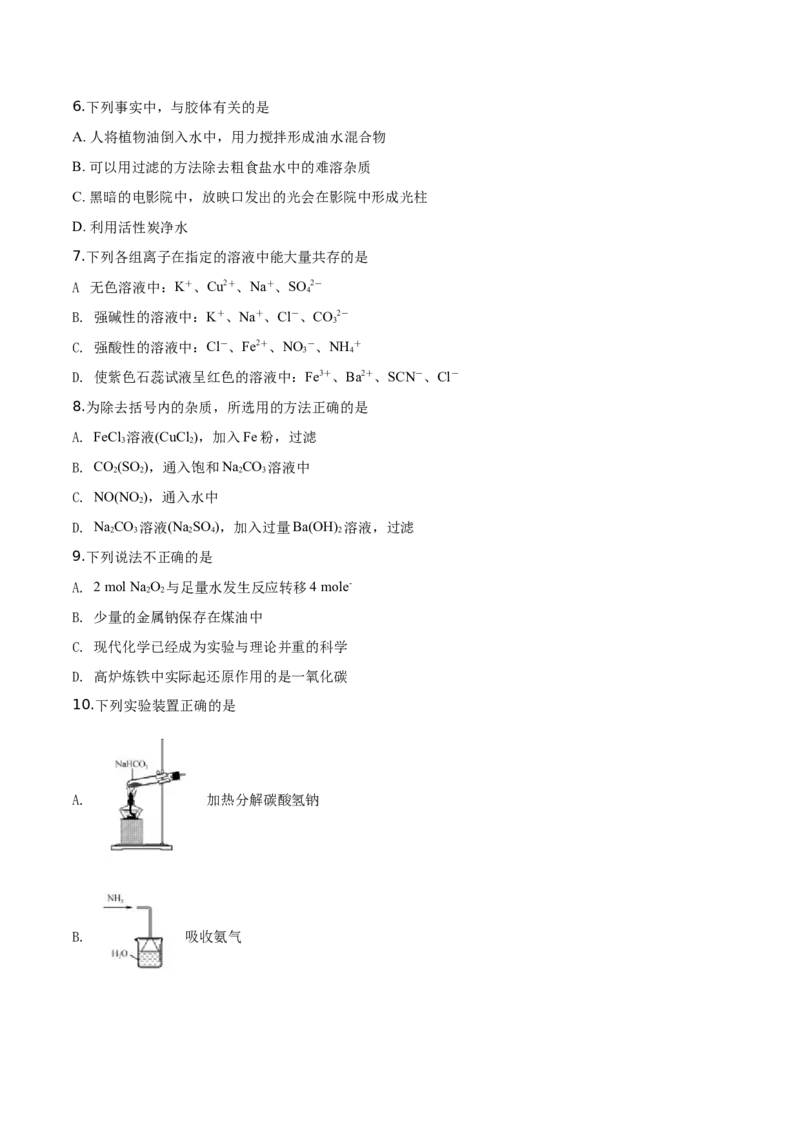
10.下列实验装置正确的是
A. 加热分解碳酸氢钠
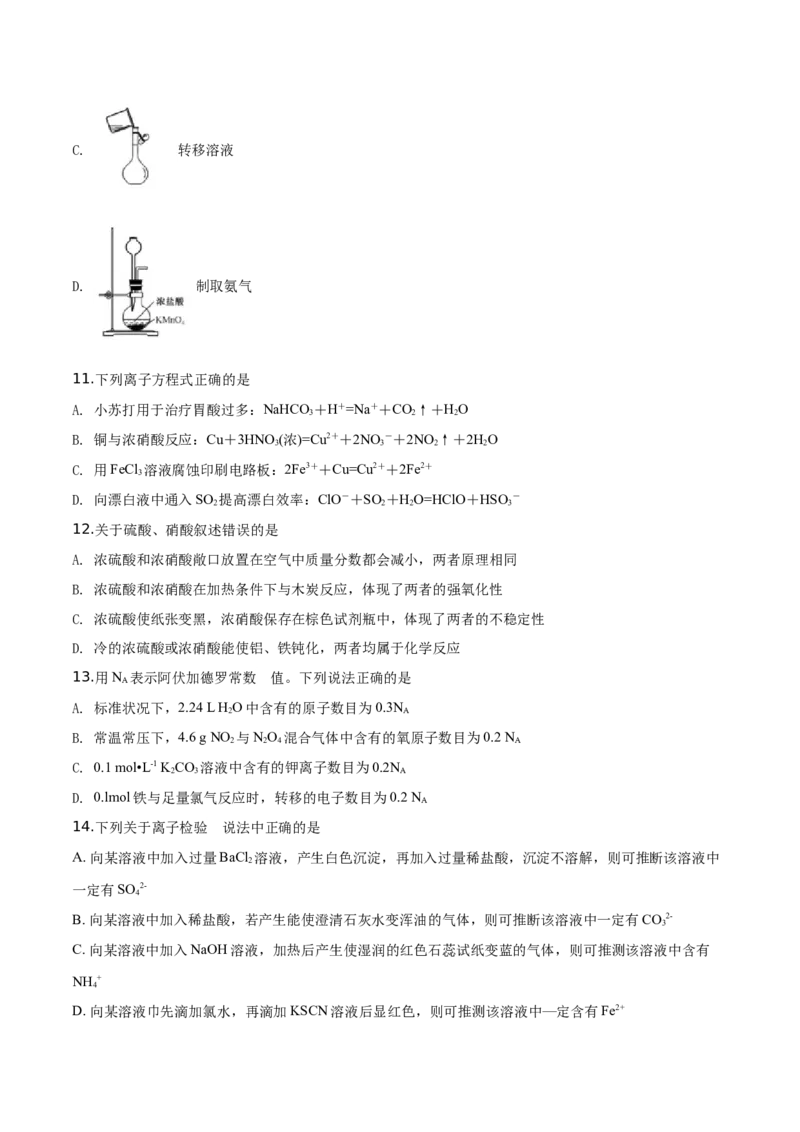
B. 吸收氨气C. 转移溶液
D. 制取氨气
11.下列离子方程式正确的是
A. 小苏打用于治疗胃酸过多:NaHCO +H+=Na++CO↑+HO
3 2 2
B. 铜与浓硝酸反应:Cu+3HNO(浓)=Cu2++2NO -+2NO ↑+2HO
3 3 2 2
C. 用FeCl 溶液腐蚀印刷电路板:2Fe3++Cu=Cu2++2Fe2+
3
D. 向漂白液中通入SO 提高漂白效率:ClO-+SO +HO=HClO+HSO -
2 2 2 3
12.关于硫酸、硝酸叙述错误的是
A. 浓硫酸和浓硝酸敞口放置在空气中质量分数都会减小,两者原理相同
B. 浓硫酸和浓硝酸在加热条件下与木炭反应,体现了两者的强氧化性
C. 浓硫酸使纸张变黑,浓硝酸保存在棕色试剂瓶中,体现了两者的不稳定性
D. 冷的浓硫酸或浓硝酸能使铝、铁钝化,两者均属于化学反应
13.用N 表示阿伏加德罗常数 的值。下列说法正确的是
A
A. 标准状况下,2.24 L H O中含有的原子数目为0.3N
2 A
B. 常温常压下,4.6 g NO 与NO 混合气体中含有的氧原子数目为0.2 N
2 2 4 A
C. 0.1 mol•L-1 K CO 溶液中含有的钾离子数目为0.2N
2 3 A
D. 0.lmol铁与足量氯气反应时,转移的电子数目为0.2 N
A
14.下列关于离子检验 的说法中正确的是
A. 向某溶液中加入过量BaCl 溶液,产生白色沉淀,再加入过量稀盐酸,沉淀不溶解,则可推断该溶液中
2
一定有SO 2-
4
B. 向某溶液中加入稀盐酸,若产生能使澄清石灰水变浑油的气体,则可推断该溶液中一定有CO2-
3
C. 向某溶液中加入NaOH溶液,加热后产生使湿润的红色石蕊试纸变蓝的气体,则可推测该溶液中含有
NH +
4
D. 向某溶液巾先滴加氯水,再滴加KSCN溶液后显红色,则可推测该溶液中—定含有Fe2+15.为了防止枪支生锈,常采用化学处理使枪支的钢铁零件表面生成Fe O 的致密保护层— “发蓝”。化学处
3 4
理过程中,其中一步反应为3Fe + NaNO +5NaOH =3Na FeO+H O+NH ↑。下列叙述不正确的是
2 2 2 2 3
A. 该处理过程不会产生污染 B. 上述反应中铁被氧化
C. NO -的氧化性大于FeO2- D. 反应中转移2mole-,生成还原产物
2 2
16.化学计盘在化学中占有重要地位,请回答下列问题。
(1)相同质量的SO 和SO 所含氧原子的个数比为______。
2 3
(2)质量相同的A、B两种气体,在同温同压下,A的分子数比B多,则A的密度_____ B的密度(填>、=、
<)。
(3)焦亚硫酸纳(Na SO)是常用食品抗氧化剂,常用于葡萄酒、果脯等食品中。果脯中的Na SO 的使用量
2 2 5 2 2 5
是以游离的SO 来计算的,我国规定每千克果脯中SO 的最高含量是0.35g。
2 2
①下列试剂可用于检测SO 的是_________。
2
A.I B.HC1 C. H SO D.CS
2 2 4 2
②某500g果脯样品经检测得知含有SO 的物质的量为0.005 mol,该产品是否合格_________ (填“是”或“否”)。
2
(4)“84消毒液”是常用的含氯消毒剂,可以利用Cl 与NaOH反应制得该产品。反应的离子方程式为_______。
2
“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84g•cm-3)的浓硫酸配制1
000 mL 0.50 mol • L-1的稀硫酸用于增强“84消毒液”的消毒能力。需用量筒量取浓硫酸的体积为
_________mL。
17.A、B、C、X均为中学常见的物质,它们之间有如下转化关系(反应条件及副产物已略去)。
(1)若A和X均为单质,B为可使品红溶液褪色的气体,则反应②的化学方程式为____。
(2)若A、B、C为含钠元素的化合物,X为无色无味气体,则反应②的化学方程式为______ 。
(3)若A为稀硝酸,B溶液和硫氰酸钾溶液反应后溶液显红色,则反应②的离子方程式为_____。若向C的
溶液中加入氢氧化钠溶液产生白色沉淀,在空气中迅速变成_____,最后变成_______,白色沉淀发生上述
变化的原因 ______(用化学方程式表示)。56 g X与足量的稀硝酸发生反应,被还原的HNO 为
3
__________g。
18.氨是一种重要的化工产品,也是重要的化工原料。某化学兴趣小组在实验室制备氨并完成相关性质实
验。
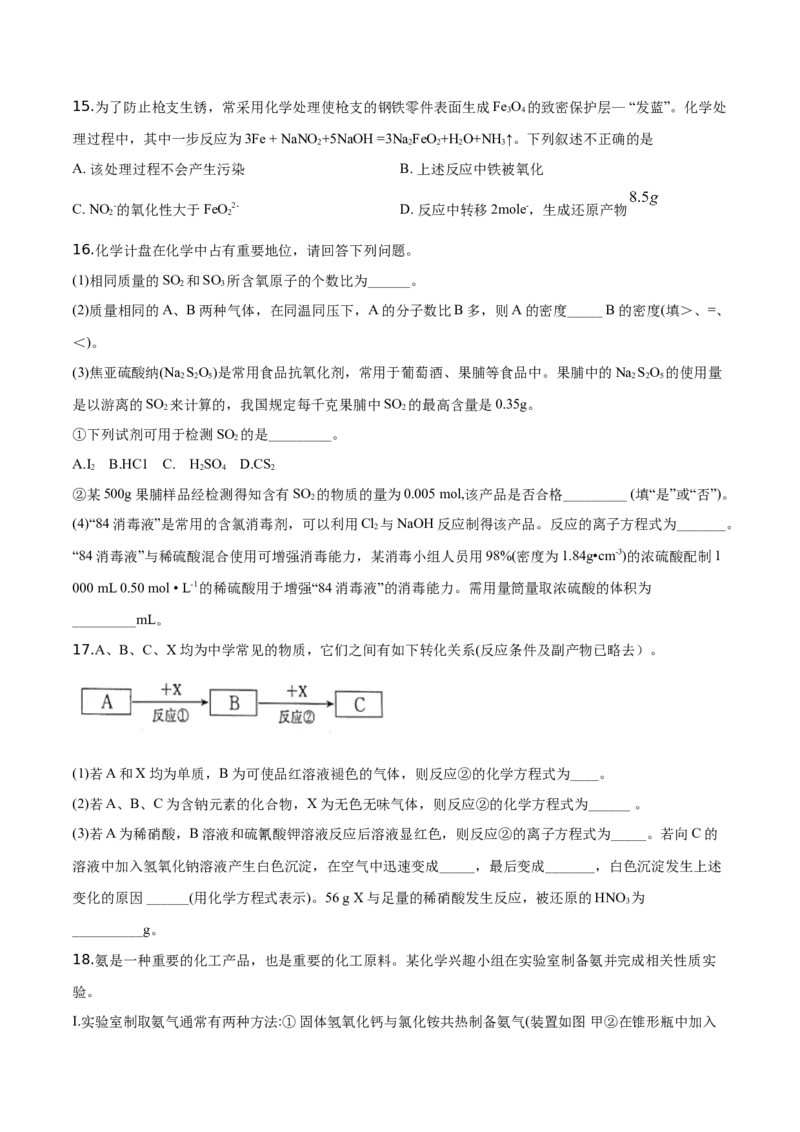
I.实验室制取氨气通常有两种方法:①固体氢氧化钙与氯化铵共热制备氨气(装置如图 甲②在锥形瓶中加入NaOH固体,在分液漏斗中加入浓氨水制备氨气(装置如图乙)。请回答:
(1)用方法①制备并收集NH 。装置甲中生成NH 的化学方程式为______。用圆底烧瓶收集NH 的方法为
3 3 3
_____(填“向上排空气法”或“向下排空气法”),检验圆底烧瓶中已收集满氨气的方法是_______。
(2)利用装置乙可用方法②制取氨气,利用该装置还可制取_____(填字母)等气体。
a.H b.CO c.Cl
2 2 2
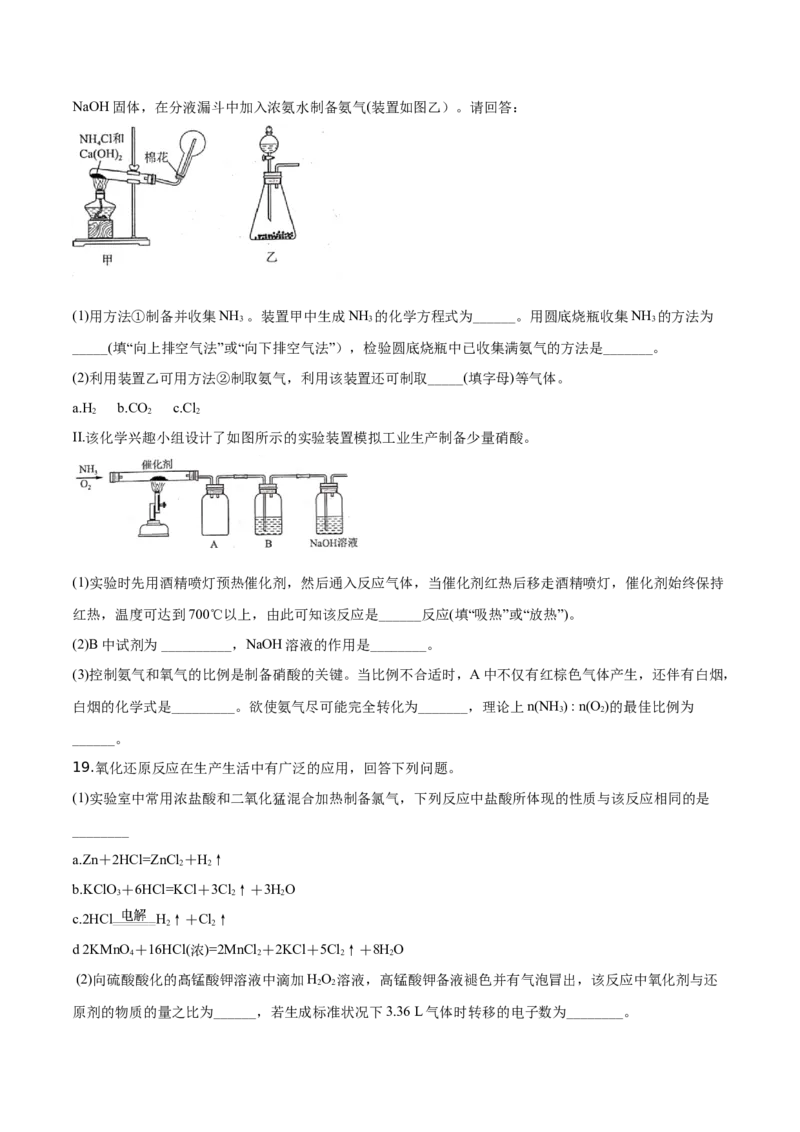
II.该化学兴趣小组设计了如图所示的实验装置模拟工业生产制备少量硝酸。
(1)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后移走酒精喷灯,催化剂始终保持
红热,温度可达到700℃以上,由此可知该反应是______反应(填“吸热”或“放热”)。
(2)B中试剂为 __________,NaOH溶液的作用是________。
(3)控制氨气和氧气的比例是制备硝酸的关键。当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟,
白烟的化学式是_________。欲使氨气尽可能完全转化为_______,理论上n(NH ) : n(O)的最佳比例为
3 2
______。
19.氧化还原反应在生产生活中有广泛的应用,回答下列问题。
(1)实验室中常用浓盐酸和二氧化猛混合加热制备氯气,下列反应中盐酸所体现的性质与该反应相同的是
________
a.Zn+2HCl=ZnCl +H↑
2 2
b.KClO +6HCl=KCl+3Cl↑+3HO
3 2 2
c.2HCl H↑+Cl↑
2 2
.
d2KMnO +16HCl(浓)=2MnCl +2KCl+5Cl↑+8HO
4 2 2 2
(2)向硫酸酸化的髙锰酸钾溶液中滴加HO 溶液,高锰酸钾备液褪色并有气泡冒出,该反应中氧化剂与还
2 2
原剂的物质的量之比为______,若生成标准状况下3.36 L气体时转移的电子数为________。(3)向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,发生反应的离子方程式为
2 2 2
________。
20.铁在人体中不是以游离态的形式存在,而是以Fe2+和Fe3+形式存在。Fe2+易被吸收,给贫血者补充铁时,
应给予含Fe2+的盐。服用维生素C,有利于人体对铁元素的吸收。
(1)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作 用下转化成亚铁盐。
此反应的离子方程式______。
(2)工业盐的主要成分是NaNO ,曾多次发生过因误食NaNO 而中毒的事件,其原因是NaNO 把人体内的
2 2 2
Fe2+转化为Fe3+而失去与O 结合的能力,这说明NaNO 具有________性。
2 2
(3)“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人
体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
①操作1的名称是__________。
②试剂2为______溶液(填化学式)。
③加入新制氯水,溶液中发生反应的离子方程式是__________。