文档内容
专题一 《物质构成的奥秘》综合检测
1.B 2.A 3.C 4.D 5.A 6.B 7.D 8.C 9.B 10.C 11.CD 12.BD 13.AC
+3
14.(1)①5H ②1Cu ③ 2CO2- ④ Fe(2)① A ② F ③ C ④ E
2 3
15.(1)原子 离子 (2)①10 ②阴离子 O2—(3)氯化氢分子总是在不断地运动着
16.(1)0 +2(2)Zn HgO (3)还原性(4)分类、集中
点燃
17.(1)①D E ②最外层电子数少于4 ③阳 (2)S+O SO
2 2
18.(1)6(2)7(3)8(4)非金属(5)NH HCO
4 3
19.(1)①22.99 ②5 ③NaCl
(2)①过滤(或蒸馏或吸附或沉淀等合理答案)。②肥皂水 ③CO ④洗脸水用来拖地板
2
等合理答案。
20. (1) 17 核电荷数(或质子数)不同 (2) 氯(或Cl) A
21.(1)错误 正 (2)② HO Cl- MgO
2 2
22. (1)60 (2)7:8 (3)53%
23. (1)127:39:48 (1分) (2)59.3%(127/214) (1分)
(3)每500g食盐中少加碘的质量为(40mg一25mg)÷2=7.5mg (1分)
则每500g食盐中少加碘酸钾的质量为7.5mg÷59.3%=12.6mg (1分)
专题二 《物质的化学变化》综合检测
1.C 2.C 3.C 4.B 5.B 6.B 7.C 8.D 9.A 10.D 11.BD 12.BD 13.CD
14(. 1)SO; Fe2+; HSO ; NH ; NaCO (2)4P+5O 2P O (3)3CO+Fe O
2 4 3 2 3 2 2 5 2 3
2Fe+3CO (4)HSO +Ba(OH) BaSO ↓+2H O
2 2 4 2 4 2
15.(1)B (2)2Al + Fe O 高温 2Fe+ Al O 化学
2 3 2 3
点燃
16. (1)5 溶解(2)32:202:36(16:101:18) S S+O SO
粉尘 2 2
(3)2SO +O 2SO SO +H O=H SO (3)AB
2 2 3 3 2 2 4
点燃
17. (1)C (2)化合 (3)2H +O 2HO
2 2 2
18.(1)肥皂水(2)①FeCl +Al= Al Cl+Fe ②2HCl +Mg (OH) ==== MgCl + 2H O
3 3 2 2 2
复分解反应
19.(1)Al(OH) + 3HCl AlCl + 3H O (2) 灰白色粉末状、铵态氮肥
3 3 2
(3)C + 60O 60CO
60 2 2
20.(1)②,①③(2)防止氧气进去与氢气混合引起爆炸(3)盐酸
(4)CaCO +2HCl==CaCl +H O+CO↑(或Fe O+6HCl==2FeCl +3H O) 白色沉淀
3 2 2 2 2 3 3 2
21.(1)396 (2)84:11:4 (3)C
22. (1) 2.64
(2) 解:设10g样品中碳酸钙的质量为x
CaCO +2HCl==CaCl +H O+CO↑
3 2 2 2
100 44
1x 3.52g
x=8g
此石头纸中碳酸钙的质量分数为:
(3) 44.48
专题三
1.D 2.C 3.C 4.C 5.A 6.C 7.B 8.B 9.D 10.C 11.AC 12.CD 13.CD
14.(1)工业废水或生活污水的任意排放,不合理使用农药、化肥等任写一种即可沉淀、蒸馏、吸
附、过滤、煮沸等任写一种即可 (2)CO +1
2
15. (1)实验室用KClO 制O 时MnO 做催化剂能加快反应速率
3 2 2
(2)木炭燃烧时O 不足生成CO,O 充足生成CO
2 2 2
(3)留在空气中和在氧气中燃烧现象不同(其他答案正确也可)
16.(1)H O+C1 = HCl+ HClO (2)分解反应 (3)Cl 、O (4)+1价 (5)在化学变化中,分
2 2 2 2
子可分成原子,原子不可分。(其他答案正确也可)
点燃 点燃
17.② 燃烧更旺,发出白光;C + O CO; ④ 明亮的蓝紫色火焰;S + O SO
2 2 2 2
反应物浓度越大,反应越剧烈
18.2KClO 2KCl+3O↑ (1)常温反应,不需加热(或操作简便) (2)反应速率快
3 2
(3)便于回收二氧化锰 (4)制得的氧气纯净(或无污染)
19.(1)化合反应 条件都是点燃 2Mg+O ==== 2MgO ②是气体化合物与氧气反应(其他
2
答案正确也可) (2)生成物都是氧化物
20. 2HO 2HO+O↑(或2KClO 2KCl+3O ↑
2 2 2 2 3 2
或2KMnO KMnO +MnO+O ↑); B(或A); C和D(或C、D)
4 2 4 2 2
剧烈燃烧(或火星四射或生成黑色固体或放出热量); 3Fe+2O Fe O
2 3 4
生成的二氧化碳中混有氯化氢气体(或盐酸浓度较高,挥发出了氯化氢气体或石灰
水变质或二氧化碳的量很少)
21.仪器名称:锥形瓶 收集方法:排水集气法【 结 论】在相同条件下,HO 生成O 的快
2 2 2
慢与催化剂种类有关【 反 思】质量和化学性质【假 设】浓度或质量分数或温度等【实验
方案】在同温下,取二份质量相等的不同浓度的HO 溶液,分别加入质量相等的同种催化剂,
2 2
测量各收集一瓶气体所需的时间
22.(1)水分子(H O分子) (2)滤去不溶性 吸附一些可溶性 (本题答案不分先后顺序)
2
(3)②(饱和)Na CO 溶液 CaCl +Na CO=2NaCl+CaCO ↓(只写此化学方程式即给分,再写
3 3 2 2 3 3
Ca(OH) +Na CO=2Na0H+CaCO ↓不扣分也不加分)④取上述滤液少许于试管中,滴加少量肥皂
2 2 3 3
水,振荡 产生较多泡沫
23.t 1.92g 98%
3
2专题四
1.D 2.B 3.C 4.D 5.D 6.A 7.A 8.C 9.C 10.D 11.AB 12.AC 13.CD
14、5 6 4 1 2 7 3 8
15、(1)本身不燃烧 也不支持燃烧 密度比空气大(2)地球温度变高 冰川融化
16、(1)减少矿物质的燃烧 多植树 (2)①释放 ②CO+HO===H CO
2 2 2 3
17、2H 电极 润滑剂
18、CO O H CH , H CH ,CO H CH ,CH
2 2 4 2 4 2 4 4
点燃
19、乙,O ,CO , 3 CH+2O ====CO +2H O
2 4 2 2 2
20.(1)用点燃的木条 灼热的氧化铜 紫色石蕊溶液 澄清的石灰水
(2)①氧气会使食品中某些成分氧化,氧气有利于某些微生物生长;二氧化碳则相反,可防止食
品氧化,抑制微生物生长。因此,二氧化碳的猜想更合理。
②用注射器抽取袋内气体通入少量澄清的石灰水中。若石灰水变浑浊,则猜想正确;反之,则不
正确。
21、1 长颈漏斗;集气瓶;烧杯2 大理石;石灰石;稀盐酸;大理石逐渐溶解;表面有大量气泡
生成3 澄清石灰水变浑浊4 石蕊变红; 5 下层先熄灭;不燃烧,也不支持燃烧;密度比空
气大6 CaCO +2HCl=CaCl +HO+CO↑
3 2 2 2
22. (1)易燃,无腐蚀性或低毒(2)4∶10∶3 106
23.(1)否 90% (2) 3.96g
专题五
1.B 2.B 3.D 4.A 5.D 6.A 7.A 8.C 9.B 10.C 11.CD 12.BD 13.AB
14.物理性质 固体 优良导体 较大 较高
15.(1)常温下Hg是液体,其余金属为固体 (2)镁 (3) 可燃
16.铁粉 过滤 Fe+CuSO ===Cu+FeSO
4 4
点燃
17.剧烈燃烧,火星四射 3Fe+2O Fe O Fe O·xH高O温 疏松
2 3 4 2 3 2
18.(1)Fe Fe+CuSO ===Cu+FeSO (2)C C+2CuO 2Cu+CO↑ (3)H H +
4 4 2 2 2
CuO Cu+HO
2 高温
19.(1)高炉 (1分) (2)3CO+Fe O 2Fe+3CO (2分)(3)促使反应更加剧烈,并获得更多的
2 3 2
热量(1分)(4)加入稀盐酸,有气泡产生的为铁粉,否则为生石灰
20. (1) ……Mg ……Fe……Ag……(2)银(3)过滤Fe(4) Fe+H SO =FeSO+H ↑;置换
2 4 4 2
21. (1)铁>锰>铜 (2) 硫酸铜(或硫酸亚铁)溶液中 (3)锰片放在硫酸铜溶液中,铁片放入硫酸
溶液中[实验及结论]有气体放出,锰片、铁片逐渐减少。[拓展探究]③,①②④也可以验证四种金
属的活动性顺序。
22.[猜想]氧气 二氧化碳 [设计与实验]⑴B ⑵A ⑶氧气 二氧化碳 铜生锈需要水
补充的实验为铜+水+氧气
23.(1)32.5% (2)0.2 (3)13.6g/(6.5g+40g-0.2g)=29.4%
3专题六
1.D2.B 3.A 4.D 5.D 6.C 7.B 8.C 9.B 10.C 11.AC 12.AB 13.BC
14.⑴小于 ⑵加入适量甲物质(降温或蒸发溶剂至少量晶体析出)⑶饱和 等于
15.B>C>A(或B、C、A或BCA); 65;B>C>A(或B、C、A或BCA)
16.(1)10;(2)甲的溶解度>乙的溶解度;(3)加溶剂(或加水或升温); (4)降温结晶(或冷却热饱
和溶液)
17. (1)不断运动(2)随压强减小而减小(或随压强增大而增大)(3)Na CO(或NaHCO 或洗洁精等
2 3 3
其他答案合理均给分)
18. 烧杯底部有固体析出 塑料板下沉 加入氯化钠固体(或升高温度后再加硝酸钾固体
等)
19. ⑴A 温度在 t 时,B、C的溶解度相等 ⑵冷却热饱和溶液(或降温结晶)
1
⑶C Mg+ 2HCl= MgCl + H ↑
2 2
20.(1)①瓶塞应倒放在桌面上 ②称量NaCl的天平上,砝码和药品的位置应调换过来(2分)
(2)小于(1分)(3)称量NaCl的实际质量比计算质量大 加入水的实际量比计算量小
21. (1)2NaOH+MgCl =Mg(OH) ↓+2NaCl (2分)NaCO+CaCl =CaCO ↓+2NaCl (2分)
2 2 2 3 2 3
(2)HSO (1分)(3)C (1分)(4)50 (1分) 有固体析出 (1分)
2 4
22.(1)NaCO+2HCl==2NaCl+H O+CO↑ NaOH+HCl==NaCl+H O
2 3 2 2 2
(2) 过滤 充分除尽溶液中的氢氧化钙 (3)玻璃棒 搅拌,加快溶解
23. (1)67.5% (2) 50g(3)15.1%
专题七
1.D 2.B 3.B 4.A 5.B 6.D 7.D 8.B 9.B 10.D 11.AB 12.AC 13.AB 14.
物质 化学式 类别 物质 化学式 类别
盐酸 HCl 酸 消石灰 Ca(OH) 碱
2
石灰石 CaCO 盐 生石灰 CaO 氧化物
3
纯碱 NaCO 盐 苛性钠 NaOH 碱
2 3
15. (1)水 (2)二氧化碳 (3)熟石灰 (4)乙酸
16.
(1)Al(OH) +3HCl====AlCl +3H O(2)CaCO +2HCl====CaCl +H O+CO↑ Mg(OH) +2HCl====
3 3 2 3 2 2 2 2
MgCl +2H O(3)CO +Ca(OH) ====CaCO↓+H O
2 2 2 2 3 2
(4)CO +2NaOH====Na CO+H O NaCO+H SO ====Na SO +H O+CO↑
2 2 3 2 2 3 2 4 2 4 2 2
(5)不能 Fe+CuSO====FeSO +Cu
4 4
17.NaCl;HCl(或氯化钠,氯化氢);石蕊试液(活泼金属、碳酸盐等合理即可);液体变红(有气泡
等,对应合理即可)
18.CaO+H O=Ca(OH) ; 碱性 ;PH试纸 ;CO+Ca(OH) =CaCO ↓+H O
2 2 2 2 3 2
19. (1)甲 氧化钙可以进一步与水反应生成氢氧化钙(2)
实验步骤及操作方法 预期的实验现象 结论
41.取少量过氧化钙放入试管,加足量水, 燃着的木条燃烧更旺(带 有氧气生成
并且将燃烧的(带火星的)木条放在试管口 火星的木条复燃)
2.将试管中的溶液通入适量的二氧化碳 溶液变浑浊 有氢氧化钙生成
20.将生成的气体通入到澄清的石灰水中,石灰水变浑浊
【作出猜想】嚼碎后服用疗效快(或嚼碎后药物与胃酸的反应快;或反应物的接触面积增大,化
学反应加快)
【设计实验】一片研碎的药片
【拓展探究】(1)对身体无害 (2)碳酸盐与盐酸作用生成二氧化碳气体,加重胃溃疡病情
21.(1)4.4 (2)NaCl 、HCl (3)解:73g10%的稀盐酸中含HCl的质量是:
73g×10%=7.3g 设参加反应的碳酸钠的质量为x,反应生成的氯化钠的质量为y
NaCO + 2HCl = 2NaCl + CO ↑ + H O
2 3 2 2
106 73 117
X 7.3g y
73 7.3g
= x=10.6g
106 x
73 7.3g
= y=11.7g
117 y
烧杯里不饱和溶液中溶质的质量为: 117.g + (22.3g-10.6g) = 23.4g
专题八
1.A 2.D 3.D 4.B 5.D 6.D 7.B 8.D 9.A 10.D 11.BC 12.BD 13.AC
14. (1)干冰 (2)氢气 (3)盐酸 (4)氢氧化钠 (5)碳酸钙
15. (1)H O (2)SO (或SO ) (3)NaOH (4)NaNO
2 3 2 3
16.无明显变化 变红色 溶液浑浊,颜色变浅(或消失)说明:本题第三空两现象要答全
17.NaOH、CuCl 、NaCO NaOH、HNO、Fe O 【说明:本题属开放性答案,其它合理答
2 2 3 3 2 3
案 也 可 】 (2)NaCO+2HCl==2NaCl+H O+CO↑[ 或 NaOH+HCl==NaCl+H O 或
2 3 2 2 2
2NaOH+CuCl ==Cu(OH) ↓+2NaCl或NaCO+CuCl ==CuCO↓+2NaCl等]【说明:所写化学方
2 2 2 3 2 3
程式要与以上三空对应,只有得分的物质,该化学方程式才能得分,否则不给分】
18. (1)< (2)影响人类健康(或使森林大面积枯死、或建筑物腐蚀损坏、或土壤酸化等等,符合
题意均给分)(3) Ca(OH) +H SO ==CaSO +2H O (4) B
2 2 4 4 2
19.(1)H+ 能使紫色石蕊试液变红,使无色酚酞试液不变色;能与碱发生中和反应;能与较活泼
金属反应;等 (任写两条) (2)H(O ) CaO+H O=Ca(OH) (3) 用洁净的玻璃棒蘸取待测水
2 2 2 2
样,滴到pH试纸上,把pH试纸显示的颜色与标准比色卡比较,读出pH。
20.溶解 过滤 蒸发 结晶 玻璃棒 搅拌,加速溶解 引流 搅拌,防止液滴飞溅
搅拌,防止晶体飞溅
21.
探究步骤 可能观察到的现象 结论
(1)NaCl溶液(或AgNO AgNO(或NaCl)
3 3
溶液)
若无白色沉淀生成 两溶液恰好完全反应
5(2)AgNO(或NaCl) 若有白色沉淀生成 NaCl溶液过量(或AgNO 溶液过量)
3 3
22. 猜想二:真、假“珍珠粉”在水中的溶解性可能不同
方案二:取样,分别加入适量水中并搅拌,观察它们溶解性有无差异
猜想三:真、假“珍珠粉”与酸反应现象可能不同
方案三:取样,分别加入适量稀盐酸,观察现象有无差异
猜想四:真、假“珍珠粉”灼烧后可能有不同现象
方案四:取样,在酒精灯火焰上灼烧片刻,观察颜色、状态变化
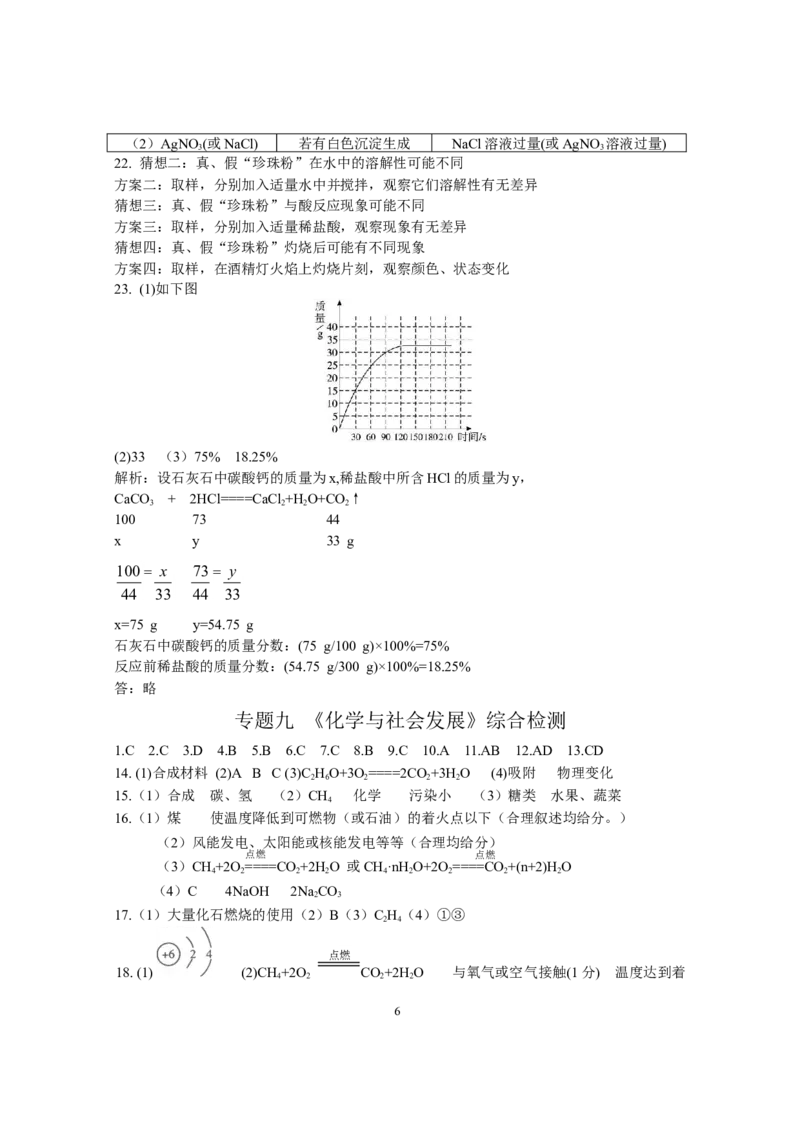
23. (1)如下图
(2)33 (3)75% 18.25%
解析:设石灰石中碳酸钙的质量为x,稀盐酸中所含HCl的质量为y,
CaCO + 2HCl====CaCl +H O+CO↑
3 2 2 2
100 73 44
x y 33 g
100= x 73 = y
44 33 44 33
x=75 g y=54.75 g
石灰石中碳酸钙的质量分数:(75 g/100 g)×100%=75%
反应前稀盐酸的质量分数:(54.75 g/300 g)×100%=18.25%
答:略
专题九 《化学与社会发展》综合检测
1.C 2.C 3.D 4.B 5.B 6.C 7.C 8.B 9.C 10.A 11.AB 12.AD 13.CD
14. (1)合成材料 (2)A B C (3)C HO+3O====2CO+3H O (4)吸附 物理变化
2 6 2 2 2
15.(1)合成 碳、氢 (2)CH 化学 污染小 (3)糖类 水果、蔬菜
4
16.(1)煤 使温度降低到可燃物(或石油)的着火点以下(合理叙述均给分。)
(2)风能发电、太阳能或核能发电等等(合理均给分)
点燃 点燃
(3)CH+2O ====CO +2H O 或CH·nH O+2O====CO +(n+2)H O
4 2 2 2 4 2 2 2 2
(4)C 4NaOH 2NaCO
2 3
17.(1)大量化石燃烧的使用(2)B(3)C H(4)①③
2 4
点燃
18. (1) (2)CH
4
+2O
2
CO
2
+2H
2
O 与氧气或空气接触(1分) 温度达到着
6点燃
火点 (3)2NO
2
+2xCO
2
N
2
+2XCO
2
(无催化剂不扣分) (4)B
(5)CO+H O == HCO(2分) 2NaOH+CO==NaCO+H O(2分)
2 2 2 3 2 2 3 2
19. (1)甲 CH+2O CO+2H O (2)SO (或二氧化硫) 置换反应
4 2 2 2 2
(3)不污染环境(或减少碳排放、节约化石能源等)(其他合理答案均可给分)
20.(1)Cu、C、Zn MnO NH Cl、ZnCl 淀粉
2 4 2
(2)②过滤 二氧化锰和炭粉 ③灼烧(或暴露在空气中加强热) ④取样于试管中,加
入氢氧化钠溶液并加热(把湿润的红色石蕊试纸放在试管口),强烈刺激性气味(或湿润
的红色石蕊试纸变蓝色) NH Cl+NaOH==NaCl+HO+NH ↑
4 2 3
21. (1)2.2 g 与包装说明不符
专题十 《科学探究》综合检测
1.C 2.C 3.A 4.B 5.C 6.A 7.A 8.D 9.B 10.C 11.AB 12.AC 13.BC
14. (1) ①I ②A ③D ④G ⑤B ⑥C或I或C、I (2) A和C (3) C
15. (1)红色粉末变黑,澄清石灰水变浑浊(只需回答一种现象即可)
(2)没有尾气处理装置 (3)Fe O+3CO 2Fe +3CO
2 3 2
16.(1)18.5 (2)烧杯 (3) ⑤ ③ ① ④ ②
17.(1)铁架台 BD C E (2)固体粉末由黑色变为红色 澄清石灰水 点燃(或套上气球,或
套上塑料袋。)
(3) (见右图。导管“短进”1分、“长出”1分。若把导气管画成线
→ →
条、且是短进长出,总体扣1分)
(4)在a处套上一个夹好铁夹的橡胶管,在b处用酒精灯微热(或用
手握玻璃管),②中有气泡放出;冷却后在②中左边导管形成一个稳定
的液柱,说明气密性良好。
18.实验现象:无现象 结论:铝能与稀硫酸发生反应,反应速率较快 Al Cr Cu(或
“②”) 回答问题: (1)除去金属表面氧化物(或污物) (2) Cr+H SO=CrSO+H ↑
2 4 4 2
(3) 无法比较铬和铝的金属活动性强弱 (4) A1、CrSO 溶液、Cu 归纳:①通过金属与酸反应
4
判断金属活动性强弱 ②通过金属与盐溶液反应判断金属活动性强弱
19. 猜想②:(1分)(NH )SO(或硫酸铵)【实验探究】(1)④ [2NH Cl+Ca(OH) =CaCl +2H O+
4 2 4 4 2 2 2
2NH ↑,或(NH )SO +Ca(OH) =CaSO +2H O+2NH ↑,或
3 4 2 4 2 4 2 3
NH HCO +Ca(OH) =CaCO +2H O+NH ↑]
4 3 2 3 2 3
(2)HCl溶液(或盐酸) ③ (3)BaCl 溶液(或氯化钡溶液) 无白色沉淀 有白色沉淀
2
(NH )SO +BaCl ==BaSO ↓+2NHCl
4 2 4 2 4 4
20.【知识回放】⑴HSO +2NaOH=NaSO +2H O ⑵HSO +Ba(NO)=BaSO↓+2HNO
2 4 2 4 2 2 4 3 2 4 3
或KCO+Ba(NO)=BaCO ↓+2KNO
2 3 3 2 3 3
【挖掘实质】Ba2+和NO -或Ba2+和2NO -;2H++CO 2-=HO+CO↑或2H++CO 2-=HCO ,
3 3 3 2 2 3 2 3
HCO=HO+CO↑ (若未配平,生成物未标注箭头,不扣分)
2 3 2 2
【实践运用】Ba2+和SO 2-或Ba2+和CO2-或H+和CO2-;H+、Na+、K+和NO -(必须答全四种得1
4 3 3 3
7分)
溶液中可能含有的离子 设计实验验证(实验步骤、现象及对应的结论)
可能性一:Ba2(+ 同时答两种 取上述溶液少量于试管中,加入少量硫酸钠溶液。若出现白色沉
或两种以上离子的不得分, 淀,则说明上述溶液中含有Ba2+;若没有出现白色沉淀,则说明
下同。) 上述溶液中不含有Ba2+。
取上述溶液少量于试管中,加入少量硝酸钡溶液。若出现白色沉
淀,则说明上述溶液中含有SO 2-;若没有出现白色沉淀,则说明
可能性二:SO 2- 4
4 上述溶液中不含有SO 2-。
4
取上述溶液少量于试管中,加入少量硫酸钠溶液。若出现白色沉
可能性三:Ba2+或SO 2- 淀,则说明上述溶液中含有Ba2+,不含有SO 2-。(若没有出现白
4 4
色沉淀,必须验证SO 2-)(其他答案合理给分。)
4
【知识升华】
溶液中的离子能否大量共存或者离子是否参加化学反应,参加化学反应的离子是否有剩
余。(意义表达准确,都可给分。)
8