文档内容
精选练习8 四种常见气体的检验和吸收
一、CO、CO、HO、H 的检验和吸收: 1、检验和吸收的方法:
2 2 2
检 验 吸 收
试 剂 现 象 试 剂 装 置
CO 澄清石灰水 变浑浊 NaOH 溶液 洗气瓶
2
NaOH 固体、CaO、CaCl U形管、干燥管
2
HO 无水CuSO 变蓝色
2 4
浓硫酸 洗气瓶
H CuO +CuSO 变红色、变蓝色 CuO 硬质玻璃管
2 4
CO CuO +石灰水 变红色、变浑浊 CuO 硬质玻璃管
2、检验的顺序:HO→CO→H→CO
2 2 2
具体步骤:用CuSO 检验水蒸气的存在→用澄清石灰水检验二氧化碳的存在→吸收二氧化碳→吸收水蒸
4
气→通过灼热的氧化铜发生反应→再用CuSO 检验水蒸气(验证氢气的存在)→再用澄清石灰水检验二氧
4
化碳(验证一氧化碳的存在)
3、吸收的顺序:先吸收CO,再吸收水蒸气。
2
二、有关练习题: 1、某同学用锌粒与浓盐酸反应制取氢气,由于浓盐酸具有挥发性,制得的氢气中含有
氯化氢和水蒸气。氯化氢气体极易溶于水。为了得到纯净而干燥的氢气,可通过下列部分装置来完成。请根
据下图回答问题:
② ③ A B C D
浓
① 硫
水
酸
甲 乙 丙 丁 戊 己
(1)写出标有①②③编号仪器的名称:① ,② ,③ 。
(2)写出锌与盐酸反应的化学方程式: ;
(3)氢气的发生装置应选用 ,收集装置应选用 。 (用甲、乙、丙……表示)
(4)装置连接顺序为:气体发生装置接 → → 接 → →接收集装置(用A、B、
C、D表示) CuO
2、某学生为了验证氢气还原氧化铜的产物,设计了 稀硫酸
C
右图实验装置。
(1)写出编号仪器的名称: 锌
① 粒 ②
① ,② 。
无水硫
(2)本实验需要加热的装置字母编号为 。 酸铜
A B
(3)装置B、C中可观察到的现象分别为:
B 。 C
。
(4)装置A还可以用于 ;(填 ①或②) ①氯酸钾分解制氧气 ②大理石跟盐酸反应制二氧化碳
(5)为了达到实验目的,使根据现象得出的结论更科学,上述实验装置添加酒精灯后还存在缺陷,请提
出简要修改方案: 。
3、水煤气是一种重要的工业气体燃料和化工原料,水蒸气通过炽热的煤(或焦炭)层所生成的混合气体是
水煤气,其主要成分是一氧化碳和氢气,未经净化的水煤气往往还含有杂质水蒸气和二氧化碳。
c d e f 初
g h
CuO
a b
澄清石灰水 无水硫酸铜
浓硫酸
(A) (B) (C) (D)(1)为了证明水煤气中含有上述四种物质,连接上图各装置的正确顺序是(填写各接口字母,每种装置
根据需要均可多次选择,并且接口序号不变):
水煤气→( )( )接( )( )接( )( )接( )( )接( )( )接( )( )→尾气
(2)写出D中发生反应的化学方程式: 。
4、利用下列图示装置制取纯净、干燥的氢气,并用氢气还原氧化铜来测定铜的相对原子质量。
(1)装置的连接顺序是:9接( )接( )接( )接( )接( )接( )接( );
1 2 3 4 5 CuO 6 稀 硫
酸
7 8 9
浓 浓
锌
硫 硫
酸 酸 无水CaCl 2
Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ
(2)装置Ⅰ的作是 (3)装置Ⅱ的作用是
(4)装置Ⅲ中观察到的实验现象是 (5)加热CuO之前必须进行
的操作是
5、某混合气体中可能含有CO、CO、H 和O 中的一种或几种,依次通过澄清石灰水、灼热的氧化铜和
2 2 2
无水硫酸铜时,依次出现石灰水变浑浊、氧化铜变红色、无水硫酸铜变蓝色的现象,由此推断:
(1)原混合气体中一定含有 ,(2)原混合气体中一定没有 ,可能含有 。
6、无色混合气体中可能存在水蒸气、一氧化碳、二氧化碳、氯化氢和氢气。将混合气体通过浓硫酸,气
体体积没有变化;再通过澄清石灰水后,没有出现浑浊现象,但气体体积缩小一半。尾气导出后能燃烧,燃烧
后产生的气体能使无水硫酸铜变蓝色,却不能使澄清石灰水变浑浊。则该气体中一定存在(填分子式)
;一定不存在 。
写出发生的有关反应的化学方程式:
8、乙醇是以高粱、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源。在汽油中加入适量乙醇
作为汽油燃料,可节省石油资源,减少汽车尾气的污染。 乙醇(CHO)完全燃烧时生成CO 和HO。如果氧
2 6 2 2
气不充足,乙醇燃烧可能还有CO生成。现用下图装置进行实验,确证乙醇燃烧产物中有CO、CO 和HO。请
2 2
回答下列问题:
CuO
乙醇燃烧产物
无 水 澄 清 氢氧化 澄 清 澄 清
硫酸铜 石灰水 钠 石灰水 石灰水
A B 溶 C D E F
液
(1)能确证产物中有HO的现象是: ;能确证产物中有CO的现象是: 。
2
(2)实验时可观察到装置B中石灰水变浑浊,D中石灰水无变化。B装置的作用是: ;C
装置的作用是: ;D装置的作用是: ;
(3)若乙醇燃烧的产物中CO和CO 总质量为25.5g,其中碳元素和氧元素的质量比为2∶5,则参加反应
2
的乙醇的质量是 g,产物中HO的质量为 g。
2
(4)科学家发现海底埋藏着大量的“可燃冰”—甲烷的水合物。质量相等的甲烷和乙醇在氧气充足的条件
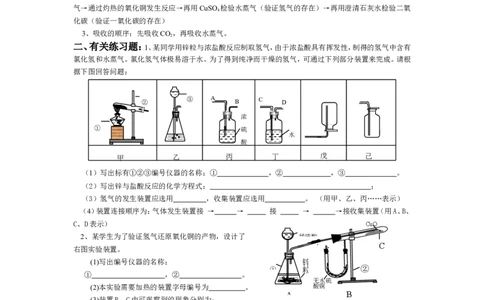
下,产生二氧化碳的质量较多的是 。9、如下图所示,A管中盛有干燥的炭粉,C管中盛有干燥的氧化铜粉末,B、D两个U形管中装有碱石
灰(氢氧化钠和氧化钙的固体混合物),用来吸收CO 气体。将3.0g干燥的CO 气体全部通入A管进行实验,
2 2
实验结束后,B管质量增加0.8g,D管质量增加3.3g。
A B C D
计算进入C管和离开C管的CO的质量各是多少?
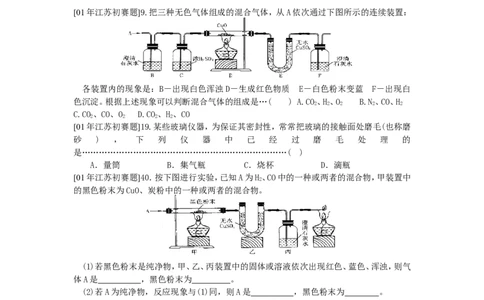
[01年江苏初赛题]9.把三种无色气体组成的混合气体,从A依次通过下图所示的连续装置:
各装置内的现象是:B-出现白色浑浊D-生成红色物质 E-白色粉末变蓝 F-出现白
色沉淀。根据上述现象可以判断混合气体的组成是…( ) A.CO、H、O B.N、CO、H
2 2 2 2 2
C.CO、CO、O D.CO、H、CO
2 2 2 2
[01年江苏初赛题]19.某些玻璃仪器,为保证其密封性,常常把玻璃的接触面处磨毛(也称磨
砂 ) , 下 列 仪 器 中 已 经 过 磨 毛 处 理 的
是………………………………………………………………( )
A.量筒 B.集气瓶 C.烧杯 D.滴瓶
[01年江苏初赛题]40.按下图进行实验,已知A为H、CO中的一种或两者的混合物,甲装置中
2
的黑色粉末为CuO、炭粉中的一种或两者的混合物。
(1)若黑色粉末是纯净物,甲、乙、丙装置中的固体或溶液依次出现红色、蓝色、浑浊,则气
体A是 ,黑色粉末为 。
(2)若A为纯净物,反应现象与(1)同,则A是 ,黑色粉末为 。
(3)若第(1)问中,乙装置的物质增重3.6g,红色物质,丙装置中的物质增重4.4g,则至少
需通入 g气体。
(4)若第(2)问中,甲装置生成6.4g红色物质,乙装置中物质增重O.9g,则至少需要
g黑色粉末。40.(1)C0,H,CuO(1分) (2)H,CuO C(1分) (3)3.2(1分)
2 2
(4)8.3(1分)
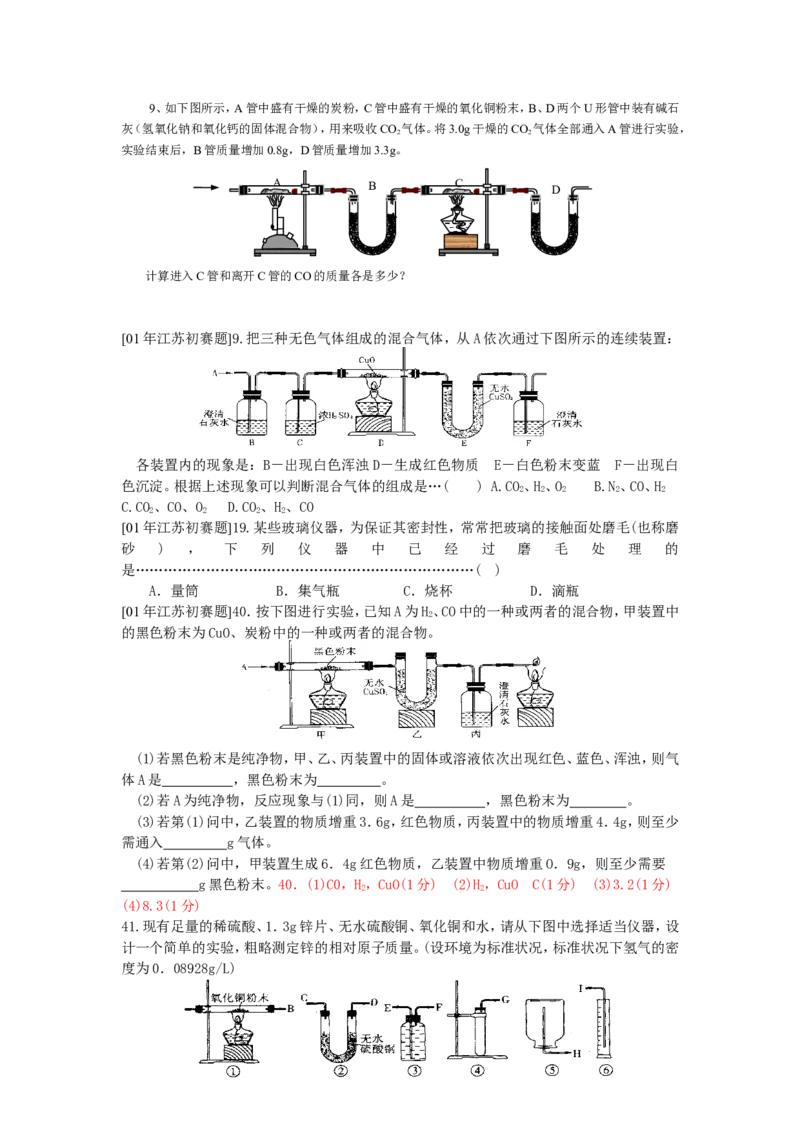
41.现有足量的稀硫酸、1.3g锌片、无水硫酸铜、氧化铜和水,请从下图中选择适当仪器,设
计一个简单的实验,粗略测定锌的相对原子质量。(设环境为标准状况,标准状况下氢气的密
度为0.08928g/L)(1)应选用的装置是(填写装置代号) 。(2)所用装置的连接顺序是
(填写各接口的字母序号) 。(3)如果实验中,测得量筒中水的体
积为450mL,请列式计算锌的粗略的相对原子质量。
。
41.(1)③④⑥(1分) (2)G接F、E接I(3)设锌的相对原子质量为m。
Zn+HSO→ZnSO+H↑
2 4 4 2
m 2
1.3g 0.45L×0.08928g/L=0.04g m=65答:锌的相对原子质量约为65
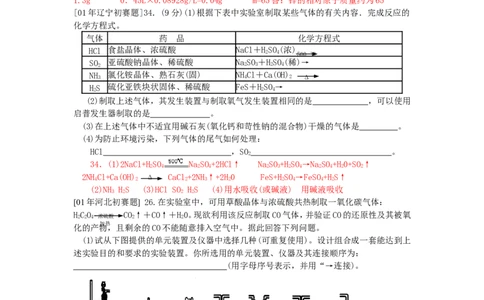
[01年辽宁初赛题]34.(9分)(1)根据下表中实验室制取某些气体的有关内容.完成反应的
化学方程式。
气体 药 品 化学方程式
HCl 食盐晶体、浓硫酸 NaCl+HSO(浓)
2 4 500 ℃
SO 亚硫酸钠晶体、稀硫酸 NaSO+HSO(稀)→
2 2 3 2 4
NH 3 氯化铵晶体、熟石灰(固) NH 4 Cl+Ca(OH) 2 Δ
HS 硫化亚铁块状固体、稀硫酸 FeS+HSO→
2 2 4
(2)制取上述气体,其发生装置与制取氧气发生装置相同的是 ,可以使用
启普发生器制取的是 。
(3)在上述气体中不适宜用碱石灰(氧化钙和苛性钠的混合物)干燥的气体是 。
(4)为防止环境污染,下列气体的尾气如何处理:
HCl ,SO 。
2
34.(1)2NaCl+HSO NaSO+2HCl↑ NaSO+HSO→NaSO+H0+SO↑
2 4 2 4 2 3 2 4 2 4 2 2
2NHCl+Ca(OH) Δ CaCl+2NH↑+2H0 FeS+HSO→FeSO+HS↑
4 2 2 3 2 2 4 4 2
(2)NH HS ( 3)HCl SO HS (4)用水吸收(或碱液) 用碱液吸收
3 2 2 2
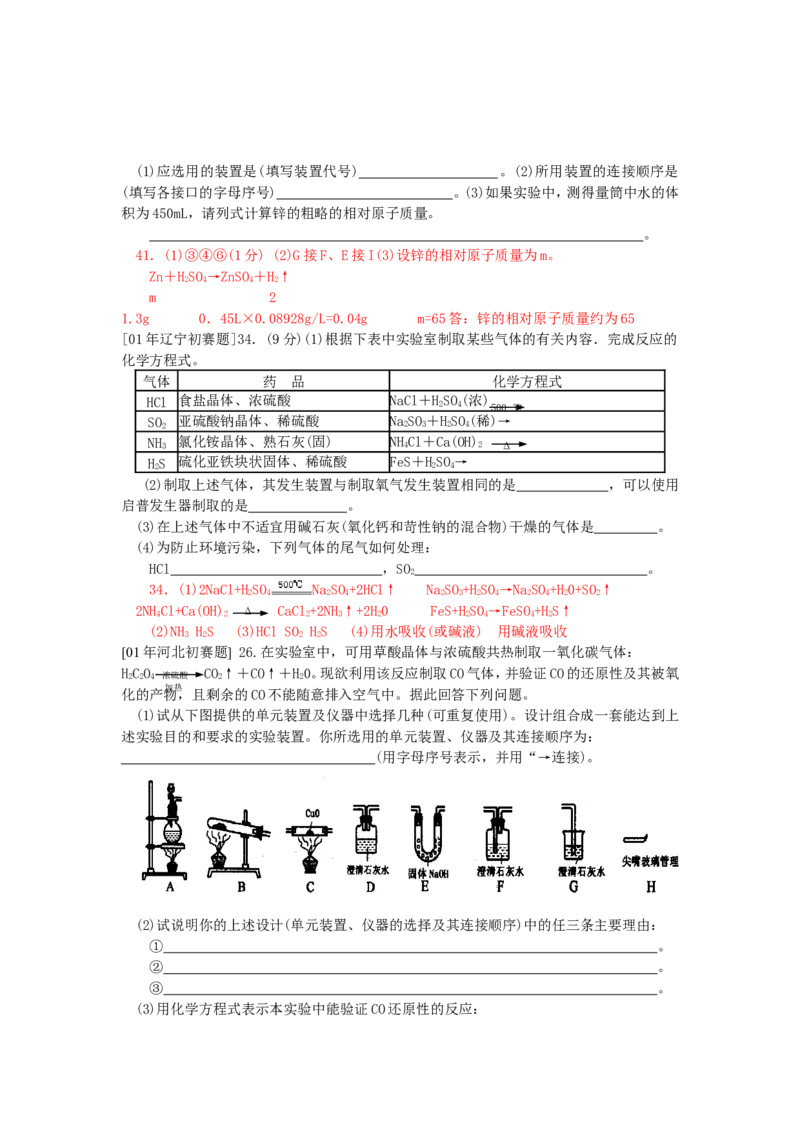
[01年河北初赛题] 26.在实验室中,可用草酸晶体与浓硫酸共热制取一氧化碳气体:
HCO CO↑+CO↑+H0。现欲利用该反应制取CO气体,并验证CO的还原性及其被氧
2 2 4 浓硫酸 2 2
加热
化的产物,且剩余的CO不能随意排入空气中。据此回答下列问题。
(1)试从下图提供的单元装置及仪器中选择几种(可重复使用)。设计组合成一套能达到上
述实验目的和要求的实验装置。你所选用的单元装置、仪器及其连接顺序为:
(用字母序号表示,并用“→连接)。
(2)试说明你的上述设计(单元装置、仪器的选择及其连接顺序)中的任三条主要理由:
① 。
② 。
③ 。
(3)用化学方程式表示本实验中能验证CO还原性的反应:;
(4)用化学方程式表示检验CO氧化产物的反应:
。
26.(1)A→E→F→C→F→H (2)①由于是采用固液反应制取CO,故气体发生装置只能选
择A。
②为确保进入C装置的气体只有CO,故在此之前用 E装置除去CO,并用F确认除净CO。③
2 2
为验证CO氧化产物中含有CO,故在C装置后连接F装置来确认。
2
(3)CO+Cu0 Cu+CO 2C0+O 2CO (4)CO+Ca(OH)→CaCO↓+H0
2 2 2 2 2 3 2
[01年河北初赛题]28.有氢气、甲烷、一氧化碳三种气体。将它们分别点燃,并使燃烧后的产
物依次通过无水硫酸铜和澄清石灰水。各自实验现象如下表所述,请在表格中写出相应气体
的化学式。
无水硫酸铜的变化现象 澄清石灰水的变化现象 结 论
不变 变浑浊
白色变成蓝色 不变
白色变成蓝色 变浑浊
28.CO,H,CH
2 4
[01年山西初赛题]39.已知氨气(NH)极易溶于水,其水溶液显碱性。实验室欲用氨气代替氢
3
气还原氧化铜,并测定铜的相对原子质量。该反应生成物为氮气、铜和水。实验装置如下图所
示:实验完成后测定Cu和生成水的质量分别为m(Cu)和m(HO)。试回答下列问题:
2
(1)写出标有字母仪器的名称:a ,b 。
(2)写出氨气还原氧化铜的化学方程式 。
(3)装置A的作用是 。
(4)装置C的作用是 。
(5)装置D的作用是 。
(6)请写出计算Cu的相对原子质量的数学表达式 。
(7)若无D装置,则计算出来的Cu的相对原子质量是偏 (填高、低或不变)。
39.除标明分数者外,其余每空1分。
(1)酒精灯,铁架台 (2)2NH+3CuO N2+3Cu+3H0 (2分)
3 2
(3)除去氨气中的水蒸气 (4)吸收反应生成的水 (5)吸收未反应的氧气,防止空气中
水蒸气进入C(2分) (6) 18m(Cu)/m(HO) (2分) (7)偏低
2
[01年山西初赛题]31.(6分)请从下图中选用适当的装置,设计组装一套实验装置来验证某
混合气体是由H、CO和HCl组成的,并回答下列问题:(注意,图中装置不得重复使用,有的装
2
置可不选用)[01年辽宁初赛题](1)所选用装置的正确连接顺序是 (只要求写出图中装置
的序号);
(2)选用第一个装置的作用是 ,选用第二个装置的作用是 ,其
化学方程式为 。
(3)连接后首尾装置中出现的现象是 。
31.(6分) (1)④、⑥、①、⑦、⑤ (2分,按顺序正确连接3个的给1分) (2)验证混合
气体中有HCl存在;除水;CaO+ HO=Ca(OH)(各1分) (3)④中有白色沉淀;⑤中出现浑浊。
2 2
(1分).(错一个不给分)
[01年辽宁初赛题]32.(4分)某校化学课外活动小组的同学设计了一套能验证一每化碳性质
并带有一定趣味性的实验,效果明显。实验装置如下图所示:当打开开关a(同时在尖嘴处放
一火源),通入适量的一氧化碳后,关闭开关a和b,并撤掉火源。约10~15分钟后,可观察到
A中鱼仍活着,B中蛙死亡,C中鲜红的血液变成黑色。然后打开开关b,同时再在尖嘴导管处
点燃。
试回答:
(1)A中结果说明 ;
(2)B中结果说明 ;
(3)C中结果说明 ;
(4)在尖嘴导管处点燃的目的是 。
32.(每空1分,共4分) (1)一氧化碳难溶于水;(2)一氧化碳具有毒性; (3)一氧化碳
与血红蛋白反应是产生毒性的原因;(4)防止一氧化碳气体进入空气中,污染环境。
[01年辽宁初赛题]
33.(4分)某学生为了测定由两种元素组成的
气态化合物X的组成,做了如右图所示的实验,
把气体X由A缓缓送入装有CuO的装置B中,
使之完全反应,得到以下结果:
①实验前B管及药品的质量为21.3克,
实验后为18.9克,B中CuO变成了Cu;
②C管中收集到的物质是HO;③D处收集到1.4克N。根据实验结果,回答下列问题:
2 2
(1)C中收集到水的质量是 克;(2)X物质的式量为 ;
(3)实验中B处反应的化学方程式: 。
33.(4分)(1)2.7克(1分)(2)17(1分)(3)2NH+3CuO 3Cu+3HO+N (2分)
3 2 2
[01年黑龙江初赛题]
9.实验室制取、干燥、检验二氧化碳气体,应选用的一组试剂是………………( C )
A.碳酸钠、稀盐酸;浓硫酸;苛性钠 B.石灰石、稀盐酸;烧碱;石灰水
C.石灰石、稀盐酸;浓硫酸;石灰水 D.石灰石、稀硫酸;浓硫酸;石灰水
[01年黑龙江初赛题]
37.如图装置可以收集以下气体:H、CH、CO、HCl、SO、NH、CO。
2 4 2 2 3
(1)若集气瓶是干燥的,气体由A管进入,可收集的气体有
(2)若将集气瓶盛满水,收集气体并测量气体的体积,可以收集并测量的体积的气体有 。此时气体应由 管进入,由 管通向量筒。
37.(1)CO,HCl,SO (2)H,CH,CO,B,A
2 2 2 4
[01年黑龙江初赛题]
39.(5分)现有如下10种装置,请用它们的序号回答下列问题:
试回答:(1)实验室制取CO 气体应选用的装置为 和 ;
2
(2)若制取干燥、纯净的二氧化碳气体并进行氧化铜转化为铜的实验,应该让发生装置
导出的混合气体通过→ → → → 。
(3)某气体可能含有HCl,CO,H,CO中的一种或几种,该气体依次经过H,E,C,F,发现H
2 2
中无变色现象,E中粉末由黑色变成红色,C中固体由白色变为蓝色,F中石灰水变
浑浊,则该气体中肯定有 ,肯定没有 。
39.(1)B、K (2)B→A→D→G→E (3)CO,HCl和CO
2
[01年湖北初赛题]
28.(5分)5月31日是世界无烟日,吸烟有害健康,科学实一验表明香烟所产生的烟雾中,
至少有300多种化合物不同程度对人体有害。为了鉴定该烟雾中是否存在CO 和CO,在对香
2
烟燃烧产生的烟雾进行适当处理后依次通过足量的以下试剂:①澄清石灰水②浓硫酸③灼
热的黑色氧化铜粉末④澄清石灰水,发现①、④中澄清石灰水变浑浊。试回答
(1)①现象说明 。
(2)烟雾中是否存在CO ,做出此判断依据的实验现象为 。
28.(5分)(1)燃烧产物中存在CO(1分) (2)存在(2分), ④中澄清石灰水变浑浊(2分)
2
[01年山东初赛题]
24.雷利是英国物理学家和化学家,他曾用以下两种方法测定氮气的密度。
方法一:将除去水蒸气和二氧化碳的空气通过烧红的装有铜屑的玻璃管,将空气中的氧
气全部除去,测得氮气的密度为1.2572克/升。
方法二:将氨气通过炽热的氧化铜,生成铜、水和氮气,除去水蒸气和剩余的氨气后,测
得氮气的密度为1.2505克/升。试回答以下问题:
(1)方法二中发生反应的化学方程为 。
(2)为除去空气中的水蒸气和二氧化碳,可供选择的装置如下:
如果气流流向自左向右,在你选择的装置中,各导管口的连接顺序是(各接口用图中字
母表示): ;
所选装置中盛放的物质按先后顺序分别为 。
(3)两种方法所测得的氮气密度数值不同,你认为哪种方法测得的较为准确?并说明理
由:。
24.(1)3 CuO+2NH→3Cu+N+3HO(2分) (2)BAGH或GHBA;氢氧化钠溶液,浓硫酸(3分)
3 2 2
(3)第二种方法(1分)。因为第一种方法没有除去空气中的稀有气体(2分)
[01年广东初赛题]
25.现有A贮气瓶中的混合气体(主要有CO,内含少量 CO),以A为原料制备纯净干燥的
2
CO去还原氧化铜,并验证反应产物。依照图示装置回答:
(1)请用字母标号表示装置连接的正确顺序:A→ → → → → ;
(2)C装置中观察到的现象是 ;
(3)B装置的作用是 ;其反应方程式是 。
(4)D装置的作用是 ;
(5)上述整套装置中发生的化学反应,其中属于化合反应的化学方程式为:
。
25.(11分)①D F C B E (3分) ②黑色粉末逐渐变红色 (1分) ③验证反应产
物 (1 分) CO+Ca(OH)→CaCO↓+H0 (2 分) ④吸收混合气体中的 CO (2 分)
2 2 3 2 2
⑤2CO+O 2CO (2分)
2 2
[01年海南初赛题]
34.水煤气是工业上生产氢气的原料之一,水煤气中除含有一氧化碳和氢气外,常混有二
氧化碳和水蒸气。验证水煤气中含有一氧化碳和水蒸气,可用下面的实验装置:
回答下列问题:
(1)上述装置的先后正确顺序是(用代号填写):
水煤气一→( )一→( )一→( )一→( )一→( )一→尾气。
(2)在实验过程中.A装置的玻璃管中观察到的现象是 ,在B中观察到的现象是
,在E中观察到的现象是 。
(3)尾气是否可以排入空气中?为什么?
。
34.(1)DCAEB (2)黑色的粉末逐渐变为红色;澄清的石灰水变浑浊;白色粉末逐渐变蓝
(3)不能:因为其中可能含有未反应完的CO。
01年重庆初赛题]
23.根据下面给出的药品和实验装置,设计一个实验,粗略测定由铜和锌两种金属组成的合金 黄铜中锌的质量分数(黄铜已加工成粉末)。
药品:稀硫酸、浓硫酸、氧化铜
实验装置:
另有托盘天平可用,根据你设计的实验方案回答下列问题:
(1)你选用的药品是 。
(2)你选用的实验装置有(填装置序号) 。若需要组装,则连接的顺序是(用
装置接口处的编号表示) (若不需要组装,则不填)。
(3)称取a克黄铜粉末样品进行实验,实验中你测定的其他数据是( )
A.生成H 的体积b升
2
B.反应前仪器和药品的质量c克
C.反应后剩余固体的质量d克
D.反应后仪器和药品的质量e克
(4)计算合金中锌的质量分数(可能用到的数据:相对原子质量:Zn-65,Cu-64,0-16,H-
l;在实验条件下,2.0克H 的体积为22.4升)。
2
23.(1)稀硫酸(2)
(2)方案一:A、E、F ①、⑧、⑨、⑦;方案二:A;方案三:A、G(4分)
(3)方案一:A; 方案二:B、D; 方案三:C(2分)
(4)方案一:w(zn)=65b/22.4a ×100%
方案二:w(zn)=65(c--e)/2a ×100%
方案三:w(Zn)=(a—d)/a ×100% (3分)
[第(3)、(4)问的要与第(2)问的方案相同才能得分]