文档内容
反应热和热化学方程式
【学习目标】
1、理解反应热和焓变的含义
2、掌握热化学方程式的概念和意义,并会准确书写热化学方程式
【主干知识梳理】
一、反应热与焓变
1、反应热与焓变
(1)反应热
①含义:在等温条件下,化学反应体系向环境释放或从环境吸收的热量,称为化学反应的热效应,简称反应
热
②符号:ΔH
③单位: kJ·mol - 1 或kJ/mol
④测定方法:利用量热计直接测定
(2)内能、焓、焓变
①内能(符号为U):体系内物质的各种能量的总和,受温度、压强和物质的聚集状态等影响
②焓(符号为H):与物质内能有关的物理量
③焓变:焓变(∆H):是变化前后物质的焓值差,化学反应的焓变,为生成物的总焓值与反应物的总焓值之差,
即: Δ H = H ( 生成物 ) - H ( 反应物 )
④在等压条件下进行的化学反应(严格地说,对反应体系做功还有限定,中学阶段一般不考虑),其反应热等于
反应的焓变,符号: Δ H ,单位:kJ/mol(或 kJ·mol - 1 )
【微点拨】
①焓(H)是与内能有关的物理量,内能描述的是物质所具有的能量,是物质固有的性质之一。不同的物质,其
焓不同;相同的物质,如果温度或压强不同,物质的状态不同,其焓也会不同
②焓、焓变、反应热代表的意义不同;焓只有正值,而焓变有正值、负值之分
2、化学反应过程中能量变化的原因
(1)从反应热的量化参数——键能的角度分析:化学反应是旧键断裂,新键生成的反应,两者吸收和释放能量的
差异表现为反应能量的变化。化学键的断裂和形成时吸收和放出的能量差别是化学反应伴随能量变化的本质
原因
化学反应的过程
新键生成释放的能量大于旧键断裂吸收的能量,则反应放热
规律
新键生成释放的能量小于旧键断裂吸收的能量,则反应吸热
(2)从反应物和生成物焓(H)的变化角度分析
反应物总焓大于生成物总焓,反应放热
反应物总焓小于生成物总焓,反应吸热
3、符号的规定:规定放热反应的∆H为“—””吸热反应的∆H为“+”,即:放热反应的∆H<0,吸热反应
的∆H>0【微点拨】
①放热反应和吸热反应是针对化学反应而言,物质三态之间的变化有能量的变化,但属物理变化,故不属于
放热反应或吸热反应
②放热反应和吸热反应取决于反应物和生成物总能量的相对大小,与反应条件并无必然的关系
③∆H不仅应用在化学反应中,它还应用于任何有能量变化的过程,如:HO(l)→HO(g) ∆H>0;共价键的
2 2
断裂,吸收能量,∆H>0;原子间通过共用电子对形成共价键,放出能量,∆H<0
【对点训练1】
1、下列说法中正确的是( )
A.化学反应中的能量变化都表现为热量变化
B.焓变是指1 mol物质参加反应时的能量变化
C.在一个确定的化学反应关系中,反应物的总焓与生成物的总焓一定不同
D.在一个确定的化学反应关系中,反应物的总焓总是高于生成物的总焓
2、下列说法不正确的是( )
A.恒压条件下的焓变在数值上等于变化过程中的热效应 B.焓变的符号是ΔH
C.焓变的单位通常是kJ·mol-1 D.硝酸铵溶于水是吸热反应
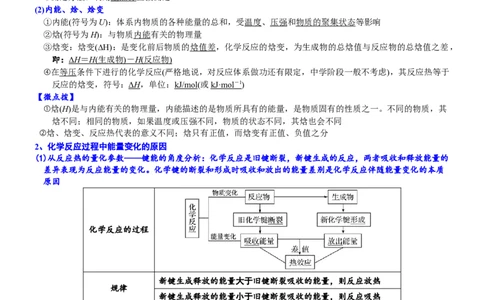
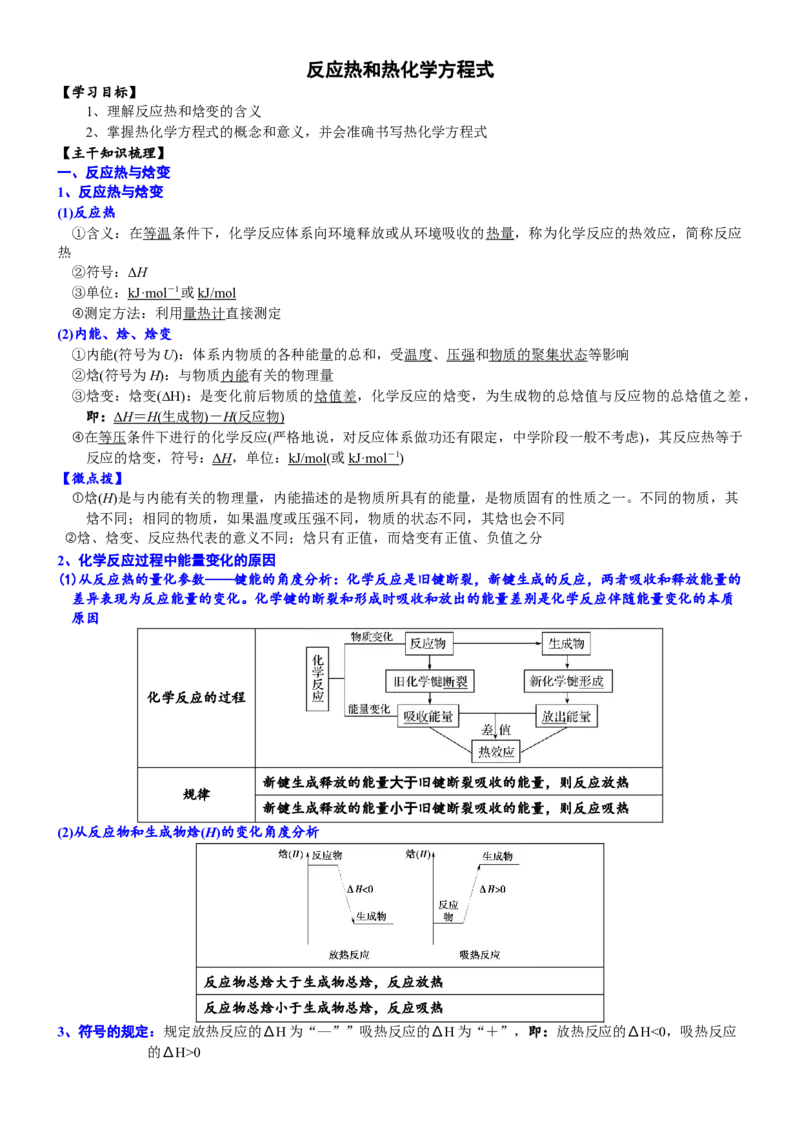
3、由图分析,下列说法正确的是( )
A.A→B+C和B+C→A两个反应吸收或放出的能量不等 B.A→B+C ΔH<0
C.A具有的焓高于B和C具有的焓的总和 D.A→B+C ΔH>0,则B+C→A ΔH<0
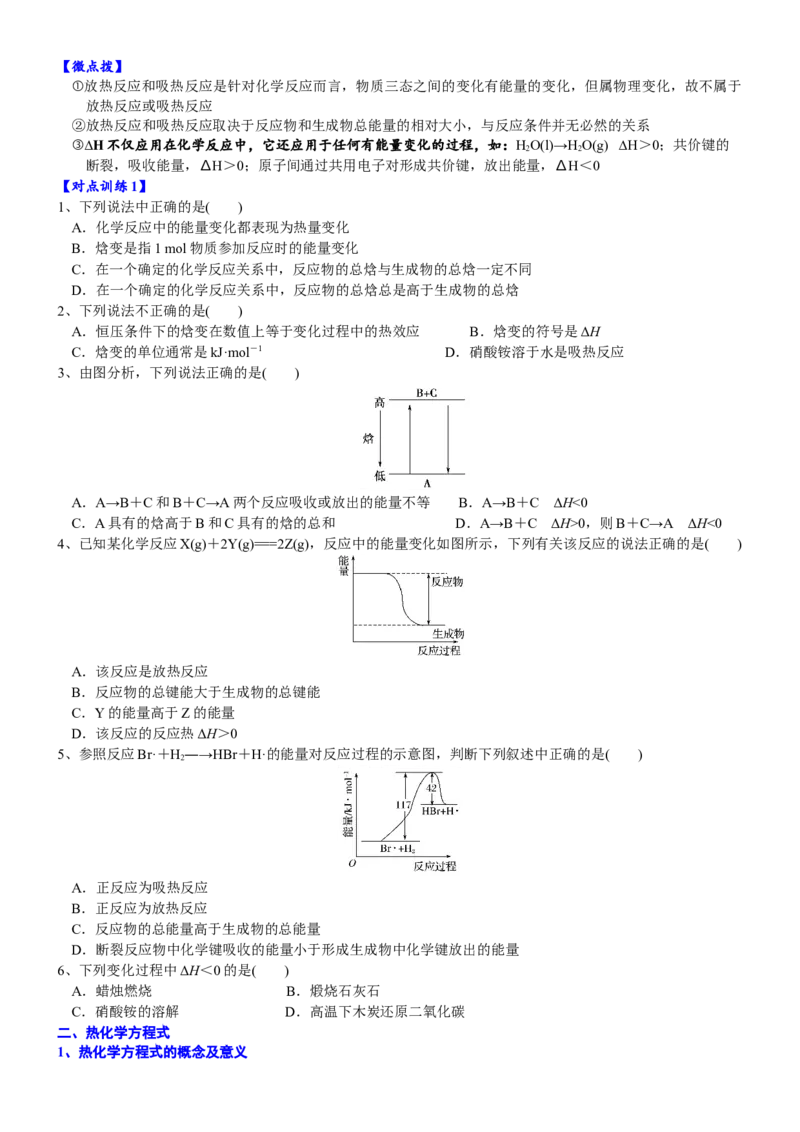
4、已知某化学反应X(g)+2Y(g)===2Z(g),反应中的能量变化如图所示,下列有关该反应的说法正确的是( )
A.该反应是放热反应
B.反应物的总键能大于生成物的总键能
C.Y的能量高于Z的能量
D.该反应的反应热ΔH>0
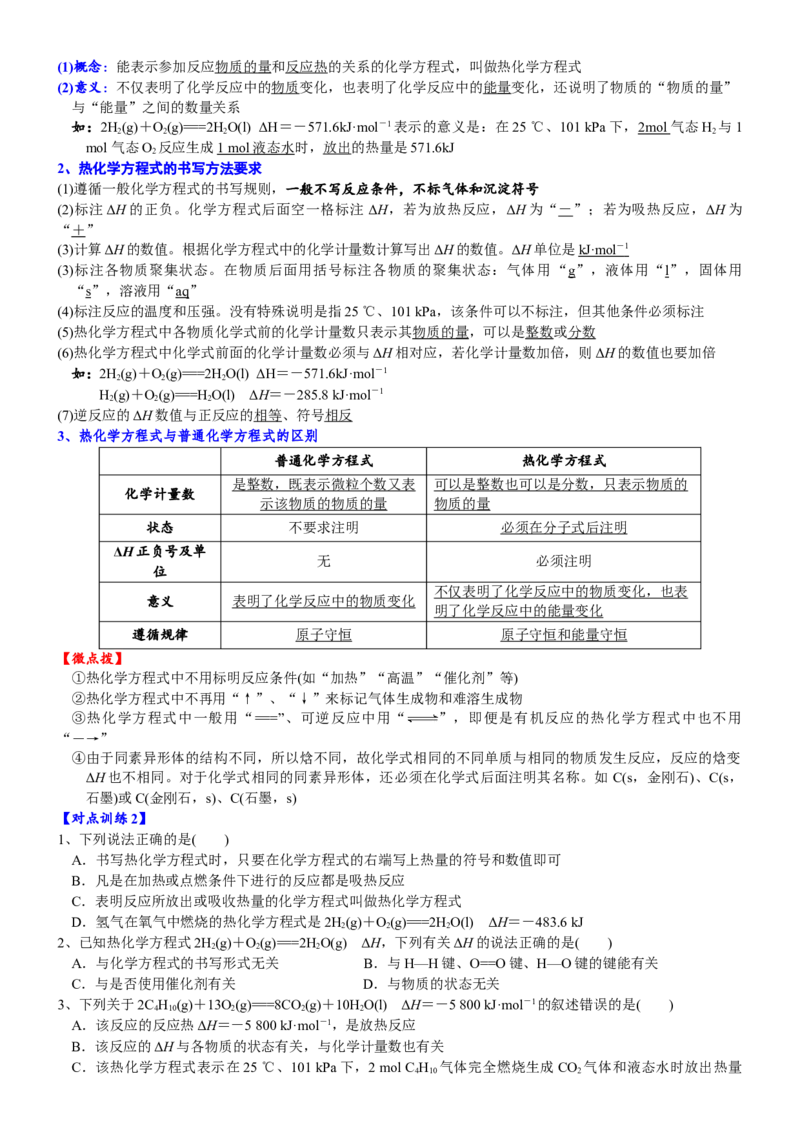
5、参照反应Br·+H―→HBr+H·的能量对反应过程的示意图,判断下列叙述中正确的是( )
2
A.正反应为吸热反应
B.正反应为放热反应
C.反应物的总能量高于生成物的总能量
D.断裂反应物中化学键吸收的能量小于形成生成物中化学键放出的能量
6、下列变化过程中ΔH<0的是( )
A.蜡烛燃烧 B.煅烧石灰石
C.硝酸铵的溶解 D.高温下木炭还原二氧化碳
二、热化学方程式
1、热化学方程式的概念及意义(1)概念:能表示参加反应物质的量和反应热的关系的化学方程式,叫做热化学方程式
(2)意义:不仅表明了化学反应中的物质变化,也表明了化学反应中的能量变化,还说明了物质的“物质的量”
与“能量”之间的数量关系
如:2H(g)+O(g)===2H O(l) ΔH=-571.6kJ·mol-1表示的意义是:在25 ℃、101 kPa下, 2 mol 气态H 与1
2 2 2 2
mol 气态O 反应生成 1 mol 液态水 时,放出的热量是571.6kJ
2
2、热化学方程式的书写方法要求
(1)遵循一般化学方程式的书写规则,一般不写反应条件,不标气体和沉淀符号
(2)标注ΔH的正负。化学方程式后面空一格标注 ΔH,若为放热反应,ΔH为“-”;若为吸热反应,ΔH为
“+”
(3)计算ΔH的数值。根据化学方程式中的化学计量数计算写出ΔH的数值。ΔH单位是 kJ·mol - 1
(3)标注各物质聚集状态。在物质后面用括号标注各物质的聚集状态:气体用“g”,液体用“l”,固体用
“s”,溶液用“aq”
(4)标注反应的温度和压强。没有特殊说明是指25 ℃、101 kPa,该条件可以不标注,但其他条件必须标注
(5)热化学方程式中各物质化学式前的化学计量数只表示其物质的量,可以是整数或分数
(6)热化学方程式中化学式前面的化学计量数必须与ΔH相对应,若化学计量数加倍,则ΔH的数值也要加倍
如:2H(g)+O(g)===2H O(l) ΔH=-571.6kJ·mol-1
2 2 2
H(g)+O(g)===HO(l) ΔH=-285.8 kJ·mol-1
2 2 2
(7)逆反应的ΔH数值与正反应的相等、符号相反
3、热化学方程式与普通化学方程式的区别
普通化学方程式 热化学方程式
是整数,既表示微粒个数又表 可以是整数也可以是分数,只表示物质的
化学计量数
示该物质的物质的量 物质的量
状态 不要求注明 必须在分子式后注明
ΔH正负号及单
无 必须注明
位
不仅表明了化学反应中的物质变化,也表
意义 表明了化学反应中的物质变化
明了化学反应中的能量变化
遵循规律 原子守恒 原子守恒和能量守恒
【微点拨】
①热化学方程式中不用标明反应条件(如“加热”“高温”“催化剂”等)
②热化学方程式中不再用“↑”、“↓”来标记气体生成物和难溶生成物
③热化学方程式中一般用“===”、可逆反应中用“ ”,即便是有机反应的热化学方程式中也不用
“―→”
④由于同素异形体的结构不同,所以焓不同,故化学式相同的不同单质与相同的物质发生反应,反应的焓变
ΔH也不相同。对于化学式相同的同素异形体,还必须在化学式后面注明其名称。如 C(s,金刚石)、C(s,
石墨)或C(金刚石,s)、C(石墨,s)
【对点训练2】
1、下列说法正确的是( )
A.书写热化学方程式时,只要在化学方程式的右端写上热量的符号和数值即可
B.凡是在加热或点燃条件下进行的反应都是吸热反应
C.表明反应所放出或吸收热量的化学方程式叫做热化学方程式
D.氢气在氧气中燃烧的热化学方程式是2H(g)+O(g)===2HO(l) ΔH=-483.6 kJ
2 2 2
2、已知热化学方程式2H(g)+O(g)===2HO(g) ΔH,下列有关ΔH的说法正确的是( )
2 2 2
A.与化学方程式的书写形式无关 B.与H—H键、O==O键、H—O键的键能有关
C.与是否使用催化剂有关 D.与物质的状态无关
3、下列关于2C H (g)+13O(g)===8CO(g)+10HO(l) ΔH=-5 800 kJ·mol-1的叙述错误的是( )
4 10 2 2 2
A.该反应的反应热ΔH=-5 800 kJ·mol-1,是放热反应
B.该反应的ΔH与各物质的状态有关,与化学计量数也有关
C.该热化学方程式表示在25 ℃、101 kPa下,2 mol C H 气体完全燃烧生成CO 气体和液态水时放出热量
4 10 25800kJ
D.该反应表明2 mol丁烷燃烧时一定会放出5 800 kJ的热量
4、下列对H(g)+Cl(g)===2HCl(g) ΔH(298 K)=-184.6 kJ·mol-1的叙述正确的是( )
2 2
A.1分子H 和Cl 反应,放出热量184.6 kJ
2 2
B.1 mol H (g)完全反应生成2 mol HCl(g),放出的热量为184.6 kJ
2
C.在101 kPa、25 ℃的条件下,1 mol H (g)和1 mol Cl (g)完全反应生成2 mol HCl(g)放出的热量为184.6 kJ
2 2
D.在101 kPa、25 ℃的条件下,1 mol H (g)和1 mol Cl (g)完全反应生成2 mol HCl(g)吸收的热量为184.6 kJ
2 2
三、焓变(ΔH)的计算方法
1、焓变与物质化学键断裂与形成的关系:ΔH=反应物总键能-生成物总键能
2、焓变与反应物、生成物能量的关系:ΔH=生成物的总能量-反应物的总能量=H(生成物)-H(反应物)
常见物质中的化学键数目
CO(C===O
物质 2 CH(C-H) P(P-P) SiO(Si-O) 石墨 金刚石 S(S-S) Si
) 4 4 2 8
键数 2 4 6 4 1.5 2 8 2
【对点训练3】
1、氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量。在反应过程中,断裂1 mol H 中的化学键消耗
2
的能量为Q kJ,断裂1 mol F 中的化学键消耗的能量为Q kJ,形成1 mol HF中的化学键释放的能量为 Q
1 2 2 3
kJ。下列关系式中正确的是( )
A.Q+Q<2Q B.Q+Q>2Q C.Q+Q<Q D.Q+Q>Q
1 2 3 1 2 3 1 2 3 1 2 3
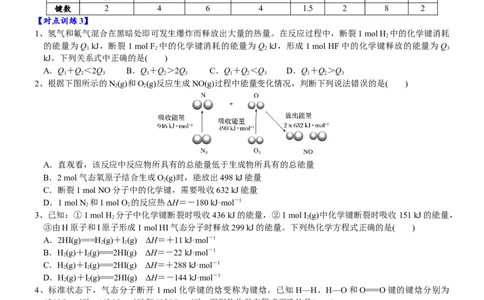
2、根据下图所示的N(g)和O(g)反应生成NO(g)过程中能量变化情况,判断下列说法错误的是( )
2 2
A.直观看,该反应中反应物所具有的总能量低于生成物所具有的总能量
B.2 mol气态氧原子结合生成O(g)时,能放出498 kJ能量
2
C.断裂1 mol NO分子中的化学键,需要吸收632 kJ能量
D.1 mol N 和1 mol O 的反应热ΔH=-180 kJ·mol-1
2 2
3、已知:①1 mol H 分子中化学键断裂时吸收436 kJ的能量,②1 mol I (g)中化学键断裂时吸收151 kJ的能量,
2 2
③由H原子和I原子形成1 mol HI气态分子时释放299 kJ的能量。下列热化学方程式正确的是( )
A.2HI(g)===H(g)+I(g) ΔH=+11 kJ·mol-1
2 2
B.H(g)+I(g)===2HI(g) ΔH=-22 kJ·mol-1
2 2
C.H(g)+I(g)===2HI(g) ΔH=+288 kJ·mol-1
2 2
D.H(g)+I(g)===2HI(g) ΔH=-144 kJ·mol-1
2 2
4、标准状态下,气态分子断开1 mol化学键的焓变称为键焓。已知 H—H、H—O和O===O键的键焓分别为
436 kJ·mol-1、463 kJ·mol-1和495 kJ·mol-1,下列热化学方程式正确的是( )
A.HO(g)===H(g)+O(g) ΔH=-485 kJ·mol-1
2 2 2
B.HO(g)===H(g)+O(g) ΔH=+485 kJ·mol-1
2 2 2
C.2H(g)+O(g)===2HO(g) ΔH=+485 kJ·mol-1
2 2 2
D.2H(g)+O(g)===2HO(g) ΔH=-485 kJ·mol-1
2 2 2
【课后作业】
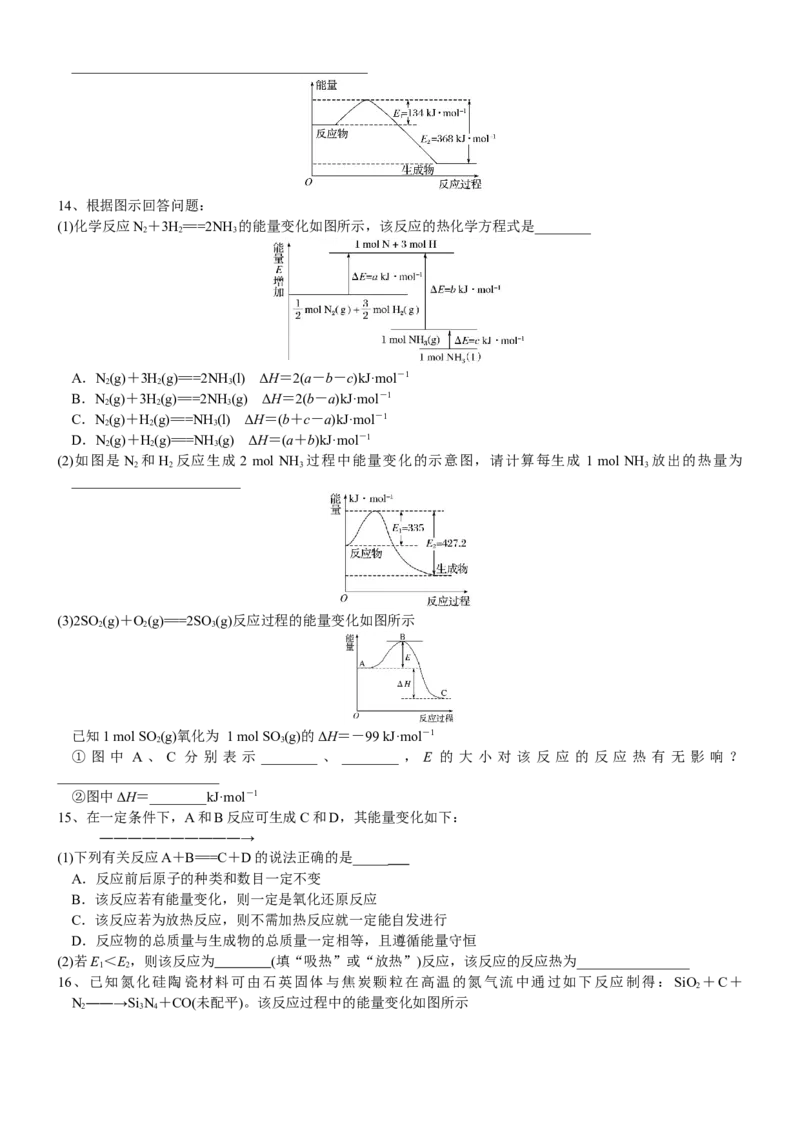
1、下列图示变化为吸热反应的是( )2、一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中•和代表不同元素的原子。下列关于此
反应说法错误的是( )
A.一定属于吸热反应 B.一定属于可逆反应
C.一定属于氧化还原反应 D.一定属于分解反应
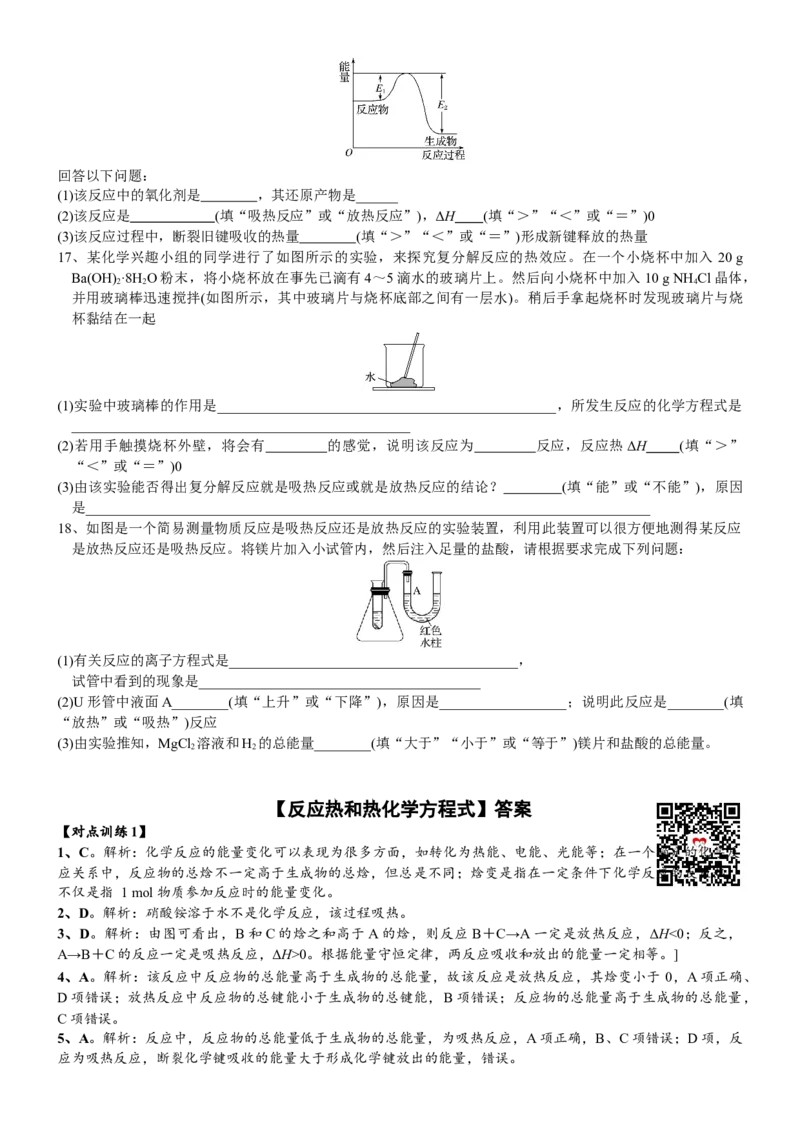
3、工业合成氨的反应为N(g)+3H(g) 2NH (g),已知下列化学键的键能(拆开或形成1 mol化学键所吸收或
2 2 3
放出的热量),下列说法正确的是( )
化学键 键能/kJ·mol-1
H—H 436
N—H 391
N≡N 946
A.该反应为吸热反应 B.该反应中反应物的总能量高于生成物的总能量
C.反应热ΔH=92 kJ·mol-1 D.生成1 mol NH 放出92 kJ热量
3
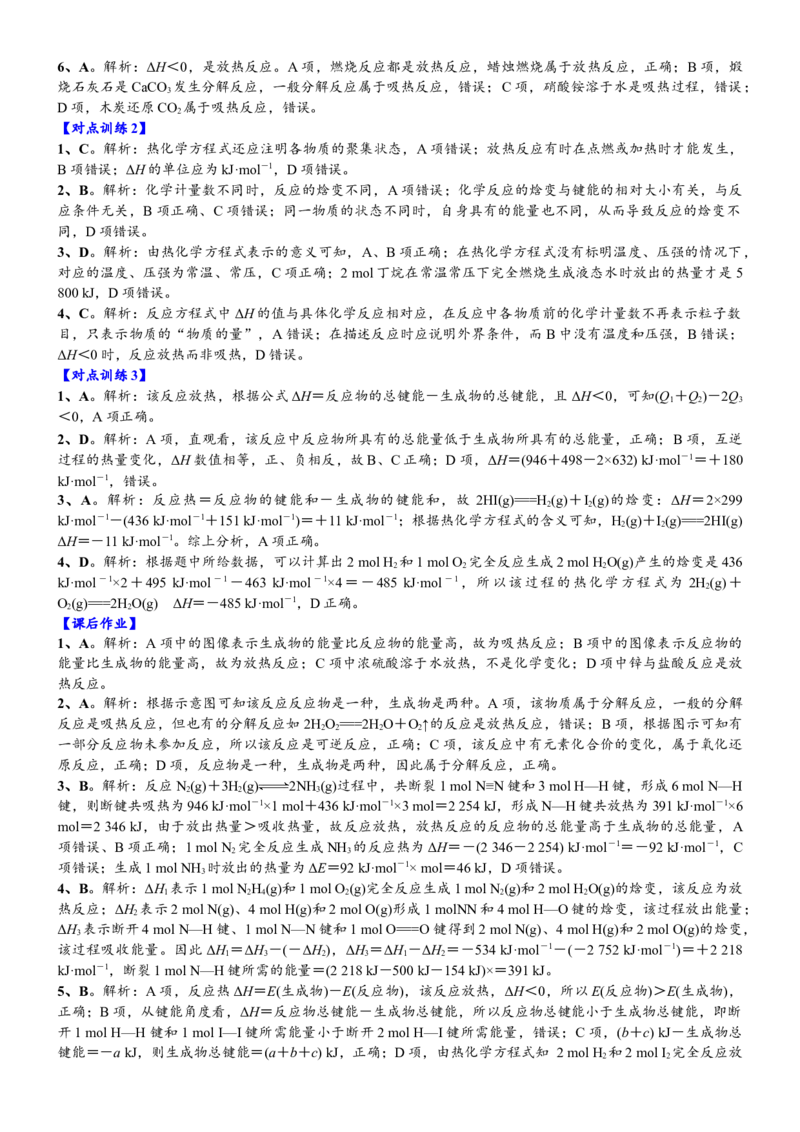
4、肼(H N-NH )是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂 1 mol化学键所需的能量
2 2
(kJ):N≡N为942、O===O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是( )
A.194 B.391 C.516 D.658
5、H 和I 在一定条件下发生反应:H(g)+I(g)2HI(g) ΔH=-a kJ·mol-1。已知:
2 2 2 2
(a、b、c均大于零)
下列说法不正确的是( )
A.该反应中反应物的总能量高于生成物的总能量
B.断开1 mol H—H键和1 mol I—I键所需能量大于断开2 mol H—I键所需能量
C.断开2 mol H—I键所需能量约为(a+b+c) kJ
D.向密闭容器中加入2 mol H 和2 mol I ,充分反应后放出的热量小于2a kJ
2 2
6、已知2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1,则下列关于热化学方程式2HO(l)===2H(g)+O(g)
2 2 2 2 2 2
的ΔH的说法中正确的是( )
A.方程式中的化学计量数表示分子数 B.该反应的ΔH大于零
C.该反应的ΔH=-571.6 kJ·mol-1 D.该反应可表示36 g水分解时的热效应7、 下列热化学方程式书写正确的是( )
A.2SO +O 2SO ΔH=-196.6 kJ·mol-1
2 2 3
B.H(g)+O(g)===HO(l) ΔH=-285.8 kJ·mol-1
2 2 2
C.2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ
2 2 2
D.C(s)+O(g)=== CO (g) ΔH=+393.5 kJ·mol-1
2 2
8、NH 是一种高效清洁的火箭燃料。0.25 mol N H(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下
2 4 2 4
列热化学方程式中正确的是( )
A.NH(g)+O(g)===N(g)+HO(g) ΔH=+267 kJ·mol-1
2 4 2 2 2
B.NH(g)+O(g)===N(g)+2HO(g) ΔH=-534 kJ·mol-1
2 4 2 2 2
C.NH(g)+O(g)===N(g)+2HO(g) ΔH=+534 kJ·mol-1
2 4 2 2 2
D.NH(g)+O(g)===N(g)+2HO(l) ΔH=-133.5 kJ·mol-1
2 4 2 2 2
9、标准状态下,气态分子断开1 mol化学键的焓变称为键焓。已知H—H、H—O和O==O键的键焓分别为436
kJ/mol、463 kJ/mol和495kJ/mol,下列热化学方程式正确的是( )
A.HO(g)===H(g)+O(g) ΔH=-485 kJ·mol-1
2 2 2
B.HO(g)===H(g)+O(g) ΔH=+485 kJ·mol-1
2 2 2
C.2H(g)+O(g)===2HO(g) ΔH=+485 kJ·mol-1
2 2 2
D.2H(g)+O(g)===2HO(g) ΔH=-485 kJ·mol-1
2 2 2
10、下列关于热化学方程式的描述或结论正确的是( )
选项 已知热化学方程式 有关描述或结论
A 3O(g)===2O(g) ΔH=+242.6 kJ·mol-1 氧气的能量比臭氧的高
2 3
B C H(g)===C H(g)+CH(g) ΔH>0 丙烷比乙烯稳定
3 8 2 4 4
含10.0 g NaOH的稀溶液与稀盐酸
C NaOH(aq)+HCl(aq)===NaCl(aq)+HO(l) ΔH=-57.3kJ/mol
2 完全中和,放出的热量约为14.3 kJ
①2C(石墨,s)+2O(g)===2CO(g) ΔH;
D 2 2 1 ΔH>ΔH
②2C(石墨,s)+O(g)===2CO(g) ΔH 1 2
2 2
11、依据事实,写出下列反应的热化学方程式。
(1)1 mol N (g)与适量H(g)反应,生成2 mol NH (g),放出92.4 kJ热量
2 2 3
__________________________________________________________
(2)1 mol Cu(s)与适量O(g)反应,生成CuO(s),放出157 kJ热量
2
__________________________________________________________
(3)23 g C HO(l)和一定量的氧气混合点燃,恰好完全反应,生成CO(g)和HO(l),放出683.5 kJ的热量。
2 6 2 2
____________________________________________________________
12、已知两个氢气燃烧生成水的热化学方程式:
H(g)+O(g)===HO(g) ΔH=a kJ·mol-1
2 2 2
2H(g)+O(g)===2HO(l) ΔH=b kJ·mol-1
2 2 2
请回答下列问题(|b|表示b的绝对值):
(1)若2 mol H (g)完全燃烧生成水蒸气,则放出的热量 (填“>”“<”或“=”)|b| kJ
2
(2)反应热的关系:2a (填“>”“<”或“=”)b
(3)若已知H(g)+O(g)===HO(g) ΔH=-242 kJ·mol-1,且氧气中1 mol O==O键完全断裂时吸收热量496 kJ,
2 2 2
水蒸气中1 mol H—O键形成时放出热量463 kJ,则氢气中1 mol H—H键断裂时吸收的热量为______
13、请分析下列有关NO、NO 的内容,然后填空。
2
(1)下图所示为N(g)和O(g)生成NO(g)过程中的能量变化。
2 2
由上图写出N(g)和O(g)生成NO(g)的热化学方程式:___________________________________________
2 2
(2)下图是1 mol NO 和CO反应生成CO 和NO过程中能量变化示意图,请写出NO 和CO反应的热化学方程式
2 2 2__________________________________________
14、根据图示回答问题:
(1)化学反应N+3H===2NH 的能量变化如图所示,该反应的热化学方程式是________
2 2 3
A.N(g)+3H(g)===2NH (l) ΔH=2(a-b-c)kJ·mol-1
2 2 3
B.N(g)+3H(g)===2NH (g) ΔH=2(b-a)kJ·mol-1
2 2 3
C.N(g)+H(g)===NH (l) ΔH=(b+c-a)kJ·mol-1
2 2 3
D.N(g)+H(g)===NH (g) ΔH=(a+b)kJ·mol-1
2 2 3
(2)如图是 N 和H 反应生成 2 mol NH 过程中能量变化的示意图,请计算每生成 1 mol NH 放出的热量为
2 2 3 3
________________________
(3)2SO (g)+O(g)===2SO (g)反应过程的能量变化如图所示
2 2 3
已知1 mol SO (g)氧化为 1 mol SO (g)的ΔH=-99 kJ·mol-1
2 3
① 图 中 A 、 C 分 别 表 示 ________ 、 ________ , E 的 大 小 对 该 反 应 的 反 应 热 有 无 影 响 ?
_______________________
②图中ΔH=________kJ·mol-1
15、在一定条件下,A和B反应可生成C和D,其能量变化如下:
――――――――――→
(1)下列有关反应A+B===C+D的说法正确的是_____
A.反应前后原子的种类和数目一定不变
B.该反应若有能量变化,则一定是氧化还原反应
C.该反应若为放热反应,则不需加热反应就一定能自发进行
D.反应物的总质量与生成物的总质量一定相等,且遵循能量守恒
(2)若E<E,则该反应为 (填“吸热”或“放热”)反应,该反应的反应热为________________
1 2
16、已知氮化硅陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:SiO +C+
2
N――→Si N+CO(未配平)。该反应过程中的能量变化如图所示
2 3 4回答以下问题:
(1)该反应中的氧化剂是 ,其还原产物是______
(2)该反应是 (填“吸热反应”或“放热反应”),ΔH (填“>”“<”或“=”)0
(3)该反应过程中,断裂旧键吸收的热量 (填“>”“<”或“=”)形成新键释放的热量
17、某化学兴趣小组的同学进行了如图所示的实验,来探究复分解反应的热效应。在一个小烧杯中加入 20 g
Ba(OH) ·8H O粉末,将小烧杯放在事先已滴有4~5滴水的玻璃片上。然后向小烧杯中加入10 g NH Cl晶体,
2 2 4
并用玻璃棒迅速搅拌(如图所示,其中玻璃片与烧杯底部之间有一层水)。稍后手拿起烧杯时发现玻璃片与烧
杯黏结在一起
(1)实验中玻璃棒的作用是________________________________________________,所发生反应的化学方程式是
________________________________________________
(2)若用手触摸烧杯外壁,将会有 的感觉,说明该反应为 反应,反应热ΔH (填“>”
“<”或“=”)0
(3)由该实验能否得出复分解反应就是吸热反应或就是放热反应的结论? (填“能”或“不能”),原因
是________________________________________________________________________________
18、如图是一个简易测量物质反应是吸热反应还是放热反应的实验装置,利用此装置可以很方便地测得某反应
是放热反应还是吸热反应。将镁片加入小试管内,然后注入足量的盐酸,请根据要求完成下列问题:
(1)有关反应的离子方程式是_________________________________________,
试管中看到的现象是________________________________________
(2)U形管中液面A________(填“上升”或“下降”),原因是__________________;说明此反应是________(填
“放热”或“吸热”)反应
(3)由实验推知,MgCl 溶液和H 的总能量________(填“大于”“小于”或“等于”)镁片和盐酸的总能量。
2 2
【反应热和热化学方程式】答案
【对点训练1】
1、C。解析:化学反应的能量变化可以表现为很多方面,如转化为热能、电能、光能等;在一个确定的化学反
应关系中,反应物的总焓不一定高于生成物的总焓,但总是不同;焓变是指在一定条件下化学反应的反应热,
不仅是指 1 mol 物质参加反应时的能量变化。
2、D。解析:硝酸铵溶于水不是化学反应,该过程吸热。
3、D。解析:由图可看出,B和C的焓之和高于A的焓,则反应B+C→A一定是放热反应,ΔH<0;反之,
A→B+C的反应一定是吸热反应,ΔH>0。根据能量守恒定律,两反应吸收和放出的能量一定相等。]
4、A。解析:该反应中反应物的总能量高于生成物的总能量,故该反应是放热反应,其焓变小于 0,A项正确、
D项错误;放热反应中反应物的总键能小于生成物的总键能,B项错误;反应物的总能量高于生成物的总能量,
C项错误。
5、A。解析:反应中,反应物的总能量低于生成物的总能量,为吸热反应,A项正确,B、C项错误;D项,反
应为吸热反应,断裂化学键吸收的能量大于形成化学键放出的能量,错误。6、A。解析:ΔH<0,是放热反应。A项,燃烧反应都是放热反应,蜡烛燃烧属于放热反应,正确;B项,煅
烧石灰石是CaCO 发生分解反应,一般分解反应属于吸热反应,错误;C项,硝酸铵溶于水是吸热过程,错误;
3
D项,木炭还原CO 属于吸热反应,错误。
2
【对点训练2】
1、C。解析:热化学方程式还应注明各物质的聚集状态,A项错误;放热反应有时在点燃或加热时才能发生,
B项错误;ΔH的单位应为kJ·mol-1,D项错误。
2、B。解析:化学计量数不同时,反应的焓变不同,A项错误;化学反应的焓变与键能的相对大小有关,与反
应条件无关,B项正确、C项错误;同一物质的状态不同时,自身具有的能量也不同,从而导致反应的焓变不
同,D项错误。
3、D。解析:由热化学方程式表示的意义可知,A、B项正确;在热化学方程式没有标明温度、压强的情况下,
对应的温度、压强为常温、常压,C项正确;2 mol丁烷在常温常压下完全燃烧生成液态水时放出的热量才是5
800 kJ,D项错误。
4、C。解析:反应方程式中ΔH的值与具体化学反应相对应,在反应中各物质前的化学计量数不再表示粒子数
目,只表示物质的“物质的量”,A错误;在描述反应时应说明外界条件,而B中没有温度和压强,B错误;
ΔH<0时,反应放热而非吸热,D错误。
【对点训练3】
1、A。解析:该反应放热,根据公式ΔH=反应物的总键能-生成物的总键能,且ΔH<0,可知(Q +Q)-2Q
1 2 3
<0,A项正确。
2、D。解析:A项,直观看,该反应中反应物所具有的总能量低于生成物所具有的总能量,正确;B项,互逆
过程的热量变化,ΔH数值相等,正、负相反,故B、C正确;D项,ΔH=(946+498-2×632) kJ·mol-1=+180
kJ·mol-1,错误。
3、A。解析:反应热=反应物的键能和-生成物的键能和,故 2HI(g)===H (g)+I(g)的焓变:ΔH=2×299
2 2
kJ·mol-1-(436 kJ·mol-1+151 kJ·mol-1)=+11 kJ·mol-1;根据热化学方程式的含义可知,H(g)+I(g)===2HI(g)
2 2
ΔH=-11 kJ·mol-1。综上分析,A项正确。
4、D。解析:根据题中所给数据,可以计算出2 mol H 和1 mol O 完全反应生成2 mol H O(g)产生的焓变是436
2 2 2
kJ·mol-1×2+495 kJ·mol-1-463 kJ·mol-1×4=-485 kJ·mol-1,所以该过程的热化学方程式为 2H(g)+
2
O(g)===2H O(g) ΔH=-485 kJ·mol-1,D正确。
2 2
【课后作业】
1、A。解析:A项中的图像表示生成物的能量比反应物的能量高,故为吸热反应;B项中的图像表示反应物的
能量比生成物的能量高,故为放热反应;C项中浓硫酸溶于水放热,不是化学变化;D项中锌与盐酸反应是放
热反应。
2、A。解析:根据示意图可知该反应反应物是一种,生成物是两种。A项,该物质属于分解反应,一般的分解
反应是吸热反应,但也有的分解反应如2HO===2H O+O↑的反应是放热反应,错误;B项,根据图示可知有
2 2 2 2
一部分反应物未参加反应,所以该反应是可逆反应,正确;C项,该反应中有元素化合价的变化,属于氧化还
原反应,正确;D项,反应物是一种,生成物是两种,因此属于分解反应,正确。
3、B。解析:反应N(g)+3H(g) 2NH (g)过程中,共断裂1 mol N≡N键和3 mol H—H键,形成6 mol N—H
2 2 3
键,则断键共吸热为946 kJ·mol-1×1 mol+436 kJ·mol-1×3 mol=2 254 kJ,形成N—H键共放热为391 kJ·mol-1×6
mol=2 346 kJ,由于放出热量>吸收热量,故反应放热,放热反应的反应物的总能量高于生成物的总能量,A
项错误、B项正确;1 mol N 完全反应生成NH 的反应热为ΔH=-(2 346-2 254) kJ·mol-1=-92 kJ·mol-1,C
2 3
项错误;生成1 mol NH 时放出的热量为ΔE=92 kJ·mol-1× mol=46 kJ,D项错误。
3
4、B。解析:ΔH 表示1 mol N H(g)和1 mol O (g)完全反应生成1 mol N (g)和2 mol H O(g)的焓变,该反应为放
1 2 4 2 2 2
热反应;ΔH 表示2 mol N(g)、4 mol H(g)和2 mol O(g)形成1 molNN和4 mol H—O键的焓变,该过程放出能量;
2
ΔH 表示断开4 mol N—H键、1 mol N—N键和1 mol O===O 键得到2 mol N(g)、4 mol H(g)和2 mol O(g)的焓变,
3
该过程吸收能量。因此ΔH =ΔH -(-ΔH),ΔH =ΔH -ΔH =-534 kJ·mol-1-(-2 752 kJ·mol-1)=+2 218
1 3 2 3 1 2
kJ·mol-1,断裂1 mol N—H键所需的能量=(2 218 kJ-500 kJ-154 kJ)×=391 kJ。
5、B。解析:A项,反应热ΔH=E(生成物)-E(反应物),该反应放热,ΔH<0,所以E(反应物)>E(生成物),
正确;B项,从键能角度看,ΔH=反应物总键能-生成物总键能,所以反应物总键能小于生成物总键能,即断
开1 mol H—H 键和1 mol I—I键所需能量小于断开2 mol H—I键所需能量,错误;C项,(b+c) kJ-生成物总
键能=-a kJ,则生成物总键能=(a+b+c) kJ,正确;D项,由热化学方程式知 2 mol H 和2 mol I 完全反应放
2 2出的热量为2a kJ,但该反应是可逆反应,反应不能完全进行到底,所以放出的热量小于2a kJ,正确。
6、B。解析:在书写热化学方程式时,若反应物和生成物对换,则 ΔH的符号相反,数值不变,故B项正确,
C项不正确;D项未注明水为液态。
7、B。解析:A项中反应物和生成物都未标明聚集状态;C项中ΔH的单位不正确;D项中为放热反应,ΔH符
号应为“-”。
8、B。解析:该反应为放热反应,A、C错误,0.25 mol NH(g)完全燃烧生成氮气和气态水,放出133.5 kJ热量,
2 4
则1 mol N H(g)完全燃烧生成氮气和气态水放出热量为534 kJ,B项正确、D项错误。
2 4
9、D。解析:根据题中所给数据,可以计算出2 mol H (g)和1 mol O (g)完全反应生成2 mol H O(g)产生的焓变
2 2 2
是436 kJ·mol-1×2+495 kJ·mol-1-463 kJ·mol-1×4=-485 kJ·mol-1,所以该过程的热化学方程式为 2H(g)+
2
O(g)===2H O(g) ΔH=-485 kJ·mol-1,D正确。
2 2
10、C。解析:由给出的热化学方程式可知,该反应为吸热反应,故臭氧的能量比氧气的高,A项错误;丙烷
吸收能量,分解为乙烯和甲烷两种物质,无法比较反应物与生成物之一的稳定性,B项错误;由已知热化学方程
式可知1 mol NaOH与HCl完全反应放出57.3 kJ热量,故含10.0 g NaOH的稀溶液与稀盐酸完全反应放出的热量
为14.325 kJ≈14.3 kJ,C项正确;ΔH 、ΔH 均小于0,燃烧越充分放出的热量越多,ΔH越小,故ΔH <ΔH ,D
1 2 1 2
项错误。
11、(1)N (g)+3H(g) 2NH (g) ΔH=-92.4 kJ·mol-1
2 2 3
(2)Cu(s)+O(g)===CuO(s) ΔH=-157 kJ·mol-1
2
(3)C HO(l)+3O(g)===2CO(g)+3HO(l) ΔH=-1 367 kJ·mol-1
2 6 2 2 2
解析:此类题的思路:首先根据题意写出物质的变化过程,如(1)中:N(g)+3H(g)2NH(g),并定N 前化学
2 2 3 2
计量数为1,此时的ΔH即为-92.4 kJ·mol-1,再在前部分的基础上加上ΔH=-92.4 kJ·mol-1即可。
12、(1)< (2)> (3)436 kJ
解析:(1)水蒸气转化为液态水是放热的过程,故2 mol H (g)完全燃烧生成水蒸气,放出的热量小于|b|kJ。
2
(2)由于a和b均小于0,两个反应的化学计量数相同时,生成液态水放出的热量大于生成气态水放出的热量,
故2a>b。(3)ΔH=断裂旧化学键吸收的总能量-形成新化学键放出的总能量,设断裂1 mol H—H键时吸收的热
量为x kJ,即-242=x+496×-463×2,解得x=436。
13、(1)N (g)+O(g)===2NO(g) ΔH=+180 kJ·mol-1
2 2
(2)NO(g)+CO(g)===CO(g)+NO(g) ΔH=-234 kJ·mol-1
2 2
解析:(1)反应热等于断键吸收的能量与成键放出的能量的差值,则根据示意图可知反应热=946 kJ·mol-1+498
kJ·mol-1-2×632 kJ·mol-1=180 kJ·mol-1,热化学方程式为N(g)+O(g)===2NO(g) ΔH=+180 kJ·mol-1。
2 2
(2)根据图像可知,反应物的总能量高于生成物的总能量,因此是放热反应,则反应热 ΔH=E -E =134 kJ·mol
1 2
-1-368 kJ·mol-1=-234 kJ·mol-1。
14、(1)A
(2)46.1 kJ
(3)①反应物总能量 生成物总能量 无影响 ②-198
解析:(1)由图可以看出,mol N(g)和 mol H(g)的化学键断裂吸收的能量为a kJ,形成1 mol NH (g)放出的能量
2 2 3
为b kJ,所以N(g)+H(g)===NH(g) ΔH=(a-b)kJ·mol-1,而1 mol 的NH (g)转化为1 mol 的NH (l)放出的热
2 2 3 3 3
量为c kJ,所以有:N(g)+H(g)===NH(l) ΔH=(a-b-c)kJ·mol-1,即:N(g)+3H(g)===2NH(l) ΔH=2(a
2 2 3 2 2 3
-b-c)kJ·mol-1。
(2)由题图可知生成2 mol NH 放出热量为427.2 kJ-335 kJ=92.2 kJ,则生成1 mol NH 放出热量为46.1 kJ。
3 3
(3)①由图示可知,A表示反应物总能量,C表示生成物总能量,E值不影响A、C的能量值。故能量E的大小
对该反应的反应热无影响。②ΔH对应2 mol SO (g)转化为2 mol SO (g)的焓变,其值为2×(-99 kJ·mol-1)=-
2 3
198 kJ·mol-1。
15、(1)AD
(2)吸热 ΔH=(E -E ) kJ·mol-1
2 1
解析:(1)每个化学反应都遵循质量守恒和能量守恒,原子数目和种类不会改变,A、D项正确;任何化学反应
都伴随着能量变化,不一定为氧化还原反应,B项错误;某一反应是放热反应还是吸热反应,与反应条件无关,
加热是为了使旧化学键断裂,引发化学反应,C项错误。(2)若E <E ,反应吸收能量,ΔH=(E -E) kJ·mol-1
1 2 2 1
>0;相反若E>E,反应放出能量,ΔH=(E-E) kJ·mol-1<0。
1 2 2 1
16、(1)N Si N
2 3 4(2)放热反应 <
(3)<
解析:(1)SiO +C+N――→Si N +CO(未配平),反应中碳元素的化合价由0升高到+2,氮元素的化合价由0
2 2 3 4
降低到-3,故反应中的氧化剂是N ,还原产物为Si N 。(2)该反应过程中,反应物的总能量大于生成物的总能
2 3 4
量,则该反应为放热反应,ΔH<0。(3)由(2)中分析可知,该反应为放热反应,故断裂旧键吸收的热量小于形成
新键放出的热量。
17、(1)使混合物充分接触并发生反应 Ba(OH) ·8HO+2NH Cl===BaCl +2NH ↑+10HO
2 2 4 2 3 2
(2)冰凉 吸热 >
(3)不能 只进行了一个复分解反应的实验,不能科学地得出结论
解析:由实验现象可知,该反应是一个吸收热量的反应,反应中体系温度下降,手触摸烧杯外壁时会有冰凉感,
故该反应为吸热反应,反应热ΔH>0;因为只研究了一个复分解反应的热效应,故无法确定复分解反应的热效
应类型。
18、(1)Mg+2H+===Mg2++H↑ 镁片溶解,有气泡产生
2
(2)下降 反应放出的热量使锥形瓶内气压增大 放热
(3)小于
解析:镁片与盐酸的反应是放热反应,是由于反应物的总能量高于生成物的总能量,放出的热量使锥形瓶内气
压增大,导致U形管左端液面下降,右端液面上升。