文档内容
影响化学反应速率的因素
【学习目标】
1、掌握影响化学反应速率的主要因素
2、理解外界条件(浓度、温度、压强、催化剂等)对化学反应速率的影响
【主干知识梳理】
一、影响化学反应速率的主要因素——内因
不同的化学反应,具有不同的反应速率,因此,参加反应的物质的本身性质是决定化学反应速率的主要因素
如:形状大小相同的铁、铝分别与等浓度的盐酸反应生成氢气的速率:铁小于铝
【对点训练1】
1、下列各组化学反应,反应速率最快的是( )
选项 反应物 反应物浓度 反应温度
A H 和F 均为0.02mol·L-1 5℃
2 2
B H 和Br 均为1mol·L-1 200℃
2 2
C H 和Cl 均为1mol·L-1 100℃
2 2
D H 和N 均为4mol·L-1 300℃
2 2
二、影响化学反应速率的外界因素——外因
1、浓度对化学反应速率的影响
(1)实验探究——硫代硫酸钠与硫酸的反应
取两支大小相同的试管,分别加入2 mL 和 1 mL 0.1mol/L Na SO 溶液,向盛有1
2 2 3
实验过程 mL 0.1mol/L Na SO 溶液的试管中加入1 mL 蒸馏水,摇匀。再同时向上述两支试管
2 2 3
中加入2 mL 0.1mol/L H SO 溶液,振荡。观察、比较两支试管中溶液出现浑浊的快慢
2 4
化学方程式 Na SO+HSO ===Na SO +S↓+SO ↑+HO
2 2 3 2 4 2 4 2 2
加入0.1mol/L Na SO 加入水的体 加入0.1mol/L HSO
实验编号 2 2 3 2 4 出现浑浊的快慢
溶液的体积/mL 积/mL 溶液的体积/mL
1 2 0 2
2 1 1 2
实验结论
(2)影响规律:当其他条件不变时,增大反应物的浓度,可以增大化学反应速率;减小反应物的浓度,可以减小
化学反应速率
【微点拨】
①浓度对化学反应速率的影响只适用于气体或溶液的反应,对于纯固体或液体的反应物,一般情况下其浓度
是常数,因此改变它们的量不会改变化学反应速率
②固体物质的反应速率与接触面积有关,颗粒越细,表面积越大,反应速率就越快。块状固体可以通过研细来
增大表面积,从而加快化学反应速率
③对于离子反应,只有实际参加反应的各离子浓度发生变化,才会引起化学反应速率的改变
④随着化学反应的进行,反应物的浓度会逐渐减小,因此一般反应速率也会逐渐减小
【对点训练2】
1、对反应A+B AB来说,常温下按以下情况进行反应: 四者反应速率的大小关系是( )
①20mL溶液中含A、B各0.01mol ②50mL溶液中含A、B各0.05mol
③0.1mol·L-1的A、B溶液各10mL ④0.5mol·L-1的A、B溶液各50mL
A.②>①>④>③ B.④>③>②>① C.①>②>④>③ D.①>②>③>④
2、把下列4种X溶液,分别加入到4个盛有10 mL 2 mol·L-1盐酸的烧杯中,并加水稀释到50 mL,此时X与
盐酸缓缓地进行反应,其中反应速率最大的是( )
A.20 mL,3 mol·L-1 B.20 mL,2 mol·L-1 C.10 mL,4 mol·L-1 D.10 mL,2 mol·L-1
2、压强对化学反应速率的影响
(1)影响规律:对于气体反应,当其他条件不变时,增大压强,气体体积缩小,浓度增大,化学反应速率加快;
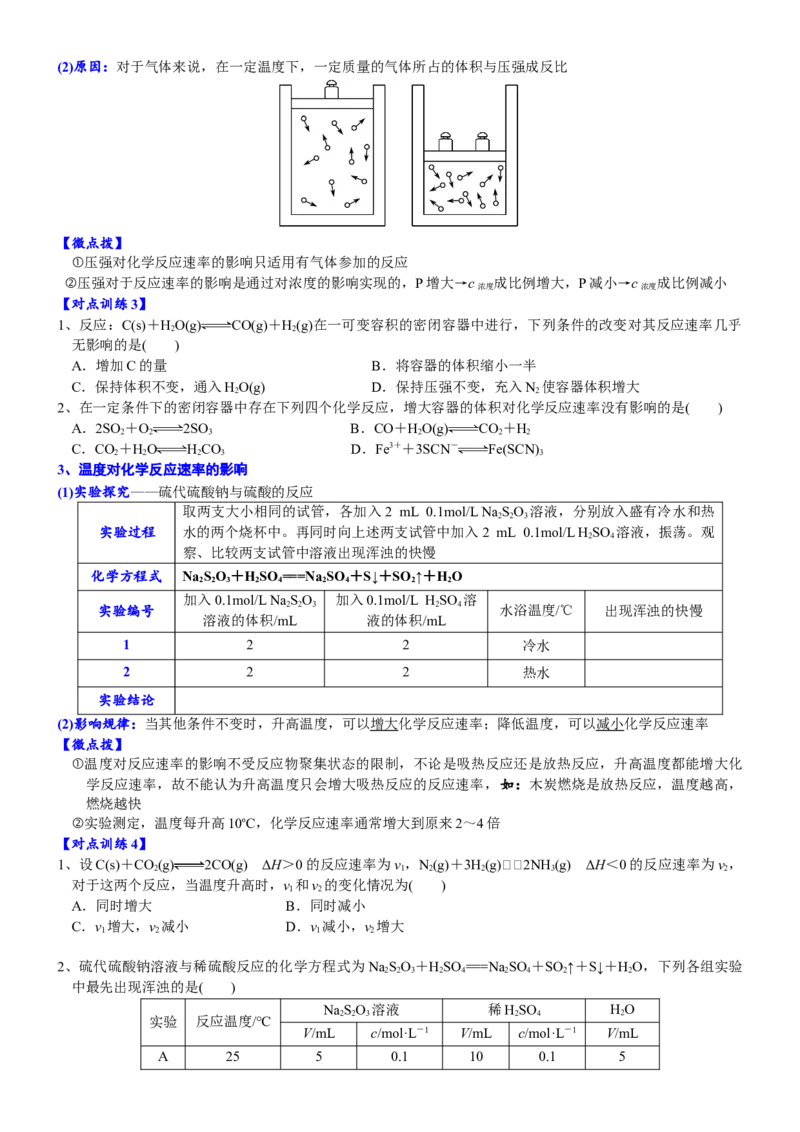
减小压强,气体体积增大,浓度减小,化学反应速率减慢(2)原因:对于气体来说,在一定温度下,一定质量的气体所占的体积与压强成反比
【微点拨】
①压强对化学反应速率的影响只适用有气体参加的反应
②压强对于反应速率的影响是通过对浓度的影响实现的,P增大→c
浓度
成比例增大,P减小→c
浓度
成比例减小
【对点训练3】
1、反应:C(s)+HO(g) CO(g)+H(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎
2 2
无影响的是( )
A.增加C的量 B.将容器的体积缩小一半
C.保持体积不变,通入HO(g) D.保持压强不变,充入N 使容器体积增大
2 2
2、在一定条件下的密闭容器中存在下列四个化学反应,增大容器的体积对化学反应速率没有影响的是( )
A.2SO +O 2SO B.CO+HO(g) CO+H
2 2 3 2 2 2
C.CO+HO HCO D.Fe3++3SCN- Fe(SCN)
2 2 2 3 3
3、温度对化学反应速率的影响
(1)实验探究——硫代硫酸钠与硫酸的反应
取两支大小相同的试管,各加入2 mL 0.1mol/L Na SO 溶液,分别放入盛有冷水和热
2 2 3
实验过程 水的两个烧杯中。再同时向上述两支试管中加入2 mL 0.1mol/L H SO 溶液,振荡。观
2 4
察、比较两支试管中溶液出现浑浊的快慢
化学方程式 Na SO+HSO ===Na SO +S↓+SO ↑+HO
2 2 3 2 4 2 4 2 2
加入0.1mol/L Na SO 加入0.1mol/L HSO 溶
实验编号 2 2 3 2 4 水浴温度/℃ 出现浑浊的快慢
溶液的体积/mL 液的体积/mL
1 2 2 冷水
2 2 2 热水
实验结论
(2)影响规律:当其他条件不变时,升高温度,可以增大化学反应速率;降低温度,可以减小化学反应速率
【微点拨】
①温度对反应速率的影响不受反应物聚集状态的限制,不论是吸热反应还是放热反应,升高温度都能增大化
学反应速率,故不能认为升高温度只会增大吸热反应的反应速率,如:木炭燃烧是放热反应,温度越高,
燃烧越快
②实验测定,温度每升高10oC,化学反应速率通常增大到原来2~4倍
【对点训练4】
1、设C(s)+CO(g) 2CO(g) ΔH>0的反应速率为v ,N(g)+3H(g)2NH(g) ΔH<0的反应速率为v ,
2 1 2 2 3 2
对于这两个反应,当温度升高时,v 和v 的变化情况为( )
1 2
A.同时增大 B.同时减小
C.v 增大,v 减小 D.v 减小,v 增大
1 2 1 2
2、硫代硫酸钠溶液与稀硫酸反应的化学方程式为NaSO +HSO ===Na SO +SO ↑+S↓+HO,下列各组实验
2 2 3 2 4 2 4 2 2
中最先出现浑浊的是( )
NaSO 溶液 稀HSO HO
2 2 3 2 4 2
实验 反应温度/℃
V/mL c/mol·L-1 V/mL c/mol·L-1 V/mL
A 25 5 0.1 10 0.1 5B 25 5 0.2 5 0.2 10
C 35 5 0.1 10 0.1 5
D 35 5 0.2 5 0.2 10
4、催化剂对化学反应速率的影响
(1)实验探究
向三支大小相同的试管中各加入2 mL 10%HO 溶液,再向其中的两支试管中分别加
实验过程 2 2
入少量MnO 粉末和2滴1mol/LFeCl 溶液。观察、比较三支试管中气泡出现的快慢
2 3
化学方程式 2HO=====2HO+O↑
2 2 2 2
实验操作
实验现象 ①有少量气泡出现;②产生大量气泡;③产生大量气泡
实验结论 MnO 、FeCl 可以使HO 分解的速率加快
2 3 2 2
(2)影响规律:当其他条件不变时,使用催化剂,化学反应速率增大
【对点训练5】
1、亚氯酸盐(如NaClO)可用作漂白剂,在常温下不见光时可保存一年,但在酸性溶液中因生成亚氯酸而发生分
2
解:5HClO===4ClO ↑+H++Cl-+2HO。分解时,刚加入硫酸,反应缓慢,随后突然反应释放出大量
2 2 2
ClO ,这是因为( )
2
A.酸使亚氯酸的氧化性增强 B.溶液中的H+起催化作用
C.溶液中的Cl-起催化作用 D.逸出的ClO 使反应生成物的浓度降低
2
2、下列说法正确的是( )
A.催化剂能使不发生反应的物质发生反应
B.在化学反应前后,催化剂的化学性质不变,质量改变
C.催化剂能改变化学反应速率
D.电解水时,往水中加入少量NaOH,可使电解速率明显加快,所以NaOH是这个反应的催化剂
5、其他因素对化学反应速率的影响
(1)固体表面积:固体颗粒越小,其单位质量的表面积越大,与其他反应物的接触面积越大,化学反应速率越大。
(2)反应物状态:一般来说,配成溶液或反应物是气体,都能增大反应物之间的接触面积,有利于增大反应速率。
(3)形成原电池:可以增大氧化还原反应的反应速率。
(4)其它方法:光辐照、放射线辐照、超声波、电弧、强磁场、高速研磨,均是行之有效的改变化学反应速率的
方法(块状)
【对点训练6】
1、已知反应:CaCO (块状)+2HCl===CaCl +HO+CO↑,下列措施中可使生成CO的速率加快的是( )
3 2 2 2 2
A.增加HCl的浓度 B.加水
C.增加同浓度盐酸的量 D.改加CaCO 粉末
3
2、过量铁与少量稀硫酸反应,为了加快反应速率,但是又不影响生成氢气的总量,可以采取的措施是( )
A.加入适量NaCl溶液 B.加入适量的水
C.加入几滴硫酸铜溶液 D.再加入少量同浓度的稀硫酸
三、“惰性”气体对化学反应速率的影响
1、惰性气体:化学反应速率中的“惰性气体”指的是不与反应物、生成物(体系中)任何成分发生化学反应的气
体。如:向N + 3H 2NH 充入CO、He,其中CO、He则称为惰性气体
2 2 3 2 2
2、惰性气体对化学反应速率的影响:以反应N + 3H 2NH 为例
2 2 3
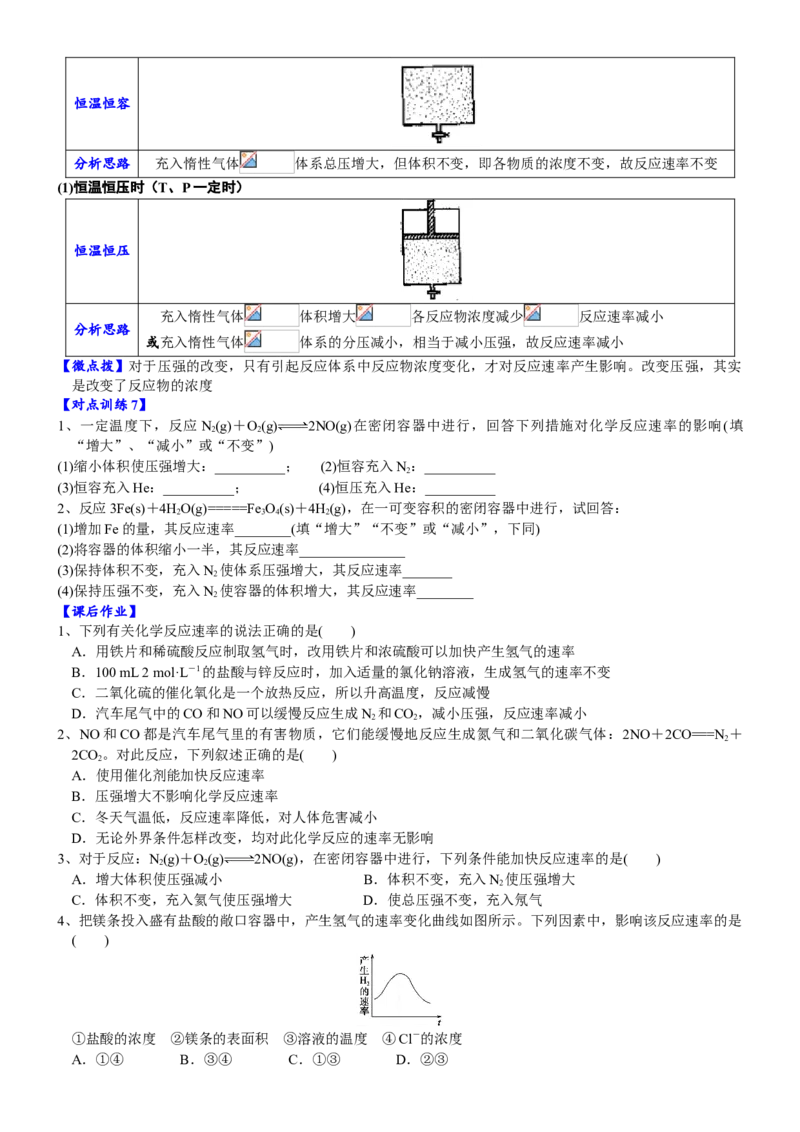
(1)恒温恒容时(T、V一定时)恒温恒容
分析思路 充入惰性气体 体系总压增大,但体积不变,即各物质的浓度不变,故反应速率不变
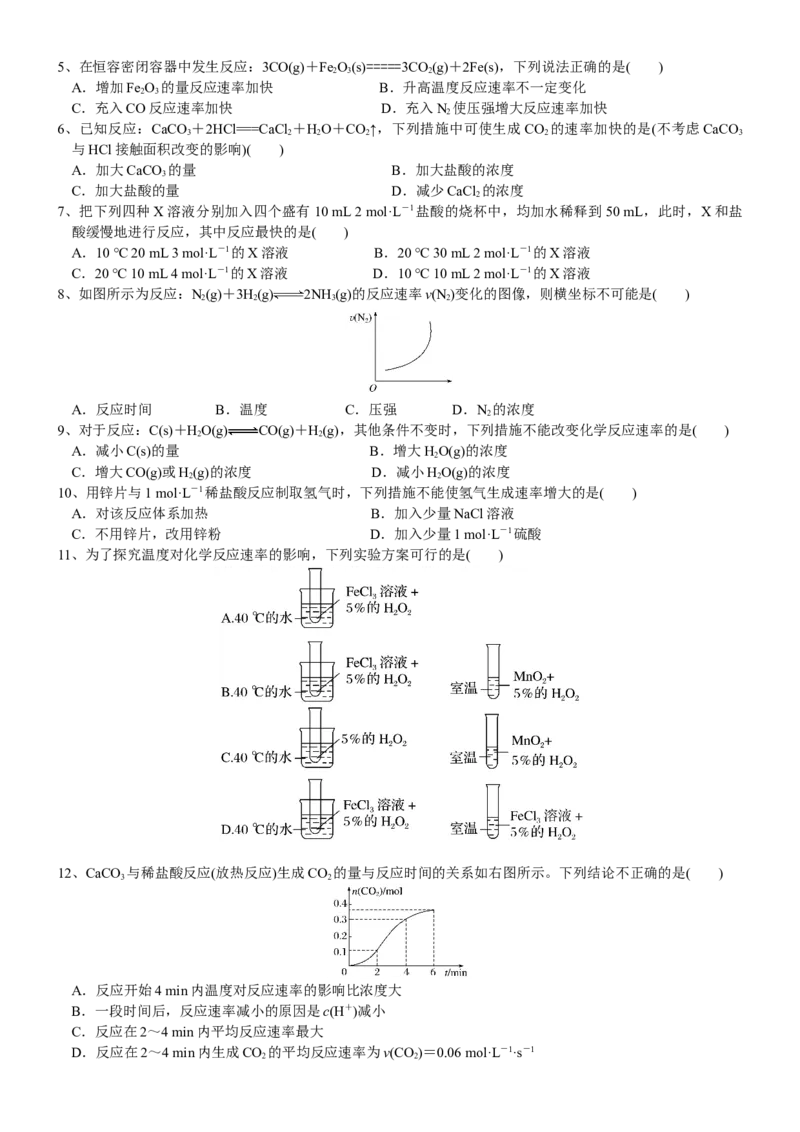
(1)恒温恒压时(T、P一定时)
恒温恒压
充入惰性气体 体积增大 各反应物浓度减少 反应速率减小
分析思路
或充入惰性气体 体系的分压减小,相当于减小压强,故反应速率减小
【微点拨】对于压强的改变,只有引起反应体系中反应物浓度变化,才对反应速率产生影响。改变压强,其实
是改变了反应物的浓度
【对点训练7】
1、一定温度下,反应N(g)+O(g) 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填
2 2
“增大”、“减小”或“不变”)
(1)缩小体积使压强增大:__________; (2)恒容充入N:__________
2
(3)恒容充入He:__________; (4)恒压充入He:__________
2、反应3Fe(s)+4HO(g)=====Fe O(s)+4H(g),在一可变容积的密闭容器中进行,试回答:
2 3 4 2
(1)增加Fe的量,其反应速率________(填“增大”“不变”或“减小”,下同)
(2)将容器的体积缩小一半,其反应速率_______________
(3)保持体积不变,充入N 使体系压强增大,其反应速率_______
2
(4)保持压强不变,充入N 使容器的体积增大,其反应速率________
2
【课后作业】
1、下列有关化学反应速率的说法正确的是( )
A.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
B.100 mL 2 mol·L-1的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
C.二氧化硫的催化氧化是一个放热反应,所以升高温度,反应减慢
D.汽车尾气中的CO和NO可以缓慢反应生成N 和CO,减小压强,反应速率减小
2 2
2、NO和CO都是汽车尾气里的有害物质,它们能缓慢地反应生成氮气和二氧化碳气体:2NO+2CO===N +
2
2CO。对此反应,下列叙述正确的是( )
2
A.使用催化剂能加快反应速率
B.压强增大不影响化学反应速率
C.冬天气温低,反应速率降低,对人体危害减小
D.无论外界条件怎样改变,均对此化学反应的速率无影响
3、对于反应:N(g)+O(g) 2NO(g),在密闭容器中进行,下列条件能加快反应速率的是( )
2 2
A.增大体积使压强减小 B.体积不变,充入N 使压强增大
2
C.体积不变,充入氦气使压强增大 D.使总压强不变,充入氖气
4、把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化曲线如图所示。下列因素中,影响该反应速率的是
( )
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①③ D.②③5、在恒容密闭容器中发生反应:3CO(g)+Fe O(s)=====3CO(g)+2Fe(s),下列说法正确的是( )
2 3 2
A.增加Fe O 的量反应速率加快 B.升高温度反应速率不一定变化
2 3
C.充入CO反应速率加快 D.充入N 使压强增大反应速率加快
2
6、已知反应:CaCO +2HCl===CaCl +HO+CO↑,下列措施中可使生成CO 的速率加快的是(不考虑CaCO
3 2 2 2 2 3
与HCl接触面积改变的影响)( )
A.加大CaCO 的量 B.加大盐酸的浓度
3
C.加大盐酸的量 D.减少CaCl 的浓度
2
7、把下列四种X溶液分别加入四个盛有10 mL 2 mol·L-1盐酸的烧杯中,均加水稀释到50 mL,此时,X和盐
酸缓慢地进行反应,其中反应最快的是( )
A.10 ℃ 20 mL 3 mol·L-1的X溶液 B.20 ℃ 30 mL 2 mol·L-1的X溶液
C.20 ℃ 10 mL 4 mol·L-1的X溶液 D.10 ℃ 10 mL 2 mol·L-1的X溶液
8、如图所示为反应:N(g)+3H(g) 2NH (g)的反应速率v(N )变化的图像,则横坐标不可能是( )
2 2 3 2
A.反应时间 B.温度 C.压强 D.N 的浓度
2
9、对于反应:C(s)+HO(g) CO(g)+H(g),其他条件不变时,下列措施不能改变化学反应速率的是( )
2 2
A.减小C(s)的量 B.增大HO(g)的浓度
2
C.增大CO(g)或H(g)的浓度 D.减小HO(g)的浓度
2 2
10、用锌片与1 mol·L-1稀盐酸反应制取氢气时,下列措施不能使氢气生成速率增大的是( )
A.对该反应体系加热 B.加入少量NaCl溶液
C.不用锌片,改用锌粉 D.加入少量1 mol·L-1硫酸
11、为了探究温度对化学反应速率的影响,下列实验方案可行的是( )
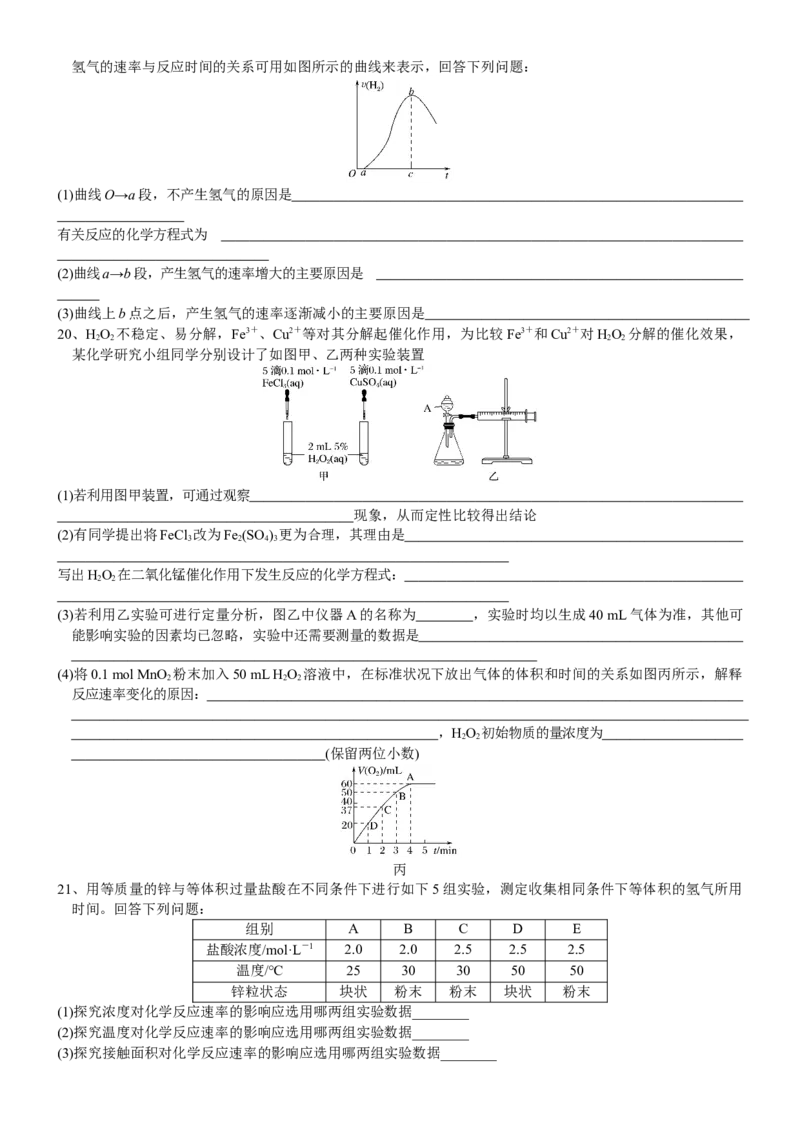
12、CaCO 与稀盐酸反应(放热反应)生成CO 的量与反应时间的关系如右图所示。下列结论不正确的是( )
3 2
A.反应开始4 min内温度对反应速率的影响比浓度大
B.一段时间后,反应速率减小的原因是c(H+)减小
C.反应在2~4 min内平均反应速率最大
D.反应在2~4 min内生成CO 的平均反应速率为v(CO)=0.06 mol·L-1·s-1
2 213、减小反应容器的体积而使压强增大,该方法对下列化学反应的速率无影响的是( )
A.CO(g)+Ca(OH) ===CaCO ↓+HO B.H(g)+I(g) 2HI(g)
2 2 3 2 2 2
C.NaCl+AgNO===AgCl↓+NaNO D.N(g)+3H(g) 2NH (g)
3 3 2 2 3
14、下列措施能明显增大化学反应速率的是( )
A.钠与水反应增大水的用量
B.将稀硫酸改为98%的浓硫酸与锌反应制取氢气
C.在硫酸溶液与氢氧化钠溶液反应时,增大压强
D.恒温恒容条件下,在合成氨反应中增加氮气的量
15、在相同条件下,做HO 分解对比实验时,其中①加入MnO 催化,②不加MnO 催化。下图是反应放出O
2 2 2 2 2
的体积随时间的变化关系示意图,其中正确的是( )
16、按要求填空
(1)形状大小相同的铁、铝分别与等浓度的盐酸反应生成氢气的速率:铁______铝(填“大于”、“小于”或“等
于”)
(2)对于Fe+2HCl===FeCl +H↑,改变下列条件对生成氢气的速率有何影响?(填“增大”、“减小”或“不
2 2
变”)
①升高温度:________;②增大盐酸浓度:__________; ③增大铁的质量:__________;
④增加盐酸体积:____________;⑤把铁片改成铁粉:____________;⑥滴入几滴 CuSO 溶液:
4
____________;
⑦加入 NaCl 固体:________;⑧加入 CHCOONa 固体__________;⑨加入一定体积的 NaSO 溶液
3 2 4
___________
(3)若把(2)中的稀盐酸改成“稀硝酸”或“浓硫酸”是否还产生H,为什么?
2
17、在密闭容器中发生下列反应:I(g)+H(g)2HI(g)(正反应为放热反应)。起始时,n(H )=a mol,n(I)=b
2 2 2 2
mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减
小”或“不变”)
编号 改变的条件 反应速率
(1) 升高温度
(2) 加入正催化剂
(3) 再充入a mol H
2
(4) 将容器的容积扩大到原来的2倍
(5) 保持容积不变,通入b mol Ne
18、某学生为了探究锌与盐酸反应过程中速率的变化,在100 mL稀盐酸中加入足量的锌,用排水集气法收集反
应放出的氢气,实验记录如下:
时间/min 1 2 3 4 5
氢气体积/mL 50 120 232 290 310
(1) (填“0~1”“1~2”“2~3”“3~4”或“4~5”)min时间段反应速率最大,原因是__________________(填“反
应物浓度增大”或“溶液温度升高”)
(2) (填“0~1”“1~2”“2~3”“3~4”或“4~5”)min时间段反应速率最小,原因是_____________________(填
“反应物浓度减小”或“溶液温度降低”)
(3)如果要减缓反应速率而又不减少产生氢气的量,下列措施你认为可行的是______
A.加入蒸馏水 B.通入HCl气体 C.加入NaOH固体
19、把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1 H SO 溶液的烧杯中,该铝片与HSO 反应产生
2 4 2 4氢气的速率与反应时间的关系可用如图所示的曲线来表示,回答下列问题:
(1)曲线O→a段,不产生氢气的原因是
有关反应的化学方程式为
(2)曲线a→b段,产生氢气的速率增大的主要原因是
(3)曲线上b点之后,产生氢气的速率逐渐减小的主要原因是
20、HO 不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对HO 分解的催化效果,
2 2 2 2
某化学研究小组同学分别设计了如图甲、乙两种实验装置
(1)若利用图甲装置,可通过观察
现象,从而定性比较得出结论
(2)有同学提出将FeCl 改为Fe (SO ) 更为合理,其理由是
3 2 4 3
写出HO 在二氧化锰催化作用下发生反应的化学方程式:
2 2
(3)若利用乙实验可进行定量分析,图乙中仪器A的名称为 ,实验时均以生成40 mL气体为准,其他可
能影响实验的因素均已忽略,实验中还需要测量的数据是
(4)将0.1 mol MnO 粉末加入50 mL H O 溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示,解释
2 2 2
反应速率变化的原因:
,HO 初始物质的量浓度为
2 2
(保留两位小数)
丙
21、用等质量的锌与等体积过量盐酸在不同条件下进行如下5组实验,测定收集相同条件下等体积的氢气所用
时间。回答下列问题:
组别 A B C D E
盐酸浓度/mol·L-1 2.0 2.0 2.5 2.5 2.5
温度/℃ 25 30 30 50 50
锌粒状态 块状 粉末 粉末 块状 粉末
(1)探究浓度对化学反应速率的影响应选用哪两组实验数据________
(2)探究温度对化学反应速率的影响应选用哪两组实验数据________
(3)探究接触面积对化学反应速率的影响应选用哪两组实验数据________(4)上述5组实验中测定收集等体积的氢气需要时间最短的是________
(5)实验完成后,某同学又用A组实验药品滴加两滴氯化铜,发现产生氢气的速率明显加快,解释速率加快的原
因是________________
22、下列事实中,判断什么因素影响了化学反应的速率
(1)集气瓶中有H 和Cl 的混合气体,在瓶外点燃镁条时发生爆炸:______________________________
2 2
(2)黄铁矿煅烧时需粉碎成细小的矿粒:____________________________________
(3)KI晶体和HgCl 晶体混合后无明显现象,若一起投入水中,很快生成红色的HgI :____________________
2 2
(4)熔化的KClO 放出气泡很慢,撒入少量MnO 很快产生气体:________________________
3 2
(5)同浓度、同体积的盐酸中放入同样大小的锌粒和镁块,产生气体有快有慢:________________________
(6)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速率不同:__________________
(7)夏天的食品易霉变,冬天就不易发生该现象:____________________________________
(8)葡萄糖在空气中燃烧时需要较高的温度,可是在人体内正常体温(37 ℃)下,就可以被氧化,这是因为:
______________________________________________________
23、某探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如表所示:
实验编号 锌的形态 反应温度/℃ 收集100 mL氢气所需时间/s
Ⅰ 薄片 15 200
Ⅱ 薄片 25 90
Ⅲ 粉末 25 10
(1)该实验的目的是探究 、 对锌和稀盐酸反应速率的影响
(2)实验Ⅰ和Ⅱ表明 ,化学反应速率越大。
(3)能表明固体的表面积对反应速率有影响的实验编号是_______和_______
(4)请设计一个实验方案证明盐酸的浓度对该反应的速率的影响:___________________________________
【影响化学反应速率的因素】答案【对点训练1】
1、A。解析:对于不同的化学反应,反应物的化学性质是反应速率的决定性因素,题中F 的氧化性最强,与H
2 2
反应的速率最快。
【对点训练2】
1、A。解析:①中c(A)=c(B)==0.5mol·L-1;②中c(A)=c(B)==1mol·L-1;③中c(A)=c(B)==0.05mol·L-
1;④中c(A)=c(B)==0.25mol·L-1;在其他条件一定的情况下,浓度越大,反应速率越大,所以反应速率由大
到小的顺序为②>①>④>③。
2、A。解析:此题主要考查浓度对化学反应速率的影响,X溶液的浓度大小决定了反应速率的快慢。此题很容
易错选C选项,实际上应考虑加水稀释后溶液中X的浓度,同一体积的溶液中X的物质的量越大,浓度就越大,
A中X的物质的量最大,故反应速率最大。
【对点训练3】
1、A。解析:增加C的用量,由于是固体,对其浓度无影响,对化学反应速率无影响,A项正确;容器体积压
缩一半,气态物质浓度增大,化学反应速率加快,B项错误;体积不变,通入HO(g),增大反应物浓度,化学
2
反应速率加快,C项错误;压强不变充入N ,体积增大气态反应物和生成物浓度圴减小,反应速率减小,D项
2
错误。
2、D。解析:增大容器的体积相当于减小压强,压强只对有气体参加或生成的反应速率有影响,对于没有气体
参加或生成的反应速率无影响,D项正确。
【对点训练4】
1、A。解析:升高温度时,不论吸热反应还是放热反应,反应速率都增大。
2、D。解析:当有多个外界条件时,要对比找出其相同条件和不同条件,然后比较判断。影响化学反应速率的
因素很多,本题从浓度和温度两个因素考查,结合选项知混合液体积都为 20 mL,根据浓度越大、温度越高,
反应速率越快,可以推知D选项正确。
【对点训练5】
1、C。解析:由题目信息可知,NaClO 在酸性溶液中生成亚氯酸,生成的亚氯酸在刚加入硫酸时反应缓慢,随
2
后突然反应加快,这说明分解生成的产物中某种物质起了催化剂的作用且该物质反应前不存在,故正确答案为
C。
2、C。解析:催化剂能改变反应速率,但不会引发反应,A项错误,C项正确;催化剂在反应前后的质量和化
学性质都不变,B项错误;在水中加入NaOH,增大了水的导电能力,NaOH不是催化剂,D项错误。
【对点训练6】
1、AD
2、C。解析:若加入NaCl溶液或水,会将稀硫酸稀释,c(H+)减小,反应速率减慢;若加入几滴CuSO 溶液,
4
则发生反应Fe+Cu2+===Cu+Fe2+,析出的Cu与Fe、稀硫酸形成原电池,反应速率加快且不影响生成H 的总
2
量;若再加入少量同浓度的稀硫酸,因Fe过量,则生成H 的总量增大,且反应速率不会改变。
2
【对点训练7】
1、(1)增大 (2)增大 (3)不变 (4)减小
2、(1)不变 (2)增大 (3)不变 (4)减小
解析:(1)由于Fe是固体,改变Fe的量,反应物浓度不变,故反应速率不变。(2)将容器的体积缩小一半,则反
应物浓度增大,故反应速率增大。(3)容器的体积不变,充入N,反应物浓度不变,故反应速率不变。(4)保持容
2
器内压强不变,充入N 容器体积增大,即反应物和生成物浓度均减小,故反应速率减小。
2
【课后作业】
1、D。解析:铁遇浓硫酸钝化,铁片与浓硫酸反应不能生成氢气,故A错误;向盐酸中加入氯化钠溶液,相当
于稀释了盐酸,盐酸浓度减小,反应速率减小,故B错误;升高温度,反应速率增大,与反应是吸热还是放热
无关,故C错误;有气体参加的反应,体系压强越小反应速率越小,故D正确。
2、A。解析:中学阶段,一般催化剂默认为正催化剂,使用(正)催化剂能加快反应速率,A正确;增大压强反
应速率增大,B错误;冬天气温低,反应速率降低,因为 NO、CO都有毒,对人类危害增大,C错误;改变温
度、压强等外界条件,化学反应速率会改变,D错误。
3、B。解析:增大体积引起浓度减小,反应速率减慢;体积不变充入N,N 的浓度增大,反应速率加快;体积
2 2
不变,充入氦气,各反应物的浓度并没有改变,反应速率不变;总压不变,充入氖气,体积增大,反应物浓度
减小,反应速率减慢。4、C。解析:镁与盐酸反应的离子方程式为Mg+2H+===Mg2++H↑,与H+有关,与Cl-无关。在镁与盐酸的
2
反应中,刚开始时H+的浓度最大,反应速率应最大,但由于此反应为放热反应,温度升高,化学反应速率还会
增大,随着化学反应的进行,H+浓度逐渐减小,化学反应速率又逐渐减慢。
5、C。解析:Fe O 为固体,增加固体的量,浓度未变,反应速率不变,A错;温度对任何反应都有影响,B错;
2 3
充入CO后,c(CO)增大,反应速率加快,C正确;充入N 虽然压强增大,但并未引起浓度的变化,反应速率不
2
变,D错。
6、B。解析:加大反应物的量不影响化学反应速率,改变浓度才影响化学反应速率,由于给定的反应是不可逆
反应,因此,该化学反应的速率和生成物的浓度无关。
7、B。解析:在化学反应中,当其他条件不变时,浓度越大,反应速率越快;温度越高,反应速率越快。本题
中要综合考虑浓度和温度的影响。先比较浓度的大小,这里的浓度应该是混合以后的浓度,由于混合后各烧杯
中盐酸的浓度相等,因此只要比较X的浓度即可,X浓度越大,反应速率越快。因为反应后溶液的体积均为 50
mL,所以X的物质的量越大,浓度就越大。通过观察可知,混合后 A、B选项中X的浓度相等,且比C、D两
项的大,但B中温度更高,因此B的反应速率最大。
8、A。解析:由题图可知,v(N )随横坐标上量值的逐渐增大而增大。对反应 N(g)+3H(g) 2NH (g)来说,
2 2 2 3
其他条件不变时,升高温度、增大压强、增大N 的浓度,都能使v(N )增大。在N(g)+3H(g) 2NH (g)的反
2 2 2 2 3
应过程中,随着时间的增加,N 的浓度逐渐减小,v(N )逐渐减小。
2 2
9、A。解析:改变浓度,可以改变化学反应速率,而改变固体物质的物质的量不能改变化学反应速率,因为固
体物质的浓度可视为常数。
10、B。解析:B项,NaCl溶液不参与反应且使盐酸浓度变小;C项,改用锌粉能增大接触面积;D项,加入
HSO 能增大H+浓度。
2 4
11、D。解析:没有对比实验,A错误;催化剂不同,温度不同,无法比较,B错误;前者没有催化剂,后者有
催化剂,且温度不同,无法比较,C错误;只有温度不同,其他条件都相同,该方案可行,D正确。
12、D。解析:随着反应的进行c(H+)减小,而前4 min内反应速率变大,根据反应是放热反应,可推出前4 min
内温度对反应速率的影响比浓度大,A、B项正确;在2~4 min内n(CO)的变化量最大(或曲线的斜率最大),可
2
判断出平均反应速率最大,C项正确;由题意及图可知,该题不知道容器体积,故不能计算出反应速率。
13、C。解析:C项,反应过程中无气体物质参加或生成,故改变压强对反应速率无影响。
14、D。解析:增大水的用量对Na与水的反应速率无明显影响,A项错误;改为浓硫酸后将得不到H ,B项错
2
误;无气体参与和生成的反应,压强变化对化学反应速率无明显影响,C项错误;增大反应物的浓度可以加快
反应速率,D项正确。
15、A。解析:由图像知,横坐标为时间,纵坐标为V(O ),只要HO 的量相同,两种情况下最终产生O 的体
2 2 2 2
积相同,①中加入MnO 作催化剂,加快了HO 的分解速率,在相同时间内产生O 的体积比②大,反应结束时
2 2 2 2
所用时间短,故选A。
16、(1)小于
(2)①增大 ②增大 ③不变 ④不变 ⑤增大 ⑥增大⑦不变 ⑧减小 ⑨减小
(3)不会产生H,Fe和稀硝酸反应生成NO;常温下,Fe在浓硫酸中钝化
2
17、(1)增大 (2)增大 (3)增大 (4)减小 (5)不变
解析:(1)不论正反应是吸热还是放热,升高温度都会使化学反应速率增大。
(2)若无特别说明,通常所说的催化剂即为“正催化剂”,加入催化剂,可加快化学反应速率。
(3)再充入a mol H ,c(H )增大,化学反应速率增大。
2 2
(4)扩大容器的容积,容器内各物质的浓度减小,化学反应速率减小。
(5)在密闭容器中通入Ne(g),保持容积不变,并未改变反应物浓度,化学反应速率不变。
18、(1)2~3 溶液温度升高
(2)4~5 反应物浓度减小
(3)A
解析:锌是足量的,随着反应的进行,盐酸的浓度逐渐降低,温度逐渐升高,化学反应速率逐渐增大,反应到
一段时间以后,随着盐酸浓度的降低,反应速率又逐渐减小。计算反应速率的大小,可以根据单位时间内生成
氢气的体积的多少来进行简便的计算。
19、(1)久置的铝片表面有氧化铝薄膜,先参加反应 Al O+3HSO ===Al(SO )+3HO
2 3 2 4 2 4 3 2
(2)该反应是放热反应,体系温度升高,化学反应速率增大(3)随着反应的进行,HSO 溶液的浓度减小,化学反应速率逐渐减小
2 4
解析:(1)在空气中久置的铝片表面有氧化铝薄膜,因此,HSO 先和氧化铝反应,不产生氢气。(2)a→b段,虽
2 4
然HSO 溶液的浓度减小,但该反应是放热反应,体系温度升高,温度起主导作用,故化学反应速率增大。(3)
2 4
曲线上b点之后,HSO 溶液的浓度减小,成为影响化学反应速率的主要因素,因此化学反应速率逐渐减小。
2 4
20、(1)产生气泡的快慢
(2)可以消除阴离子不同对实验的干扰 2HO=====2HO+O↑
2 2 2 2
(3)分液漏斗 产生40 mL气体所需的时间
(4)随着反应的进行,反应物的浓度减小,反应速率减小 0.11 mol·L-1
解析:(1)通过产生气泡的快慢即可比较Fe3+和Cu2+对HO 分解的催化效果(保持其他条件相同,只改变催化剂)。
2 2
(2)FeCl 和CuSO 中阴阳离子都不相同,无法判断是阴离子起作用还是阳离子起作用,Fe (SO ) 和CuSO 的阴离
3 4 2 4 3 4
子相同,可以消除阴离子不同对实验的
干扰。(3)通过计算分别用Fe3+、Cu2+催化时生成O 的速率,来定量比较Fe3+和Cu2+对HO 分解的催化效果,
2 2 2
因此需要测量的数据是产生40 mL气体所需要的时间。(4)由于随着反应的进行,反应物浓度逐渐减小,反应速
率减慢,最终生成氧气的体积是 60 mL,即0.002 7 mol。根据2HO ~O ,c(H O)=0.005 4 mol÷0.05 L≈0.11
2 2 2 2 2
mol·L-1。
21、(1)BC
(2)CE
(3)DE
(4)E
(5)Zn与Cu2+反应生成Cu单质,在锌块表面形成Zn—Cu原电池,加快化学反应速率
22、(1)光
(2)反应物的表面积
(3)水作溶剂,增大了反应物的接触面积
(4)催化剂
(5)反应物本身的性质
(6)反应物的浓度
(7)反应温度
(8)人体内的生物酶起催化作用
解析:影响化学反应速率的因素除了浓度、温度、压强、催化剂以外,光、电磁波、超声波、反应物颗粒的大
小、溶剂的性质等也会对化学反应速率产生影响。
23、(1)固体表面积 温度 (2)温度越高
(3)Ⅱ Ⅲ
(4)在相同的温度下,采用相同形态的质量相同的锌片与两种体积相同但浓度不同的盐酸反应
解析:(1)影响化学反应速率的因素有固体表面积、温度、催化剂、浓度,对气体来说还有压强等。根据表格提
供的信息,锌有薄片和粉末两种状态,反应温度有15 ℃和25 ℃。(2)根据表格提供的信息,实验Ⅰ和实验Ⅱ中
锌片的形态相同,温度不同,温度高的收集相同体积的氢气所需时间短,说明化学反应速率大。(3)探究固体表
面积对反应速率的影响,需要温度相同。(4)探究浓度对化学反应速率的影响,必须其他条件相同,故设计的实
验方案为在相同的温度下,采用相同形态的质量相同的锌片与两种体积相同但浓度不同的盐酸反应。