文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 07 有关无明显现象反应的探究
【题型一】二氧化碳与水是否反应
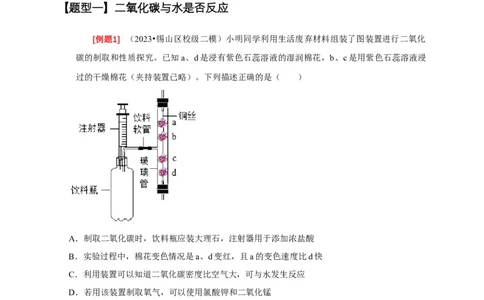
[例题1] (2023•锡山区校级二模)小明同学利用生活废弃材料组装了图装置进行二氧化
碳的制取和性质探究。已知a、d是浸有紫色石蕊溶液的湿润棉花,b、c是用紫色石蕊溶液浸
过的干燥棉花(夹持装置已略)。下列描述正确的是( )
A.制取二氧化碳时,饮料瓶应装大理石,注射器用于添加浓盐酸
B.实验过程中,棉花变色情况是a、d变红,且a的变色速度比d快
C.利用装置可以知道二氧化碳密度比空气大,可与水发生反应
D.若用该装置制取氧气,可以使用氯酸钾和二氧化锰
【解答】解:A、由于浓盐酸容易挥发产生HCl气体,与制取的二氧化碳混合使气体不纯,所以
应选用饮料瓶装大理石,注射器装稀盐酸,故该选项错误;
B、通过大理石与稀盐酸的反应可以制取二氧化碳,二氧化碳可以与水发生反应生成碳酸,可以
使紫色石蕊试液变红,因为a,d是浸有紫色石蕊溶液的湿润棉花,所以可变红,b,c是干燥的,
不变色。但由于二氧化碳的密度比空气大,所以应该先接触到 d,才能接触到a,因此a的变色
速度比d慢,故该选项错误;
C、经上述分析可知,二氧化碳密度比空气大,可与水发生反应,该选项正确;
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、此装置是固液常温型发生装置,而用氯酸钾和二氧化锰制取氧气需要加热,故不能用该装置,
该选项错误。
故选:C。
[例题2] (2023•澄城县模拟)某同学用如图所示装置验证二氧化碳的性质。已知:气体
X属于稀有气体;装置气密性良好;锥形瓶中放入的是用石蕊溶液染成紫色的干燥纸花。具体
步骤有:①从a端通入二氧化碳;②从b端通入气体X;③从分液漏斗中滴加适量水;④从
a端通入二氧化碳。下列有关该实验的说法合理的是( )
A.步骤①可观察到纸花变红
B.气体X的密度大于二氧化碳的密度
C.步骤③的目的是验证水不能使紫色石蕊变色
D.步骤④的现象说明二氧化碳显酸性
【解答】解:A、二氧化碳不能使石蕊溶液染成紫色的干燥纸花变色。该选项不正确。
B、气体X属于稀有气体,从b端进入,将二氧化碳从a端排出,短管进长管出,说明气体X的
密度小于二氧化碳的密度。该选项不正确。
C、步骤②将二氧化碳气体排出后,步骤③从分液漏斗中滴加适量水,是为验证水不能使紫色
石蕊变色。该选项正确。
D、步骤④从a端通入二氧化碳,纸花变红,说明二氧化碳和水发生了化学反应,产物显酸性。
该选项不正确。
故选:C。
[例题3] (2023•海淀区校级三模)如图所示,小组同学研究“CO 与水的反应”。三颈
2
瓶中充满CO ,将注射器中的蒸馏水缓慢注入三颈瓶中,54s至100s,缓慢将注射器拉至原刻
2
度处。实验前测得蒸馏水的pH为7,过程中用传感器采集液体pH和相对压强(将初始压强设
置为0)。下列说法不正确的是( )
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.实验前需要检查装置气密性
B.pH下降的原因是CO 和水反应生成了碳酸
2
C.压强下降可以证明CO 与水的反应
2
D.100s后CO 继续与水反应
2
【解答】解:A、该反应有气体参加反应还要测定相对压强的变化,实验前需要检查装置气密性,
故A说法正确;
B、pH下降的原因是CO 和水反应生成了碳酸,故B说法正确;
2
C、由于二氧化碳能溶于水,压强下降不可以证明CO 与水的反应,故C说法不正确;
2
D、由图示可知,100s后pH还在下降酸性增强,说明了CO 继续与水反应,故D说法正确。
2
故选:C。
1.目的:从有新物质生成的角度证明二氧化碳和水发生了反应。
2.设计本质:将新物质与原物质的性质对比。
3.方案选择:①测溶液 pH; ②观察指示剂颜色变化。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【题型二】二氧化碳与氢氧化钠是否反应
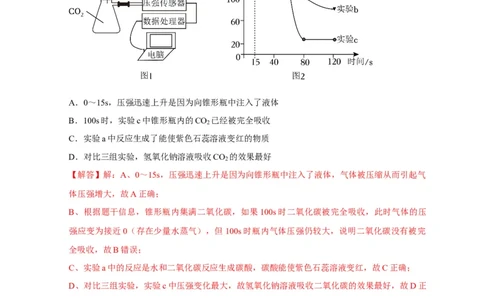
[例题4] (2024•深圳模拟)某小组用图1的装置探究CO 的化学性质。相同条件下,分
2
别将等体积的水、澄清石灰水和氢氧化钠溶液注入集满CO 的锥形瓶中,测得压强随时间的变
2
化如图2。下列说法错误的是( )
A.0~15s,压强迅速上升是因为向锥形瓶中注入了液体
B.100s时,实验c中锥形瓶内的CO 已经被完全吸收
2
C.实验a中反应生成了能使紫色石蕊溶液变红的物质
D.对比三组实验,氢氧化钠溶液吸收CO 的效果最好
2
【解答】解:A、0~15s,压强迅速上升是因为向锥形瓶中注入了液体,气体被压缩从而引起气
体压强增大,故A正确;
B、根据题干信息,锥形瓶内集满二氧化碳,如果100s时二氧化碳被完全吸收,此时气体的压
强应变为接近0(存在少量水蒸气),但100s时瓶内气体压强仍较大,说明二氧化碳没有被完
全吸收,故B错误;
C、实验a中的反应是水和二氧化碳反应生成碳酸,碳酸能使紫色石蕊溶液变红,故C正确;
D、对比三组实验,实验c中压强变化最大,故氢氧化钠溶液吸收二氧化碳的效果最好,故D正
确。
故选:B。
[例题5] (2023•耀州区模拟)如图进行实验,关闭K,向盛满CO 的U形管中注入足量
2
NaOH溶液,一段时间后,打开K并滴加足量稀盐酸,实验过程中观察到气球先变瘪后变大。
关于该实验的说法不正确的是( )
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.气球变瘪可证明二氧化碳能与氢氧化钠反应
B.滴加稀盐酸后,U形管内混合液的pH逐渐减小
C.气球变大是因为有二氧化碳产生
D.注入NaOH溶液后U形管内压强减小
【解答】解:A、二氧化碳能溶于水,则装置中的气体减少,压强减小,则气球变瘪不可证明二
氧化碳能与氢氧化钠反应,故A错误;
B、氢氧化钠与二氧化碳反应生成碳酸钠和水,碳酸钠溶液显碱性,而碳酸钠与盐酸反应生成氯
化钠、水和二氧化碳,则碱性减弱,pH减小,故B正确;
C、滴加盐酸时,有气体生成,则气球变大,故C正确;
D、氢氧化钠消耗了二氧化碳,气体减小,压强减小,故D正确。
故选:A。
(1)加入盐酸有气泡冒出:2HCl + Na CO=2NaCl+ H O+CO↑
2 3 2 2
(2)加入石灰水有沉淀产生:Ca(OH) + Na CO = CaCO↓+2NaOH
2 2 3 3
(3)加入氯化钙有沉淀产生:NaCO +CaCl = CaCO↓+2NaCl
2 3 2 3
【题型三】探究酸碱中和反应是否发生
[例题6] (2024•西城区模拟)实验小组用指示剂和传感器研究稀盐酸和稀 NaOH溶液的
反应。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)实验中观察到的现象是 ,该现象能证明盐酸和氢氧化钠发生了
化学反应,理由是 。反应的化学方程式是
。
(2)实验中用传感器测量溶液pH和温度的变化。下列说法正确的是 。
A.盐酸和氢氧化钠反应可能放出热量
B.60s时对应溶液中的溶质是NaCl
C.120s时向溶液中加入酚酞,溶液不变色
D.180s时向溶液中加入Na CO 溶液,能证明稀盐酸和稀NaOH溶液发生反应
2 3
【解答】解:(1)滴有酚酞的氢氧化钠溶液呈红色,无色酚酞溶液遇酸性溶液不变色,遇碱性
溶液变红,逐滴滴入稀盐酸,至恰好完全反应,溶液显中性,溶液由红色褪为无色,证明盐酸
和氢氧化钠发生了化学反应,盐酸和氢氧化钠反应生成氯化钠和水,反应的化学方程式为:
NaOH+HCl=NaCl+H O;
2
(2)A、曲线a~b上升,温度升高,是因为该反应放热,故A正确;
B、60s时溶液的pH大于7,溶液显碱性,氢氧化钠有剩余,溶液中的溶质是NaCl、NaOH,故
B不正确;
C、120s时溶液的pH小于7,显酸性,加入酚酞,溶液不变色,故C正确;
D、180s时溶液的pH<7,显酸性,向溶液中加入Na CO 溶液,会有气泡产生,不能证明稀盐
2 3
酸和稀NaOH溶液发生反应,故D不正确;
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故答案为:(1)溶液由红色变成了无色;溶液的颜色发生了改变;NaOH+HCl=NaCl+H O;
2
(2)AC。
[例题7] (2024•碑林区校级一模)氢氧化钠溶液和稀盐酸混合没有明显现象,它们是否
发生了反应呢?某化学兴趣小组的同学设计如图甲所示实验进行探究。他们在盛有一定量 X
溶液的烧杯中放置pH传感器和温度传感器,然后开启电磁搅拌器,从滴定管中逐滴加入Y溶
液;计算机显示两种传感器所得的数据曲线如图乙和图丙。
【实验分析】
(1)写出稀盐酸和氢氧化钠溶液反应的化学方程式 ,
该反应的基本反应类型是 。
(2)由图乙可知,图甲滴定管中的Y溶液是 (选填“NaOH溶液”或“稀盐
酸”)。
(3)关于图乙、图丙的说法正确的是 (填字母)。
A.图乙中c点表示的溶液中Na+和Cl﹣微粒数目相同
B.取图丙中d点的溶液,加入碳酸钠溶液,会产生气泡
C.取图乙a点的溶液,进行蒸发结晶,再将所得固体溶于水,测得溶液的pH=7,可以得出稀
盐酸和NaOH溶液发生了反应
(4)图丁是图甲中NaOH溶液和稀盐酸反应的微观示意图,则反应前的“ ”表示的微粒是
(填微粒符号)。
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【拓展迁移】
(5)将40g、10%的NaOH溶液与40g、10%的稀盐酸混合,充分反应后,滴入紫色石蕊溶液显
色。
【解答】解:(1)稀盐酸和氢氧化钠溶液反应生成氯化钠和水,化学方程式为 NaOH+HCl=
NaCl+H O。该反应符合两种化合物互相交换成分,生成物中有水生成的复分解反应特点。所以
2
该反应的基本反应类型是复分解反应;
(2)由图乙可知,溶液的pH由小于7到等于7到大于7,可知图甲烧杯中溶液是稀盐酸,图甲
滴定管中的Y溶液是NaOH溶液;
(3)A、图乙中b点表示盐酸与氢氧化钠恰好完全反应,b点表示的溶液中Na+和Cl−微粒数目
相同,c点时氢氧化钠过量,所以图乙中c点表示的溶液中Na+数目大于Cl−数目,故A不正确;
B、取图丙中d点的溶液中盐酸还没有反应完,所以加入碳酸钠溶液,盐酸与碳酸钠反应生成二
氧化碳气体,所以会产生气泡,故B正确;
C、由于氢氧化钠溶液pH>7,若没有反应则取图乙a点的溶液,进行蒸发结晶,再将所得固体
溶于水,测得溶液的pH>7,取图乙a点的溶液,进行蒸发结晶,再将所得固体溶于水,测得溶
液的pH=7,说明稀盐酸和NaOH溶液发生了反应,故C正确。
故选:BC;
(4)氢氧化钠与盐酸反应生成氯化钠和水,反应后溶液中,氯化钠以钠离子和氯离子的形式存
在,反应前滴加的氢氧化钠溶液中氢氧化钠以钠离子和氢氧根离子形式存在,则反应后的白色
小球与反应前滴加溶液中的白色小球都表示钠离子,所以反应前的“ ”表示的微粒是氢氧根
离子,用OH−表示;
(5)设:40g、10%的NaOH溶液与质量为x、10%的稀盐酸恰好完全反应。
NaOH + HCl =NaCl+H O ¿ 40 40g×10%
2 ¿¿¿ = ¿¿¿¿¿x=36.5g¿¿¿¿¿¿
40 ¿36.5 ¿ ¿40g×10% ¿ 36.5 x×10%
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
即40g、10%的NaOH溶液与36.5g、10%的稀盐酸恰好完全反应。所以将40g、10%的NaOH溶
液与40g、10%的稀盐酸混合,充分反应后,盐酸有剩余,酸使紫色石蕊溶液变红,所以将
40g、10%的NaOH溶液与40g、10%的稀盐酸混合,充分反应后,滴入紫色石蕊溶液显红色。
中和反应(以稀盐酸和氢氧化钠的反应为例)
实验1:NaOH溶液中加入足量稀盐酸,检验NaOH的消失
①滴加酸碱指示剂或测定溶液pH:判断溶液的酸碱性变化
②加入可溶性铜盐(或镁盐):观察是否有沉淀
实验2:稀盐酸中加入足量NaOH溶液,检验稀盐酸的消失
①加入活泼金属或碳酸盐:观察是否有沉淀
②加入难溶性碱或金属氧化物:观察固体是否溶解
1. (2024•雁塔区校级二模)某小组设计了如图的创新实验,内层小试管和外层大试管
底部分别放有用石蕊溶液染过色的滤纸片,内层小试管壁上有一小孔。下列说法不正确的是(
)
A.干燥滤纸片不变色,说明CO 不能使石蕊变色
2
B.通入CO 后润湿的滤纸片由红色变紫色
2
C.澄清石灰水变浑浊是因为碳酸钙难溶于水
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.蜡烛熄灭说明CO 不支持燃烧也不可燃
2
【解答】解:A、干燥滤纸片不变色,说明CO 不能使石蕊变色,故选项说法正确。
2
B、二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊溶液变红色,故选项说法错误。
C、二氧化碳和石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,澄清石灰水变浑浊,是因为碳酸
钙难溶于水,故选项说法正确。
D、蜡烛熄灭,说明了二氧化碳不能支持燃烧也不燃烧,故选项说法正确。
故选:B。
2. (2023•庐江县模拟)如图a、c为喷水的紫色石蕊试纸,b为干燥的紫色石蕊试纸。
下列说法正确的是( )
A.b处先变红,a、c处后变红
B.a处先变红,b处不变红
C.此实验无法证明CO 能与水反应
2
D.根据塑料瓶内现象与烧杯内现象都能证明CO 密度比空气大
2
【解答】解:A、缓慢通入二氧化碳气体,二氧化碳的密度比空气大,干燥的二氧化碳不能使紫
色石蕊变色,水和二氧化碳反应生成碳酸能使石蕊变红,所以 b处不变红,c处先变红,a处后
变红,故选项说法错误。
B、二氧化碳的密度比空气大,c处先变红,b处不变红,故选项说法错误。
C、开始a、c现象可知:水不能使紫色石蕊试纸变红,b现象可知二氧化碳不能使干燥的紫色石
蕊试纸变红,通入二氧化碳后a、c现象可知二氧化碳与水反应能使紫色石蕊试纸变红,此实验
能证明二氧化碳与水反应,故选项说法错误。
D、根据塑料瓶内现象:c处先变红,a处后变红,与烧杯内现象:蜡烛自下而上依次熄灭,都
能证明二氧化碳的密度比空气大,故选项说法正确。
故选:D。
3. (2023•阜阳模拟)如图所示(干冰常温下易升华),下列有关说法不正确的是(
)
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.从微观角度,干冰是由分子构成的物质
B.干冰升华是物理变化
C.U形管内右端红墨水液面升高
D.烧杯中澄清石灰水变浑浊
【解答】解:A、干冰是固态二氧化碳,从微观角度分析,干冰是由二氧化碳分子构成的,故选
项说法正确。
B、干冰升华是由固体变为气体,只是状态的改变,没有新物质的生成,属于物理变化,故选项
说法正确。
C、干冰升华吸收热量,大试管内温度降低,压强减小,可以观察到U型管内右端红墨水液面降
低,故选项说法错误。
D、干冰升华是由固体变为气体,二氧化碳气体使得澄清石灰水变浑浊,故选项说法正确。
故选:C。
4. (2023•宿豫区一模)某同学利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,
并用pH传感器和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图下列说法
错误的是( )
A.图2中b点所示溶液中的溶质是NaCl和NaOH
B.将图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.图3中e→f变化趋势可说明该反应是放热反应
【解答】解:A、由图2知该反应是将盐酸滴入氢氧化钠溶液中;盐酸与氢氧化钠反应生成氯化
钠和水,b点pH大于7,说明氢氧化钠有剩余,故b点所示溶液中的溶质是NaCl和NaOH,A
正确;
B、图2中d点pH小于7,盐酸过量,溶液中溶质为氯化钠和HCl,加热蒸干过程中HCl挥发掉,
所得固体只有氯化钠,为纯净物,B正确;
C、图2中c点pH=7,盐酸与氢氧化钠恰好完全反应,c→d过程是盐酸过量,溶液中NaCl的
质量不变,C错误;
D、图3中e→f变化趋势可说明该反应是放热反应,D正确;
故选:C。
5. (2023•高新区二模)小莉同学用稀盐酸和氢氧化钠溶液对酸碱中和反应进行了如下
探究,用pH传感器测得烧杯内溶液的pH变化图象(如图二),同时用温度传感器测得烧杯
内温度变化图象(如图三),实验过程中保温良好,忽略热量散失。下列说法错误的是
( )
A.该实验是将氢氧化钠溶液滴入盐酸中
B.据图三说明中和反应是放热反应
C.图二中的A点反应程度与图三中的B点对应
D.C点对应溶液中溶质成分是NaCl和NaOH
【解答】解:A、图象中pH的变化是从小于7逐渐增大到大于7,可知原溶液显酸性,然后不
断的加入碱性溶液,使pH增大,说明是把氢氧化钠溶液滴加到稀盐酸中,故选项说法正确。
B、至B点温度逐渐升高,图三说明中和反应是放热反应,故选项说法正确。
C、A点时溶液的pH为11,大于7,溶液显碱性,是完全反应后继续滴加氢氧化钠溶液,则图
二中的A点反应程度与图三中的B点和C点之间对应,故选项说法错误。
D、点时滴加X溶液的质量为 60g,由B图可知,pH大于7,显碱性,溶质成分是 NaCl和
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
NaOH,故选项说法正确。
故选:C。
6. (2023•成安县一模)电导率是衡量溶液导电能力大小的物理量,在相同条件下,电
导率与离子浓度(单位体积内的离子数)成正比,盐酸和氢氧化钠反应电导率曲线如图所示,
以下分析不正确的是( )
A.电导率减小可能是由于溶液中离子数量逐渐减小
B.M点时NaOH溶液与稀盐酸恰好完全反应
C.N点时溶液中的离子数大于P点
D.该实验证明溶液中始终含有带电的粒子
【解答】解:A、电导率减小,是由于溶液中离子浓度逐渐减小,该选项说法不正确;
B、M点时电导率最低,是因为NaOH溶液与稀盐酸恰好完全反应,离子浓度最小,该选项说法
正确;
C、N点时氢氧化钠过量,溶液中的离子数大于P点,该选项说法正确;
D、该实验中电导率始终大于0,证明溶液中始终含有带电的粒子,该选项说法正确。
故选:A。
7. (2023•泰安二模)某兴趣小组同学将pH传感器分别插入三只盛有相同体积蒸馏水的
烧杯中,打开磁力搅拌器,同时采集数据,再向三只烧杯中同时分别加入适量的柠檬酸、氯化
钠、氢氧化钠三种固体。实验数据如图所示,下列说法不正确的是( )
A.①表示氢氧化钠溶于水,说明OH﹣浓度越大pH越大
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.②表示氯化钠溶于水,pH=7说明溶液中无自由移动离子
C.③表示柠檬酸溶于水,说明H+浓度越大pH越小
D.柠檬酸溶液和氢氧化钠能发生中和反应
【解答】解:A.曲线①可知溶液的pH>7,且逐渐的增大,则溶液呈碱性,向烧杯中加入的物
质为NaOH,碱溶液中OH﹣浓度越大,碱性越强,pH越大,故A正确;
B.曲线②溶液可知的pH=7,则溶液一直呈中性,烧杯中加入的物质为NaCl,NaCl的溶液中含
有自由移动的Na+、Cl﹣,故B错误;
C.曲线③可知溶液的pH<7,且逐渐的减小,则溶液呈酸性,向烧杯中加入的物质为柠檬酸,
酸溶液中H+浓度越大,酸性越强,pH越小,故C正确;
D.柠檬酸溶液含有H+,氢氧化钠溶液中含有OH﹣,则两溶液混合后能发生中和反应,故D正确。
故选:B。
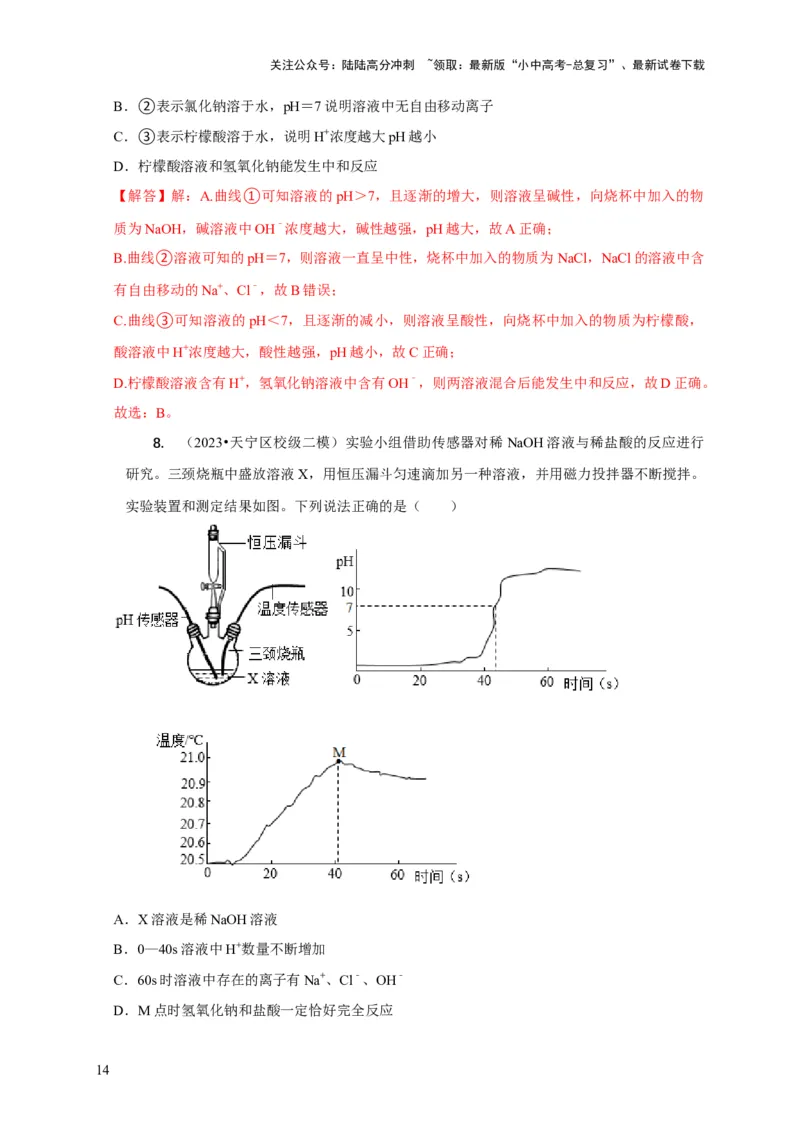
8. (2023•天宁区校级二模)实验小组借助传感器对稀NaOH溶液与稀盐酸的反应进行
研究。三颈烧瓶中盛放溶液X,用恒压漏斗匀速滴加另一种溶液,并用磁力投拌器不断搅拌。
实验装置和测定结果如图。下列说法正确的是( )
A.X溶液是稀NaOH溶液
B.0—40s溶液中H+数量不断增加
C.60s时溶液中存在的离子有Na+、Cl﹣、OH﹣
D.M点时氢氧化钠和盐酸一定恰好完全反应
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【解答】解:A、由pH图像可知溶液pH是小于7显酸性的,随时间逐渐增大的最后 pH大于
7,故是将稀NaOH溶液滴入稀盐酸,X溶液是稀盐酸,故A不正确;
B、由图可知,0—40s时pH不断增大,说明随着不断滴入稀NaOH溶液,溶液中H+数量不断减
少,故B不正确;
C、60s时溶液pH大于10,说明碱已经过量,此时溶液中存在的离子有 Na+、Cl﹣、OH﹣,故C
正确;
D、M点时对应时间为40s,此时溶液pH还小于7,说明氢氧化钠和盐酸还没完全反应,盐酸还
有剩余,故D不正确;
故选:C。
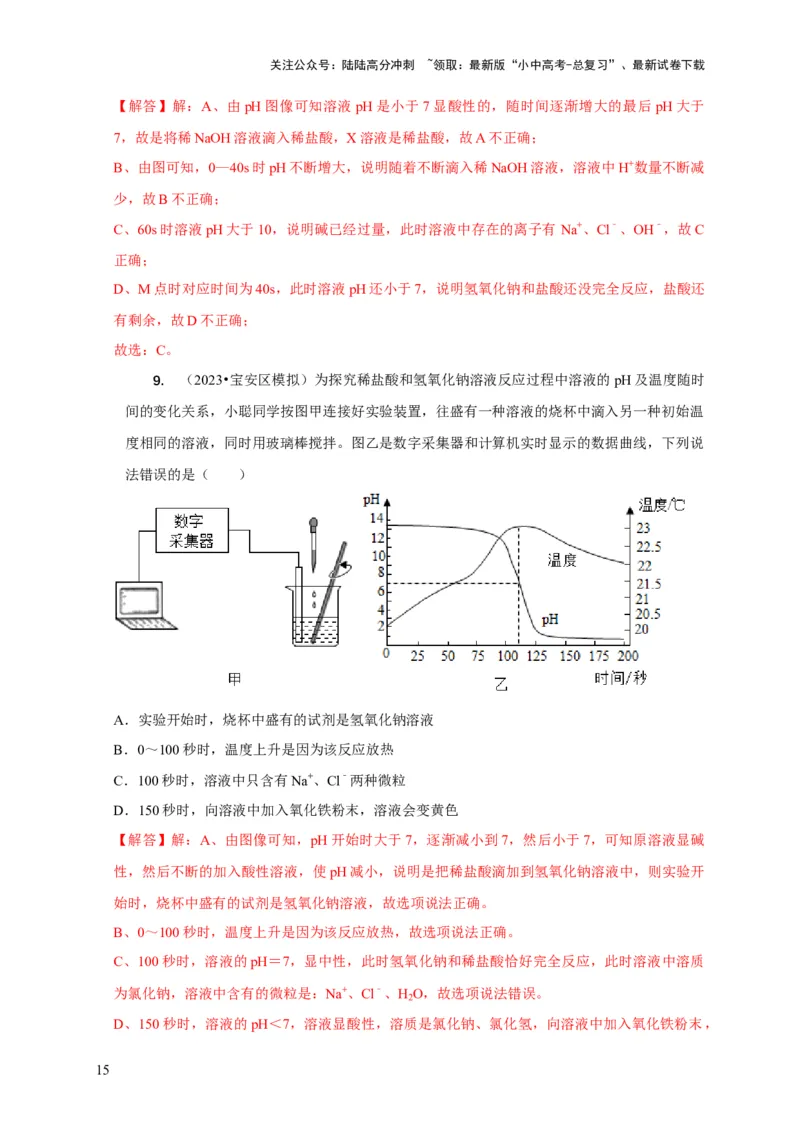
9. (2023•宝安区模拟)为探究稀盐酸和氢氧化钠溶液反应过程中溶液的pH及温度随时
间的变化关系,小聪同学按图甲连接好实验装置,往盛有一种溶液的烧杯中滴入另一种初始温
度相同的溶液,同时用玻璃棒搅拌。图乙是数字采集器和计算机实时显示的数据曲线,下列说
法错误的是( )
A.实验开始时,烧杯中盛有的试剂是氢氧化钠溶液
B.0~100秒时,温度上升是因为该反应放热
C.100秒时,溶液中只含有Na+、Cl﹣两种微粒
D.150秒时,向溶液中加入氧化铁粉末,溶液会变黄色
【解答】解:A、由图像可知,pH开始时大于7,逐渐减小到7,然后小于7,可知原溶液显碱
性,然后不断的加入酸性溶液,使pH减小,说明是把稀盐酸滴加到氢氧化钠溶液中,则实验开
始时,烧杯中盛有的试剂是氢氧化钠溶液,故选项说法正确。
B、0~100秒时,温度上升是因为该反应放热,故选项说法正确。
C、100秒时,溶液的pH=7,显中性,此时氢氧化钠和稀盐酸恰好完全反应,此时溶液中溶质
为氯化钠,溶液中含有的微粒是:Na+、Cl﹣、H O,故选项说法错误。
2
D、150秒时,溶液的pH<7,溶液显酸性,溶质是氯化钠、氯化氢,向溶液中加入氧化铁粉末,
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
氧化铁和稀盐酸反应生成氯化铁和水,溶液会变黄色,故选项说法正确。
故选:C。
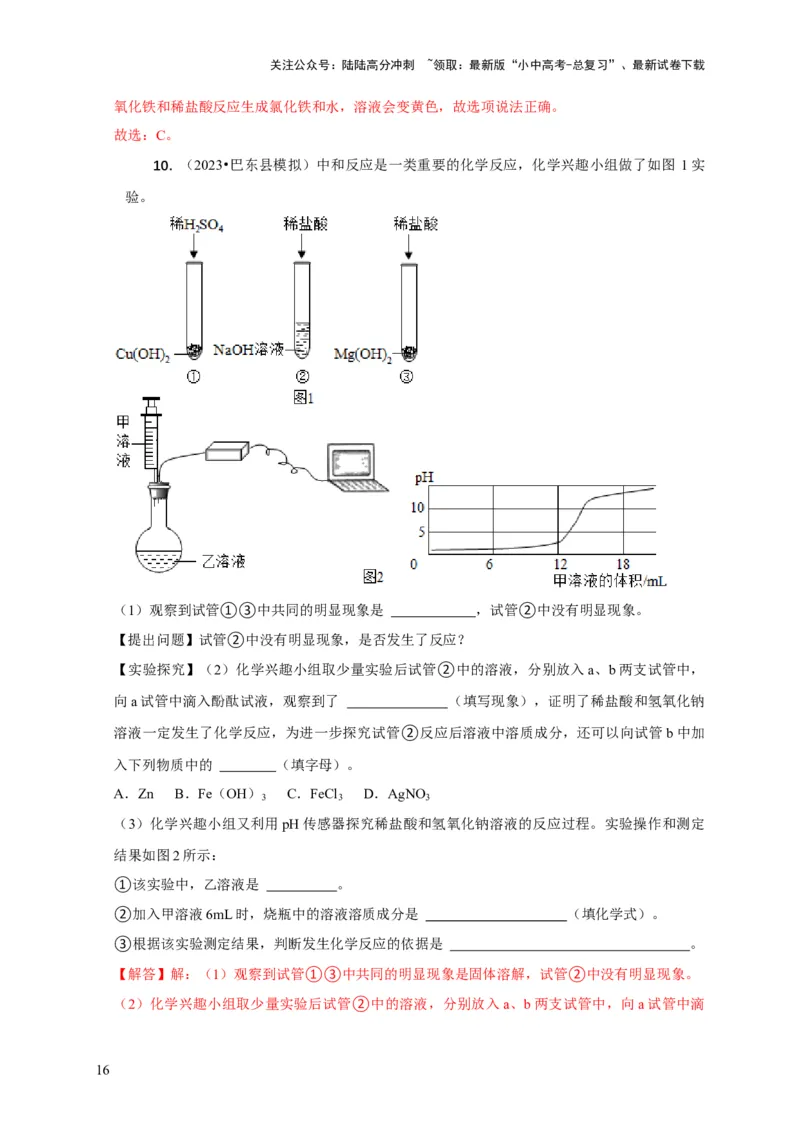
10. (2023•巴东县模拟)中和反应是一类重要的化学反应,化学兴趣小组做了如图 1实
验。
(1)观察到试管①③中共同的明显现象是 ,试管②中没有明显现象。
【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】(2)化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,
向a试管中滴入酚酞试液,观察到了 (填写现象),证明了稀盐酸和氢氧化钠
溶液一定发生了化学反应,为进一步探究试管②反应后溶液中溶质成分,还可以向试管b中加
入下列物质中的 (填字母)。
A.Zn B.Fe(OH) C.FeCl D.AgNO
3 3 3
(3)化学兴趣小组又利用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程。实验操作和测定
结果如图2所示:
①该实验中,乙溶液是 。
②加入甲溶液6mL时,烧瓶中的溶液溶质成分是 (填化学式)。
③根据该实验测定结果,判断发生化学反应的依据是 。
【解答】解:(1)观察到试管①③中共同的明显现象是固体溶解,试管②中没有明显现象。
(2)化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,向a试管中滴
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
入酚酞试液,观察到了溶液不变色,说明氢氧化钠消失,证明了稀盐酸和氢氧化钠溶液一定发
生了化学反应,为进一步探究试管②反应后溶液中溶质成分,还可以向试管b中加入下列物质
中的Zn、Fe(OH) ,是因为如果稀盐酸过量,则锌、氢氧化铁能够溶解,如果恰好完全反应,
3
锌和氢氧化铁不能溶解。
(3)①该实验中,溶液pH由小于7逐渐升高,则乙溶液是稀盐酸。
②加入甲溶液6mL时,稀盐酸过量,烧瓶中的溶液溶质成分是反应生成的氯化钠和过量的氯化
氢。
③根据该实验测定结果,判断发生化学反应的依据是溶液pH由小于7逐渐变成大于7。
17