文档内容
二○一五年聊城市初中学生学业水平考试
化学试题(含答案全解全析)
(选择题 共40分)
可能用到的相对原子质量:H—1 C—12 O—16 S—32 Cu—64 Zn—65
一、选择题(本题包括16小题,共40分。每小题只有一个选项符合题意。1~8小题每题2
分,9~16小题每题3分)
1.空气是一种宝贵的自然资源,分离液态空气不能得到的气体是( )
A.氧气 B.稀有气体
C.氮气 D.氢气
2.下列在厨房中发生的变化属于物理变化的是( )
A.水果榨汁 B.冬瓜腐烂
C.铁锅生锈 D.煤气燃烧
3.以下的“水”属于纯净物的是( )
A.雨水 B.矿泉水C.海水 D.蒸馏水
4.下列符号表示两个氢原子的是( )
A.2H+ B.2H C.H D.2H
2 2
5.下列洗涤方式应用乳化作用的是( )
A.用汽油除去衣服上的油污
B.用水洗去盘子中的水果渣
C.用洗洁精清洗餐具上的油污
D.用盐酸清洗水壶的水垢
6.下列微观解释不正确的是( )
A.氨水挥发——分子不断运动
B.将二氧化碳气体制成干冰,体积变小——分子的体积变小
C.18 g水中大约有6.02×1023个水分子——分子的质量很小
D.50 mL酒精和50 mL水混合后总体积小于100 mL——分子间有间隔
7.在日常生活中,下列做法正确的是( )
A.用甲醛浸泡虾仁
B.焙制糕点时添加含小苏打的发酵粉
C.用霉变的谷物做饲料
D.为防止骨质疏松,长期摄入过量的钙元素
8.下列实验操作中,不正确的是( )9.2015年“世界水日”“中国水周”的宣传主题为“节约水资源,保障水安全”。下列有关
水的认识中错误的是( )
A.大量使用农药、化肥,不会造成水体污染
B.水通过三态变化实现天然循环
C.水是生命之源,保护水资源包括防止水体污染和节约用水两方面
D.随意丢弃废电池易造成水土重金属污染
10.根据你的生活经验和所学的化学知识,判断下列做法不能达到目的的是( )
A.用灼烧闻气味的方法区分羊毛线和棉线
B.用碳酸氢钠治疗胃酸过多
C.用燃烧的小木条放入集气瓶内来检验二氧化碳是否集满
D.用肥皂水涂在蚊虫叮咬处止痒
11.观察是学习化学的重要方法之一,以下是某同学记录的化学实验现象,其中符合事实的是(
)
A.敞开浓盐酸试剂瓶口冒出白雾
B.用pH试纸测得某溶液的pH=1.4
C.铵态氮肥与碱共热放出无色无味气体
D.马铃薯片遇到碘酒后颜色不变
12.很多饮料中都含有柠檬酸(C H O )。下列关于柠檬酸的说法中正确的是( )
6 8 7
A.属于氧化物
B.由6个碳原子、8个氢原子和7个氧原子组成
C.分子中氧元素的质量分数最大
D.分子中碳、氢、氧三种元素的质量比为6∶8∶7
13.下列有关物质的归类错误的是( )
选项 物质 归类
A 白酒、糖水、食盐水 常见溶液
B 蛋白质、油脂、维生素 营养物质
C 风能、氢能、太阳能 清洁能源
D 生铁、玻璃、玻璃钢 复合材料
14.如图所示是两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,下列说法
正确的是( )
A.化学反应前后原子的种类不变
B.生成物一定是氧化物
C.化学反应前后分子的种类不变
D.该反应属于置换反应15.“类推”是化学学习过程中常用的思维方法。现有以下类推结果,其中正确的是( )
A.因为碱溶液呈碱性,所以呈碱性的溶液一定是碱溶液
B.金属铝与盐酸反应生成AlCl 和H ,所以金属铁与盐酸反应生成FeCl 和H
3 2 3 2
C.因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件
D.因为蜡烛燃烧生成二氧化碳和水,所以蜡烛中一定含有碳元素和氢元素
16.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )
选项 物质(括号内为杂质) 试剂 操作方法
A NaCl溶液(Na CO ) Ca(OH) 溶液 过滤
2 3 2
B KNO (NaCl) H O 蒸发、过滤
3 2
C N (O ) 足量铜粉 加热
2 2
D 稀硫酸(稀盐酸) 适量氯化钡溶液 过滤
(非选择题 共60分)
二、填空题(本题包括4小题,共28分)
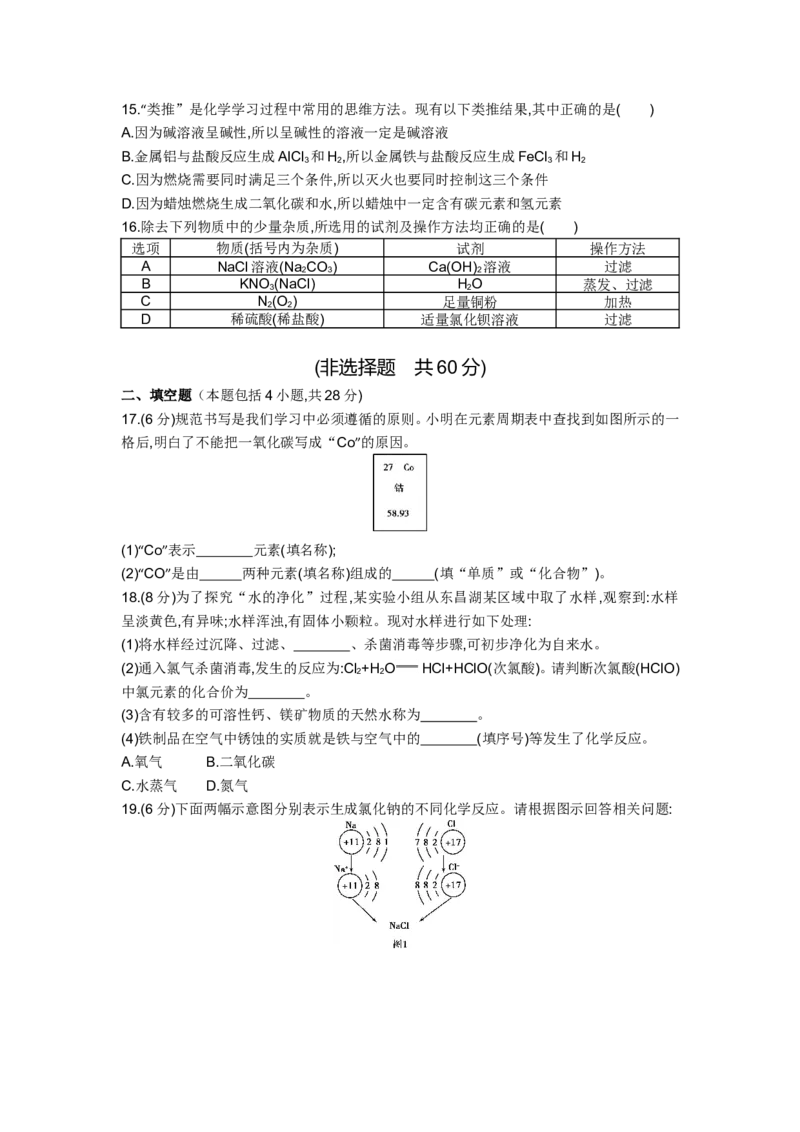
17.(6分)规范书写是我们学习中必须遵循的原则。小明在元素周期表中查找到如图所示的一
格后,明白了不能把一氧化碳写成“Co”的原因。
(1)“Co”表示 元素(填名称);
(2)“CO”是由 两种元素(填名称)组成的 (填“单质”或“化合物”)。
18.(8分)为了探究“水的净化”过程,某实验小组从东昌湖某区域中取了水样,观察到:水样
呈淡黄色,有异味;水样浑浊,有固体小颗粒。现对水样进行如下处理:
(1)将水样经过沉降、过滤、 、杀菌消毒等步骤,可初步净化为自来水。
(2)通入氯气杀菌消毒,发生的反应为:Cl +H O HCl+HClO(次氯酸)。请判断次氯酸(HClO)
2 2
中氯元素的化合价为 。
(3)含有较多的可溶性钙、镁矿物质的天然水称为 。
(4)铁制品在空气中锈蚀的实质就是铁与空气中的 (填序号)等发生了化学反应。
A.氧气 B.二氧化碳
C.水蒸气 D.氮气
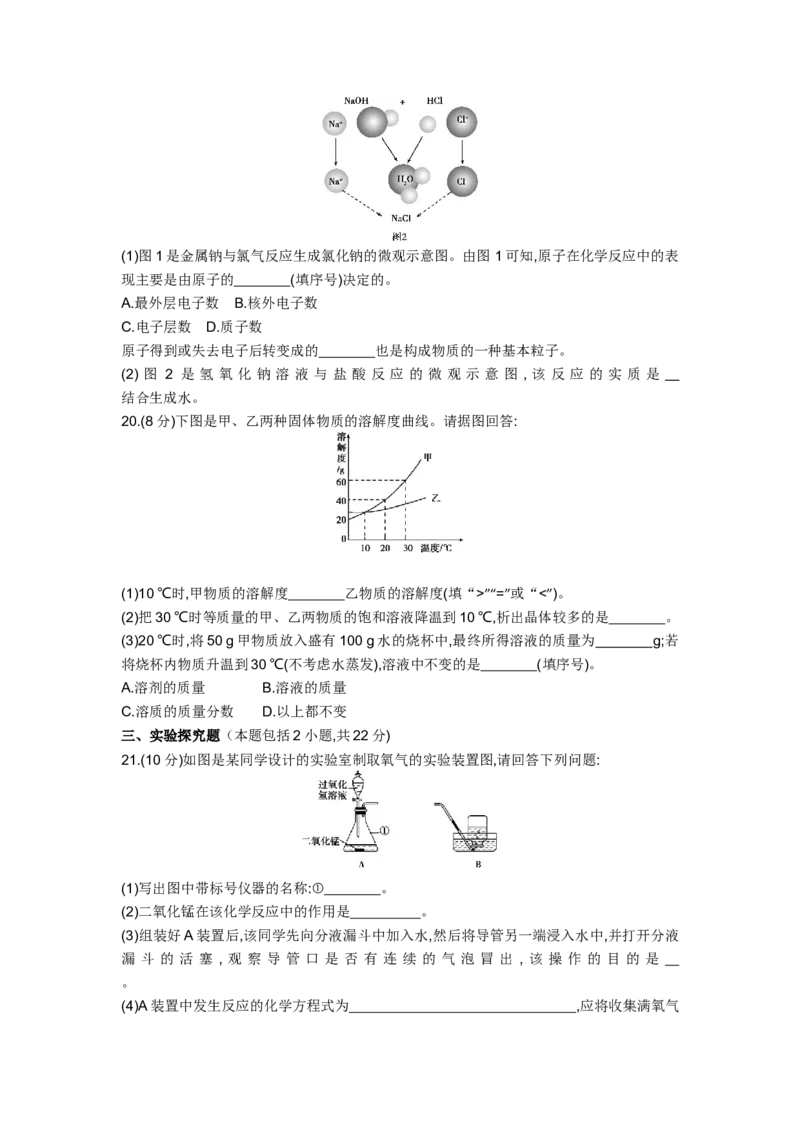
19.(6分)下面两幅示意图分别表示生成氯化钠的不同化学反应。请根据图示回答相关问题:(1)图1是金属钠与氯气反应生成氯化钠的微观示意图。由图 1可知,原子在化学反应中的表
现主要是由原子的 (填序号)决定的。
A.最外层电子数 B.核外电子数
C.电子层数 D.质子数
原子得到或失去电子后转变成的 也是构成物质的一种基本粒子。
(2) 图 2 是 氢 氧 化 钠 溶 液 与 盐 酸 反 应 的 微 观 示 意 图 , 该 反 应 的 实 质 是
结合生成水。
20.(8分)下图是甲、乙两种固体物质的溶解度曲线。请据图回答:
(1)10 ℃时,甲物质的溶解度 乙物质的溶解度(填“>”“=”或“<”)。
(2)把30 ℃时等质量的甲、乙两物质的饱和溶液降温到10 ℃,析出晶体较多的是 。
(3)20 ℃时,将50 g甲物质放入盛有100 g水的烧杯中,最终所得溶液的质量为 g;若
将烧杯内物质升温到30 ℃(不考虑水蒸发),溶液中不变的是 (填序号)。
A.溶剂的质量 B.溶液的质量
C.溶质的质量分数 D.以上都不变
三、实验探究题(本题包括2小题,共22分)
21.(10分)如图是某同学设计的实验室制取氧气的实验装置图,请回答下列问题:
(1)写出图中带标号仪器的名称:① 。
(2)二氧化锰在该化学反应中的作用是 。
(3)组装好A装置后,该同学先向分液漏斗中加入水,然后将导管另一端浸入水中,并打开分液
漏 斗 的 活 塞 , 观 察 导 管 口 是 否 有 连 续 的 气 泡 冒 出 , 该 操 作 的 目 的 是
。
(4)A装置中发生反应的化学方程式为 ,应将收集满氧气的集气瓶 放在桌面上。
22.(12分)呼吸面具中“氧气再生剂”的主要成分是淡黄色固体过氧化钠(Na O ),使用后变
2 2
成白色固体。某兴趣小组对白色固体的成分进行了探究:
【查阅资料】2Na O +2CO 2Na CO +O
2 2 2 2 3 2
2Na O +2H O 4NaOH+O ↑
2 2 2 2
【提出猜想】根据呼出的气体中含有较多的 ,对白色固体作出如下猜想:
猜想Ⅰ:氢氧化钠 猜想Ⅱ:碳酸钠 猜想Ⅲ:氢氧化钠和碳酸钠
【实验验证】
实验操作 实验现象 实验结论
(1)取少量样品溶于水,加入适量 产生白色沉淀 该反应的化学方程式为
(2)将上述反应后的混合物过滤,取滤液
证明猜想Ⅲ正确
加入
【得出结论】猜想Ⅲ成立。
【拓展应用】“氧气再生剂”的保存方法是 。
四、计算题(本题包括1小题,共10分)
23.(10分)现将10 g铜锌(Cu-Zn)合金放入到一定质量的稀硫酸中恰好完全反应,过滤得到
100 g溶质质量分数为16.1%的溶液。据此请完成下列问题:
(1)生成氢气 g;
(2)稀硫酸中H SO 的质量是 g;
2 4
(3)合金中铜的质量分数是多少?
答案全解全析:
1.D 空气中各成分按体积分数,氮气约占78%,氧气约占21%,稀有气体约占0.94%,二氧化
碳约占0.03%,其他气体和杂质约占0.03%,氢气在空气中的含量极小,故分离液态空气不能
得到氢气,故选D。
2.A 水果榨汁没有生成新物质,属于物理变化;冬瓜腐烂、铁锅生锈、煤气燃烧都生成了新物
质,属于化学变化,故选A。
3.D 雨水、矿泉水、海水中都溶解了一些其他物质,属于混合物;蒸馏水中只有水一种物质,
属于纯净物,故选D。
4.B 2H+表示2个氢离子;2H表示2个氢原子;H 表示1个氢气分子;2H 表示2个氢气分子,
2 2
故选B。
评析 本题考查化学用语表示的意义,是中考中的高频考点,也是易错点,难度不大。解题的关
键是熟练掌握元素符号前面、右下角、正上方、右上角的数字表示的意义。
5.C 汽油除去油污,是汽油把油污溶解了,故A不符合题意;用水洗去水果渣,是利用水流将
水果渣从盘子表面冲洗掉,故B不符合题意;洗洁精洗去油污,利用了乳化原理,故C符合题意;
盐酸洗去水垢,属于发生化学反应,故D不符合题意。
6.B 氨水挥发,是因为氨气分子不断运动到空气中,故A正确;二氧化碳气体制成干冰,体积变小,是因为分子间的间隔变小,故B错误;18 g水中大约有6.02×1023个水分子,说明水分子
的质量很小,故C正确;酒精和水混合后体积变小,是因为分子间有间隔,故D正确。
评析 本题考查分子的基本性质,属于基础题。只要正确记忆分子的基本性质即可正确解答。
7.B 甲醛有毒,对人体有害,故A错误;小苏打是发酵粉的主要成分,故B正确;霉变的谷物中
含有毒物质,故C错误;长期摄入过量的钙元素对人体有害,故D错误。
8.B 稀释浓硫酸时,应将浓硫酸沿器壁慢慢倒入水中,并用玻璃棒不断搅拌,故B错误。
9.A 大量使用农药、化肥会造成水体污染,故A错误。
评析 本题主要考查水资源的保护,是中考中的热点问题,难度不大,属于基础题。只要熟记水
资源的保护措施及水污染的来源和防治措施即可正确解答。
10.C 灼烧时,羊毛线有烧焦羽毛的气味,棉线没有,故A能达到目的;治疗胃酸过多主要用含
有碳酸氢钠或氢氧化铝的药物,故B能达到目的;应将燃着的木条放在集气瓶口来检验二氧
化碳是否收集满,故C不能达到目的;蚊虫的毒液显酸性,肥皂水显碱性,能发生中和反应从而
减轻痛痒,故D能达到目的。
11.A 浓盐酸有挥发性,敞口放置时,挥发出的氯化氢与水蒸气结合形成白雾,故A符合;用
pH试纸测得的pH是整数,故B不符合;铵态氮肥与碱共热,产生有刺激性气味的气体,故C不
符合;马铃薯中的淀粉遇碘变蓝,故D不符合。
12.C 柠檬酸中有C、H、O三种元素,不属于氧化物,故A错误;柠檬酸由C、H、O三种元素组
成,每个柠檬酸分子由6个碳原子、8个氢原子和7个氧原子构成,故B错误;由柠檬酸分子的
构成,及各元素的相对原子质量可推知,氧元素的质量分数最大,故C正确;柠檬酸中C、H、O
三种元素的质量比=(12×6)∶(1×8)∶(16×7)=9∶1∶14,故D错误。
13.D 白酒、糖水、食盐水都是常见的溶液,故A正确;蛋白质、油脂、维生素都属于营养物质,
故B正确;风能、氢能、太阳能使用后没有污染,都属于清洁能源,故C正确;生铁属于金属材料
玻璃属于无机非金属材料,玻璃钢属于复合材料,故D错误。
14.A 化学反应前后原子的种类、数目、质量都不改变,故A正确;生成物中不能确定有氧元
素,故B错误;化学反应前后分子的种类一定发生改变,故C错误;从微观示意图看出,该反应
是两种单质反应生成一种化合物,属于化合反应,故D错误。
15.D 碱溶液显碱性,显碱性的溶液不一定是碱溶液,如碳酸钠溶液显碱性,碳酸钠属于盐,故
A错误;铁与稀盐酸反应生成FeCl 和H ,故B错误;只需要破坏燃烧三个条件中的一个即可
2 2
达到灭火目的,故C错误;蜡烛燃烧生成二氧化碳和水,根据化学反应前后元素的种类不变,可
知蜡烛中一定含有碳元素和氢元素,故D正确。
16.C 碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,虽然除去了碳酸钠,但是引入了
新的杂质氢氧化钠,故A错误;除去硝酸钾中的氯化钠,应该用降温结晶的方法,故B错误;铜粉
在加热的条件下,能和氧气反应,而不能和氮气反应,故C正确;氯化钡和稀硫酸反应,和稀盐酸
不反应,故D错误。
17.答案 (6分)(1)钴 (2)碳、氧 化合物
解析 (1)从图中看出Co表示钴元素。(2)CO由碳元素和氧元素组成,属于化合物。
18.答案 (8分)(1)吸附 (2)+1 (3)硬水 (4)AC(选对1个给1分,错选1个不得分)
解析 (1)将水样经过沉降、过滤、吸附、消毒杀菌等步骤,可初步得到自来水。
(2)设Cl的化合价为x,则(+1)+x+(-2)=0,x=+1。
(3)含有较多的可溶性钙、镁矿物质的天然水称为硬水。
(4)铁制品生锈是铁与空气中的氧气、水发生了化学反应。
19.答案 (6分)(1)A 离子 (2)氢离子(或H+)和氢氧根离子(或OH-)
解析 (1)从图1看出,原子在化学反应中的表现主要是由原子的最外层电子数决定的。原子
得到或失去电子后变成离子,离子也是构成物质的一种粒子。(2)中和反应的实质是酸中的氢离子(H+)和碱中的氢氧根离子(OH-)结合生成水。
20.答案 (8分)(1)= (2)甲 (3)140 A
解析 (1)从溶解度曲线看出,10 ℃时,甲、乙两种物质的溶解度相等。(2)30 ℃时,甲的溶解度
大于乙,等质量的甲、乙两种物质的饱和溶液降温到10 ℃时,甲析出的晶体多。(3)20 ℃时,甲
物质的溶解度为40 g,将50 g甲物质放入100 g 水中,只能溶解40 g,得到140 g饱和溶液;如
果升温到30 ℃,甲物质的溶解度变大,没有溶解的甲物质继续溶解,溶液中溶质增加,溶液的
质量也增大,而溶剂的质量还是100 g,所以溶质的质量分数也变大。
评析 本题考查溶解度曲线的意义,有一定难度,属于易错题。正确理解溶解度曲线的意义是
解题的关键。
21.答案 (10 分)(1)锥形瓶 (2)催化作用 (3)检查装置的气密性 (4)2H O
2 2
2H O+O ↑ 正
2 2
解析 (1)根据常见仪器的名称可知①为锥形瓶。
(2)过氧化氢分解时,二氧化锰起催化作用。
(3)该操作的目的是检查装置的气密性。
(4)过氧化氢在二氧化锰作催化剂的条件下,分解生成水和氧气,化学方程式为:2H O
2 2
2H O+O ↑。因为氧气的密度大于空气,所以收集满氧气的集气瓶要正放在桌面上。
2 2
评析 本题考查气体的制取方法,难度不大,属于基础题。根据实验室制取氧气的原理、步骤
逐一解答即可。
22.答案 (12分)【提出猜想】水蒸气和二氧化碳(水蒸气写成水、写化学式也给分,答对一种
给1分)
【实验验证】(1)氯化钡溶液(其他合理答案均可得分)(写化学式也给分)
BaCl +Na CO BaCO ↓+2NaCl(其他合理答案均可得分)
2 2 3 3
(2)酚酞试液(紫色石蕊试液或氯化铜溶液) 溶液变红色(溶液变蓝或生成蓝色沉淀等合理答
案均可,但两空必须一致)
【拓展应用】密封存放干燥处
解析 【提出猜想】呼出的气体中含有较多的二氧化碳和水蒸气。
【实验验证】取少量样品溶于水,加入适量的氯化钡溶液,产生白色沉淀,说明有碳酸钠,碳酸钠
与氯化钡反应生成碳酸钡白色沉淀和氯化钠;充分反应后过滤,取滤液加入无色酚酞试液,溶
液变红色,证明含有氢氧化钠,因此猜想Ⅲ正确。
【拓展应用】“氧气再生剂”的主要成分是淡黄色固体过氧化钠(Na O ),它能与二氧化碳和
2 2
水蒸气反应,因此保存方法是密封存放干燥处。
评析 本题既考查了实验步骤的设计,又考查了化学方程式的书写,综合性比较强。实验探究
题是近几年中考的热点题型,它包括实验方法和实验过程的探究、实验结论和实验规律的探
究等。
23.答案 (10分)(1)0.2(2分)
(2)9.8(2分)
(3)生成ZnSO 的质量为100 g×16.1%=16.1 g(1分)
4
设合金中锌的质量为x(1分)
Zn+H SO ZnSO +H ↑(1分)
2 4 4 2
65 161
x 16.1 g
65∶x=161∶16.1 gx=6.5 g(1分)
合金中铜的质量分数为 ×100%=35%(2分)
答:合金中铜的质量分数为35%。
解析 根据题意可知,生成的硫酸锌的质量=100 g×16.1%=16.1 g,然后根据化学方程式计算
出氢气的质量、反应的硫酸的质量、反应的锌的质量,即可求解。
评析 本题是一道有关化学方程式的计算题,难度不大,只要熟练掌握有关化学方程式计算的
步骤、要点,即可完成解答。