文档内容
2024 年中考押题预测卷【武汉卷】
化 学
(考试时间:50分钟 试卷满分:50分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cl-35.5 Fe-56 Ti-48
第Ⅰ卷
一、选择题(本题8小题,每小题只有一个选项符合题意。每小题3分,共24分)
1.下列对石墨性质的描述中,属于化学性质的是( )
A.灰黑色固体 B.还原性
C.难溶于水 D.优良导电性
2.规范的实验操作是完成实验的基本保障。下列操作正确的是( )
A. 熄灭酒精灯 B. 读取液体体积
C. 加热固体 D. 倾倒液体
3.一种获取饮用水的简易净水装置如图所示。下列说法错误的是( )
A.pp棉滤网可以除去难溶性杂质
B.活性炭的作用是除去色素和异味
C.所得到的净化水为纯净物
D.细菌可以通过pp棉滤网
4.氮和镓的原子结构示意图及镓在元素周期表中的信息如图所示,下列说法正确的是( )A.镓元素位于第三周期,属于金属元素 B.镓原子核内有31个中子
C.镓的相对原子质量是69.72g D.氮化镓的化学式为GaN
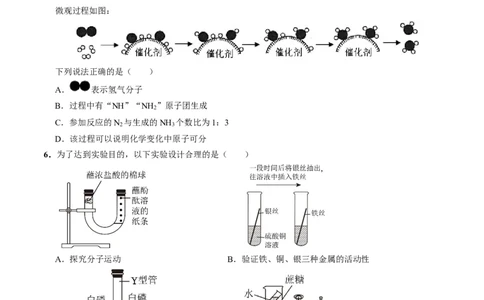
5.NH 的合成开启了工业催化新纪元,为世界粮食增产做出了巨大贡献。以 N 和H 为反应物合成NH 的
3 2 2 3
微观过程如图:
下列说法正确的是( )
A. 表示氢气分子
B.过程中有“NH”“NH ”原子团生成
2
C.参加反应的N 与生成的NH 个数比为1:3
2 3
D.该过程可以说明化学变化中原子可分
6.为了达到实验目的,以下实验设计合理的是( )
A.探究分子运动 B.验证铁、铜、银三种金属的活动性
C.探究可燃物燃烧需与氧气接触 D.验证质量守恒定律
7.甲、乙、丙、丁是初中化学常见物质,它们之间有如图所示转化关系(部分反应物、生成物及反应条
件已略去,“—”表示相邻的两种物质能发生反应,“→”表示某一物质经一步反应可转化为另一种物
质)。下列说法错误的是( )A.若乙为氧气,则甲可以是碳、氢气或一氧化碳
B.若甲为金属氧化物,乙为碳,则丙是氧气
C.若丙为氧气,则乙可以是具有还原性的物质
D.符合该转化关系所涉及的物质可以是固体、液体和气体
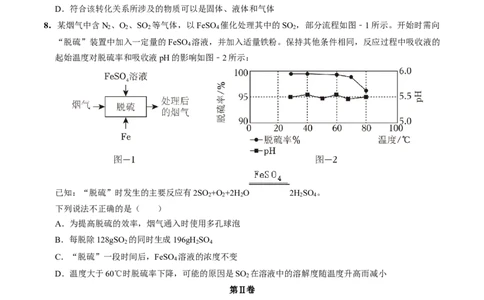
8.某烟气中含N 、O 、SO 等气体,以FeSO 催化处理其中的SO ,部分流程如图﹣1所示。开始时需向
2 2 2 4 2
“脱硫”装置中加入一定量的FeSO 溶液,并加入适量铁粉。保持其他条件相同,反应过程中吸收液的
4
起始温度对脱硫率和吸收液pH的影响如图﹣2所示:
已知:“脱硫”时发生的主要反应有2SO +O +2H O 2H SO 。
2 2 2 2 4
下列说法不正确的是( )
A.为提高脱硫的效率,烟气通入时使用多孔球泡
B.每脱除128gSO 的同时生成196gH SO
2 2 4
C.“脱硫”一段时间后,FeSO 溶液的浓度不变
4
D.温度大于60℃时脱硫率下降,可能的原因是SO 在溶液中的溶解度随温度升高而减小
2
第Ⅱ卷
二、非选择题(本题包括5小题,共26分)
9.(4分)多彩的“碳”装点多姿的生活。让我们一起走进“碳”的世界,了解碳及其化合物。
(1)碳单质的种类很多。“钻石恒久远,一颗永流传”所指的碳单质是 (写名称)。
(2)二氧化碳灭火器,用于图书、档案等的灭火,其主要灭火原理是 。
(3)煤气是一种重要的含碳燃料,写出其主要成分燃烧的化学方程式: 。
10.(4分)生活在盐湖、碱湖附近的人们传承下来的劳动经验是“夏天晒盐(NaCl),冬天捞碱
(Na CO )”。
2 3
【资料】NaCl和Na CO 两种物质在不同温度时的溶解度如表。
2 3温度/℃ 0 10 20 30 40
溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6
Na CO 7.0 12.5 22.0 40.0 48.8
2 3
(1)20℃时,将20.0g氯化钠溶解在50.0g水中,得到 (填“饱和”或“不饱和”)溶液。
(2)“冬天捞碱”得到的主要成分为Na CO ,提取表格信息并解释冬天能捞到碱的原因是
2 3
。
(3)将溶质质量分数为20.0%的氯化钠溶液50.0g加水稀释成10.0%,需要加水的质量是 g。
(4)下列说法正确的 (填标号)。
a.等质量的固体配成20℃的饱和溶液所需水的质量:NaCl<Na CO
2 3
b.20℃时饱和溶液的溶质质量分数:NaCl>Na CO
2 3
c.冬天捞得的“碱”若含有少量NaCl,则可用蒸发结晶提纯Na CO
2 3
d.检验捞得的“碱”中含有NaCl的操作:溶于水,加入稀盐酸,观察现象
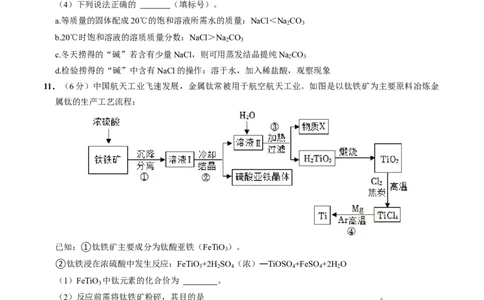
11.(6分)中国航天工业飞速发展,金属钛常被用于航空航天工业。如图是以钛铁矿为主要原料冶炼金
属钛的生产工艺流程:
已知:①钛铁矿主要成分为钛酸亚铁(FeTiO )。
3
②钛铁浸在浓硫酸中发生反应:FeTiO +2H SO (浓)═TiOSO +FeSO +2H O
3 2 4 4 4 2
(1)FeTiO 中钛元素的化合价为 。
3
(2)反应前需将钛铁矿粉碎,其目的是 。
(3)溶液Ⅱ的主要溶质为TiOSO ,加热时和水发生反应,经过滤得到H TiO 。已知X的溶质是一种
4 2 3
初中化学常见的酸,写出该反应的化学方程式 。
(4)步骤④发生的反应为TiCl +2Mg═2MgCl +Ti,此反应需要在Ar氛围下进行,其中Ar的作用是
4 2
。
(5)若在制备过程中有20%的钛元素损失,最终获得4.8t的单质钛,则20t钛铁矿中钛酸亚铁的质量分
数为 。
12.(6分)烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中常含有杂质碳酸钠。某科学学习小
组同学围绕工业烧碱样品纯度测定问题,展开了讨论与探究。(原理思路)利用Na CO 与稀H SO 反应产生CO ,通过CO 质量的测定,确定样品中碳酸钠的质量,
2 3 2 4 2 2
从而计算样品纯度。
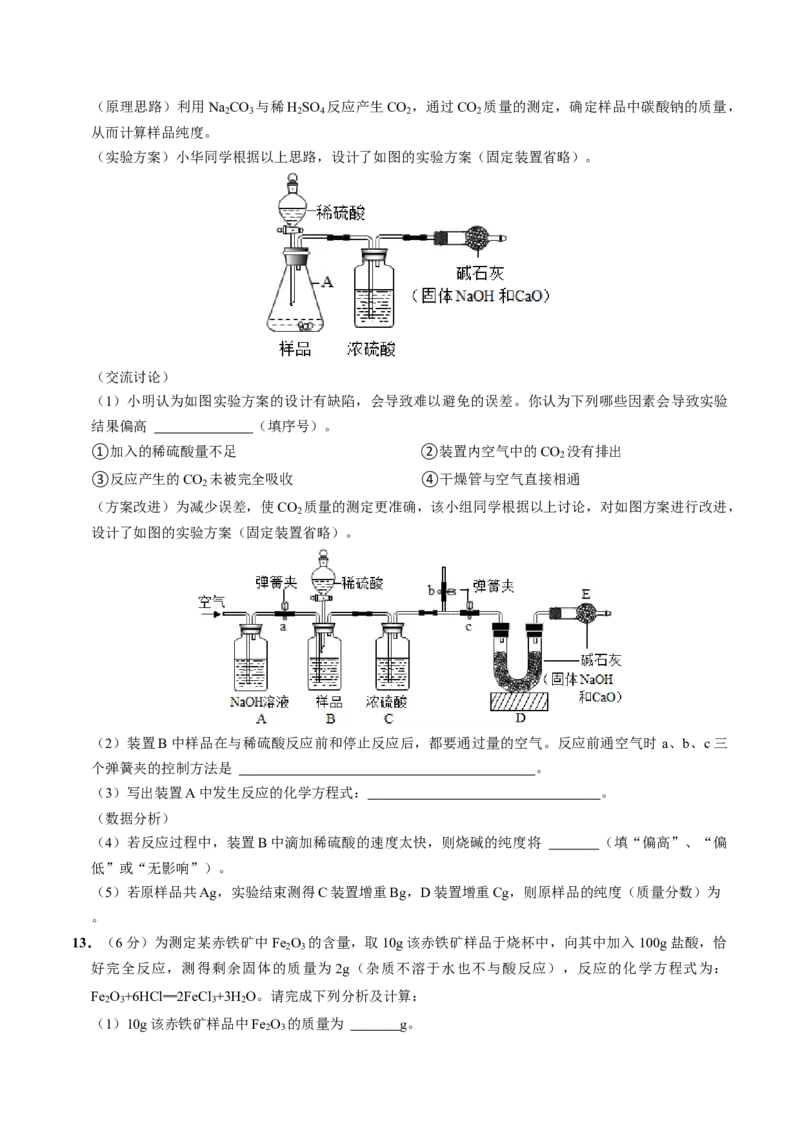
(实验方案)小华同学根据以上思路,设计了如图的实验方案(固定装置省略)。
(交流讨论)
(1)小明认为如图实验方案的设计有缺陷,会导致难以避免的误差。你认为下列哪些因素会导致实验
结果偏高 (填序号)。
①加入的稀硫酸量不足 ②装置内空气中的CO 没有排出
2
③反应产生的CO 未被完全吸收 ④干燥管与空气直接相通
2
(方案改进)为减少误差,使CO 质量的测定更准确,该小组同学根据以上讨论,对如图方案进行改进,
2
设计了如图的实验方案(固定装置省略)。
(2)装置B中样品在与稀硫酸反应前和停止反应后,都要通过量的空气。反应前通空气时 a、b、c三
个弹簧夹的控制方法是 。
(3)写出装置A中发生反应的化学方程式: 。
(数据分析)
(4)若反应过程中,装置B中滴加稀硫酸的速度太快,则烧碱的纯度将 (填“偏高”、“偏
低”或“无影响”)。
(5)若原样品共Ag,实验结束测得C装置增重Bg,D装置增重Cg,则原样品的纯度(质量分数)为
。
13.(6分)为测定某赤铁矿中Fe O 的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g盐酸,恰
2 3
好完全反应,测得剩余固体的质量为2g(杂质不溶于水也不与酸反应),反应的化学方程式为:
Fe O +6HCl═2FeCl +3H O。请完成下列分析及计算:
2 3 3 2
(1)10g该赤铁矿样品中Fe O 的质量为 g。
2 3(2)计算稀盐酸中溶质的质量分数。(写出计算过程)。