文档内容
班级 姓名 学号 分数
人教版化学九年级下期中模拟卷(二)
(时间:60分钟,满分100分)
一、选择题(20小题,每小题2分,共40分)
1、【2020四川攀枝花】将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是( )
A.高锰酸钾 B.菜籽油 C.面粉 D.白糖
【答案】D
【解析】A、高锰酸钾溶于水形成紫红色溶液,不符合题意;
B、菜籽油不溶于水,与水混合形成乳浊液,不符合题意;
C、面粉不溶于水,与水混合形成悬浊液,不符合题意;
D、白糖溶于水形成无色溶液,符合题意。故选D。
2、【2020江苏扬州】不同的物质溶于水后会形成酸碱性不同的溶液,下列溶液显酸性的是( )
A.食醋 B.氨水 C.NaCl溶液 D.NaCO 溶液
2 3
【答案】A
【解析】A、食醋的成分有醋酸,溶液显酸性,选项正确;
B、氨水是碱,溶液呈碱性,选项错误;
C、NaCl溶液溶液呈中性,选项错误;
D、NaCO 俗称纯碱,溶液呈碱性,选项错误。
2 3
故选A。
3、下列物质属于碱的是( )
A. HO B. NaHCO C.Ca(OH) D.HBO
2 3 2 3 3
【答案】C
【解析】碱是由金属离子和氢氧根离子构成的,A为氧化物,B属于盐,C属于碱,D是酸,故选C。
4、【2020湖南邵阳】下列有关溶液的说法正确的是( )
A.均一、稳定的液体一定是溶液
B.稀释浓硫酸时,会放出大量的热
C.降低温度,不饱和溶液一定能变成饱和溶液
D.实验室利用氯化钠固体和水配制50g质量分数为6%的氯化钠溶液的步骤是:计算、量取、溶解、贮存
【答案】B【解析】A、均一的、稳定的液体不一定是溶液,如水,故A错误;
B、稀释浓硫酸时,会放出大量的热,故B正确;
C、降低温度,不饱和溶液不一定能变成饱和溶液,有些溶质的溶解度随温度降低而升高,温度降低后还
是不饱和溶液,故C错误;
D、实验室配制50克溶质质量分数为6%的氯化钠溶液,首先计算配制溶液所需氯化钠的质量和水的体积,
再称量所需的氯化钠和量取水,最后进行溶解。故实验室配制50克溶质质量分数为6%的氯化钠溶液的步
骤是计算、称量、量取、溶解、贮存。故D错误。
故选B。
5、【2020山东滨州】已知A、B、C、D是四种金属单质,A能从B的硝酸盐溶液中置换出B,但A不能与稀
盐酸反应;相同条件下,C、D能与稀盐酸反应产生H ,且D比C反应剧烈。则四种金属的活动性由强到弱
2
的顺序是( )
A.D>C>A>B B.A>B>C>D C.B>A>C>D D.D>C>B>A
【答案】A
【解析】A能置换出B,说明A比B活泼,C、D能与稀盐酸反应产生H 且D比C反应剧烈,而A不能,说明
2
D比C活泼,C比 A活泼,故活动顺序 D>C>A>B,故选A。
6、【2020湖南株洲】常温下,一些饮料或食物的近似pH如下:
食物 柠檬汁 橙子汁 西瓜汁 鸡蛋清
pH 2.2~2.4 3.6~4.3 5.3~6.1 7.6~8.0
下列说法中正确的是( )
A.胃酸过多的人应多喝柠檬汁
B.西瓜汁和鸡蛋清显碱性
C.西瓜汁比柠檬汁酸性强
D.柠檬汁和橙子汁显酸性
【答案】D
【解析】A、柠檬汁pH 范围是2.2~2.4,pH<7,显酸性,胃酸过多的人应尽量少喝柠檬汁,否则会加重病
情,故错误。
B、西瓜汁pH 范围是5.3~6.1,pH<7,显酸性,鸡蛋清pH 范围是7.6~8.0,pH﹥7,显碱性,故错误。
C、西瓜汁pH 范围是5.3~6.1,柠檬汁pH 范围是2.2~2.4,均小于7,且柠檬汁的pH小于西瓜汁,则柠檬
汁比西瓜汁的酸性强,故错误。
D、柠檬汁pH 范围是2.2~2.4,橙子汁pH 范围是3.6~4.3,均小于7,则柠檬汁和橙子汁显酸性,故正确。故选D。
7、【2019广西北部湾】下列措施中,不能防止金属制品锈蚀的是( )
A.在表面刷漆 B.在表面涂油 C.在表面镀铬 D.用湿布擦拭
【答案】D
【解析】A、在表面刷漆,能隔绝氧气和水,能防止金属制品锈蚀,故选项错误。
B、在表面涂油,能隔绝氧气和水,能防止金属制品锈蚀,故选项错误。
C、在表面镀铬,能隔绝氧气和水,能防止金属制品锈蚀,故选项错误。
D、用湿布擦拭,金属制品能与氧气、水分充分接触,不能防止金属制品锈蚀,故选项正确。
故选:D。
8、下列关于浓硫酸的说法正确的是( )
A.易挥发 B.有腐蚀性 C.无吸水性 D.密度比水小
【答案】B
【解析】浓硫酸具有吸水性、腐蚀性、不挥发,密度比水大,溶解放热的性质,故选择B。
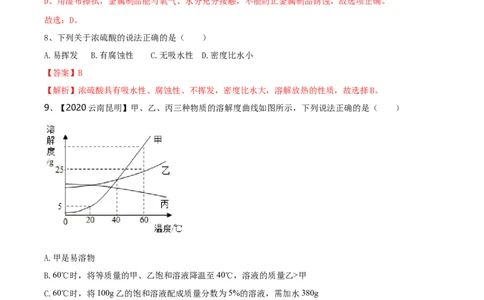
9、【2020云南昆明】甲、乙、丙三种物质的溶解度曲线如图所示,下列说法正确的是( )
A.甲是易溶物
B.60℃时,将等质量的甲、乙饱和溶液降温至40℃,溶液的质量乙>甲
C.60℃时,将100g乙的饱和溶液配成质量分数为5%的溶液,需加水380g
D.甲中混有少量丙,若要得到较纯净的甲,常采用蒸发结晶的方法
【答案】B
【解析】A、由图可知,20℃时,甲的溶解度是5g,属于可溶物,不符合题意;
B、由图可知,60℃时,溶解度:甲>乙,该温度下,饱和溶液的溶质质量分数:甲>乙,故等质量的甲、
乙饱和溶液中溶质质量:甲>乙,40℃时,溶解度:甲=乙,故该温度下,饱和溶液的溶质质量分数:甲=
乙,溶质质量:甲=乙,故降温后,析出晶体的质量:甲>乙,溶液的质量:乙>甲,符合题意;C、由图可知,60℃时,乙的溶解度是25g,乙的饱和溶液的溶质质量分数为: ,
将100g乙的饱和溶液配成质量分数为5%的溶液,根据稀释前后,溶质的质量不变,设加水的质量为x,
则100g×20%=(100g+x)5%,x=300g,不符合题意;
D、由图可知,甲的溶解度随温度的升高而增加,且受温度影响较大,丙的溶解度随温度的升高而减小,
故甲中混有少量丙,若要得到较纯净的甲,常采用降温结晶的方法,不符合题意。
故选B。
10、【2020湖北天门等四市】有关金属与金属材料的说法中错误的是( )
A.银的导电性比铜好,但电线一般用铜制,主要与价格和资源等因素有关
B.生铁和钢都是铁合金,但钢中的含碳量比生铁中高
C.铝合金门窗耐腐蚀性好,硬度高
D.焊锡是锡和铅的合金,其熔点低,可以用于焊接金属
【答案】B
【解析】A、银的导电性比铜好,但电线一般用铜制,主要与银价格贵和资源等因素有关,A正确;
B、生铁和钢都是铁合金,但钢中的含碳量比生铁中低,B错误;
C、合金相对于纯金属,耐腐蚀性更好,硬度更大,铝合金门窗耐腐蚀性好,硬度高,C正确;
D、合金熔点相较于纯金属偏低,焊锡是锡和铅的合金,其熔点低,可以用于焊接金属,D正确。
故选:B。
11、【2019湖南邵阳】下列物质不能与稀硫酸发生反应的是( )
A.CuO B.Ag C.BaCl D.Mg(OH)
2 2
【答案】B
【解析】A、CuO能与稀硫酸反应生成硫酸铜和水,故选项错误。
B、银的位置排在氢的后面,活动性比氢弱,不能与稀硫酸发生置换反应,故选项正确。
C、氯化钡能与稀硫酸反应生成硫酸钡沉淀和盐酸,故选项错误。
D、氢氧化镁能与稀硫酸反应生成硫酸镁和水,故选项错误。 故选:B。
12、【2020北京】不同温度下 KNO 的溶解度如下表所示,下列说法正确的是( )
3
温度/℃ 20 30 40
溶解度/g 31.6 45.8 63.9
A.20℃ 时,100g KNO 饱和溶液中溶质质量为31.6g
3
B.30℃ 时,100g KNO 饱和溶液的溶质质量分数为 45.8%
3
C.30℃ 时,将50g KNO 放入100g 水中得到150g 溶液
3D.40℃ 时,100g 水最多溶解63.9g KNO
3
【答案】D
【解析】A.溶质质量=溶液质量×溶质质量分数,20℃ 时,100g KNO 饱和溶液中溶质质量为
3
100g[31.6g/100g+31.6g]100% 24.01g,A 选项错误;
B. 饱和溶液中溶质质量分数S / (100g+S)100%, 30℃ 时,100g KNO 饱和溶液的溶质质量分数为
3
45.8g / 100g 45.8g 100% 31.41%,B 选项错误;
C.溶液质量=溶质质量+容质质量,由图表可知,30℃ 时,100g 水最多溶解 45.8g KNO ,溶液质量为
3
45.8g+100g=145.8g,C 选项错误;
D. 由图表可知,40℃ 时,KNO 的溶解度为63.9g,即40℃ 时,100g 水最多溶解63.9g KNO ,D
3 3
选项正确。
故选 D。
13、滴入无色酚酞溶液后不显色的溶液,若滴入紫色石蕊溶液,下列说法正确的是( )
A.一定显红色 B.可能为紫色 C.可能显蓝色 D.一定显无色
【答案】B
【解析】滴入无色酚酞不显色的溶液可能为中性,也可能为酸性,所以滴入石蕊后可能为紫色或赭红色。
14、【2020湖南郴州】为了验证镁、铜、银三种金属的活动性顺序,某同学设计了如下实验,只需进行
其中三个就能达到实验目的,你认为不必进行的是( )
A.将镁片放入稀盐酸中
B.将铜片放入稀盐酸中
C.将镁片放入硝酸银溶液中
D.将铜片放入硝酸银溶液中
【答案】C
【解析】①将镁片放入稀盐酸中,反应生成氢气,说明镁的金属活动性比氢强;即Mg>H;
②将铜片放入稀盐酸中,无明显现象,说明铜和稀盐酸不反应,说明铜的金属活动性比氢弱;即H>Cu;
③将镁片放入硝酸银溶液中,镁与AgNO 溶液反应置换出银,说明了活动性Mg>Ag;
3
④将铜片放入硝酸银溶液中,铜与AgNO 溶液反应置换出银,说明了活动性Cu>Ag;
3
根据①②④,即可得出Mg>H,H>Cu,Cu>Ag,由此可得出三种金属活动性镁>铜>银。故将镁片放
入硝酸银溶液中的实验不需进行。故选C。
15、【2020湖南益阳】下列物质混合,能发生反应且反应后溶液质量减少的是( )
A.铜丝与稀硫酸 B.稀硫酸与NaOH溶液
C.铁锈与稀硫酸 D.铜丝与AgNO 溶液
3
【答案】D
【解析】A、在金属活动性顺序中,铜排在氢后,铜与稀硫酸不反应,溶液质量不变,不符合题意;B、稀硫酸与氢氧化钠反应生成硫酸钠和水,反应后,无沉淀、气体生成,反应后,溶液质量增大,不符
合题意;
C、铁锈的主要成分是氧化铁,氧化铁与稀硫酸反应生成硫酸铁和水,反应后,溶液质量增加,不符合题
意;
D、铜与硝酸银反应: ,64份铜置换出216份银,固体质量增加,溶液质
量减小,符合题意。
故选D。
16、【2019湖南郴州】把一枚无锈铁钉放在硫酸铜溶液中,一段时间后,可出现的是( )
A.溶液蓝色变浅直至无色 B.铁钉表面析出红色物质 C.产生大量气泡 D.溶液质量增加
【答案】B
【解析】A、铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,溶液蓝色变浅直至浅绿色,故选项说法错误。
B、铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,铁钉表面析出红色物质,故选项说法正确。
C、铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,没有气泡产生,故选项说法错误。
D、铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,每56份质量的铁可置换出64份质量的铜,溶液的质量
会减少,故选项说法错误。
故选:B。
17、【2020广东深圳】如图为Ca(OH) 的溶解度曲线;如表为20℃时溶解度的相对大小。下列说法正
2
确的是( )
溶解度/g 一般称为
<0.01 难溶
0.01~1 微溶
1~10 可溶
>10 易溶A.Ca(OH) 属于易溶物质
2
B.Ca(OH) 的溶解度随温度的升高而增大
2
C.30℃时,Ca(OH) 的饱和溶液中溶质与溶剂的质量比为3:20
2
D.70℃时Ca(OH) 的饱和溶液,降温到50℃时没有析出固体
2
【答案】D
【解析】A、Ca(OH) 属于易溶物质错误,属于微溶物质,因为在20°C时,氢氧化钙的溶解度大约是0.17g ;故
2
选项错误;
B、Ca (OH ) 的溶解度随温度的升高而增大错误,因为Ca ( OH ) 的溶解度随温度的升高而减小;故选项错
2 2
误;
C、30°C时 ,Ca ( OH ) 的饱和溶液中溶质与溶剂的质量比=0.15g:100g=3 :2000,3 :20错误;故选项错误;
2
D、70°C时Ca ( OH ) 的饱和溶液。降温到50°C时没有析出固体正确,因为降温饱和溶液变为不饱和溶
2
液;故选项正确;故选:D.
18、【2019山东青岛】下列与洗涤有关的做法不合理的是( )
A.用洗洁精洗去餐具上的油污
B.用汽油洗去沾在衣服上的油渍
C.用白醋洗去水壶中的水垢(水垢的主要成分是碳酸钙和氢氧化镁)
D.用纯碱溶液洗去铁制品表面的铁锈
【答案】D
【解析】A、洗洁精具有乳化作用,能将大的油滴分散成细小的油滴随水冲走,故选项说法正确。
B、汽油能溶解油污,可用汽油洗去沾在衣服上的油渍,故选项说法正确。
C、水垢的主要成分是碳酸钙和氢氧化镁,均能与酸反应,可用白醋洗去水壶中的水垢,故选项说法正确。
D、铁锈的主要成分是氧化铁,不能与碳酸钠溶液反应,不能用纯碱溶液洗去铁制品表面的铁锈,故选项
说法错误。
故选:D。
19、【2020湖南益阳】下列各组物质的溶液中,不另加试剂则无法鉴别出来的是( )
A.HSO NaOH CuSO
2 4 4
B.HCl NaOH NaCl
C.HSO Ca(OH) FeCl
2 4 2 3
D.HCl Ca(OH) NaCO
2 2 3
【答案】B
【解析】A、蓝色的是硫酸铜溶液,能与硫酸铜溶液反应生成蓝色沉淀的是氢氧化钠,剩下的是硫酸,不
另加试剂可以鉴别出来,不符合题意;B、将三种试剂两两混合,均无现象产生,不另加试剂则无法鉴别,符合题意;
C、黄色的是氯化铁溶液,能与氯化铁溶液反应生成红褐色沉淀的是氢氧化钙,剩下的是硫酸,不另加试
剂可以鉴别出来,不符合题意;
D、将三种试剂两两混合,只产生气泡的是盐酸,只产生白色沉淀的是氢氧化钙,既产生气泡,又产生白
色沉淀的是碳酸钠,不另加试剂可以鉴别出来,不符合题意。
故选B。
20、【2020湖北孝感】现有某铁样品5.6g,含有的杂质为镁、锌、铜中的两种或三种。向其中逐渐加入
溶质质量分数为9.8%的稀硫酸,产生氢气质量与加入稀硫酸质量的关系如下图所示。则下列结论正确的个
数是( )
①恰好完全反应时,一定没有固体剩余
②x的值为0.2
③铁样品中可能含有镁
④M点对应的溶液中含有2种或3种溶质
A.1个 B.2个 C.3个 D.4个
【答案】A
的
【解析】100g稀硫酸,恰好完全反应,生成氢气质量,消耗铁镁锌 质量分别为:
和100g稀硫酸反应的金属5.6g,可能杂质是镁和铜,可能是镁、锌,可能是镁、锌、铜的混合物。
①假如是镁、锌、铜的混合物,恰好完全反应时,一定有固体剩余,选项说法错误。
②由分析可知,生成氢气质量0.2g,x的值为0.2,选项正确。
③由分析可知,样品中含有杂质可能是镁和铜,可能是镁锌,可能是镁锌铜的混合物,样品中一定有镁,
选项说法错误。
④M点表示硫酸过量,样品中含有杂质可能是镁和铜,可能是镁锌,可能是镁锌铜的混合物,对应的溶液中含有的溶质是硫酸,硫酸亚铁,硫酸镁,可能还含有硫酸锌,选项说法错误。
故正确说法一个,故选:A。
二、填空题(5小题,每空2分,共36分)
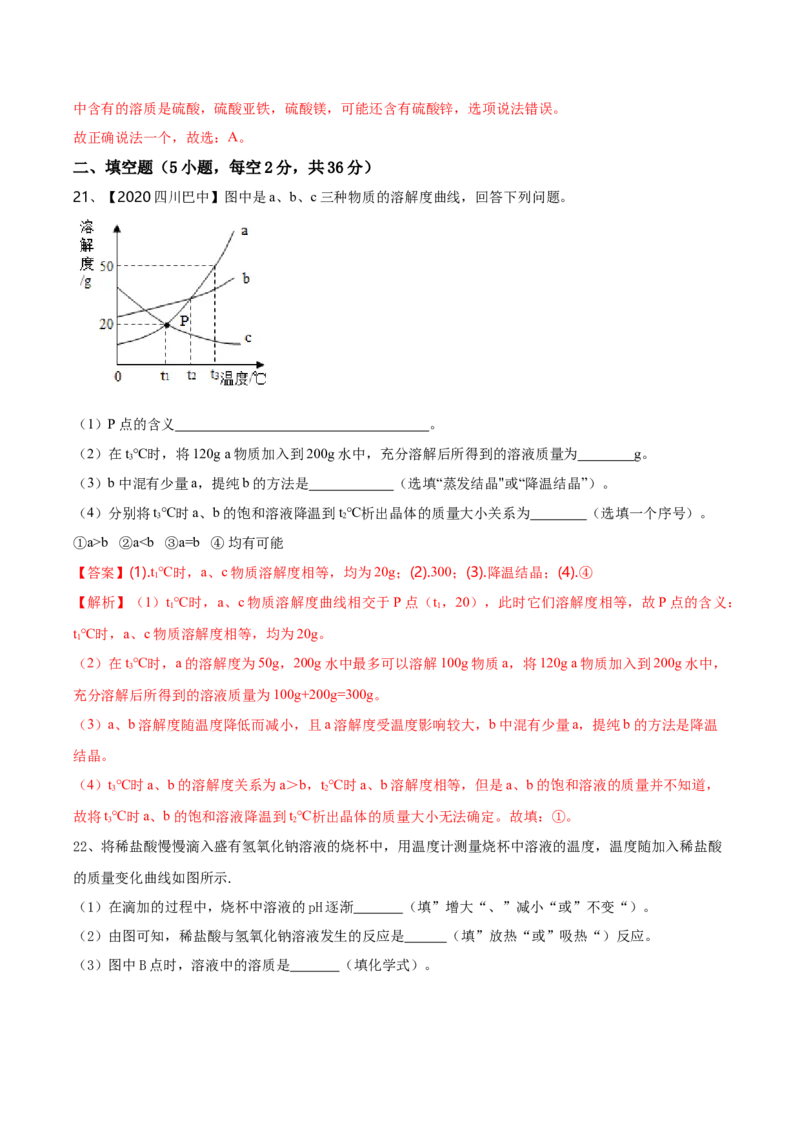
21、【2020四川巴中】图中是a、b、c三种物质的溶解度曲线,回答下列问题。
(1)P点的含义 。
(2)在t℃时,将120g a物质加入到200g水中,充分溶解后所得到的溶液质量为 g。
3
(3)b中混有少量a,提纯b的方法是 (选填“蒸发结晶"或“降温结晶”)。
(4)分别将t℃时a、b的饱和溶液降温到t℃析出晶体的质量大小关系为 (选填一个序号)。
3 2
①a>b ②a3.15g,所以Y溶液为饱和溶液;继续升温至50℃得到Z,50℃时,KNO 的溶解度为85.5g,10g水中最多溶解KNO 的质量为8.55g>5 g,所得溶液为不饱和
3 3
溶液。则X、Y、Z中为饱和溶液的是Y。
(4)40℃时,KNO 和KCl的溶解度分别为63.9g、40.0g。10℃时,KNO 和KCl的溶解度分别为20.9g、
3 3
31.0g。
A、40℃时,KNO 和KCl的溶解度分别为63.9g、40.0g,所以硝酸钾饱和溶液中水的质量小于氯化钾饱和
3
溶液中水的质量,故选项错误;
B、40℃时,KNO 和KCl的溶解度分别为63.9g、40.0g。10℃时,KNO 和KCl的溶解度分别为20.9g、
3 3
31.0g。降温至10℃时,析出的KNO 晶体质量比析出的KCl晶体质量大,故选项正确;
3
C、对于饱和溶液的溶质的质量分数= ,降温至10℃时,KNO 和KCl的溶解度分别为
3
20.9g、31.0g,所以硝酸钾饱和溶液的质量分数小于氯化钾饱和溶液的质量分数,故选项错误;
D、20℃时,KNO 和KCl的溶解度分别为31.6g、34.0g,30℃时,KNO 和KCl的溶解度分别为45.8g、
3 3
37.0g,所以当温度降至20℃和30℃之间的某一温度,两种溶液的质量分数可能相等,故选项正确。故选
BD。
25、【2020重庆B】纽扣电池是生活中常用的电源,下图是银锌纽扣电池的构造示意图,回答下列问题。
(1)纽扣电池的外壳可以加工得很薄,说明金属具有_____性。
(2)氧化银加热分解可以得到两种单质,其化学反应方程式为_______。
(3)该电池中涉及的铁、锌、银三种金属,它们的金属活动性由强到弱的顺序是_____,为了验证该结论,
某同学向质量、外形相同的铁片、锌片、银片中分别加入足量15%的稀盐酸,以下现象中不能成为该结论
证据的是________(填序号)。
A 银表面没有气泡生成
B 铁表面最终生成气体的总量比锌多C 铁表面产生气泡的速率比锌慢
【答案】 (1).延展性;(2). ;(3).锌、铁、银;B
【解析】(1)纽扣电池的外壳可以加工得很薄,说明金属具有延展性;
(2)氧化银加热分解生成银和氧气,其化学反应方程式为 ;
(3)根据金属性顺序可知,铁、锌、银三种金属活动性由强到弱的顺序是锌、铁、银;
A、银表面没有气泡生成,说明银不能与盐酸反应,证明银排在氢后,故正确;
B、铁表面最终生成气体的总量比锌多,不能证明活动性强弱,故错误;
C、铁表面产生气泡的速率比锌慢,证明铁不如锌活泼,故正确。故选B。
三、实验探究(1小题,每空2分,共16分)
26、【2020青海】陈东同学在做“盐酸中和氢氧化钠”的实验时,实验前忘记向氢氧化钠溶液中滴加酚酞
溶液,导致无法判断中和反应进行的程度,于是他对反应后溶液的酸碱性进行了探究。
【探究目的】确定反应后溶液的酸碱性
【猜想与假设】反应后溶液可能呈碱性,也可能呈________,也可能呈_______。
【实验验证】
实验操作 实验现象 实验结论
取反应后溶液少许,滴加几滴酚酞溶液 ______ 溶液呈酸性或中性
【继续验证】可以设计多种方案进行验证
实验操作 实验现象 实验结论
若粉末部分或全部溶解,溶
溶液呈______
方案1:取反应后溶液少许,加入少量 液变为蓝色
氧化铜粉末
若粉末不溶解,溶液不变色 溶液呈_____
若有气体放出,溶液变为浅 溶液呈酸性,反应的化学
方案2:取反应后溶液少许,加入少量 绿色 方程式是_______
______
若______ 溶液呈中性
【答案】(1).酸性 (2).中性(和上一空顺序可颠倒) (3).不变色 (4).酸性(5).中性 (6). 铁 (7).
Fe+2HCl═FeCl +H ↑ (8).无明显现象
2 2
【解析】
【猜想与假设】氢氧化钠溶液与稀盐酸反应生成氯化钠和水,可能恰好完全反应,也可能是稀盐酸有剩余,也可能是氢氧
化钠有剩余,故假设可能呈酸性或中性;
【实验验证】
向反应后的溶液中滴加无色酚酞溶液,实验结论是呈酸性或中性,则无色酚酞溶液不变色;
【继续实验】
方案1:加入氧化铜后,现象为粉末部分或全部溶解,溶液变为蓝色,是因为盐酸能与氧化铜反应生成氯
化