文档内容
班级 姓名 学号 分数
人教版化学九年级下第一次月考模拟卷
(范围:8、9单元)
(时间:60分钟,满分100分)
一、选择题(20小题,每小题2分,共40分)
1、常温下为液态的金属是( )
A. 汞 B. 金 C. 银 D. 铝
【答案】A
【解析】常温下,铝、银、金等大多数金属都是固体,但金属汞熔点最低,常温下为液态。故选A。
2、【2020湖南益阳】将少量下列厨房中常见的物质分别放入水中,充分搅拌,可形成溶液的是( )
A.植物油 B.面粉 C.食盐 D.胡椒粉
【答案】C
【解析】A、植物油不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误;
B、面粉不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误;
C、食盐易溶于水,形成均一、稳定的混合物,属于溶液,故选项正确;
D、胡椒粉不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误。
故选C。
3、下列物品主要是由合金制成的是( )
A.塑料水杯 B.青铜铸像 C.汽车轮胎 D.羊毛大衣
【答案】B
【解析】A、塑料属于有机合成材料,错误;
B、青铜属于合金,正确;
C、轮胎是橡胶制成的,属于有机合成材料,错误;
D、羊毛属于天然材料,错误;
故选:B。
4、《吕氏春秋》记载“金(即铜单质)柔锡(即锡单质)柔,合两柔则刚(即坚硬)”。这句话说明合
金具有的特性是( )
A.合金的熔点一般比其组分低 B.合金的硬度一般比其组分大
C.合金的抗腐蚀性一般比其组分强 D.合金的耐磨性一般比其组分好
【答案】B
【解析】合金与其组分相比:硬度大、熔点低、抗腐蚀性增强,这里说的是硬度大。故选:B。
5、实验室用氯化钠和水配制50g质量分数为6%的氯化钠溶液。下列说法正确的是( )
A.实验步骤:计算、量取、溶解、装瓶、贴签
B.量取水时,用规格为50mL的量筒
C.实验过程中玻璃棒搅拌的作用是散热
D.若在量取水时俯视读数量取,则配制溶液的溶质质量分数小于6%
【答案】B
【解析】A、用氯化钠和水配制50g质量分数为6%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质
量,再称量所需的氯化钠和量取水,最后进行溶解、装瓶、贴签,故选项说法错误。
B、溶质质量=溶液质量×溶质的质量分数,配制 50g质量分数为6%的氯化钠溶液,需氯化钠的质量=
50g×6%=3g;溶剂质量=溶液质量﹣溶质质量,则所需水的质量=50g﹣3g=47(合47mL),可用规格为
50mL的量筒,故选项说法正确。
C、实验过程中玻璃棒搅拌的作用是加快溶解速率,故选项说法错误。
D、用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质
量分数偏大,故选项说法错误。
故选:B。
6、下列金属中,金属活动性最弱的是( )
A.金 B.银 C.铜 D.铁
【答案】A
【解析】根据金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au,则
可知金属活动性大小为:铁>铜>银>金,所以金属活动性最弱的是金。
故选A。
7、下列说法正确的是( )
A.铁是地壳中含量最多的金属元素 B.铁制品在潮湿的空气中容易生锈
C.多数合金的熔点高于它的成分金属 D.铝制品在空气中耐腐蚀是因为铝不活泼
【答案】B
【解析】A、铝是地壳中含量最多的金属元素,故选项说法错误。
B、铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,铁制品在潮湿的空气中容易生锈,
故选项说法正确。
C、多数合金的熔点低于它的成分金属,故选项说法错误。
D、铝制品在空气中耐腐蚀,是因为铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止
内部的铝进一步被氧化,故选项说法错误。故选:B。
8、下列关于溶液的说法正确的是( )
A.溶液具有均一性、稳定性 B.长期放置后不会分层的液体一定是溶液
C.气体的溶解度随压强增大而减小 D.医用酒精是75%的乙醇溶液,乙醇作溶剂
【答案】A
【解析】A、溶液是均一、稳定的混合物,故正确。
B、长期放置后不会分层的液体不一定是溶液,例如蒸馏水,故错误;
C、气体的溶解度随温度的升高而降低,随着压强的增大而增大,故错误;
D、医用酒精是75%的乙醇的水溶液,水作溶剂,故错误。
故选:A。
9、下列防锈措施不合理的是( )
A.钢管存放在干燥的地方 B.用盐水清洗菜刀
C.及时清除铁制品表面的锈渍 D.在铁管表面镀上一层不易锈蚀的金属
【答案】B
【解析】A、钢管存放在干燥的地方,能防止铁与水分接触,能防止铁锈蚀,故选项防锈措施正确;
B、用盐水清洗菜刀,盐水能加快铁锈蚀的速率,故选项防锈措施错误;
C、铁锈很疏松,及时清除铁制品表面的锈渍,能防止铁锈蚀,故选项防锈措施正确;
D、在铁管表面镀上一层不易锈蚀的金属,能防止铁锈蚀,故选项防锈措施正确;
10、现有Y、Y、Z三种金属,如果把X、Y和Z分别放入稀硫酸中,X和Z溶解并产生气体,Y无变化;如
果把X放入Z的盐溶液中,过一会儿,在X的表面有Z析出。根据以上实验事实,判断X,Y和Z的金属活
动性顺序( )
A.X>Y>Z B.Y>Z>X C.X>Z>Y D.Z>X>Y
【答案】C
【解析】把X、Y和Z分别放入稀硫酸中,X和Z溶解并产生气体,Y无变化,说明X和Z的金属活动性比Y
强;把X放入Z的盐溶液中,过一会儿,在X的表面有Z析出,说明X比Z的金属活动性强,故X,Y和Z
的金属活动性顺序为:X>Z>Y。
故选C。
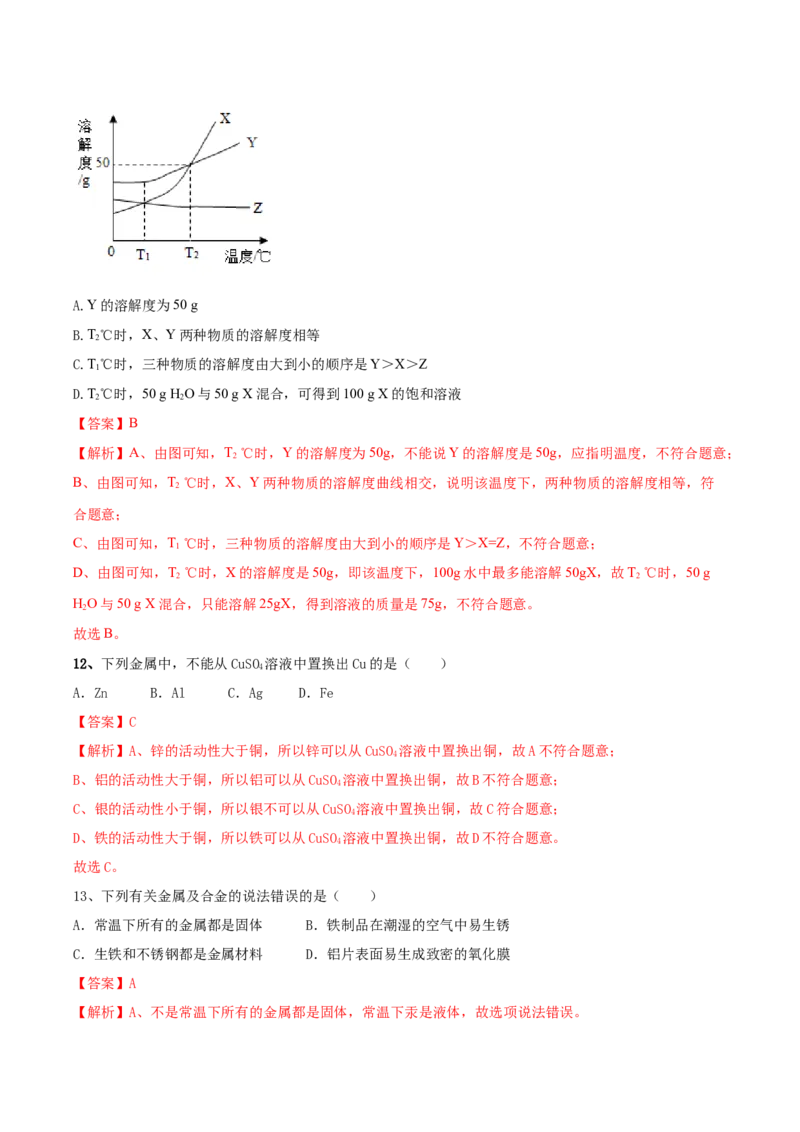
11、【2020新疆】X、Y、Z三种物质的溶解度曲线如图所示,下列说法正确的是( )A.Y的溶解度为50 g
B.T℃时,X、Y两种物质的溶解度相等
2
C.T℃时,三种物质的溶解度由大到小的顺序是Y>X>Z
1
D.T℃时,50 g HO与50 g X混合,可得到100 g X的饱和溶液
2 2
【答案】B
【解析】A、由图可知,T ℃时,Y的溶解度为50g,不能说Y的溶解度是50g,应指明温度,不符合题意;
2
B、由图可知,T ℃时,X、Y两种物质的溶解度曲线相交,说明该温度下,两种物质的溶解度相等,符
2
合题意;
C、由图可知,T ℃时,三种物质的溶解度由大到小的顺序是Y>X=Z,不符合题意;
1
D、由图可知,T ℃时,X的溶解度是50g,即该温度下,100g水中最多能溶解50gX,故T ℃时,50 g
2 2
HO与50 g X混合,只能溶解25gX,得到溶液的质量是75g,不符合题意。
2
故选B。
12、下列金属中,不能从CuSO 溶液中置换出Cu的是( )
4
A.Zn B.Al C.Ag D.Fe
【答案】C
【解析】A、锌的活动性大于铜,所以锌可以从CuSO 溶液中置换出铜,故A不符合题意;
4
B、铝的活动性大于铜,所以铝可以从CuSO 溶液中置换出铜,故B不符合题意;
4
C、银的活动性小于铜,所以银不可以从CuSO 溶液中置换出铜,故C符合题意;
4
D、铁的活动性大于铜,所以铁可以从CuSO 溶液中置换出铜,故D不符合题意。
4
故选C。
13、下列有关金属及合金的说法错误的是( )
A.常温下所有的金属都是固体 B.铁制品在潮湿的空气中易生锈
C.生铁和不锈钢都是金属材料 D.铝片表面易生成致密的氧化膜
【答案】A
【解析】A、不是常温下所有的金属都是固体,常温下汞是液体,故选项说法错误。B、铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,铁制品在潮湿的空气中易生锈,
故选项说法正确。
C、生铁和不锈钢都是铁的合金,都是金属材料,故选项说法正确。
D、铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,铝片表面易生成致密的氧化膜,故选
项说法正确。
故选:A。
14、根据下列实验装置图,以下说法中错误的是( )
A.a处固体由黑色逐渐变为红棕色
B.反应过程中可观察到b处的澄清石灰水变浑浊
C.CO有毒,通常在c处将其点燃或用气囊收集以防止污染空气
D.该实验可验证CO的还原性
【答案】A
【解析】A、一氧化碳与氧化铁反应生成铁和二氧化碳,故看到的现象为玻璃管中红色固体变为黑色,说
法错误;
B、该反应有二氧化碳生成,则试管b处澄清的石灰水变浑浊,故B说法正确;
C、尾气中可能有一氧化碳,一氧化碳有毒,所以一定要进行尾气处理,故说法正确;
D、一氧化碳还原氧化铁实验可验证CO的还原性,说法正确。
故选A。
15、根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是( )
A.用铁制容器盛盐酸 B.用铜制容器盛盐酸
C.用铁制容器盛硝酸银溶液 D.用铜制容器盛硝酸银溶液
【答案】B
【解析】A、由于铁在氢前,因此铁可以和盐酸反应,故A不符合题意;
B、由于铜在氢后,因此铜不能和盐酸反应,故B符合题意;
C、由于铁在银前,因此金属铁可以和硝酸银溶液反应,故C不符合题意;
D、由于铜在银前,因此铜可以和硝酸银溶液反应,故D不符合题意。故选B。
16、将锌片分别放入下列四种溶液中,一段时间后,溶液质量会减轻的是( )
A.HSO B.AgNO C.FeSO D.MgSO
2 4 3 4 4
【答案】B
【解析】A、锌与稀HSO 反应生成了硫酸锌和氢气,锌的质量减少,溶液质量会增大,故A错误;
2 4
B、锌与硝酸银反应置换出银,置换出的银的质量大于锌,故溶液质量减轻,故B正确;
C、锌与FeSO 反应置换出铁,置换出的铁的质量小于锌,溶液质量会增大,故C错误;
4
D、锌与MgSO 不反应,溶液的质量不变,故D错误。
4
故选B。
17、【2020甘肃天水】将金属M的粉末放入盛有硝酸铜溶液的烧杯中,充分反应后,溶液呈无色,继续
向烧杯中加入一定量的硝酸银溶液,充分反应后过滤,得到滤渣和蓝色滤液。根据上述实验分析,下列说
法错误的是( )
A.金属活动性强弱顺序:M>Cu>Ag
B.滤渣中可能有金属M
C.滤液中至少含有两种溶质
D.滤渣中一定有Ag
【答案】B
【解析】A、溶液呈无色,M和硝酸铜溶液反应,则M的金属活动性强于铜,加入一定量的硝酸银溶液,
充分反应后过滤,得到滤渣和蓝色滤液,铜和硝酸银反应生成硝酸铜和银,则铜的金属活动性强于银,则
金属活动性强弱顺序:M>Cu>Ag,故A正确;
B、M的金属活动性最强,M和硝酸铜溶液和硝酸银均反应,充分反应后过滤,得到滤渣和蓝色滤液,故
滤渣中没有金属M,故B不正确;
C、加入一定量的硝酸银溶液,充分反应后过滤,得到滤渣和蓝色滤液,则滤液中含有M的盐溶液和硝酸
铜,可能含有硝酸银,故至少含有两种溶质,故C正确;
D、加入一定量的硝酸银溶液,充分反应后过滤,得到滤渣和蓝色滤液,铜和硝酸银反应生成硝酸铜和银,
则滤渣中一定有Ag,故D正确。故选B。
18、某温度下,在100g质量分数为20%的KNO 不饱和溶液甲中加入10gKNO 固体,恰好得到饱和溶液乙,
3 3
下列说法正确的是( )
A.该温度下,KNO 的溶解度为30g B.乙溶液的质量分数为30%
3
C.降低温度,可以使甲溶液变成饱和溶液 D.升高温度,甲、乙两溶液的质量分数都增大
【答案】C【解析】某温度下,在100g质量分数为20%的KNO 不饱和溶液甲中加入10gKNO 固体,恰好得到饱和溶液
3 3
乙,即100g×20%+10g=30g硝酸钾,溶于水,形成100g+10g=110g溶液,即某温度下,30g硝酸钾溶于
110g﹣30g=80g水,形成110g饱和溶液。
A、溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量某温度下,30g硝
酸钾溶于80g水,形成110g饱和溶液,则该温度下,KNO 的溶解度大于30g,故选项说法错误;
3
B、乙溶液的质量分数为 ×100%<30%,故选项说法错误;
C、硝酸钾的溶解度随着温度的降低而减小,降低温度,可以使甲溶液变成饱和溶液,故选项说法正确;
D、升高温度,硝酸钾的溶解度增大,但甲、乙溶液的组成没有发生改变,甲、乙两溶液的质量分数都不
变,故选项说法错误;
故选C。
19、【2020山西】小明自制了一杯蔗糖水(无固体剩余),用于缓解运动后出现的低血糖症状,之后他结
合下表蔗糖的溶解度数据,归纳出以下问题,其中正确的是( )
温度/℃ 0 10 20 40 60 80 100
溶解度/g 182 191 204 238 287 362 487
A.配制的蔗糖溶液下层比上层甜
B.降温,糖水中一定有晶体析出
C.20℃时,蔗糖饱和溶液质量一定为304g
D.升温,糖水中蔗糖的质量分数不变
【答案】D
【解析】A、溶液具有均一、稳定性,配制的蔗糖溶液上下层一样甜,不符合题意;
B、由表中数据可知,蔗糖的溶解度随温度的升高而增加,饱和溶液降温后一定有溶质析出,但是不饱和
溶液不一定有溶质析出,不符合题意;
C、20℃时,蔗糖的溶解度是204g,即100g水中最多能溶解204g蔗糖,当溶剂质量为100g时,该温度下,
饱和溶液质量一定为304g,如果溶剂质量不是100g,则饱和溶液质量不是304g,不符合题意;
D、由表中数据可知,蔗糖的溶解度随温度的升高而增加,升温后,蔗糖的溶解度增加,不会有溶质析出,
溶质、溶剂质量不变,蔗糖的溶质质量分数不变,符合题意。
故选D。
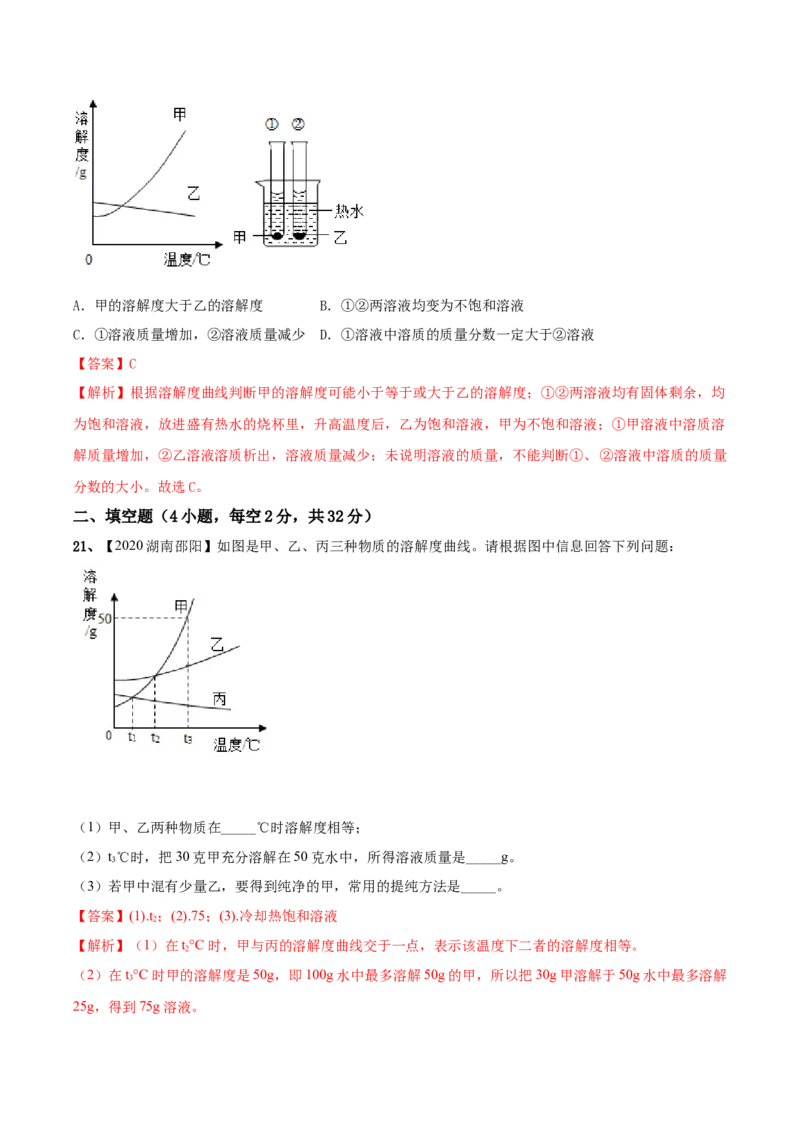
20、甲、乙两种固体的溶解度曲线如图所示。将①②两支试管中的甲、乙饱和溶液(均有少量未溶解的固
体)放进盛有热水的烧杯里,升高温度后,下列有关说法正确的是( )A.甲的溶解度大于乙的溶解度 B.①②两溶液均变为不饱和溶液
C.①溶液质量增加,②溶液质量减少 D.①溶液中溶质的质量分数一定大于②溶液
【答案】C
【解析】根据溶解度曲线判断甲的溶解度可能小于等于或大于乙的溶解度;①②两溶液均有固体剩余,均
为饱和溶液,放进盛有热水的烧杯里,升高温度后,乙为饱和溶液,甲为不饱和溶液;①甲溶液中溶质溶
解质量增加,②乙溶液溶质析出,溶液质量减少;未说明溶液的质量,不能判断①、②溶液中溶质的质量
分数的大小。故选C。
二、填空题(4小题,每空2分,共32分)
21、【2020湖南邵阳】如图是甲、乙、丙三种物质的溶解度曲线。请根据图中信息回答下列问题:
(1)甲、乙两种物质在_____℃时溶解度相等;
(2)t℃时,把30克甲充分溶解在50克水中,所得溶液质量是_____g。
3
(3)若甲中混有少量乙,要得到纯净的甲,常用的提纯方法是_____。
【答案】(1).t;(2).75;(3).冷却热饱和溶液
2
【解析】(1)在t°C 时,甲与丙的溶解度曲线交于一点,表示该温度下二者的溶解度相等。
2
(2)在t°C 时甲的溶解度是50g,即100g水中最多溶解50g的甲,所以把30g甲溶解于50g水中最多溶解
3
25g,得到75g溶液。(3)由甲、乙物质的溶解度曲线可以知道,甲物质的溶解度随温度的升高而明显增大,乙物质的溶解度
随温度的升高变化不大,所以若在混有少量乙的甲中提纯甲,应采用冷却热饱和溶液的方法。
22、【2020山东滨州】铝、铜、铁是生活中常见的金属。
(1)铝在空气中具有很好的抗腐蚀性能的原因是 。
(2)用铜制作导线主要是利用铜具有良好的 性;
(3)焊接铁制品时,通常先用稀盐酸除去其表面的铁锈,反应的化学方程式为_________。
【答案】(1).铝能和氧气反应生成一层致密的氧化膜,阻止铝继续腐蚀;(2).导电;(3).
【解析】
(1)铝在空气中具有很好的抗腐蚀性能的原因是:铝能和氧气反应生成一层致密的氧化膜,阻止铝继续
腐蚀。
(2)用铜制作导线主要是利用铜具有良好的导电性;
(3)用稀盐酸除去铁制品表面的铁锈,铁锈的主要成分是氧化铁,盐酸能和氧化铁反应生成氯化铁和水,
反应的化学方程式为 。
23、某同学将甲、乙固体各32克分别加入100克水中后,进行了如图1所示的实验。甲、乙两种固体的溶
解度曲线如图2所示,回答下列问题:
(1)10℃时,甲、乙两种物质的溶解度大小关系:甲 乙(填“<”、“>”或“=”)。
(2)m的取值范围 <m≤ 。
(3)40℃时,取等质量的甲、乙两种物质的饱和溶液分别蒸发等量的水后,恢复到40℃,析出晶体的质
量:甲 乙(填“<”、“>”或“=”);若再降温到 20℃时,溶液的质量:甲 乙(填“<”、
“>”或“=”)。
【答案】(1)<;(2)3,48;(3)>,<。
【解析】(1)40℃,甲物质的烧杯底部有固体剩余,所以甲物质的溶解度大于乙物质的溶解度,10℃时,
甲、乙两种物质的溶解度大小关系:甲<乙;
(2)40℃时,甲物质的溶解度是80g,乙物质的溶解度是35g,所以将甲、乙固体各32克分别加入100克水中后,甲物质有晶体析出,乙物质不会析出晶体,m的取值范围是:3<m≤48;
(3)40℃时,甲物质的溶解度大于乙物质的溶解度,所以取等质量的甲、乙两种物质的饱和溶液分别蒸
发等量的水后,恢复到40℃,析出晶体的质量:甲>乙,若再降温到20℃时,甲物质溶解度受温度变化影
响较大,所以溶液的质量:甲<乙。
24、在人类社会的发展进程中,金属起着重要的作用。
(1)青铜是铜锡合金,其属于 (填“金属材料”或“合成材料”)。
(2)某些铁制零件防锈措施是涂油,其防锈原理是 。工人师傅常用稀盐酸除铁锈,其反应的
化学方程式是 。
(3)铝合金广泛应用于飞机制造业,可增加飞机的载重量以及提高运行速度,这是利用了铝合金
(答一点即可)的优良性能。
(4)向硝酸银和硝酸铝的混合溶液中加入一定量的铁粉,观察到溶液由无色变为浅绿色后,对混合物进
行过滤,则滤液中一定含有的溶质是 。
【答案】(1)金属材料。(2)隔绝氧气和水;FeO+6HCl═2FeCl+3HO。(3)密度小。
2 3 3 2
(4)硝酸铝、硝酸亚铁。
【解析】(1)青铜是铜锡合金,其属于金属材料。
故填:金属材料。
(2)某些铁制零件防锈措施是涂油,其防锈原理是隔绝氧气和水;
工人师傅常用稀盐酸除铁锈,是因为氧化铁能和稀盐酸反应生成氯化铁和水,其反应的化学方程式是:
FeO+6HCl═2FeCl+3HO。
2 3 3 2
故填:隔绝氧气和水;FeO+6HCl═2FeCl+3HO。
2 3 3 2
(3)铝合金广泛应用于飞机制造业,可增加飞机的载重量以及提高运行速度,这是利用了铝合金密度小
的优良性能。
故填:密度小。
(4)向硝酸银和硝酸铝的混合溶液中加入一定量的铁粉,观察到溶液由无色变为浅绿色后,对混合物进
行过滤,则滤液中一定含有的溶质是不能反应的硝酸铝和反应生成的硝酸亚铁。
故填:硝酸铝、硝酸亚铁。
三、实验探究(2小题,每空2分,共20分)
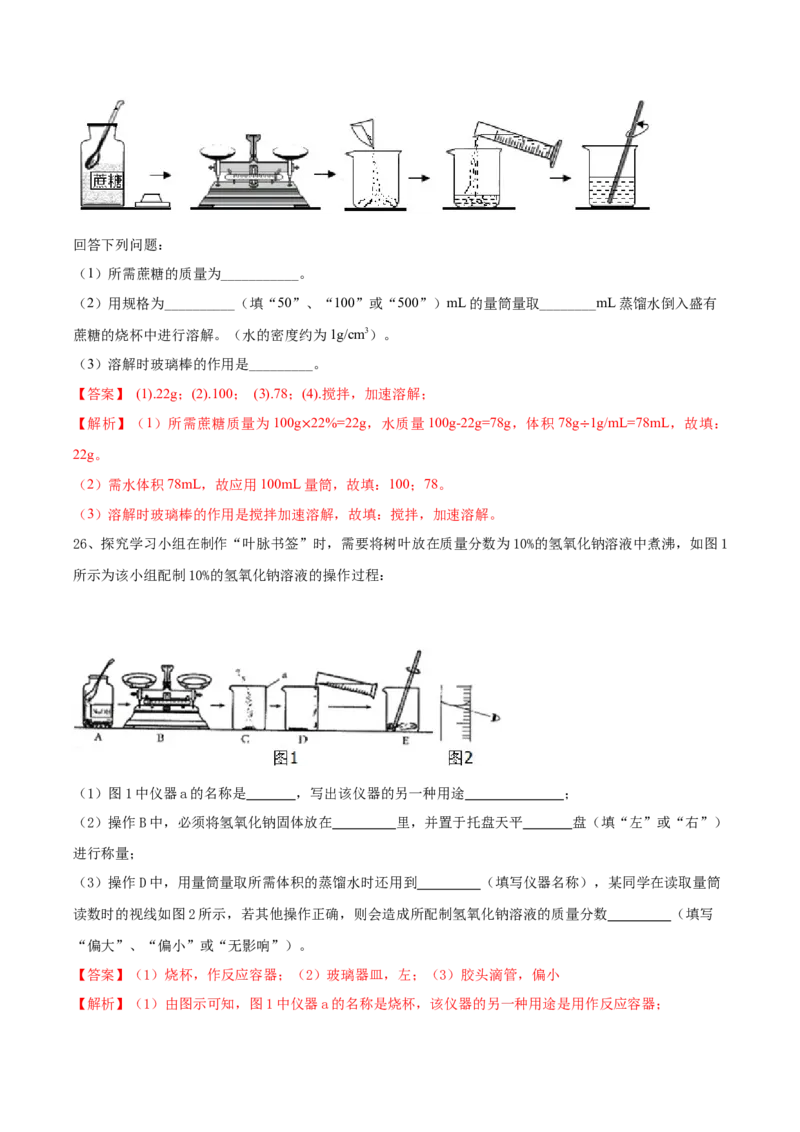
25、【2020四川宜宾】实验室按下图步骤配制100g质量分数为22%的蔗糖溶液。回答下列问题:
(1)所需蔗糖的质量为___________。
(2)用规格为__________(填“50”、“100”或“500”)mL的量筒量取________mL蒸馏水倒入盛有
蔗糖的烧杯中进行溶解。(水的密度约为1g/cm3)。
(3)溶解时玻璃棒的作用是_________。
【答案】 (1).22g;(2).100; (3).78;(4).搅拌,加速溶解;
【解析】(1)所需蔗糖质量为100g 22%=22g,水质量100g-22g=78g,体积78g 1g/mL=78mL,故填:
22g。 × ÷
(2)需水体积78mL,故应用100mL量筒,故填:100;78。
(3)溶解时玻璃棒的作用是搅拌加速溶解,故填:搅拌,加速溶解。
26、探究学习小组在制作“叶脉书签”时,需要将树叶放在质量分数为10%的氢氧化钠溶液中煮沸,如图1
所示为该小组配制10%的氢氧化钠溶液的操作过程:
(1)图1中仪器a的名称是 ,写出该仪器的另一种用途 ;
(2)操作B中,必须将氢氧化钠固体放在 里,并置于托盘天平 盘(填“左”或“右”)
进行称量;
(3)操作D中,用量筒量取所需体积的蒸馏水时还用到 (填写仪器名称),某同学在读取量筒
读数时的视线如图2所示,若其他操作正确,则会造成所配制氢氧化钠溶液的质量分数 (填写
“偏大”、“偏小”或“无影响”)。
【答案】(1)烧杯,作反应容器;(2)玻璃器皿,左;(3)胶头滴管,偏小
【解析】(1)由图示可知,图1中仪器a的名称是烧杯,该仪器的另一种用途是用作反应容器;(2)氢氧化钠是有腐蚀性的药品,在操作B中,必须将氢氧化钠固体放在玻璃器皿里,并置于托盘天平左
盘进行称量;
(3)操作D中,用量筒量取所需体积的蒸馏水时还用到胶头滴管,某同学在读取量筒读数时的视线如图2
所示,是仰视读数,量取的水偏多,若其他操作正确,则会造成所配制氢氧化钠溶液的质量分数偏小;
四、分析与计算(1小题,共8分)
27、赤铁矿的主要成分是FeO,可用于冶炼铁。有种赤铁矿中FeO 的质量分数为64%,试计算:
2 3 2 3
(1)FeO 中铁元素的质量分数为________。
2 3
(2)用100 t该赤铁矿经过充分冶炼,最多可以生产出含铁96%的生铁多少吨?(计算结果保留两位小数)
【答案】(1)70%;(2)46.67 t。
【解析】(1)70%
(2)设最多可以炼出含铁96%的生铁质量为x,
=
x≈46.67 t
答:最多可以炼出含铁96%的生铁46.67 t。
溶质的质量分数 = × 100% =19.6%
答:这种硫酸溶液中溶质的质量分数为19.6%。