文档内容
班级 姓名 学号 分数
人教版化学九年级下第一次月考模拟卷(一)
相对原子质量:H:1、C:12、O:16、Cu:64、Fe:56
(时间:60分钟,满分100分)
一、选择题(每小题2分,共40分)
1、常温下为液态的金属是( )
A. 汞 B. 金 C. 银 D. 铝
【答案】A
【解析】常温下,铝、银、金等大多数金属都是固体,但金属汞熔点最低,常温下为液态。故选A。
2、【辽宁葫芦岛】把少量下列物质分别放入足量的水中充分搅拌,可以得到溶液的是( )
A.白糖 B.泥沙 C.牛奶 D.花生油
【答案】A
【解析】A.白糖能溶于水,把少量白糖放入足量的水中充分搅拌,可以得到溶液;
B.泥沙不溶于水,把少量泥沙放入足量的水中充分搅拌,不能得到溶液;
C.牛奶不溶于水,把少量牛奶放入足量的水中充分搅拌,不能得到溶液;
D.花生油不溶于水,把少量花生油放入足量水中充分搅拌,不能得到溶液。
故选:A。
3、【湖北襄阳】下列物品主要是由合金制成的是( )
A.塑料水杯 B.青铜铸像 C.汽车轮胎 D.羊毛大衣
【答案】B
【解析】A、塑料属于有机合成材料,错误;
B、青铜属于合金,正确;
C、轮胎是橡胶制成的,属于有机合成材料,错误;
D、羊毛属于天然材料,错误;
故选:B。
4、下列物质溶于水的过程中,溶液温度会明显降低的是( )
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
【答案】B
【解析】物质在溶解时经常伴随有吸热或放热现象,如氢氧化钠固体、浓硫酸溶于放出大量的热,温度升
高;硝酸铵固体溶于水吸热,温度降低。
A、氯化钠溶于水温度基本保持不变,故选项错误。B、硝酸铵溶于水溶液温度明显降低,故选项正确。
C、浓硫酸溶于水溶液温度明显升高,故选项错误。
D、氢氧化钠溶于水溶液温度明显升高,故选项错误。
故选B。
5、下列金属中,金属活动性最弱的是( )
A.金 B.银 C.铜 D.铁
【答案】A
【解析】根据金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au,则
可知金属活动性大小为:铁>铜>银>金,所以金属活动性最弱的是金。
故选A。
6、把铁矿石、焦炭和石灰石一起加入到高炉中进行冶炼,得到的产物是( )
A.钢 B.生铁 C.纯铁 D.锰钢
【答案】B
【解析】铁矿石、焦炭在高炉中会反应,得到主要成分是铁,同时含有一定量的碳和其它杂质的生铁。
7、“一定溶质质量分数的NaOH溶液的配制”实验操作示意图如下,其中正确的是( )
A.取用NaOH B.称取NaOH C.量取一定体积的水 D.溶解NaOH固体
【答案】D
【解析】A、取用固体粉末状药品时,瓶塞要倒放,应用药匙取用,不能用手接触药品,图中瓶塞没有倒
放,图中所示操作错误;
B、氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,图中所示操作错误;
C、量取液体时,视线与液体的凹液面最低处保持水平,图中俯视读数,操作错误;
D、溶解时,用玻璃棒进行搅拌,以加快溶解速率,图中所示操作正确;
8、【江苏苏州】下列说法正确的是( )
A.铁是地壳中含量最多的金属元素 B.铁制品在潮湿的空气中容易生锈
C.多数合金的熔点高于它的成分金属 D.铝制品在空气中耐腐蚀是因为铝不活泼
【答案】B
【解析】A、铝是地壳中含量最多的金属元素,故选项说法错误。
B、铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,铁制品在潮湿的空气中容易生锈,故选项说法正确。
C、多数合金的熔点低于它的成分金属,故选项说法错误。
D、铝制品在空气中耐腐蚀,是因为铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止
内部的铝进一步被氧化,故选项说法错误。
故选:B。
9、下列洗涤方式应用乳化作用的是( )
A.用汽油除去衣服上的油污 B.用水洗去盘子中的水果渣
C.用洗洁精清洗餐具上的油污 D.用盐酸清洗水壶的水垢
【答案】C
【解析】A、用汽油洗去衣服上的油污是利用汽油能溶解油污来达到目的,利用的是溶解原理,不属于乳
化作用,故A错误;
B、用水冲洗水果渣,使水果渣与水形成溶液或浊液而被冲洗掉,不属于乳化作用,故B错误;
C、洗洁精是洗涤剂,有乳化作用,能将大的油滴分散成细小的油滴随水冲走,属于乳化作用,故C正确;
D、铁锈不溶于水,但能与盐酸反应生成氯化铁和水,不属于乳化作用,故D错误.
故选C。
10、【湖南郴州】下列关于溶液的说法正确的是( )
A.溶液具有均一性、稳定性 B.长期放置后不会分层的液体一定是溶液
C.气体的溶解度随压强增大而减小 D.医用酒精是75%的乙醇溶液,乙醇作溶剂
【答案】A
【解析】A、溶液是均一、稳定的混合物,故正确。
B、长期放置后不会分层的液体不一定是溶液,例如蒸馏水,故错误;
C、气体的溶解度随温度的升高而降低,随着压强的增大而增大,故错误;
D、医用酒精是75%的乙醇的水溶液,水作溶剂,故错误。
故选:A。
11、【.河南】如图为一氧化碳还原氧化铁实验。下列说法中正确的是( )
A.开始时应先预热玻璃管,后通入一氧化碳
B.实验中玻璃管里粉末由黑色逐渐变成红粽色C.参加反应的氧化铁和一氧化碳质量比为40:7
D.将尾气点燃或收集,可防止一氧化碳污染空气
【答案】D
【解析】A、实验开始先通入一氧化碳,排出装置内的空气后,再点燃酒精喷灯加热玻璃管中的氧化铁,
先通入一氧化碳后加热的原因是排尽玻璃管中的空气,防止发生爆炸,故选项说法错误。
B、一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,实验进行一段时间后,玻璃管A中出现的现
象是红棕色粉末逐渐变黑,故选项说法错误。
C、反应的化学方程式为:FeO+3CO2Fe+3CO ,参加反应的氧化铁和一氧化碳质量比为160:(28×3)=
2 3 2
40:21,故选项说法错误。
D、一氧化碳有毒,直接排放到空气中会污染环境,本实验的缺陷是没有设计尾气处理装置,可将玻璃管
改成尖嘴点燃或用气球收集,故选项说法正确。
故选:D。
12、现有Y、Y、Z三种金属,如果把X、Y和Z分别放入稀硫酸中,X和Z溶解并产生气体,Y无变化;如
果把X放入Z的盐溶液中,过一会儿,在X的表面有Z析出。根据以上实验事实,判断X,Y和Z的金属活
动性顺序( )
A.X>Y>Z B.Y>Z>X C.X>Z>Y D.Z>X>Y
【答案】C
【解析】把X、Y和Z分别放入稀硫酸中,X和Z溶解并产生气体,Y无变化,说明X和Z的金属活动性比Y
强;把X放入Z的盐溶液中,过一会儿,在X的表面有Z析出,说明X比Z的金属活动性强,故X,Y和Z
的金属活动性顺序为:X>Z>Y。
故选C。
13、【山东滨州】某同学选用氢氧化钠固体与水配制20g溶质质量分数为10%的氢氧化钠溶液,下列说法
错误的是( )
①需称取氢氧化钠固体2.0g;②称量前托盘天平应先检查游码是否归零,并调节平衡;③用托盘天平称量
氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量;④选用250mL量筒量取18mL的水;⑤存
放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A. ①④ B. ③④⑤ C. ④⑤ D. ②③⑤
【答案】B
【解析】①溶质质量=溶液质量×溶质的质量分数,配制20g溶质质量分数为10%的氢氧化钠溶液,需氢氧
化钠的质量=20g×10%=2g,故选项说法正确。②称量前托盘天平应先检查游码是否归零,并调节平衡,故选项说法正确。
③托盘天平的使用要遵循“左物右码”的原则,且氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,故选项
说法错误。
④溶剂质量=溶液质量-溶质质量,所需溶剂的质量为20g-2g=18g(合18mL),应用规格为20mL的量筒量
取水的体积,故选项说法错误。
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存,会造成实际量取的
水的体积偏大,则使溶质质量分数偏小,故选项说法错误。
故选:B。
14、下列金属中,不能从CuSO 溶液中置换出Cu的是( )
4
A.Zn B.Al C.Ag D.Fe
【答案】C
【解析】A、锌的活动性大于铜,所以锌可以从CuSO 溶液中置换出铜,故A不符合题意;
4
B、铝的活动性大于铜,所以铝可以从CuSO 溶液中置换出铜,故B不符合题意;
4
C、银的活动性小于铜,所以银不可以从CuSO 溶液中置换出铜,故C符合题意;
4
D、铁的活动性大于铜,所以铁可以从CuSO 溶液中置换出铜,故D不符合题意。
4
故选C。
15、下列防锈措施不合理的是( )
A.钢管存放在干燥的地方 B.用盐水清洗菜刀
C.及时清除铁制品表面的锈渍 D.在铁管表面镀上一层不易锈蚀的金属
【答案】B
【解析】A、钢管存放在干燥的地方,能防止铁与水分接触,能防止铁锈蚀,故选项防锈措施正确;
B、用盐水清洗菜刀,盐水能加快铁锈蚀的速率,故选项防锈措施错误;
C、铁锈很疏松,及时清除铁制品表面的锈渍,能防止铁锈蚀,故选项防锈措施正确;
D、在铁管表面镀上一层不易锈蚀的金属,能防止铁锈蚀,故选项防锈措施正确;
16、20℃时,四个实验小组分别取不同质量的NaCl,逐渐加人到各盛有50g水的烧杯中,不断搅拌直到不
再溶解为止,然后分别称量剩余NaCl的质量。记录数据如表:
实验小组 第一组 第二组 第三组 第四组
水的质量/g 50 50 50 50
所取NaCl的质量/g 15 20 25 30
剩余NaCl的质量/g 0 2 7 12
下列说法错误的是( )
A.20℃时,50gNaCl饱和溶液中含有18gNaClB.用蒸发的方法可以使不饱和溶液变成饱和溶液
C.第二组所得溶液的溶质与溶剂的质量比为9:25
D.相同温度下,NaCl在水里的溶解度与水的质量无关
【答案】A
【解析】由表格中的数据分析知,第一组中的15gNaCl在20℃时固体全部溶解,而第二、三、四组的NaCl
固体,在20℃时均溶解了18g,所以20℃时,NaCl固体的溶解度是18g,
A、20℃时,50g水中含有18gNaCl,故说法错误;
B、用蒸发的方法减少溶剂,可以使不饱和溶液变成饱和溶液,故说法正确;
C、第二组所得溶液的溶质与溶剂的质量比为18:50=9:25,故说法正确;
D、该实验中,相同温度下,NaCl在水里的溶解度与水的质量无关,故说法正确;
故选A。
17、【湖北黄冈】如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )
A.a的溶解度大于b的溶解度
B.P点表示t℃时a、c两物质溶解度相等
1
C.将t℃饱和的c溶液升温到t℃,得到的是不饱和溶液
1 2
D.将t℃,a、b、c三种物质的饱和溶液降温到t℃时,所得溶液中溶质质最分数由大到小的顺序为:
2 1
b>a=c
【答案】B
【解析】根据溶解度曲线判断t℃时,a的溶解度小于b的溶解度,t℃时,a的溶解度大于b的溶解度;
1 2
P点表示t℃时a、c两物质溶解度相等;c的溶解度随温度升高而减小,将t℃饱和的c溶液升温到
1 1
t℃,得到的是饱和溶液;将t℃,a、b、c三种物质的饱和溶液降温到t℃时,a、b所得溶液为饱和溶
2 2 1
液,c为不饱和溶液,所得溶液中溶质质最分数由大到小的顺序为:b>a>c。故选B。
18、向Cu(NO ) 、AgNO 的混合溶液中加入一定量的铁粉,充分反应后过滤,再向滤渣中加入稀盐酸,发
3 2 3
现没有气泡产生,则滤渣中一定含有的物质是( )
A.Fe、Cu B.Cu、Ag C.Cu D.Ag
【答案】D【解析】充分反应后过滤,再向滤渣中加入稀盐酸,发现没有气泡产生,说明滤渣中不含有铁,则滤渣中
一定含有的物质是铁和硝酸银反应生成的银。
故选D。
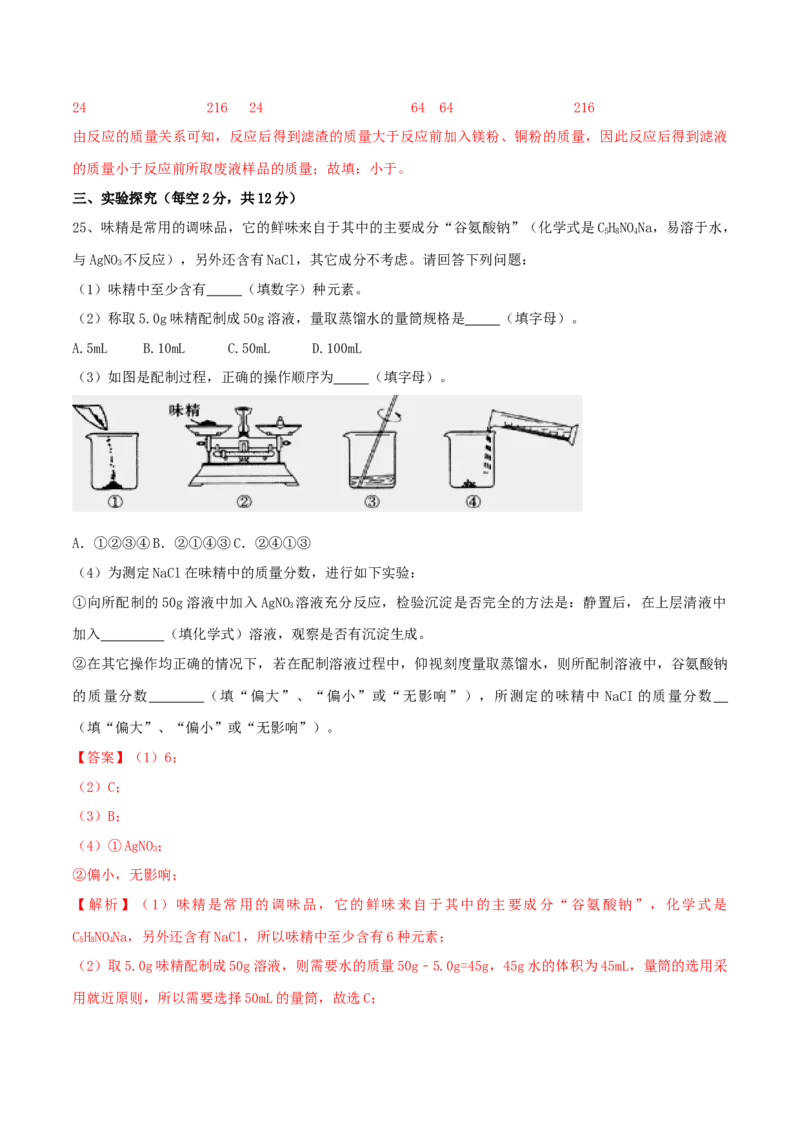
19、【湖北孝感】甲、乙两种固体的溶解度曲线如图所示。将①②两支试管中的甲、乙饱和溶液(均有少
量未溶解的固体)放进盛有热水的烧杯里,升高温度后,下列有关说法正确的是( )
A.甲的溶解度大于乙的溶解度 B.①②两溶液均变为不饱和溶液
C.①溶液质量增加,②溶液质量减少 D.①溶液中溶质的质量分数一定大于②溶液
【答案】C
【解析】根据溶解度曲线判断甲的溶解度可能小于等于或大于乙的溶解度;①②两溶液均有固体剩余,均
为饱和溶液,放进盛有热水的烧杯里,升高温度后,乙为饱和溶液,甲为不饱和溶液;①甲溶液中溶质溶
解质量增加,②乙溶液溶质析出,溶液质量减少;未说明溶液的质量,不能判断①、②溶液中溶质的质量
分数的大小。故选C。
20、某不纯的铁5.6克与足量的稀硫酸反应生成0.23克氢气,则铁中混有的物质可能是( )
A.锌 B.碳 C.铝 D.银
【答案】C
【解析】铁、锌、铝和稀硫酸反应的化学方程式及其质量关系为:
Fe+HSO=FeSO+H↑,
2 4 4 2
56 2
Zn+HSO=ZnSO+H↑,
2 4 4 2
65 22Al+3HSO═Al(SO)+3H↑,
2 4 2 4 3 2
54 6
由铁和稀硫酸与反应可知,5.6g铁和稀硫酸完全反应生成 0.2g氢气,当混有锌时生成氢气质量小于
0.2g,当混有铝时生成氢气质量大于0.2g,当混有碳、银时生成氢气质量小于0.2g,由于反应生成0.23g
氢气,因此含有的物质可能是铝。
故选C。
二、填空题(每空2分,共36分)
21、【黑龙江龙东】去年港珠澳大桥正式建成通车,它是世界上钢结构桥体最长的跨海大桥。请根据所学
知识,回答有关金属资源的下列问题。
(1)在空气中,铁与__ ___同时接触发生反应而生锈;
(2)请写出一条防止铁生锈的措施____ _;
(3)除防止金属腐蚀外,请写出保护金属资源的有效途径 。(答一点)
【答案】(1)氧气和水蒸气; (2)刷漆或涂油; (3)寻找金属替代品。
【解析】(1)铁生锈的条件是铁与氧气和水蒸气同时接触发生反应而生锈;故填:氧气和水蒸气;
(2)铁在潮湿的空气中容易生锈,所以要防止生锈应该隔绝空气或是水,故可以采取刷漆或涂油等方法
防止铁生锈;故填:刷漆或涂油;
(3)除防止金属腐蚀外,保护金属资源的有效途径还有寻找金属替代品、合理开采金属矿物、回收利用
废旧金属等,故填:寻找金属替代品。
22、【湖南衡阳】如图是甲、乙、丙三种固体物质的溶解度曲线。回答相关问题
(1)t℃时,甲物质的饱和溶液中,溶质、溶剂、溶液的质量之比为 。
3
(2)t℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数的大小关系是 (用“甲”、
2
“乙”、“丙”及“>”、“<”或“=”表示)
(3)将t℃的甲、乙、丙三种物质的饱和溶液各 100g,分别降温至t℃,所得溶液的质量最大是
3 1
(用“甲”、“乙”、“丙”填空)。
(4)现有甲、乙混合物溶液,需要从混合物溶液中提纯乙固体,采用的方法有(写出一种即可) 。【答案】(1)1:5:6;
(2)甲=丙>乙;
(3)丙;
(4)蒸发结晶;
【解答】(1)t℃时,甲物质的饱和溶液中,溶质、溶剂、溶液的质量之比=20g:100g:120g=1:5:
3
6;故答案为:1:5:6;
(2)t℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数的大小关系是:甲=丙>乙;故答案为:
2
甲=丙>乙;
(3)将t℃的甲、乙、丙三种物质的饱和溶液各100g,分别降温至t℃,所得溶液的质量最大是丙,因
3 1
为降温后甲、乙都有固体析出,丙的溶液质量不变;故答案为:丙;
(4)现有甲、乙混合物溶液,需要从混合物溶液中提纯乙固体,采用的方法是:蒸发结晶,因为乙的溶
解度受温度的影响变化不大;故答案为:蒸发结晶;
23、【辽宁辽阳】在人类社会的发展进程中,金属起着重要的作用。
(1)青铜是铜锡合金,其属于 (填“金属材料”或“合成材料”)。
(2)某些铁制零件防锈措施是涂油,其防锈原理是 。工人师傅常用稀盐酸除铁锈,其反应的
化学方程式是 。
(3)铝合金广泛应用于飞机制造业,可增加飞机的载重量以及提高运行速度,这是利用了铝合金
(答一点即可)的优良性能。
(4)向硝酸银和硝酸铝的混合溶液中加入一定量的铁粉,观察到溶液由无色变为浅绿色后,对混合物进
行过滤,则滤液中一定含有的溶质是 。
【答案】(1)金属材料。(2)隔绝氧气和水;FeO+6HCl═2FeCl+3HO。(3)密度小。
2 3 3 2
(4)硝酸铝、硝酸亚铁。
【解析】(1)青铜是铜锡合金,其属于金属材料。
故填:金属材料。(2)某些铁制零件防锈措施是涂油,其防锈原理是隔绝氧气和水;
工人师傅常用稀盐酸除铁锈,是因为氧化铁能和稀盐酸反应生成氯化铁和水,其反应的化学方程式是:
FeO+6HCl═2FeCl+3HO。
2 3 3 2
故填:隔绝氧气和水;FeO+6HCl═2FeCl+3HO。
2 3 3 2
(3)铝合金广泛应用于飞机制造业,可增加飞机的载重量以及提高运行速度,这是利用了铝合金密度小
的优良性能。
故填:密度小。
(4)向硝酸银和硝酸铝的混合溶液中加入一定量的铁粉,观察到溶液由无色变为浅绿色后,对混合物进
行过滤,则滤液中一定含有的溶质是不能反应的硝酸铝和反应生成的硝酸亚铁。
故填:硝酸铝、硝酸亚铁。
24、某化工厂的废液中主要含有硝酸银、硝酸铜.取一定量的该废液样品,加入镁粉和铜粉,充分反应后
过滤,得到滤液和滤渣. 请填写下列空格:
(1)若滤渣中有镁粉,则滤渣中除镁粉外还含有 (填写化学式,下同)。
(2)若滤渣中有铜粉,则滤液中的溶质一定含有 ,可能含有 。
(3)若滤渣中没有铜粉,则滤液中的溶质一定含有 ,可能含有 。
(4)反应后得到滤液的质量 (选填“小于”、“大于”或“等于”)反应前所取废液样品的质
量。
【答案】(1)Ag、Cu;
(2)Mg(NO);Cu(NO);
3 2 3 2
(3)Mg(NO)、Cu(NO);AgNO;
3 2 3 2 3
(4)小于。
【解析】(1)镁比铜活泼,铜比银活泼,将适量铜粉和镁粉的混合物放入一定量含有硝酸银、硝酸铜溶
液中,镁先和硝酸银反应,再和硝酸铜反应;若滤渣中有镁粉,说明镁粉过量,因此硝酸银、硝酸铜都被
置换,所以滤渣一定还含有银、铜;故填:Ag、Cu;
(2)若滤渣中有铜粉,说明硝酸银一定被反应完,镁是否过量不能确定,但镁一定参加反应生成硝酸镁,
硝酸铜是否反应不能确定,因此滤液中一定含有硝酸镁,可能含有硝酸铜,一定没有硝酸银;故填:Mg
(NO);Cu(NO);
3 2 3 2
(3)若滤渣中没有铜粉,说明镁完全反应生成硝酸镁,铜反应产生硝酸铜,硝酸银是否完全被反应,不
能确定,因此滤液中一定含有硝酸镁、硝酸铜,不能确定硝酸银;故填:Mg(NO)、Cu(NO);AgNO;
3 2 3 2 3
(4)可能发生反应的化学方程式为:
Mg+2AgNO=Mg(NO)+2Ag、Mg+Cu(NO)=Mg(NO)+Cu、Cu+2AgNO=Cu(NO)+2Ag,
3 3 2 3 2 3 2 3 3 224 216 24 64 64 216
由反应的质量关系可知,反应后得到滤渣的质量大于反应前加入镁粉、铜粉的质量,因此反应后得到滤液
的质量小于反应前所取废液样品的质量;故填:小于。
三、实验探究(每空2分,共12分)
25、味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是CHNONa,易溶于水,
5 8 4
与AgNO 不反应),另外还含有NaCl,其它成分不考虑。请回答下列问题:
3
(1)味精中至少含有 (填数字)种元素。
(2)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是 (填字母)。
A.5mL B.10mL C.50mL D.100mL
(3)如图是配制过程,正确的操作顺序为 (填字母)。
A.①②③④B.②①④③C.②④①③
(4)为测定NaCl在味精中的质量分数,进行如下实验:
①向所配制的50g溶液中加入AgNO 溶液充分反应,检验沉淀是否完全的方法是:静置后,在上层清液中
3
加入 (填化学式)溶液,观察是否有沉淀生成。
②在其它操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液中,谷氨酸钠
的质量分数 (填“偏大”、“偏小”或“无影响”),所测定的味精中 NaCI的质量分数
(填“偏大”、“偏小”或“无影响”)。
【答案】(1)6;
(2)C;
(3)B;
(4)①AgNO;
3
②偏小,无影响;
【解析】(1)味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”,化学式是
CHNONa,另外还含有NaCl,所以味精中至少含有6种元素;
5 8 4
(2)取5.0g味精配制成50g溶液,则需要水的质量50g﹣5.0g=45g,45g水的体积为45mL,量筒的选用采
用就近原则,所以需要选择50mL的量筒,故选C;(3)图①为称量完毕的味精倒入烧杯,图②为称量味精的质量,图③为进行溶解,图④为量取水后倒入
盛有味精的烧杯,所以正确的操作顺序为:②①④③,故选:B;
(4)①溶液中的氯化钠与硝酸银溶液能发生化学反应,生成氯化银白色沉淀和硝酸钠,所以向所配制的
50g溶液中加入过量的硝酸银溶液充分反应,化学式为:AgNO;
3
②仰视刻度量取蒸馏水可以造成蒸馏水的体积增大,所以仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠
质量分数偏小,但是对样品中氯化钠的质量分数不影响;
四、分析与计算(2小题,共12分)
26、人体所需的维生素C(化学式为CHO)主要从蔬菜、水果中摄取,请计算:
6 8 6
(1)维生素C中碳元素、氢元素、氧元素的质量的最简整数比为 。
(2)若要配制溶质质量分数为0.3%的维生素C溶液1000g,需要维生素C的质量为 g,水的质量为
g。
【答案】(1)3;(2)997。
【解析】(1)维生素C中,C、H、O三种元素的质量比为(12×6):(1×8):(16×6)=9:1:12,
故填:9:1:12;
(2)配制1000g溶质质量分数为0.3%的维生素C溶液,需要维生素C的质量为1000g×0.3%=3g;溶剂质
量=溶液质量﹣溶质质量,则所需水的质量=1000g﹣3g=997g
27、赤铁矿的主要成分是FeO,可用于冶炼铁。有种赤铁矿中FeO 的质量分数为64%,试计算:
2 3 2 3
(1)FeO 中铁元素的质量分数为________。
2 3
(2)用100 t该赤铁矿经过充分冶炼,最多可以生产出含铁96%的生铁多少吨?(计算结果保留两位小数)
【答案】(1)70%;(2)46.67 t。
【解析】(1)70%
(2)设最多可以炼出含铁96%的生铁质量为x,
=
x≈46.67 t答:最多可以炼出含铁96%的生铁46.67 t。