文档内容
绝密★启用前 4.某有机物(如图)是合成抗肿瘤药氨柔比星的关键中间体。下列关于该有机物分子的说法正确
的是
高三年级 3月二轮复习阶段检测 O
A.含有手性碳原子
師師
化 学 B.含有16个 σ键 帨帨 師師
O
C.能形成分子内氢键
O
D.能发生还原反应和取代反应
试卷共8页,20小题,满分100分。考试用时75分钟。
5.劳动创造了幸福,生活包含着智慧。下列对劳动项目涉及的相关化学知识表述错误的是
注意事项:
选项 劳动项目 化学知识
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡指定位置上。
A 厨师用冰箱冷藏食物延长保质期 低温能降低食品腐败反应的活化能,减慢反应速率
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
B 茶农用草木灰给茶树补充K元素 草木灰中含有较多的KCO
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷 2 3
C 果商用高锰酸钾溶液浸泡荔枝保鲜 高锰酸钾能氧化乙烯,延缓荔枝成熟
上无效。
检测员利用浓氨水检验氯气管道是否
3.考生必须保持答题卡的整洁。考试结束后,请将答题卡交回。 D 8NH+3Cl6NHCl+N
3 2 4 2
泄漏,若泄漏则会观察到白烟现象
6.生态文明建设是关系中华民族永续发展的根本大计。下列说法正确的是
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Cl—35.5 Cu—64 Re—186
A.聚氯乙烯塑料袋会造成白色污染,聚氯乙烯的单体为 CHCHCl
一、选择题:本大题共 16小题,共 44分。第 1~10小题,每小题 2分;第 11~16小题,每小题 4分。 2
B.含重金属离子的电镀废水随意排放会造成水体污染,重金属离子能使蛋白质发生盐析而失去活性
在每小题列出的四个选项中,只有一项符合题目要求。
C.酸雨对生态环境有巨大危害,c(H+)>c(OH-)的雨水均属于酸雨
1.岭南非遗技艺,彰显匠心精神。下列选项所涉及材料的主要成分属于无机非金属材料的是
D.灰霾严重影响人民身体健康,含有直径为10-5m左右灰霾粒子的霾属于胶体
7.化合物a、b、c存在如图所示转化关系,③④⑤⑥的反应条件、部分反应物或产物 !
略去。a由三种元素构成,利用a进行焰色试验,火焰呈黄色,下列说法正确的是
! #
A.热稳定性:c>b $ %&
& $
B.向 c溶液中加入过量 Ba(OH)溶液能发生⑤的转化
2
C.⑥的离子方程式可能为 CO2-+HOHCO-+OH- %
3 2 3 " #
$%!’%
D.①~⑥均未发生氧化还原反应 & &
"
A.潮州木雕摆件 B.广州檀香扇 C.佛山石湾艺术陶瓷 D.广绣百鸟争鸣图
8.物质的结构决定性质,下列对物质的性质解释错误的是
2.科技自立自强,赋能国家高质量发展。下列说法正确的是
选项 性质 解释
A.我国新一代舱外航天服采用水升华热控系统实现温控:水升华过程破坏了 H—O共价键
A 铜具有优良的导电性 Cu原子脱落下来的价电子形成电子气,电子气在电场中定向移动
B.我国首个百万吨级 CO 捕集项目建成投产:CO 的 VSEPR模型为
2 2 B 液态水凝结成冰,体积增大 氢键具有方向性
C.国内完成首条完全自主可控的8英寸 SiC晶圆生产线:SiC属于分子晶体
P
D.我国研发的 LiNbO 3 薄膜光子芯片在光通信领域具有重要应用:9 4 3 1 Nb的质子数为52 C 1molH 3 PO 3 最多能消耗2molNaOH H 3 PO 3 的结构为 HO OH OH
3.制备氯气并探究氯气的性质。下列操作不能达到实验目的的是
Ag+含有能接受电子对的空轨道,NH 中的 N原子含有孤电
3
D AgCl沉淀能溶于氨水
浓盐酸 !" # 子对
9.设 N 为阿伏加德罗常数的值。下列说法正确的是
红热的 A
铁丝 A.1mol基态 Fe原子中,价电子总数为2N
A
!" B.64gCu与足量 S完全反应,转移电子数目为2N
# A
饱和!"#$% 溶液 浓硫酸
!"#$ & C.0.1mol·L-1NaS溶液中,S2-、HS-和 HS的总数目为0.1N
% 2 2 A
A.制备 Cl B.净化 Cl C.收集 Cl D.验证 Cl的氧化性 D.标准状况下,1molP 含有共价键的总数为6N
2 2 2 2 4 A
GD·高三化学 第1页(共8页) GD·高三化学 第2页(共8页)
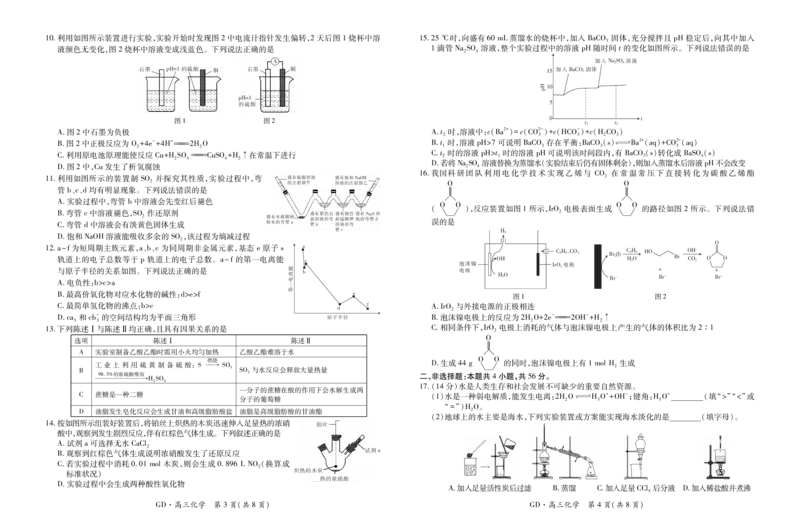
书书书10.利用如图所示装置进行实验,实验开始时发现图2中电流计指针发生偏转,2天后图 1烧杯中溶
液颜色无变化,图2烧杯中溶液变成浅蓝色。下列说法正确的是
%
石墨 !"#$的硫酸 铜 石墨 铜
!"#$
的硫酸
图1 图2
A.图2中石墨为负极
B.图2中正极反应为 O+4e-+4H+2HO
2 2
C.利用原电池原理能使反应 Cu+HSO CuSO+H↑在常温下进行
2 4 4 2
D.图2中,Cu发生了析氢腐蚀
11.利用如图所示的装置制 SO 并探究其性质,实验过程中,弯 盛有硫酸溶液 盛有饱和$!()
2 的注射器甲 溶液的注射器乙
管 b、c、d均有明显现象。下列说法错误的是
A.实验过程中,弯管 b中溶液会先变红后褪色
B.弯管 c中溶液褪色,SO 作还原剂 盛有紫色石 盛有酸性盛有$!&溶 2 盛有亚硫酸钠 %
蕊溶液的弯 高锰酸钾液的弯管’ C.弯管 d中溶液会有淡黄色固体生成 粉末的弯管! 管" 溶液的弯
管#
D.饱和 NaOH溶液能吸收多余的 SO,该过程为熵减过程
2
!
%
&
#
"
$
原子半径
GD·高三化学 第3页(共8页) GD·高三化学 第4页(共8页)
能离电一第
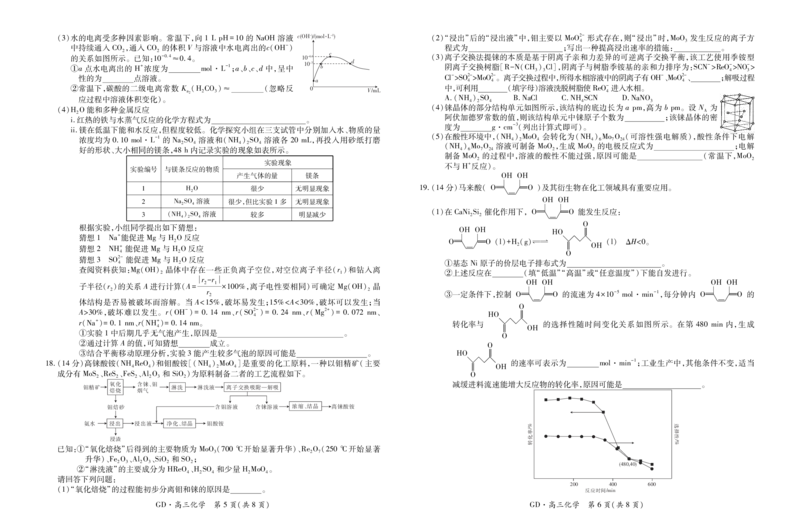
15.25℃时,向盛有60mL蒸馏水的烧杯中,加入 BaCO 固体,充分搅拌且 pH稳定后,向其中加入
3
1滴管 NaSO 溶液,整个实验过程中的溶液 pH随时间 t的变化如图所示。下列说法错误的是
2 4
加入!"$% 溶液
# &
加入’"(% 固体 )
12.a~f为短周期主族元素,a、b、c为同周期非金属元素,基态 e原子 s
轨道上的电子总数等于 p轨道上的电子总数。a~f的第一电离能
与原子半径的关系如图。下列说法正确的是
A.电负性:b>c>a
B.最高价氧化物对应水化物的碱性:d>e>f
C.最简单氢化物的沸点:b>c
D.ca和 cb-的空间结构均为平面三角形
3 3
13.下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 实验室制备乙酸乙酯时需用小火均匀加热 乙酸乙酯难溶于水
燃烧
工 业 上 利 用 硫 黄 制 备 硫 酸:S→ SO
B 3 SO 与水反应会释放大量热量
98.3%的浓硫酸吸收 3
→HSO
2 4
一分子的蔗糖在酸的作用下会水解生成两
C 蔗糖是一种二糖
分子的葡萄糖
D 油脂发生皂化反应会生成甘油和高级脂肪酸盐 油脂是高级脂肪酸的甘油酯
14.按如图所示组装好装置后,将铂丝上炽热的木炭迅速伸入足量热的浓硝
铂丝
酸中,观察到发生剧烈反应,伴有红棕色气体生成。下列叙述正确的是
A.试剂 a可选择无水 CaCl
2
试剂!
B.观察到红棕色气体生成说明浓硝酸发生了还原反应
C.若实验过程中消耗0.01mol木炭,则会生成 0.896LNO(换算成
2
炽热的木炭
标准状况)
热的浓硝酸
D.实验过程中会生成两种酸性氧化物
+*
,-
,.
-
. ! ! !
, #
A.t时,溶液中:c(Ba2+)=c(CO2-)+c(HCO-)+c(HCO)
2 3 3 2 3
B.t时,溶液 pH>7可说明 BaCO 存在平衡:BaCO(s)幑幐Ba2+(aq)+CO2-(aq)
1 3 3 3
C.t时的溶液 pH>t时的溶液 pH可说明该时间段内,有 BaCO(s)转化成 BaSO(s) 2 1 3 4
D.若将NaSO溶液替换为蒸馏水(实验结束后仍有固体剩余),则加入蒸馏水后溶液pH不会改变
2 4
16.我国科研团队利用电化学技术实现乙烯与 CO 在常温常压下直接转化为碳酸乙烯酯
2
O O
(
O
O O
),反应装置如图1所示,IrO 电极表面生成
2
O
的路径如图 2所示。下列说法错
误的是
!
"
,
’ " ! ( !’# " "#&’( ) % * + *, ,*$
#!$ % *, "# ), , ,
% %
!"# %&# $%
$% " ! !
!#
" "#$ "#$ "#$
图1 图2
A.IrO 与外接电源的正极相连
2
B.泡沫镍电极上的反应为2HO+2e-2OH-+H↑
2 2
C.相同条件下,IrO 电极上消耗的气体与泡沫镍电极上产生的气体的体积比为21
2
O O
D.生成44g
O
的同时,泡沫镍电极上有1molH 生成
2
二、非选择题:本题共4小题,共56分。
17.(14分)水是人类生存和社会发展不可缺少的重要自然资源。
(1)水是一种弱电解质,能发生电离:2HO幑幐HO++OH-;键角:HO+ (填“>”“<”或
2 3 3
“=”)HO。
2
(2)地球上的水主要是海水,下列实验装置或方案能实现海水淡化的是 (填字母)。
A.加入足量活性炭后过滤 B.蒸馏 C.加入足量CCl后分液 D.加入稀盐酸并煮沸
4(3)水的电离受多种因素影响。常温下,向 1LpH=10的 NaOH溶液 !!"#$%&’()*!+,-% (2)“浸出”后的“浸出液”中,钼主要以 MoO2-形式存在,则“浸出”时,MoO 发生反应的离子方
4 3
中持续通入 CO,通入 CO 的体积 V与溶液中水电离出的c(OH-) 程式为 ;写出一种提高浸出速率的措施: 。
2 2
!
的关系如图所示。已知:10-0.4≈0.4。 -.,/0/ (3)离子交换法提铼的本质是基于阴离子亲和力差异的可逆离子交换平衡,该工艺使用季铵型
$
①a点水电离出的 H+浓度为 mol·L-1;a、b、c、d中,呈中 -.,1 % 阴离子交换树脂[R-N(CH)Cl],阴离子与树脂季铵基的亲和力排序为:SCN->ReO->NO->
3 3 4 3
性的为 点溶液。 Cl->SO2->MoO2-。离子交换过程中,所得水相溶液中的阴离子有OH-、MoO2-、 ;解吸过程
# 4 4 4
②常温下,碳酸的二级电离常数 K(HCO)≈ (忽略反 . 中,可利用 (填字母)溶液洗脱树脂使ReO-进入水相。
a 2 3 "&(+ 4
2
应过程中溶液体积变化)。 A.(NH)SO B.NaCl C.NHSCN D.NaNO
4 2 4 4 3
(4)铼晶体的部分结构单元如图所示,该结构的底边长为 apm,高为 bpm。设 N 为
(4)HO能和多种金属反应
A
2
阿伏加德罗常数的值,则该结构单元中铼原子个数为 ;该铼晶体的密
i.红热的铁与水蒸气反应的化学方程式为 。
度为 g·cm-3(列出计算式即可)。
ii.镁在低温下能和水反应,但程度较低。化学探究小组在三支试管中分别加入水、物质的量
(5)在酸性环境中,(NH)MoO 会转化为(NH)MoO (可溶性强电解质),酸性条件下电解
浓度均为0.10mol·L-1的 NaSO 溶液和(NH)SO 溶液各 20mL,再投入用砂纸打磨 4 2 4 4 6 7 24
2 4 4 2 4
(NH)MoO 溶液可制备 MoO,生成 MoO 的电极反应式为 ;电解
好的形状、大小相同的镁条,48h内记录实验的现象如表所示。 4 6 7 24 2 2
制备 MoO 的过程中,溶液的酸性不能过强,原因可能是 (常温下,MoO
2 2
实验现象 不与 H+反应)。
实验编号 与镁条反应的物质
产生气体的量 镁条 OH OH
1 HO 很少 无明显现象
19.(14分)马来酸(O
O)及其衍生物在化工领域具有重要应用。
2
帩帩
2 NaSO 溶液 很少,但比实验1多 无明显现象 OH OH
2 4
(1)在
CaNiSi催化作用下,O
O能发生反应:
3 (NH)SO 溶液 较多 明显减少 2 2
4 2 4 帩帩
根据实验,小组同学提出如下猜想:
OH OH HO
猜想1 Na+能促进 Mg与 H
2
O反应 O
O(l)+H(g)幑幐
猜想2 NH+能促进 Mg与 HO反应 帩帩 2
4 2 O
猜想3 SO2-能促进 Mg与 HO反应
4 2
查阅资料获知:Mg(OH)晶体中存在一些正负离子空位,对空位离子半径(r)和钻入离
2 1
r-r
2 1
子半径(r)的关系 A进行计算(A= ×100%,离子电性要相同)可确定 Mg(OH) 晶
2 r 2 2
体结构是否易被破坏而溶解。当 A<15%,破坏易发生;15%<A<30%,破坏可以发生;当
A>30%,破坏难以发生。r(OH-)=0.14nm、r(SO2-)=0.24nm、r(Mg2+)=0.072nm、
4
r(Na+)=0.1nm、r(NH+)=0.14nm。
4
①实验1中后期几乎无气泡产生,原因是 。
②通过计算 A的值,可知猜想 成立。
③结合平衡移动原理分析,实验3能产生较多气泡的原因可能是 。
18.(14分)高铼酸铵(NHReO)和钼酸铵[(NH)MoO]是重要的化工原料,一种以钼精矿(主要
4 4 4 2 4
成分有 MoS、ReS、FeS、AlO 和 SiO)为原料制备二者的工艺流程如下。
2 2 2 2 3 2
氧化 含铼"钼
钼精矿 淋洗 淋洗液 离子交换吸附!解吸
焙烧 烟气
钼焙砂 含钼溶液 含铼溶液 浓缩"结晶 高铼酸铵
氨水 浸出 浸出液 净化"结晶 钼酸铵
浸渣
已知:①“氧化焙烧”后得到的主要物质为 MoO(700℃开始显著升华)、ReO(250℃开始显著
3 2 7
升华)、FeO、AlO、SiO 和 SO;
2 3 2 3 2 2
②“淋洗液”的主要成分为 HReO、HSO 和少量 HMoO。
4 2 4 2 4
请回答下列问题:
(1)“氧化焙烧”的过程能初步分离钼和铼的原因是 。
GD·高三化学 第5页(共8页) GD·高三化学 第6页(共8页)
O
(l) ΔH<0。
OH
①基态 Ni原子的价层电子排布式为 。
②上述反应在 (填“低温”“高温”或“任意温度”)下能自发进行。
OH OH OH OH
③一定条件下,控制 O O的流速为 4×10-5mol·min-1,每分钟内 O O的
帩帩 帩帩
HO
转化率与
O
O
的选择性随时间变化关系如图所示。在第 480min内,生成
OH
HO
O
O
的速率可表示为 mol·min-1;工业生产中,其他条件不变,适当
OH
减缓进料流速能增大反应物的转化率,原因可能是 。
%&& ’&& ()&
反应时间!"#$
+*率化转 选择性!+
,’-&.’&/O
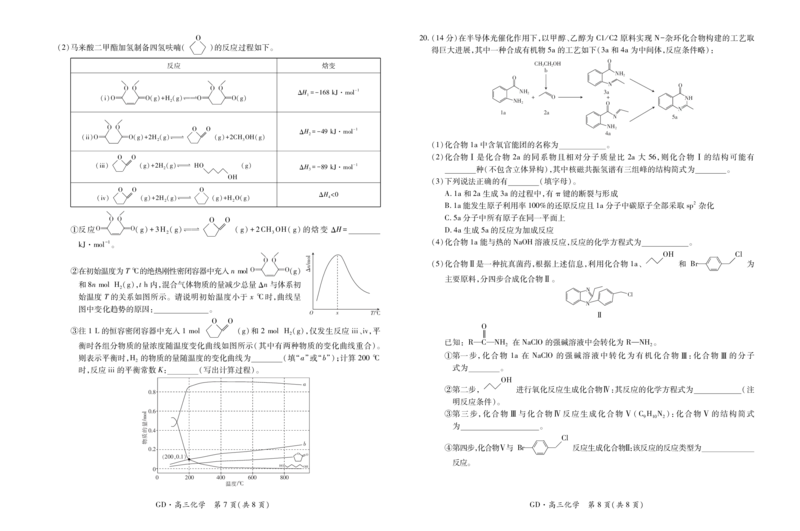
(2)马来酸二甲酯加氢制备四氢呋喃( )的反应过程如下。
反应 焓变
! ! ! !
ΔH=-168kJ·mol-1
(i)! !(g)+H(g)幑幐! !(g) 1
2
(ii)! ! ! !(g)+2H(g)幑幐 O O (g)+2CHOH(g) ΔH 2 =-49kJ·mol-1
2 3
O O
(iii) (g)+2H 2 (g)幑幐 HO (g) ΔH 3 =-89kJ·mol-1
OH
O O O
ΔH<0
(iv) (g)+2H(g)幑幐 (g)+HO(g) 4
2 2
! ! O O
①反应! !(g)+3H(g)幑幐 (g)+2CHOH(g)的焓变 ΔH=
2 3
kJ·mol-1。
# " !!!
GD·高三化学 第7页(共8页) GD·高三化学 第8页(共8页)
$#"!$! ! !
②在初始温度为T℃的绝热刚性密闭容器中充入nmol! !(g)
和8nmolH(g),th内,混合气体物质的量减少总量Δn与体系初
2
始温度 T的关系如图所示。请说明初始温度小于 x℃时,曲线呈
图中变化趋势的原因: 。
O O
③往1L的恒容密闭容器中充入1mol (g)和 2molH(g),仅发生反应 iii、iv,平
2
衡时各组分物质的量浓度随温度变化曲线如图所示(其中有两种物质的变化曲线重合)。
则表示平衡时,H 的物质的量随温度的变化曲线为 (填“a”或“b”);计算 200℃
2
时,反应 iii的平衡常数 K: (写出计算过程)。
!"#
!"$
!"%
!"&
!
! &!! %!!
温度’!
+*)(量的质物
20.(14分)在半导体光催化作用下,以甲醇、乙醇为 C1/C2原料实现 N-杂环化合物构建的工艺取
得巨大进展,其中一种合成有机物5a的工艺如下(3a和4a为中间体,反应条件略):
!
&#&#!# ’ $
%
"#
! +
" !
"# ’*
$ ( ! . "#
"# $ !
"
)* +*
" ,*
"# + -*
(1)化合物1a中含氧官能团的名称为 。
(2)化合物Ⅰ是化合物 2a的同系物且相对分子质量比 2a大 56,则化合物Ⅰ的结构可能有
种(不包含立体异构),其中核磁共振氢谱有三组峰的结构简式为 。
(3)下列说法正确的有 (填字母)。
A.1a和2a生成3a的过程中,有 π键的断裂与形成
B.1a能发生原子利用率100%的还原反应且1a分子中碳原子全部采取 sp2杂化
C.5a分子中所有原子在同一平面上
D.4a生成5a的反应为加成反应
(4)化合物1a能与热的 NaOH溶液反应,反应的化学方程式为 。
OH Cl
師師師師
(5)化合物Ⅱ是一种抗真菌药,根据上述信息,利用化合物 1a、 和 Br 为
帩帩
主要原料,分四步合成化合物Ⅱ。
!
"#
!
Ⅱ
已知:RC
!
"
!&!!"!./# , ,
-, ,-
$!! #!!
O
NH 在 NaClO的强碱溶液中会转化为 R—NH。
2 2
①第一步,化合物 1a在 NaClO的强碱溶液中转化为有机化合物Ⅲ:化合物Ⅲ的分子
式为 。
OH
②第二步, 进行氧化反应生成化合物Ⅳ:其反应的化学方程式为 (注
明反应条件)。
③第三步,化合物Ⅲ与化合物Ⅳ反应生成化合物Ⅴ(CH N):化合物Ⅴ的结构简式
9 10 2
为 。
Cl
師師師師
④第四步,化合物Ⅴ与 Br 反应生成化合物Ⅱ:该反应的反应类型为
帩帩
反应。