文档内容
高三年级 3月二轮复习阶段检测
化学参考答案
1.【答案】C
【解析】潮州木雕的主要材料为木材,主要成分为纤维素、木质素,属于有机高分子材料,A项不符合题意;广州檀
香扇的主要成分为纤维素、木质素,属于有机高分子材料,B项不符合题意;佛山石湾艺术陶瓷的主要成分为硅
酸盐,属于无机非金属材料,C项符合题意;广绣百鸟争鸣图的主要材料为蚕丝,主要成分为蛋白质,属于有机高
分子材料,D项不符合题意。
2.【答案】B
【解析】水升华是物理变化,仅破坏范德华力和氢键,H—O共价键不会断裂,A项错误;CO 中心 C原子的价层
2
电子对数为2,无孤电子对,VSEPR模型名称为直线形,B项正确;SiC是由共价键和原子形成空间网状结构的共
价晶体,C项错误;Nb(铌)的原子序数为41,质子数为41,D项错误。
3.【答案】B
【解析】KMnO 与浓盐酸在常温下即可发生反应生成Cl,装置可实现Cl的制备,A项不符合题意;Cl中混有的
4 2 2 2
HCl杂质会与饱和NaHCO 溶液反应生成CO,引入新杂质,同时Cl也会与NaHCO 溶液反应,净化Cl应选用
3 2 2 3 2
饱和食盐水除HCl,再用浓硫酸干燥,B项符合题意;Cl密度大于空气,可采用向上排空气法收集,装置应“长管
2
进气、短管出气”,C项不符合题意;红热铁丝在 Cl中燃烧生成 FeCl,Cl在此反应中作氧化剂,可验证其氧化
2 3 2
性,D项不符合题意。
4.【答案】D
【解析】手性碳原子是指连有 4个不同原子或原子团的饱和碳原子,该有机物分子中无符合此特征的碳原子,
A项错误;1分子该有机物中σ键数量为30个,B项错误;该分子中不含有与N、O或F相连的氢原子,不能形成
分子内氢键,C项错误;分子中的苯环、不饱和键可与H 发生加成反应(还原反应),分子中的烷基、苯环可发生
2
卤代等取代反应,D项正确。
5.【答案】A
【解析】低温只能减慢反应速率,无法改变反应的活化能,催化剂才能改变反应的活化能,A项错误;草木灰含有
KCO,K元素是植物生长的必需元素,B项正确;乙烯是荔枝的催熟剂,高锰酸钾具有强氧化性,可氧化乙烯,延
2 3
缓荔枝成熟,C项正确;浓氨水与氯气发生反应:8NH+3Cl6NHCl+N,NHCl是白色固体,可观察到白烟,
3 2 4 2 4
因此可用浓氨水检验氯气管道是否泄漏,D项正确。
6.【答案】A
【解析】聚氯乙烯是由氯乙烯(CHCHCl)加聚得到的高分子,难以降解,会造成白色污染,A项正确;重金属离
2
子能使蛋白质发生变性而失去生理活性,盐析是可逆过程,不会使蛋白质失活,B项错误;酸雨是指pH<5.6的雨
水,并非所有c(H+)>c(OH-)的酸性雨水都属于酸雨,C项错误;胶体的分散质粒子直径在1~100nm(10-9~10-7m)
之间,含有直径为10-5m左右灰霾粒子的霾不属于胶体,D项错误。
7.【答案】D
【解析】a进行焰色试验,火焰呈黄色,说明含Na元素,根据图中转化关系可知 a为 NaOH;NaOH与少量 CO 反
2
应生成 b(NaCO),b与 CO、HO反应生成 c(NaHCO)。NaCO 的热稳定性强于 NaHCO,A项错误;
2 3 2 2 3 2 3 3
c(NaHCO)与过量Ba(OH)反应生成NaOH、BaCO 沉淀和HO,对应转化③,并非转化⑤,B项错误;转化⑥的
3 2 3 2
离子方程式为CO2-+Ba2+BaCO↓、CO2-+Ca2+CaCO↓等,C项错误;①~⑥的所有反应中,各元素化合
3 3 3 3
价均未发生变化,均为非氧化还原反应,D项正确。
GD·高三化学 第 1页(共6页)
书书书8.【答案】C
【解析】金属铜中,Cu原子脱落的价电子形成电子气,电子气在电场中定向移动,因此铜具有优良的导电性,A项
正确;液态水凝结成冰时,氢键数目增多,氢键具有方向性,水分子通过氢键形成疏松的晶体结构,导致体积增
大,B项正确;1molHPO 最多能消耗 2molNaOH,说明 HPO 是二元酸,分子中应只有 2个可电离的羟基
3 3 3 3
(—OH),若结构中含有3个可电离的羟基,则为三元酸,可消耗3molNaOH,与事实矛盾,C项错误;Ag+含有能
接受电子对的空轨道,NH 中的N原子含有孤电子对,二者能形成可溶性物质[Ag(NH)]Cl,D项正确。
3 3 2
9.【答案】D
【解析】基态 Fe原子的价层电子排布式为 3d64s2,价电子总数为 8,因此 1mol基态 Fe原子中,价电子总数为
8N,A项错误;Cu与S反应生成CuS,64gCu与足量S完全反应,转移电子数目为 N,B项错误;未给出 NaS
A 2 A 2
!
溶液的体积,无法计算S2-、HS-和HS的总数目,C项错误;P中的化学键均为共价键: !,1molP 含有共
2 4 ! 4
!
价键的总数为6N,D项正确。
A
10.【答案】B
【解析】实验开始2天后图2烧杯溶液变成浅蓝色,说明 Cu被氧化为 Cu2+,该装置为原电池,Cu失电子发生氧
化反应,作负极,石墨作正极,A项错误;该体系为酸性环境,正极上 O 得电子,与 H+结合生成水,正极反应为
2
O+4e-+4H+2HO,B项正确;Cu在金属活动性顺序中位于H之后,常温下Cu与稀硫酸不发生置换反应生
2 2
成H,该原电池反应为Cu的吸氧腐蚀,并非析氢腐蚀,C、D项错误。
2
11.【答案】A
【解析】SO 溶于水生成亚硫酸,使紫色石蕊溶液变红,但不能漂白酸碱指示剂,溶液不会褪色,A项错误;酸性
2
高锰酸钾溶液褪色,是因为SO 被MnO-(H+)氧化,SO 作还原剂,B项正确;SO 与 NaS反应生成淡黄色的单
2 4 2 2 2
质S,C项正确;NaOH溶液吸收SO,气体被消耗,体系混乱度减小,该过程为熵减过程,D项正确。
2
12.【答案】C
【解析】a、b、c为同周期的非金属元素,原子半径:a<b<c,第一电离能:b<c<a,结合第一电离能的递变规律(同
周期ⅤA族>ⅥA族),可确定a为F、b为O、c为N;则d、e、f为第三周期元素,原子半径:d<e<f,第一电离能:e>
d>f,基态e原子s轨道上的电子总数等于p轨道上的电子总数,可确定d为Al、e为Mg、f为Na。电负性顺序为
F>O>N,即a>b>c,A项错误;金属性:Na>Mg>Al,因此最高价氧化物对应水化物的碱性:f>e>d,B项错误;b的
最简单氢化物为HO,c的最简单氢化物为NH,HO的沸点更高,C项正确;NF和 NO-的空间结构分别为三
2 3 2 3 3
角锥形和平面三角形,D项错误。
13.【答案】D
【解析】制备乙酸乙酯时用小火均匀加热,目的是防止反应物挥发、提高原料利用率,与乙酸乙酯难溶于水无因
果关系,A项不符合题意;工业上制备硫酸,S先与O 反应生成SO,SO 经催化氧化生成SO,无法直接由 S生
2 2 2 3
成SO,陈述Ⅰ错误,B项不符合题意;蔗糖是二糖,一分子蔗糖在酸的作用下水解生成一分子葡萄糖和一分子
3
果糖,陈述Ⅱ错误,C项不符合题意;油脂是高级脂肪酸的甘油酯,因此油脂在碱性条件下发生皂化反应,生成
甘油和高级脂肪酸盐,陈述Ⅰ、Ⅱ均正确,且存在因果关系,D项符合题意。
14.【答案】B
△
【解析】炽热的木炭与热的浓硝酸发生反应:C+4HNO(浓)CO↑+4NO↑+2HO,同时浓硝酸受热会发生
3 2 2 2
△
分解:4HNO 4NO↑+O↑+2HO。无水CaCl无法吸收NO 等有毒尾气,不能作为该实验的尾气处理试
3 2 2 2 2 2
剂,A项错误;反应中 N元素化合价全部降低,生成 NO,浓硝酸体现了氧化性,发生了还原反应,B项正确;浓
2
硝酸受热分解也会生NO,且存在反应 2NO 幑幐NO,无法计算,C项错误;反应生成的氧化物有 CO、NO、
2 2 2 4 2 2
HO,只有CO 属于酸性氧化物,D项错误。
2 2
GD·高三化学 第 2页(共6页)15.【答案】A
【解析】BaCO 存在溶解平衡:BaCO(s)幑幐Ba2+(aq)+CO2-(aq),t时已加入了 NaSO 溶液,发生沉淀转化:
3 3 3 2 2 4
BaCO(s)+SO2-(aq)幑幐BaSO(s)+CO2-(aq),部分 Ba2+与 SO2-结合生成 BaSO 沉淀,因此溶液中 c(Ba2+)<
3 4 4 3 4 4
c(CO2-)+c(HCO-)+c(HCO),元素守恒不成立,A项错误;t时溶液pH>7,是因为 CO2-发生水解:CO2-+HO
3 3 2 3 1 3 3 2
幑幐HCO-+OH-,证明BaCO 存在溶解平衡,B项正确;t时的溶液 pH大于 t时的溶液 pH,说明 CO2-浓度增
3 3 2 1 3
大,即有BaCO 转化成BaSO,释放出更多CO2-,C项正确;若将NaSO 替换为蒸馏水,实验结束后仍有固体剩
3 4 3 2 4
余,说明溶液仍为BaCO 的饱和溶液,温度不变,K(BaCO)不变,CO2-浓度不变,溶液pH不变,D项正确。
3 sp 3 3
16.【答案】D
【解析】该装置为电解池,IrO 电极上 Br-失电子生成 Br,为阳极,与外接电源正极相连,泡沫镍电极为阴极,
2 2
HO得电子发生还原反应生成 H 和 OH-,电极反应为 2HO+2e-2OH-+H↑,A、B项正确;总反应为
2 2 2 2
电解 O O
CH+CO+HO
2 4 2 2
GD·高三化学 第 3页(共6页)
O
+H,阳极消耗1molCH 和1molCO(共2mol气体),阴极生成1molH,相同
2 2 4 2 2
条件下,IrO 电极上消耗的气体与泡沫镍电极上产生的气体的体积比为21,C项正确;碳酸乙烯酯的摩尔质
2
量为88g·mol-1,44g碳酸乙烯酯的物质的量为0.5mol,根据总反应生成0.5mol碳酸乙烯酯时,泡沫镍电极
上有0.5molH 生成,D项错误。
2
17.【答案】(1)>(1分,唯一答案)
(2)B(1分,唯一答案)
(3)①1×10-10(2分,写10-10不扣分) d(1分,唯一答案)
②1×10-10.2(2分,写10-10.2、4×10-10.8也给分)
高温
(4)i.3Fe+4HO(g)FeO+4H(2分,物质正确1分,配平、条件错误或未写“g”扣1分,三者均有错也只扣1分)
2 3 4 2
ii.①Mg与水反应生成的Mg(OH)难溶于水,覆盖在镁条表面,隔绝了Mg与水的接触,阻止反应继续进行
2
(2分,合理即可)
②1(1分,唯一答案)
③Mg(OH)存在溶解平衡:Mg(OH)(s)幑幐Mg2+(aq)+2OH-(aq)(1分,写出 Mg(OH)的溶解平衡反
2 2 2
应式才得分),NH+与OH-反应,使平衡向溶解方向移动,破坏 Mg(OH)保护膜,使 Mg与水的反应持续
4 2
进行(1分)或
Mg(OH)存在溶解平衡:Mg(OH)(s)幑幐Mg2+(aq)+2OH-(aq)(1分,写出 Mg(OH)的溶解平衡反应
2 2 2
式才得分),OH-与NH+水解出的H+反应,使平衡向溶解方向移动,破坏Mg(OH)保护膜,使Mg与水的
4 2
反应持续进行(1分)
【解析】(1)HO中O原子有2个孤电子对,HO+中 O原子有1个孤电子对;孤电子对成键电子对的斥力大于
2 3
成键电子对之间的斥力,HO+中孤电子对更少,对成键电子对的斥力更小,因此键角:HO+>HO。
3 3 2
(2)海水淡化的核心是除去可溶性盐类杂质。活性炭仅能吸附色素和异味,无法除去可溶性盐,A项不符合题
意;蒸馏可将水蒸发冷凝,得到纯净的蒸馏水,实现海水淡化,B项符合题意;CCl无法萃取盐类,不能实现水与
4
盐的分离,C项不符合题意;加入稀盐酸煮沸无法除去可溶性盐,还会引入Cl-杂质,D项不符合题意。
(3)①NaOH抑制水的电离,a点 pH=10的 NaOH溶液中,H+全部由水电离,因此水电离出的 c(H+)=
1×10-10mol·L-1。NaOH抑制水的电离,NaCO、NaHCO 水解促进水的电离。b点为 NaOH和 NaCO 的混合
2 3 3 2 3
溶液,溶液呈碱性;c点为NaCO 溶液,水的电离程度最大,溶液呈碱性;d点为NaHCO 与HCO 的混合溶液,
2 3 3 2 3溶液呈中性。②c点为NaCO 溶液,溶液中 c(OH-)=10-4.4mol·L-1,c(H+)=10-9.6mol·L-1。c(HCO-)≈
2 3 3
c(OH-)=10-4.4mol·L-1、c(CO2-)≈(5×10-5-10-4.4)mol·L-1≈10-5mol·L-1,碳酸的二级电离常数
3
c(H+)·c(CO2-) 10-9.6×10-5
K(HCO)= 3 ≈ =10-10.2。
a2 2 3 c(HCO-) 10-4.4
3
高温
(4)i.红热的铁与水蒸气在高温条件下会反应生成 FeO 和 H:3Fe+4HO(g)FeO+4H。ii.①Mg与水
3 4 2 2 3 4 2
反应生成的Mg(OH)是难溶物,覆盖在镁条表面,隔绝 Mg与水的接触,阻止反应继续进行,因此中后期几乎
2
r-r
无气泡产生。②根据A= 2 1 ×100%可知,Na+替代Mg2+的A=28%,可以破坏晶体结构,猜想1成立;NH+替
r 4
2
代Mg2+,A≈48.6%>30%,难以破坏晶体结构,猜想2不成立;SO2-替代OH-的 A≈41.7%>30%,难以破坏晶体
4
结构,猜想3不成立。③见答案。
18.【答案】(1)ReO 和MoO 升华温度不同(1分,合理即可)
2 7 3
(2)MoO+2NH·HOMoO2-+2NH++HO(2分,物质正确1分,配平1分) 将钼焙砂粉碎(或适当升高温
3 3 2 4 4 2
度、搅拌、适当提高氨水浓度等,任写一种,1分)
(3)Cl-、SO2-(2分,1个1分) C(1分,不区分大小写)
4
6×186
(4)6(1分,写“六”不扣分) (2分,其他正确形式都给分,数量级错误扣1分)
3槡3
a2bN×10-30
2 A
(5)MoO6-+14e-+20H+7MoO+10HO(2分,物质正确1分,配平1分) 酸性过强时,H+易在阴极得电子
7 24 2 2
生成H,降低MoO 的产率(2分,意思相近即可)
2 2
【解析】(1)“氧化焙烧”过程中,生成的 ReO 易升华,变为气态进入烟气,而 MoO 升华温度较高,留在“钼焙
2 7 3
砂”中,从而实现钼和铼的初步分离。
(2)MoO 是酸性氧化物,与氨水反应生成钼酸铵和水;提高浸出速率的措施可从增大接触面积、升高温度、搅
3
拌、提高反应物浓度等角度作答。
(3)离子交换过程中,树脂上的Cl-被交换进入水相,淋洗液中的 SO2-、MoO2-与树脂亲和力弱,留在水相;阴离
4 4
子与树脂的亲和力:SCN->ReO-,因此可用NHSCN溶液洗脱树脂上的ReO-。
4 4 4
1 1 6×186 3槡3
(4)结构单元中铼原子总数=12× +2× +3=6;结构单元的质量= g,结构单元的体积= a2b×10-30cm3,
6 2 N 2
A
6×186
晶体密度= g·cm-3。
3槡3
a2bN×10-30
2 A
(5)电解时,Mo元素从+6价降至+4价,每个Mo得2个电子,7个 Mo共得14个电子,结合酸性环境配平电极
反应:MoO6-+14e-+20H+7MoO+10HO;酸性过强时,H+易在阴极放电生成H,降低MoO 的产率。
7 24 2 2 2 2
19.【答案】(1)①3d84s2(1分,唯一答案)
②低温(1分,唯一答案)
③6.4×10-6(2分) 进料流速减缓,反应物在催化剂表面的停留时间延长,反应更充分(2分,意思相近即可)
(2)①-217(1分,唯一答案)
②温度小于x℃,th时,反应未达到平衡(1分);加氢反应i、iii、iv均为气体物质的量减少的反应,初始温度
升高,反应速率加快,th内反应i、ii、iii、iv的反应程度加大,混合气体物质的量减少总量Δn增大(类似表述
即可,1分)
GD·高三化学 第 4页(共6页)③b(2分,唯一答案)
O
根据碳原子总物质的量为4mol和化学计量数关系可知a为平衡时 、HO的物质的量随温度的变化
2
曲线,则b为平衡时H 的物质的量随温度的变化曲线,根据化学计量数及投料比可知体系中 n(HO)=
2 2
O O O
1
n( )、n( )= n(H)。200℃达到平衡时,n(H)=n(HO )=0.1mol,
2 2 2
OH
O O O
1
n( )= n(H)=0.05mol(1分),因此 n( )=n(HO)=1mol-0.1mol-0.05mol=
2 2 2
c(HO )
0.1
OH 1
0.85mol;反应 iii的平衡常数 K= = =200(列出表达式或计算式得
O O 0.1 0.05
( )2×
c2(H)·c( ) 1 1
2
1分,计算出最终结果再得1分)
【解析】(1)①Ni是28号元素,基态Ni原子的价层电子排布式为3d84s2。②该加氢反应的 ΔH<0,反应后气体
分子数减少,ΔS<0;根据 ΔG=ΔH-TΔS<0反应自发,因此低温下该反应能自发进行。③第 480min内,
OH OH HO
O
O的进料流速为4×10-5mol·min-1,转化率为40%,
帩帩
O
GD·高三化学 第 5页(共6页)
O
的选择性为40%,因此第480min
OH
HO
内生成
O
O
的速率=4×10-5mol·min-1×40%×40%=6.4×10-6mol·min-1;工业上减缓进料流速,
OH
反应物在催化剂表面的停留时间延长,与催化剂接触更充分,反应更完全,因此反应物的转化率提高。
(2)①根据盖斯定律可知ΔH=ΔH+ΔH=(-168kJ·mol-1)+(-49kJ·mol-1)=-217kJ·mol-1。②温度小于
1 2
x℃,th时,反应未达到平衡,加氢反应i、iii、iv均为气体物质的量减少的反应,初始温度升高,反应速率加快,
th内反应i、ii、iii、iv的反应程度加大,混合气体物质的量减少总量Δn增大。温度高于x℃,th时,各反应达到
平衡,温度升高,平衡逆向移动,混合气体物质的量减少总量Δn减小。③见答案。
20.【答案】(1)酰胺基(1分,唯一答案)
(2)8(2分,写“八”不扣分) (CH)CCHCHO(1分,其他正确的结构简式也得分)
3 3 2
(3)AB(2分,漏选扣1分,错选不得分)
!
!""#$
△
(4)
"# $
+NaOH→ +NH
3
↑(2分,物质正确1分,配平、条件有错扣1分,二者都错也只
#%
"# &
$
扣1分,未写“↑不扣分)
(5)①CHN(1分,唯一答案)
6 8 2
催化剂
②2CHCHCHOH+O →2CHCHCHO+2HO(2分,催化剂写Cu、Ag均可,物质正确1分,配平、条件
3 2 2 2 △ 3 2 2
有错扣1分,二者都错也只扣1分)!
!
③ " (2分,其他正确的结构简式也得分)
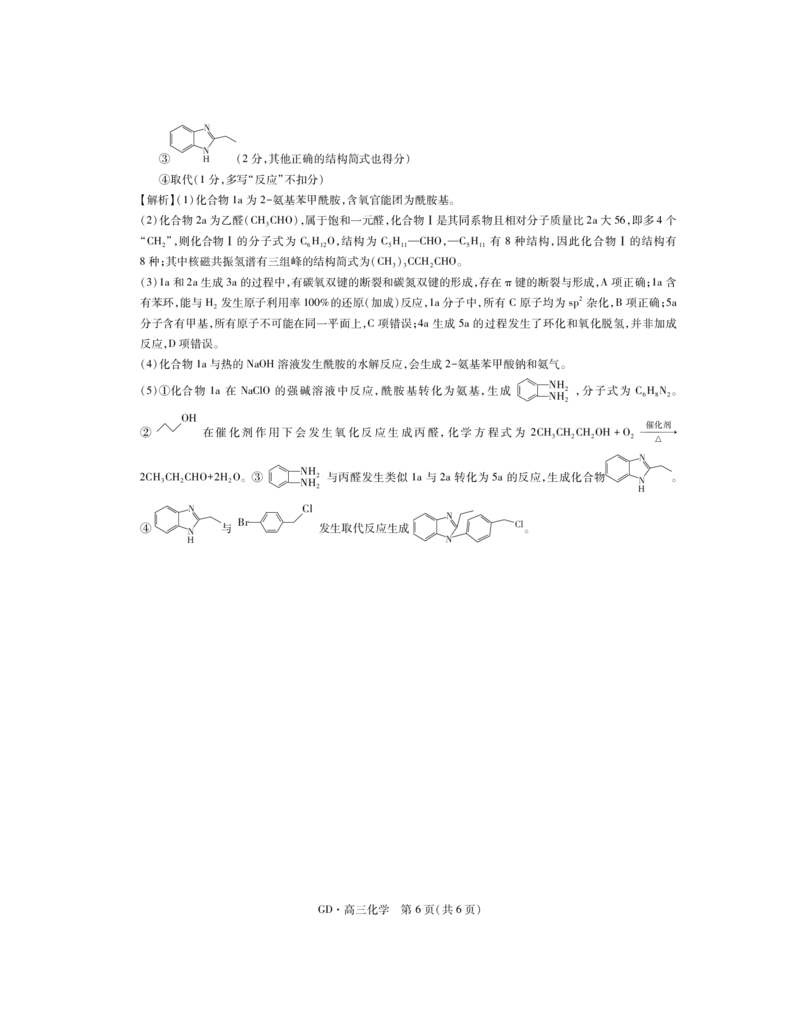
④取代(1分,多写“反应”不扣分)
【解析】(1)化合物1a为2-氨基苯甲酰胺,含氧官能团为酰胺基。
(2)化合物2a为乙醛(CHCHO),属于饱和一元醛,化合物Ⅰ是其同系物且相对分子质量比2a大56,即多4个
3
“CH”,则化合物Ⅰ的分子式为 CH O,结构为 CH —CHO,—CH 有 8种结构,因此化合物Ⅰ的结构有
2 6 12 5 11 5 11
8种;其中核磁共振氢谱有三组峰的结构简式为(CH)CCHCHO。
3 3 2
(3)1a和2a生成3a的过程中,有碳氧双键的断裂和碳氮双键的形成,存在π键的断裂与形成,A项正确;1a含
有苯环,能与H 发生原子利用率100%的还原(加成)反应,1a分子中,所有 C原子均为 sp2杂化,B项正确;5a
2
分子含有甲基,所有原子不可能在同一平面上,C项错误;4a生成5a的过程发生了环化和氧化脱氢,并非加成
反应,D项错误。
(4)化合物1a与热的NaOH溶液发生酰胺的水解反应,会生成2-氨基苯甲酸钠和氨气。
師師
NH
(5)①化合物 1a在 NaClO的强碱溶液中反应,酰胺基转化为氨基,生成帨帨 2 ,分子式为 CHN。
師師NH 6 8 2
2
OH
催化剂
② 在催化剂作用下会发生氧化反应生成丙醛,化学方程式为 2CHCHCHOH+O →
3 2 2 2 △
!
師師
NH
2CHCHCHO+2HO。③帨帨 2 与丙醛发生类似1a与2a转化为5a的反应,生成化合物 。
3 2 2 師師NH !
2 "
! Cl
師師師師
!
Br "#
④ 与 发生取代反应生成 。
! 帩帩
" !
GD·高三化学 第 6页(共6页)