文档内容
恩施州 2026 届高三第二次质量监测考试
化学解析
1.【答案】D
【解析】维生素C作抗氧化剂,具有还原性,故答案为D
2.【答案】A
【解析】稀土改性合金,改善合金性能,如耐热、耐腐蚀等,化学活性降低(必修一84页),A错;储氢
合金储氢量大,,金属氢化物既容易形成,稍微加热有容易分解,吸放氢速率快(必修一83页),B正确;
碳纤维符合材料强度大质量轻,C正确;微型蜂巢结构可有效拆解并吸收雷达波,从而达到隐身,D正确。
故答案为A
3.【答案】C
【解析】亚硫酸易溶于水,要拆开,A错;铁离子和氢氧根要反应,B错误;化合价升降不守恒,D错误。
故答案为C
4.【答案】B
【解析】K>K’,NH 碱性强于NH OH,故答案为B
3 2
5.【答案】B
【解析】银离子会和氯离子产生氯化银沉淀,A错;未调节水解液为碱性,无法产生沉淀,C错误;氢氧化
钠为稀溶液且未加热,D错误。故答案为B
6.【答案】C
【解析】X分子中酰胺键中碳氧双键不能和氢气加成,苯环和吡啶环可与氢气加成,则1molX最多与6
molH 加成,C错误;酰胺在酸或碱存在并加热的条件下可以发生水解反应(选择性必修3P ),D正确;
2 81
故答案为C。
7.【答案】A
【解析】(选择性必修1P )甲池输入精制饱和NaCl溶液,输出为稀NaCl,离子交换膜仅允许阳离子通
121
过,甲池就是氯碱工业模型示意图,即甲池为电解池,X为氯气,Y为氢气,乙池为氢气的燃料电池,A
错误;B正确,C正确;乙池输入 a%NaOH 溶液,因 Na⁺从甲池移入,正极生成 OH⁻,NaOH 浓度升高,
故输出的 b%NaOH 浓度大于输入的 a%,即a1mol/L 酸性强,亚硫酸根、亚硒酸根以亚硫酸分子和亚
硒酸分子形式存在,其方程式为2H SO +H SeO Se↓+H SO +H O(或者2Na SO +H SeO Se↓+
2 3 2 3 2 4 2 2 3 2 3
2Na SO +H O)
2 4 2
17.(除标注外,每空2分,共13分)
【答案】(1)Cu+2Fe3+=2Fe2++Cu2+
(2)CuSCN;ⅱ
(3)Fe2+(1分)
(4)2Cu2++4SCN-=2CuSCN↓+(SCN) ,氧化(1分),还原(1分),不能
2
【解析】(2)根据实验III第三组分析,排除氯化亚铜,故白色沉淀为CuSCN;根据实验II分析,假设ⅱ
成立
(4)通过对已知分析,是亚铁离子作催化剂加快了反应速率
(5)通过流程分析,该反应为2Cu2++4SCN-=2CuSCN↓+(SCN)
2
18.(每空2分,共14分)
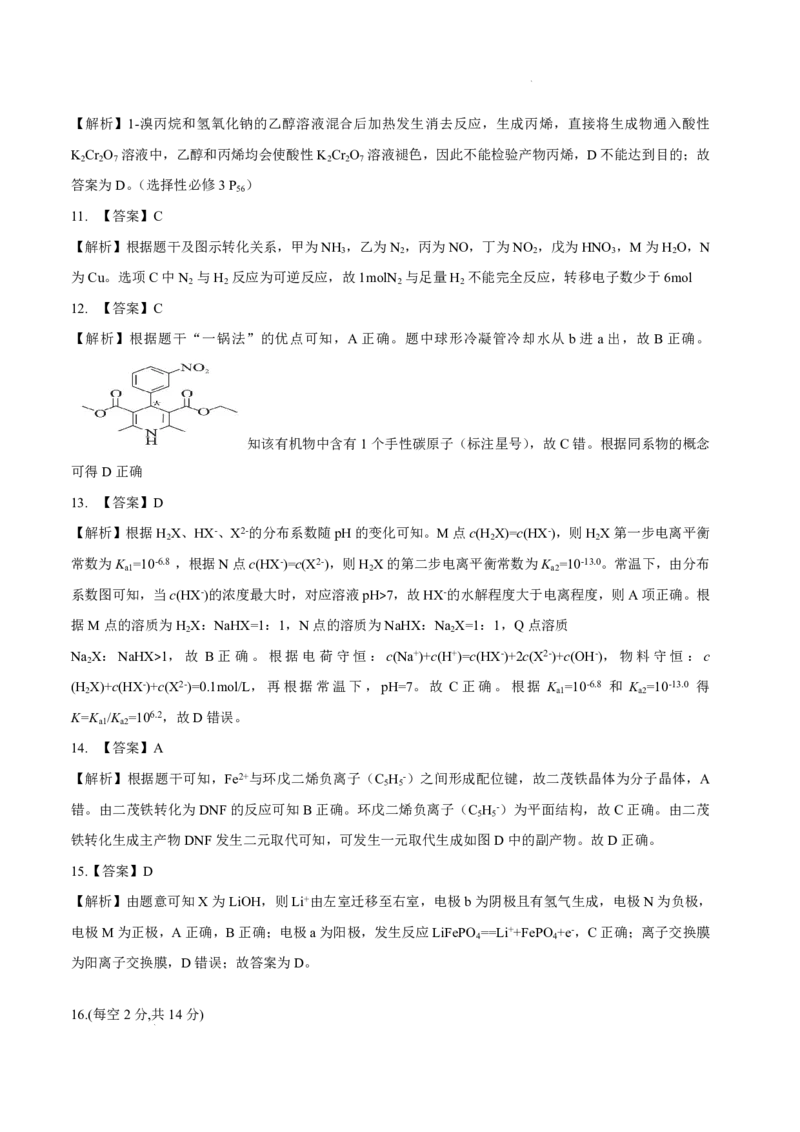
【答案】(1)
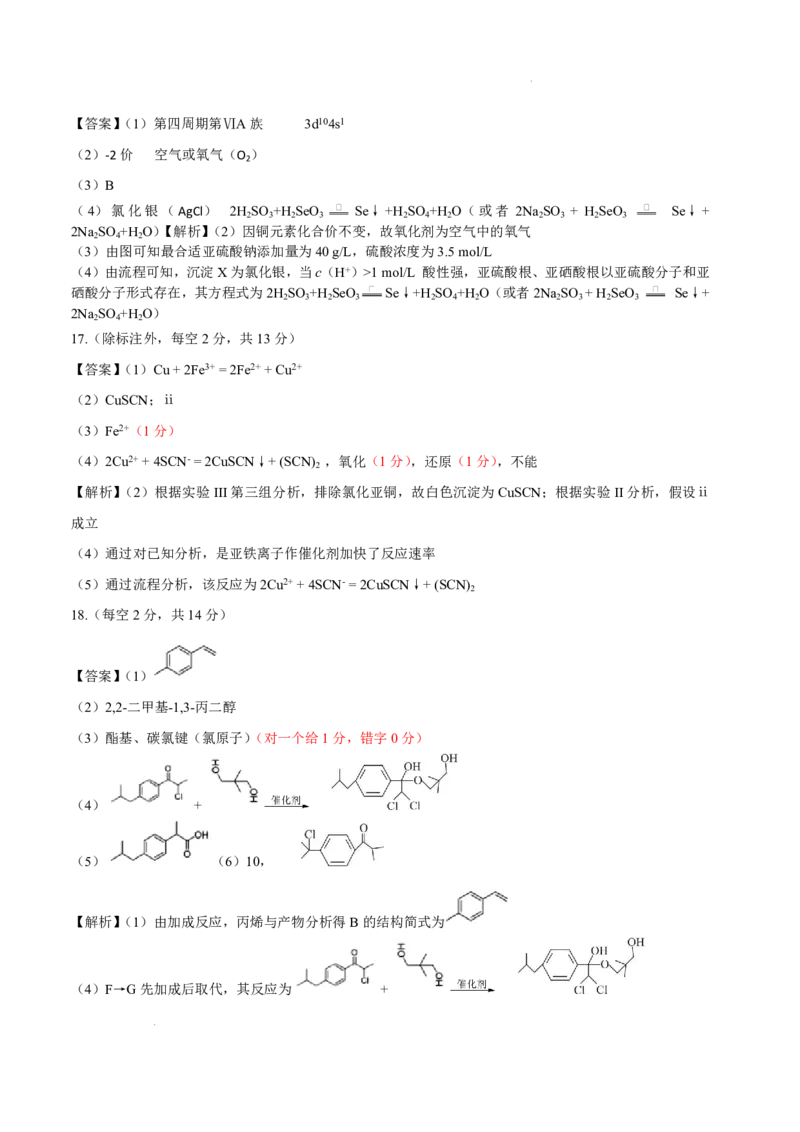
(2)2,2-二甲基-1,3-丙二醇
(3)酯基、碳氯键(氯原子)(对一个给1分,错字0分)
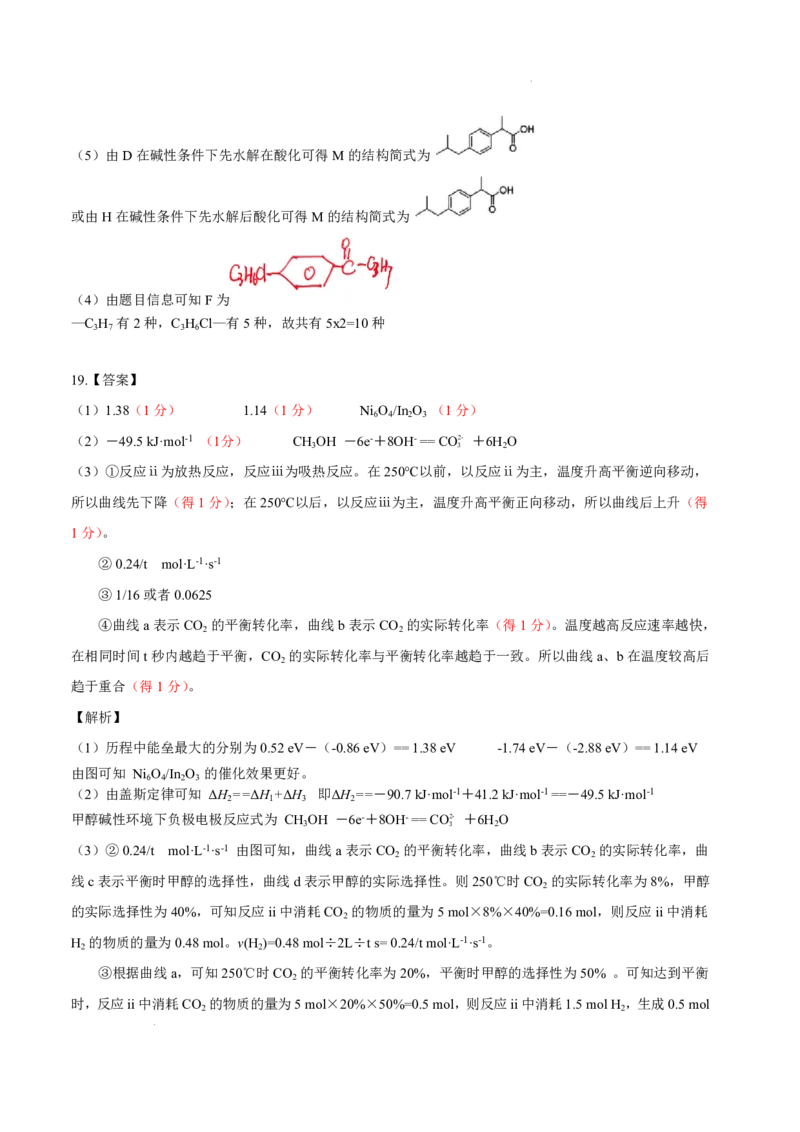
(4) +
(5) (6)10,
【解析】(1)由加成反应,丙烯与产物分析得B的结构简式为
(4)F→G先加成后取代,其反应为 +
学科网(北京)股份有限公司(5)由D在碱性条件下先水解在酸化可得M的结构简式为
或由H在碱性条件下先水解后酸化可得M的结构简式为
(4)由题目信息可知F为
—C H 有2种,C H Cl—有5种,故共有5x2=10种
3 7 3 6
19.【答案】
(1)1.38(1分) 1.14(1分) Ni O /In O (1分)
6 4 2 3
(2)-49.5kJ·mol-1 (1分) CH OH -6e-+8OH-==CO2- +6H O
3 3 2
(3)①反应ⅱ为放热反应,反应ⅲ为吸热反应。在250℃以前,以反应ⅱ为主,温度升高平衡逆向移动,
所以曲线先下降(得1分);在250℃以后,以反应ⅲ为主,温度升高平衡正向移动,所以曲线后上升(得
1分)。
②0.24/t mol·L-1·s-1
③1/16或者0.0625
④曲线a表示CO 的平衡转化率,曲线b表示CO 的实际转化率(得1分)。温度越高反应速率越快,
2 2
在相同时间t秒内越趋于平衡,CO 的实际转化率与平衡转化率越趋于一致。所以曲线a、b在温度较高后
2
趋于重合(得1分)。
【解析】
(1)历程中能垒最大的分别为0.52eV-(-0.86eV)==1.38eV -1.74eV-(-2.88eV)==1.14eV
由图可知 Ni O /In O 的催化效果更好。
6 4 2 3
(2)由盖斯定律可知 ΔH ==ΔH +ΔH 即ΔH ==-90.7kJ·mol-1+41.2kJ·mol-1==-49.5kJ·mol-1
2 1 3 2
甲醇碱性环境下负极电极反应式为 CH OH -6e-+8OH-==CO2- +6H O
3 3 2
(3)②0.24/t mol·L-1·s-1 由图可知,曲线a表示CO 的平衡转化率,曲线b表示CO 的实际转化率,曲
2 2
线c表示平衡时甲醇的选择性,曲线d表示甲醇的实际选择性。则250℃时CO 的实际转化率为8%,甲醇
2
的实际选择性为40%,可知反应ii中消耗CO 的物质的量为5mol×8%×40%=0.16mol,则反应ii中消耗
2
H 的物质的量为0.48mol。v(H )=0.48mol÷2L÷ts=0.24/tmol·L-1·s-1。
2 2
③根据曲线a,可知250℃时CO 的平衡转化率为20%,平衡时甲醇的选择性为50% 。可知达到平衡
2
时,反应ii中消耗CO 的物质的量为5mol×20%×50%=0.5mol,则反应ii中消耗1.5molH ,生成0.5mol
2 2
学科网(北京)股份有限公司CH OH,生成0.5molH O;反应iii中消耗CO 的物质的量为5mol×20%×50%=0.5mol,则反应iii中消
3 2 2
耗0.5molH ,生成0.5molCO,生成0.5molH O。平衡时反应ii中各物质的物质的量分别为n(CO )=5mol
2 2 2
×80%=4mol,n(H )=4mol-1.5mol-0.5mol=2mol,n(CH OH)=0.5mol,n(H O)=1mol。则反应ii的平衡常
2 3 2
数K=
学科网(北京)股份有限公司