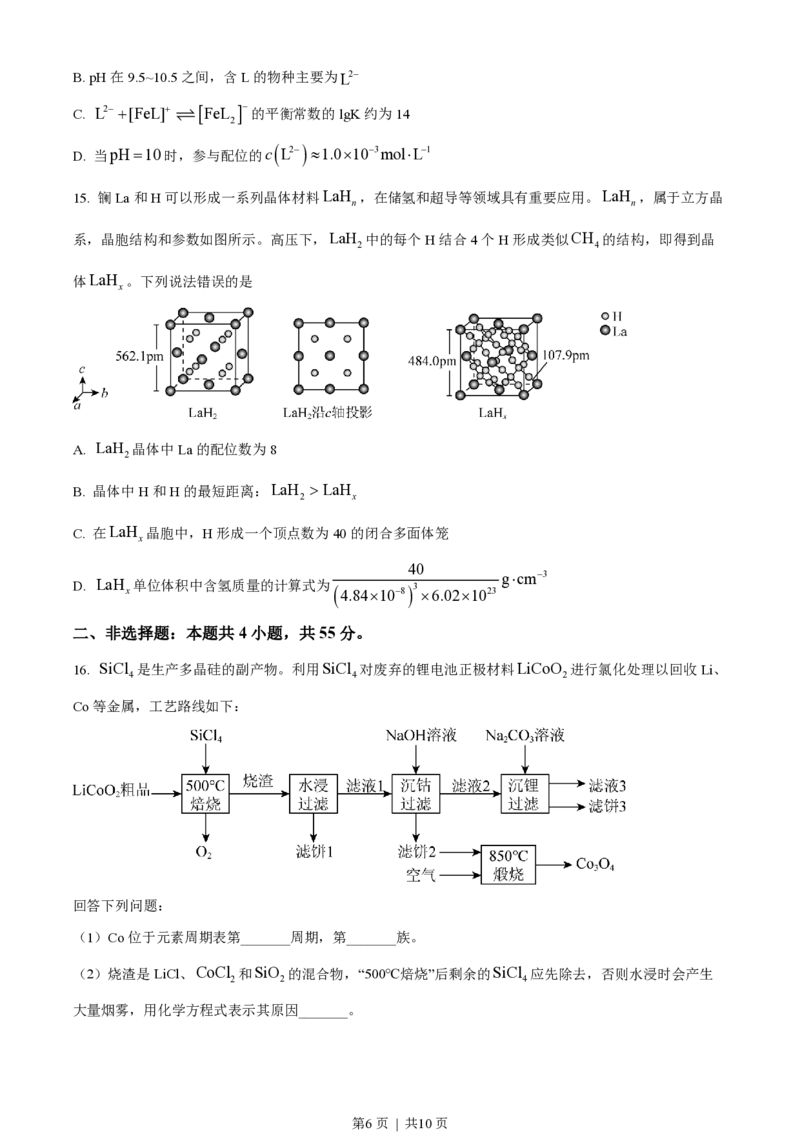文档内容
2023 年湖北省普通高中学业水平选择性考试
化学
本试卷共 8页,19题。全卷满分 100分。考试用时 75分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并认真核
准准考证号条形码上的以上信息,将条形码粘贴在答题卡,上的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答
题区域均无效。
3.选择题用 2B 铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作
答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
可能用到的相对原子质量:H1 Li7 O16 Si28 Cu64 I127 La139
一、选择题:本题共 15小题,每小题 3分,共 45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
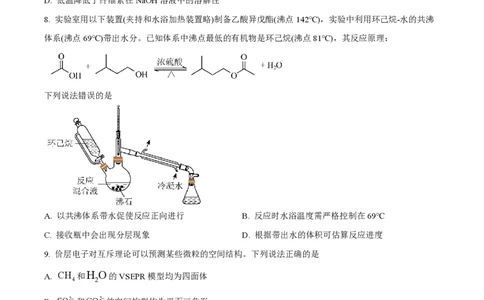
1. 2023年5月10日,天舟六号货运飞船成功发射,标志着我国航天事业进入到高质量发展新阶段。下列
不能作为火箭推进剂的是
A. 液氮-液氢 B. 液氧-液氢 C. 液态NO -肼 D. 液氧-煤油
2
2. 下列化学事实不符合“事物的双方既相互对立又相互统一”的哲学观点的是
A. 石灰乳中存在沉淀溶解平衡
B. 氯气与强碱反应时既是氧化剂又是还原剂
C. 铜锌原电池工作时,正极和负极同时发生反应
D. Li、Na、K的金属性随其核外电子层数增多而增强
3. 工业制备高纯硅的主要过程如下:
石英砂¾¾焦¾炭¾¾®粗硅¾¾HCl¾®SiHCl ¾¾H 2¾®高纯硅
1800~2000℃ 300℃ 3 1100℃
下列说法错误的是
高温
A. 制备粗硅的反应方程式为SiO +2C Si+2CO
2
B. 1molSi含Si-Si键的数目约为4´6.02´1023
C. 原料气HCl和H 应充分去除水和氧气
2
第1页 | 共10页D. 生成SiHCl 的反应为熵减过程
3
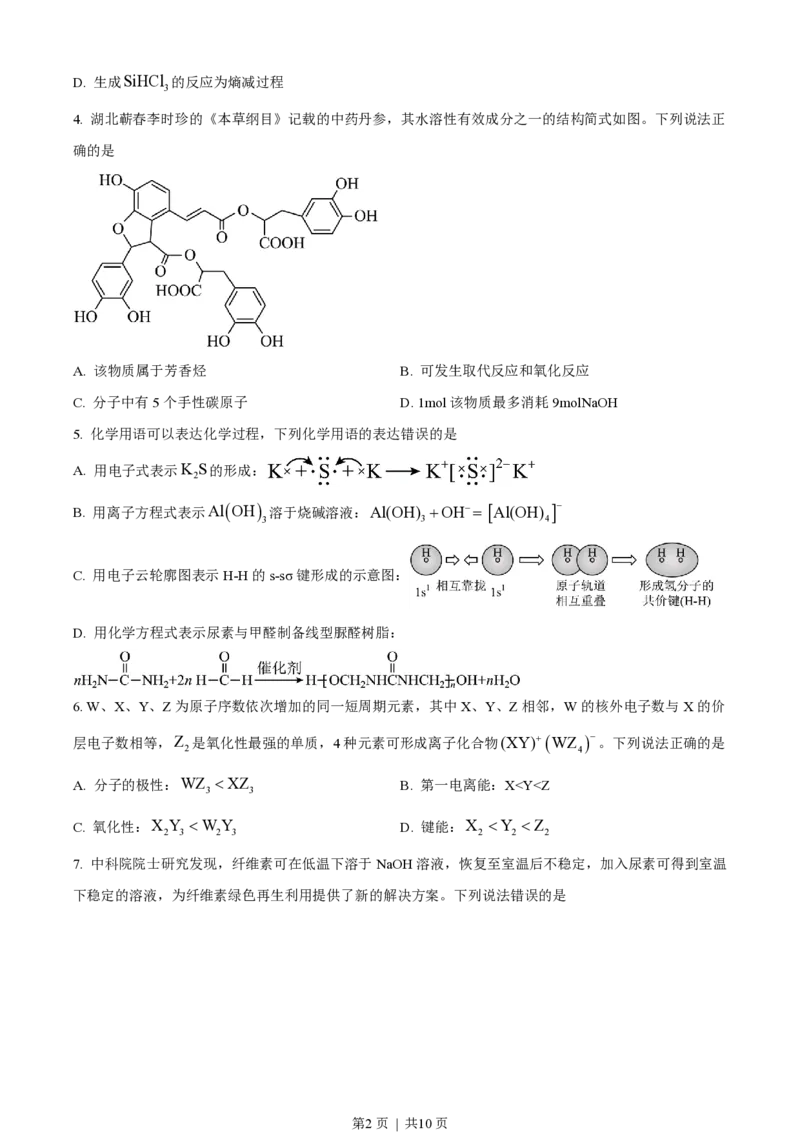
4. 湖北蕲春李时珍的《本草纲目》记载的中药丹参,其水溶性有效成分之一的结构简式如图。下列说法正
确的是
A. 该物质属于芳香烃 B. 可发生取代反应和氧化反应
C. 分子中有5个手性碳原子 D. 1mol该物质最多消耗9molNaOH
5. 化学用语可以表达化学过程,下列化学用语的表达错误的是
A. 用电子式表示K S的形成:
2
B. 用离子方程式表示AlOH 溶于烧碱溶液:Al(OH) +OH-= Al(OH) -
3 3 4
C. 用电子云轮廓图表示H-H的s-sσ键形成的示意图:
D. 用化学方程式表示尿素与甲醛制备线型脲醛树脂:
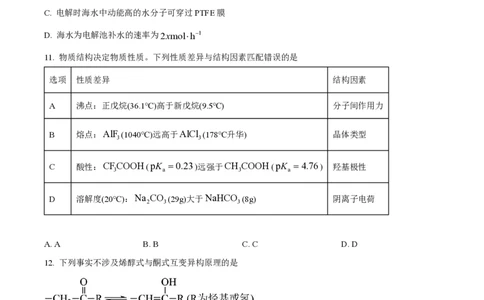
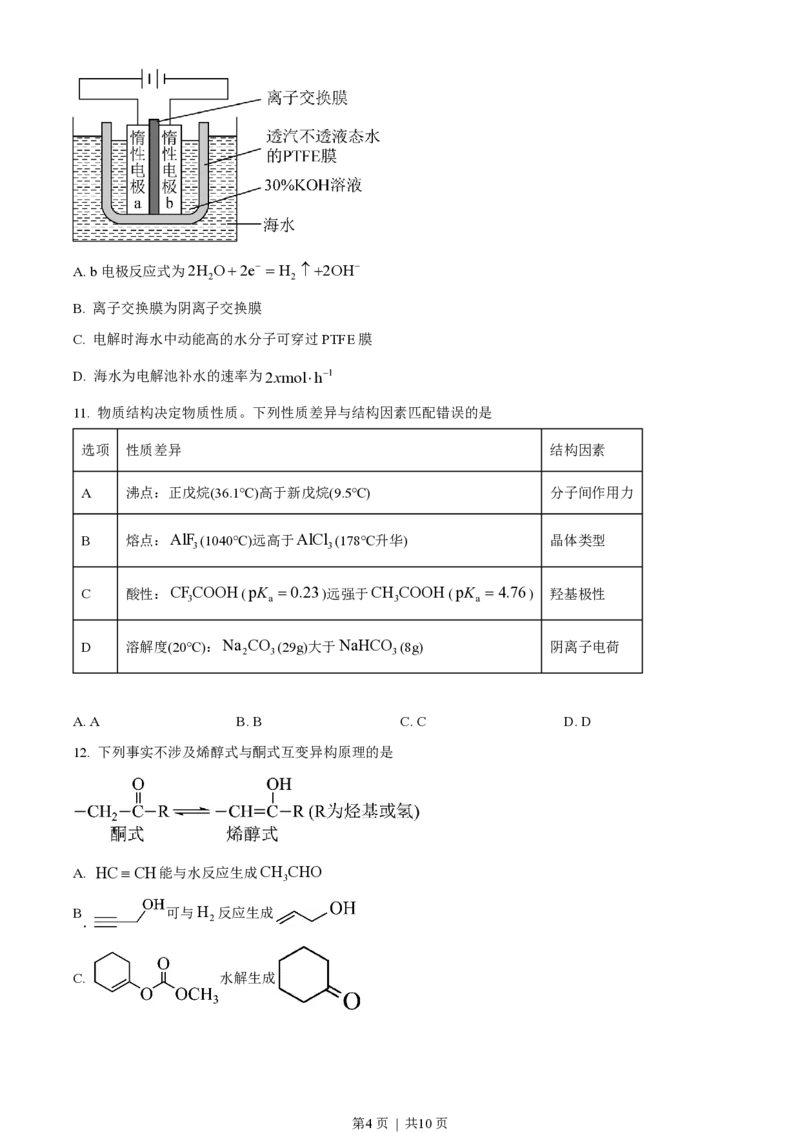
6. W、X、Y、Z为原子序数依次增加的同一短周期元素,其中X、Y、Z相邻,W的核外电子数与X的价
层电子数相等,Z 是氧化性最强的单质,4种元素可形成离子化合物(XY)+WZ - 。下列说法正确的是
2 4
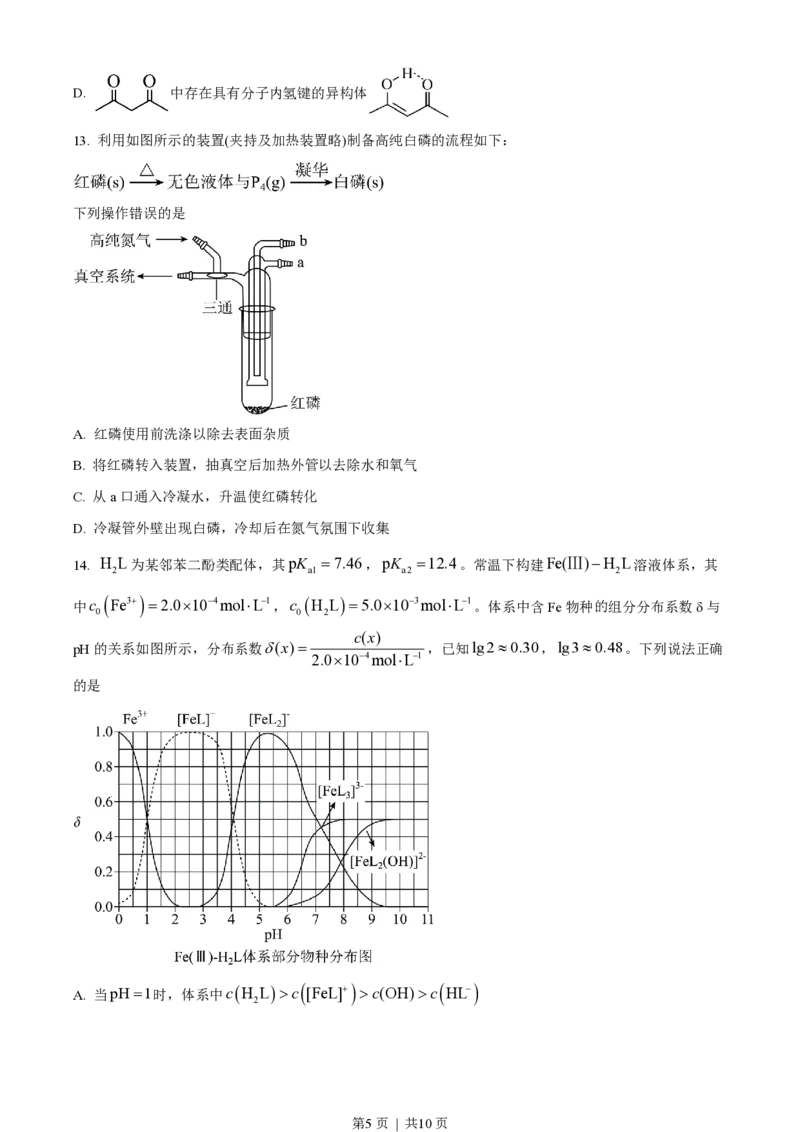
A. 分子的极性:WZ c [FeL]+ >c(OH)>c HL-
2
第5页 | 共10页B. pH在9.5~10.5之间,含L的物种主要为L2-
C. L2- +[FeL]+ FeL - 的平衡常数的lgK约为14
ƒ 2
D. 当pH =10时,参与配位的c L2- »1.0´10-3mol×L-1
15. 镧La和H可以形成一系列晶体材料LaH ,在储氢和超导等领域具有重要应用。LaH ,属于立方晶
n n
系,晶胞结构和参数如图所示。高压下,LaH 中的每个H结合4个H形成类似CH 的结构,即得到晶
2 4
体LaH 。下列说法错误的是
x
A. LaH 晶体中La的配位数为8
2
B. 晶体中H和H的最短距离:LaH >LaH
2 x
C. 在LaH 晶胞中,H形成一个顶点数为40的闭合多面体笼
x
40
g×cm-3
D. LaH x 单位体积中含氢质量的计算式为 4.84´10-83 ´6.02´1023
二、非选择题:本题共 4小题,共 55分。
16. SiCl 是生产多晶硅的副产物。利用SiCl 对废弃的锂电池正极材料LiCoO 进行氯化处理以回收Li、
4 4 2
Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第_______周期,第_______族。
(2)烧渣是LiCl、CoCl 和SiO 的混合物,“500℃焙烧”后剩余的SiCl 应先除去,否则水浸时会产生
2 2 4
大量烟雾,用化学方程式表示其原因_______。
第6页 | 共10页(3)鉴别洗净的“滤饼3”和固体Na CO 常用方法的名称是_______。
2 3
(4)已知K Co(OH) =5.9´10-15 ,若“沉钴过滤”的pH控制为10.0,则溶液中Co2+浓度为_______
sp 2
mol×L-1。“850℃煅烧”时的化学方程式为_______。
(5)导致SiCl 比CCl 易水解的因素有_______(填标号)。
4 4
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
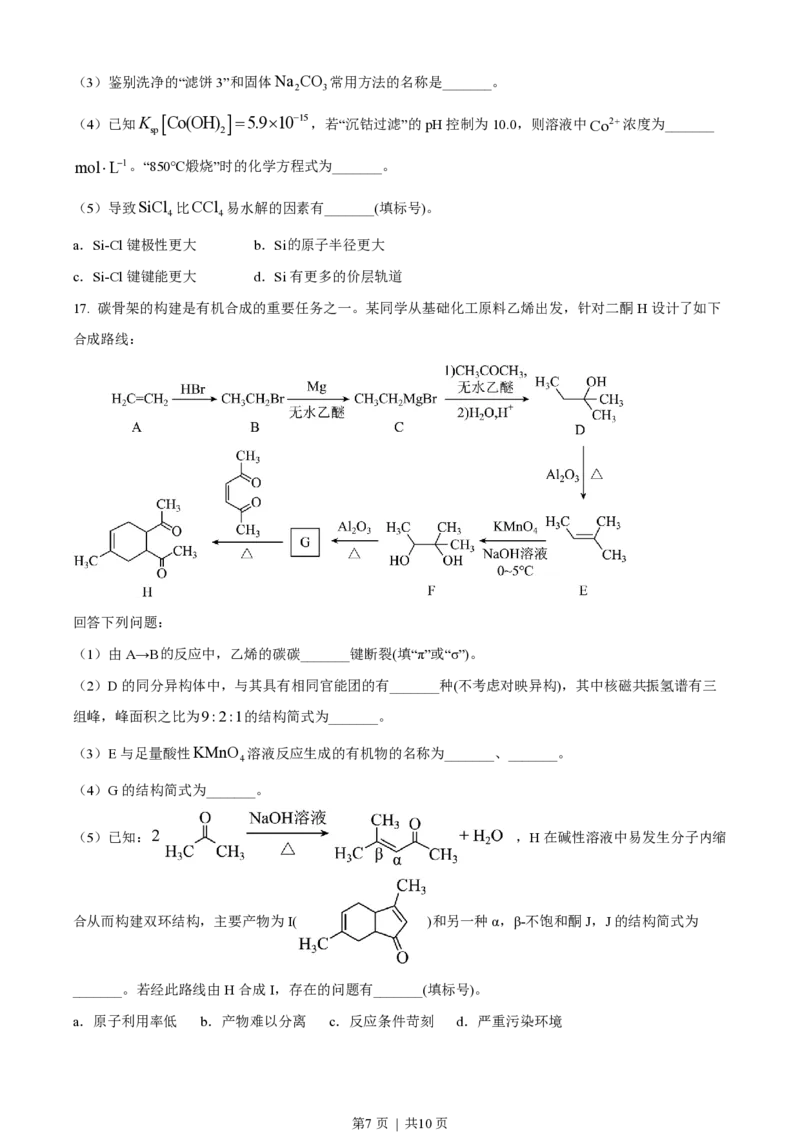
17. 碳骨架的构建是有机合成的重要任务之一。某同学从基础化工原料乙烯出发,针对二酮H设计了如下
合成路线:
回答下列问题:
(1)由A→B的反应中,乙烯的碳碳_______键断裂(填“π”或“σ”)。
(2)D的同分异构体中,与其具有相同官能团的有_______种(不考虑对映异构),其中核磁共振氢谱有三
组峰,峰面积之比为9:2:1的结构简式为_______。
(3)E与足量酸性KMnO 溶液反应生成的有机物的名称为_______、_______。
4
(4)G的结构简式为_______。
(5)已知: ,H在碱性溶液中易发生分子内缩
合从而构建双环结构,主要产物为I( )和另一种α,β-不饱和酮J,J的结构简式为
_______。若经此路线由H合成I,存在的问题有_______(填标号)。
a.原子利用率低 b.产物难以分离 c.反应条件苛刻 d.严重污染环境
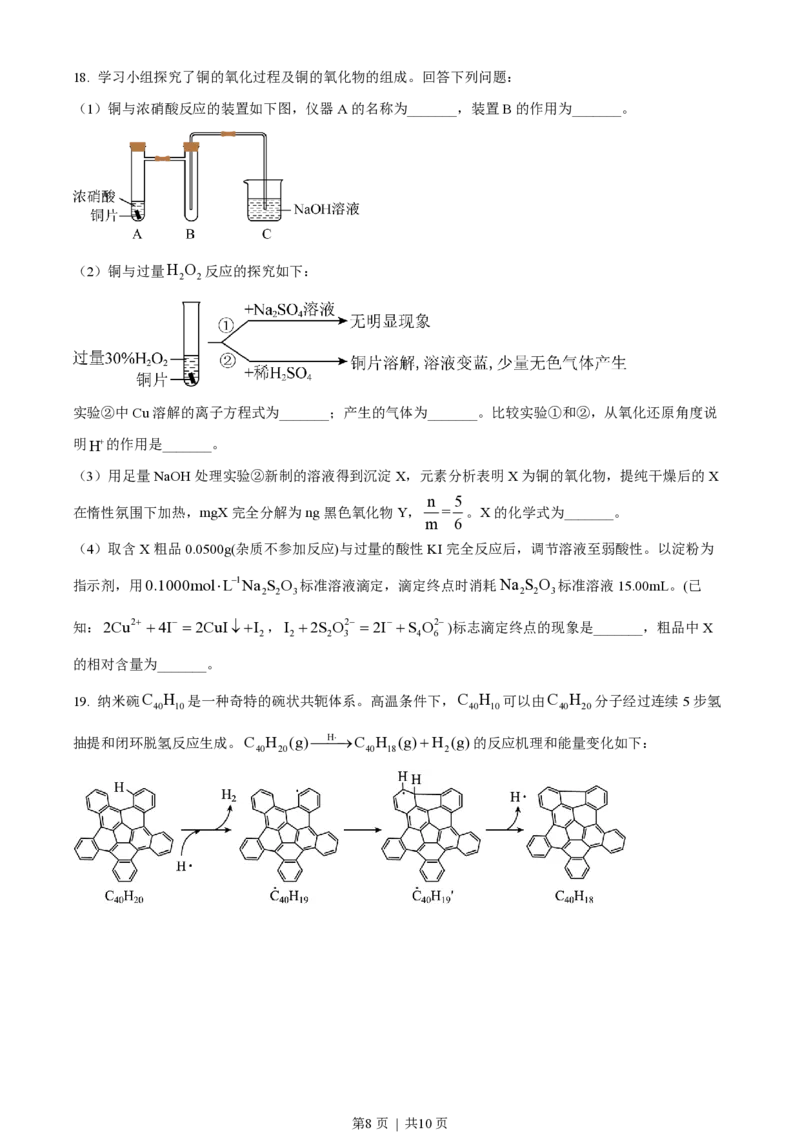
第7页 | 共10页18. 学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为_______,装置B的作用为_______。
(2)铜与过量H O 反应的探究如下:
2 2
实验②中Cu溶解的离子方程式为_______;产生的气体为_______。比较实验①和②,从氧化还原角度说
明H+的作用是_______。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X
n 5
在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y, = 。X的化学式为_______。
m 6
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为
指示剂,用0.1000mol×L-1Na S O 标准溶液滴定,滴定终点时消耗Na S O 标准溶液15.00mL。(已
2 2 3 2 2 3
知:2Cu2+ +4I- =2CuI¯+I ,I +2S O2- =2I- +S O2-)标志滴定终点的现象是_______,粗品中X
2 2 2 3 4 6
的相对含量为_______。
19. 纳米碗C H 是一种奇特的碗状共轭体系。高温条件下,C H 可以由C H 分子经过连续5步氢
40 10 40 10 40 20
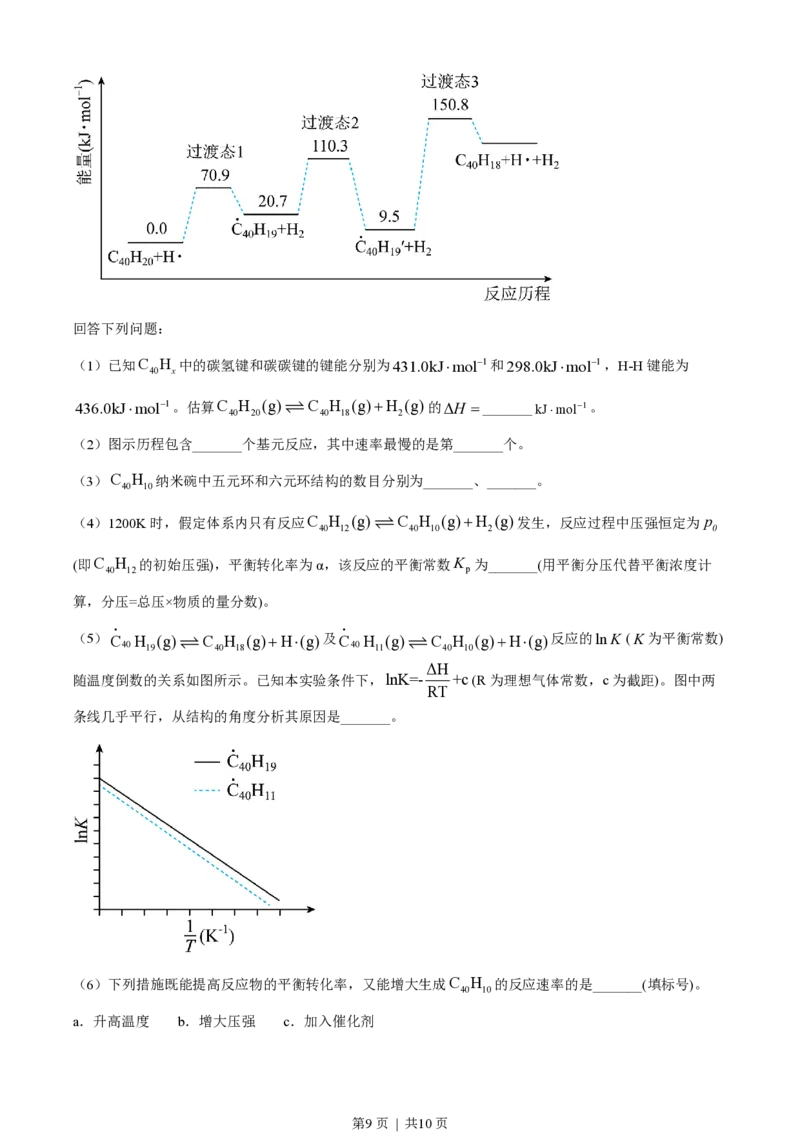
抽提和闭环脱氢反应生成。C H (g)¾H¾×®C H (g)+H (g)的反应机理和能量变化如下:
40 20 40 18 2
第8页 | 共10页回答下列问题:
(1)已知C H 中的碳氢键和碳碳键的键能分别为431.0kJ×mol-1和298.0kJ×mol-1,H-H键能为
40 x
436.0kJ×mol-1。估算C 40 H 20 (g) ƒ C 40 H 18 (g)+H 2 (g)的DH =_______kJ×mol-1。
(2)图示历程包含_______个基元反应,其中速率最慢的是第_______个。
(3)C H 纳米碗中五元环和六元环结构的数目分别为_______、_______。
40 10
(4)1200K时,假定体系内只有反应C
40
H
12
(g)
ƒ
C
40
H
10
(g)+H
2
(g)发生,反应过程中压强恒定为 p
0
(即C H 的初始压强),平衡转化率为α,该反应的平衡常数K 为_______(用平衡分压代替平衡浓度计
40 12 p
算,分压=总压×物质的量分数)。
(5)C g H (g) C H (g)+H×(g)及C g H (g) C H (g)+H×(g)反应的lnK (K为平衡常数)
40 19 ƒ 40 18 40 11 ƒ 40 10
ΔH
随温度倒数的关系如图所示。已知本实验条件下,lnK=- +c(R为理想气体常数,c为截距)。图中两
RT
条线几乎平行,从结构的角度分析其原因是_______。
(6)下列措施既能提高反应物的平衡转化率,又能增大生成C H 的反应速率的是_______(填标号)。
40 10
a.升高温度 b.增大压强 c.加入催化剂
第9页 | 共10页第10页 | 共10页