文档内容
2025 年普通高中学业水平选择性考试
化学
可能用到的相对原子质量:H—1 C—12 N—14 O—16 F—19 S—32 Co—59 I—127
Sm—150 Pb—207
一、选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
的
1. 河北省古建筑数量大,历史跨度长,种类齐全,在我国建筑史上占有非常重要 地位。下列古建筑组件
主要成分属于有机物的是
A.基石 B.斗拱 C.青瓦 D.琉璃
A. A B. B C. C D. D
2. 下列不符合实验安全要求的是
A. 酸、碱废液分别收集后直接排放 B. 进行化学实验时需要佩戴护目镜
C. 加热操作时选择合适的工具避免烫伤 D. 乙醇应存放在阴凉通风处,远离火种
3. 高分子材料在生产、生活中得到广泛应用。下列说法错误的是
A. ABS高韧性工程塑料用于制造汽车零配件 B. 聚氯乙烯微孔薄膜用于制造饮用水分离膜
C. 聚苯乙烯泡沫用于制造建筑工程保温材料 D. 热固性酚醛树脂用于制造集成电路的底板
4. 设N 是阿伏加德罗常数的值,下列说法错误的是
A
A. 18gH O晶体内氢键的数目为2N
2 A
B. 1L1mol×L-1的NaF溶液中阳离子总数为N
A
C. 28g环己烷和戊烯的混合物中碳原子的数目为2N
A
D. 铅酸蓄电池负极增重96g,理论上转移电子数为2N
A
5. 下列化学用语表述正确的是
第1页/共9页
学科网(北京)股份有限公司A. 中子数为12的氖核素:22Ne B. 氯化镁的电子式:
12
C. 甲醛分子的球棍模型: D. CO2-的价层电子对互斥模型:
3
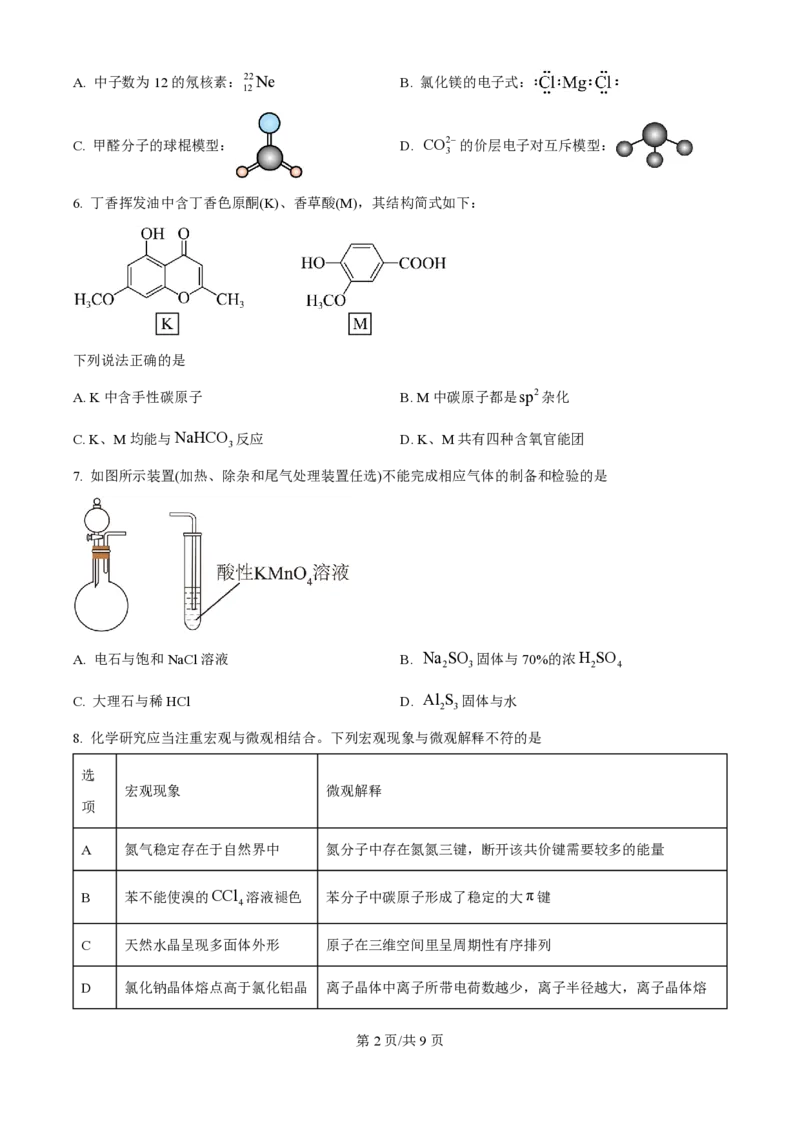
6. 丁香挥发油中含丁香色原酮(K)、香草酸(M),其结构简式如下:
下列说法正确的是
A. K中含手性碳原子 B. M中碳原子都是sp2杂化
C. K、M均能与NaHCO 反应 D. K、M共有四种含氧官能团
3
7. 如图所示装置(加热、除杂和尾气处理装置任选)不能完成相应气体的制备和检验的是
A. 电石与饱和NaCl溶液 B. Na SO 固体与70%的浓H SO
2 3 2 4
C. 大理石与稀HCl D. Al S 固体与水
2 3
8. 化学研究应当注重宏观与微观相结合。下列宏观现象与微观解释不符的是
选
宏观现象 微观解释
项
A 氮气稳定存在于自然界中 氮分子中存在氮氮三键,断开该共价键需要较多的能量
B 苯不能使溴的CCl 溶液褪色 苯分子中碳原子形成了稳定的大π键
4
C 天然水晶呈现多面体外形 原子在三维空间里呈周期性有序排列
D 氯化钠晶体熔点高于氯化铝晶 离子晶体中离子所带电荷数越少,离子半径越大,离子晶体熔
第2页/共9页
学科网(北京)股份有限公司体 点越低
A. A B. B C. C D. D
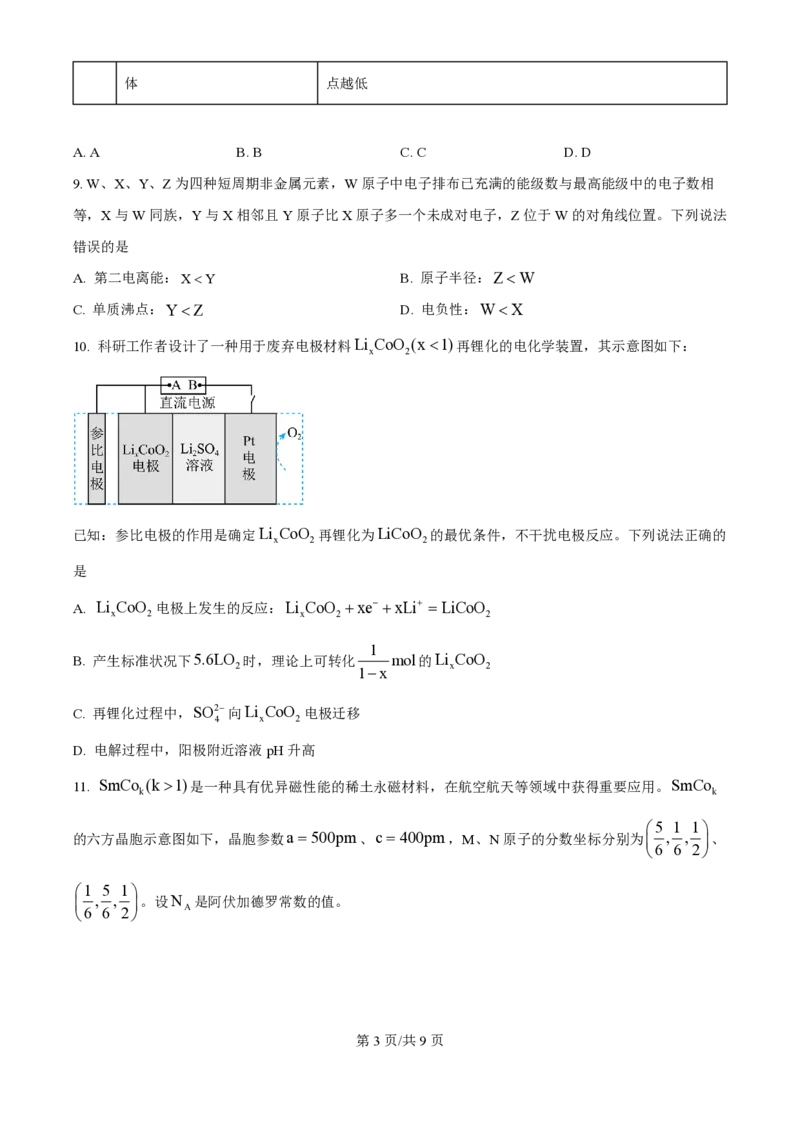
9. W、X、Y、Z为四种短周期非金属元素,W原子中电子排布已充满的能级数与最高能级中的电子数相
等,X与W同族,Y与X相邻且Y原子比X原子多一个未成对电子,Z位于W的对角线位置。下列说法
错误的是
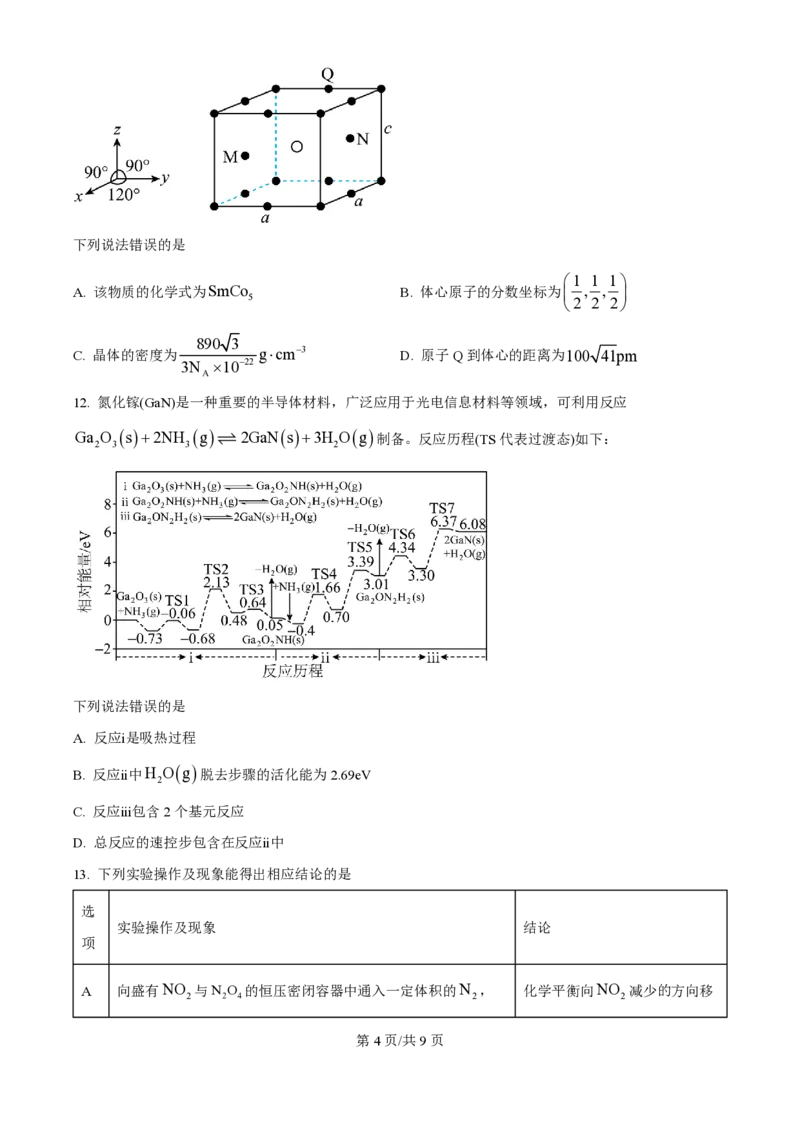
A. 第二电离能:X1)是一种具有优异磁性能的稀土永磁材料,在航空航天等领域中获得重要应用。SmCo
k k
æ5 1 1ö
的六方晶胞示意图如下,晶胞参数a =500pm、c=400pm,M、N原子的分数坐标分别为ç , , ÷、
è6 6 2ø
æ1 5 1ö
ç , , ÷。设N 是阿伏加德罗常数的值。
è6 6 2ø A
第3页/共9页
学科网(北京)股份有限公司下列说法错误的是
æ1 1 1ö
A. 该物质的化学式为SmCo B. 体心原子的分数坐标为ç , , ÷
5 è2 2 2ø
890 3
C. 晶体的密度为 g×cm-3 D. 原子Q到体心的距离为100 41pm
3N ´10-22
A
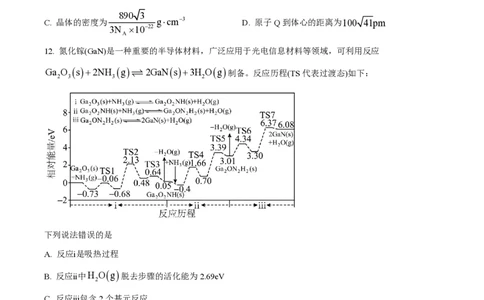
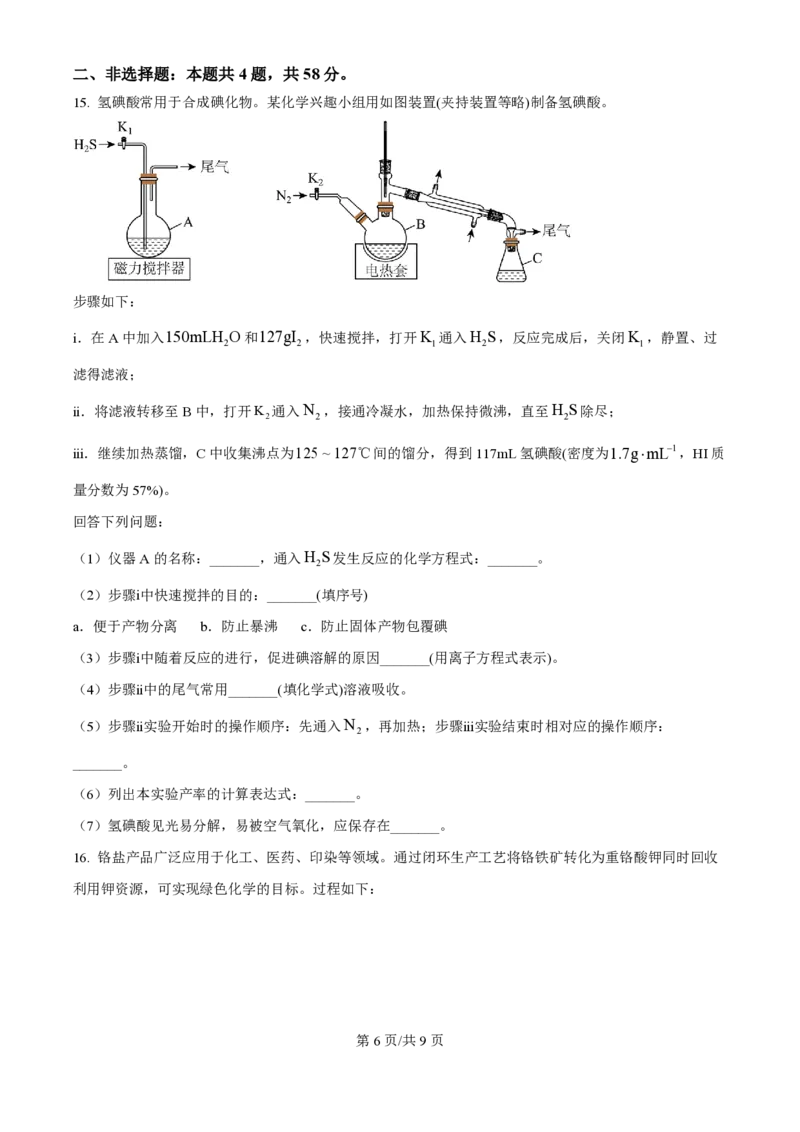
12. 氮化镓(GaN)是一种重要的半导体材料,广泛应用于光电信息材料等领域,可利用反应
Ga 2 O 3 s+2NH 3 g ƒ 2GaNs+3H 2 Og 制备。反应历程(TS代表过渡态)如下:
下列说法错误的是
A. 反应ⅰ是吸热过程
B. 反应ⅱ中H Og 脱去步骤的活化能为2.69eV
2
C. 反应ⅲ包含2个基元反应
D. 总反应的速控步包含在反应ⅱ中
13. 下列实验操作及现象能得出相应结论的是
选
实验操作及现象 结论
项
A 向盛有NO 与N O 的恒压密闭容器中通入一定体积的N , 化学平衡向NO 减少的方向移
2 2 4 2 2
第4页/共9页
学科网(北京)股份有限公司最终气体颜色变浅 动
以K CrO 为指示剂,用AgNO 标准溶液滴定溶液中的Cl-,
B 2 4 3 K AgClc CuL 4- >c CuL- >c L3-
2
第5页/共9页
学科网(北京)股份有限公司二、非选择题:本题共 4题,共 58分。
15. 氢碘酸常用于合成碘化物。某化学兴趣小组用如图装置(夹持装置等略)制备氢碘酸。
步骤如下:
ⅰ.在A中加入150mLH O和127gI ,快速搅拌,打开K 通入H S,反应完成后,关闭K ,静置、过
2 2 1 2 1
滤得滤液;
ⅱ.将滤液转移至B中,打开K 通入N ,接通冷凝水,加热保持微沸,直至H S除尽;
2 2 2
ⅲ.继续加热蒸馏,C中收集沸点为125~127℃间的馏分,得到117mL氢碘酸(密度为1.7g×mL-1,HI质
量分数为57%)。
回答下列问题:
(1)仪器A的名称:_______,通入H S发生反应的化学方程式:_______。
2
(2)步骤ⅰ中快速搅拌的目的:_______(填序号)
a.便于产物分离 b.防止暴沸 c.防止固体产物包覆碘
(3)步骤ⅰ中随着反应的进行,促进碘溶解的原因_______(用离子方程式表示)。
(4)步骤ⅱ中的尾气常用_______(填化学式)溶液吸收。
(5)步骤ⅱ实验开始时的操作顺序:先通入N ,再加热;步骤ⅲ实验结束时相对应的操作顺序:
2
_______。
(6)列出本实验产率的计算表达式:_______。
(7)氢碘酸见光易分解,易被空气氧化,应保存在_______。
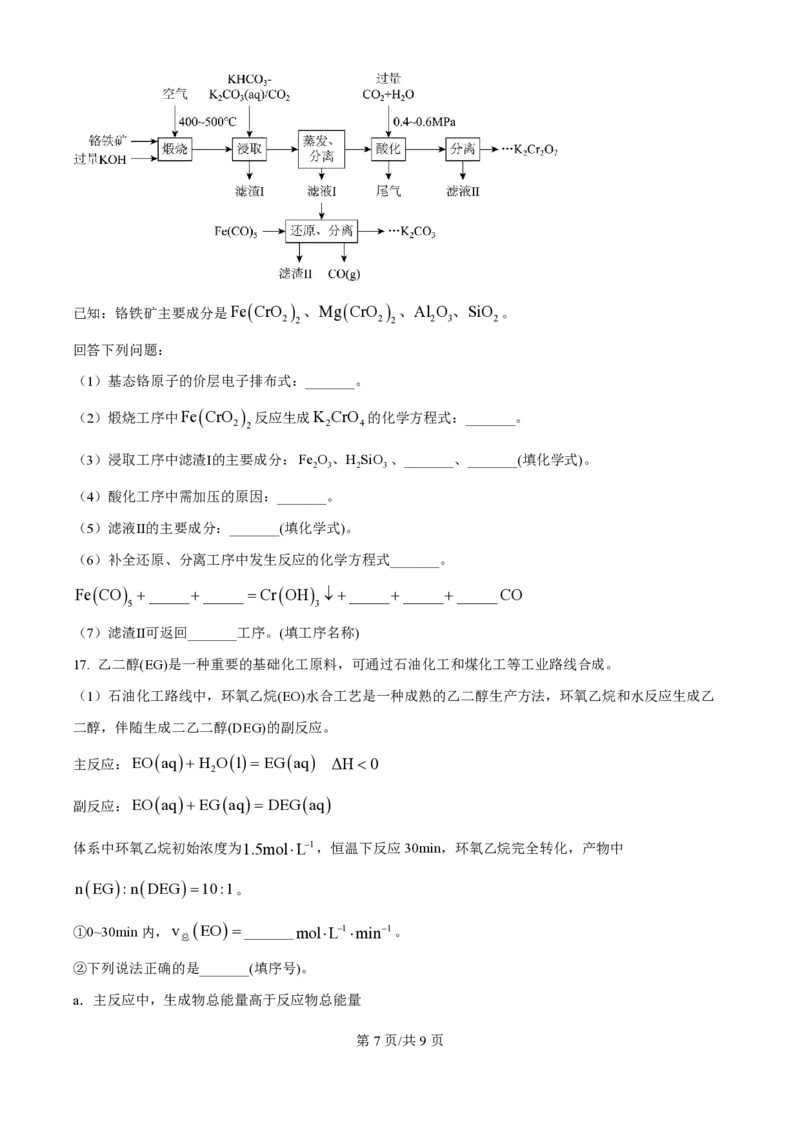
16. 铬盐产品广泛应用于化工、医药、印染等领域。通过闭环生产工艺将铬铁矿转化为重铬酸钾同时回收
利用钾资源,可实现绿色化学的目标。过程如下:
第6页/共9页
学科网(北京)股份有限公司已知:铬铁矿主要成分是FeCrO 、MgCrO 、Al O、SiO 。
2 2 2 2 2 3 2
回答下列问题:
(1)基态铬原子的价层电子排布式:_______。
(2)煅烧工序中FeCrO 反应生成K CrO 的化学方程式:_______。
2 2 2 4
(3)浸取工序中滤渣Ⅰ的主要成分:Fe O、H SiO 、_______、_______(填化学式)。
2 3 2 3
(4)酸化工序中需加压的原因:_______。
(5)滤液Ⅱ的主要成分:_______(填化学式)。
(6)补全还原、分离工序中发生反应的化学方程式_______。
FeCO +_____+_____ =CrOH ¯+_____+_____+_____CO
5 3
(7)滤渣Ⅱ可返回_______工序。(填工序名称)
17. 乙二醇(EG)是一种重要的基础化工原料,可通过石油化工和煤化工等工业路线合成。
(1)石油化工路线中,环氧乙烷(EO)水合工艺是一种成熟的乙二醇生产方法,环氧乙烷和水反应生成乙
二醇,伴随生成二乙二醇(DEG)的副反应。
主反应:EOaq+H Ol= EGaq ΔH<0
2
副反应:EOaq+EGaq= DEGaq
体系中环氧乙烷初始浓度为1.5mol×L-1,恒温下反应30min,环氧乙烷完全转化,产物中
nEG:nDEG=10:1。
①0~30min内,v EO=_______mol×L-1×min-1。
总
②下列说法正确的是_______(填序号)。
a.主反应中,生成物总能量高于反应物总能量
第7页/共9页
学科网(北京)股份有限公司b.0~30min内,v EO= v EG
总 总
c.0~30min内,v EG:v DEG=11:1
主 副
d.选择适当催化剂可提高乙二醇的最终产率
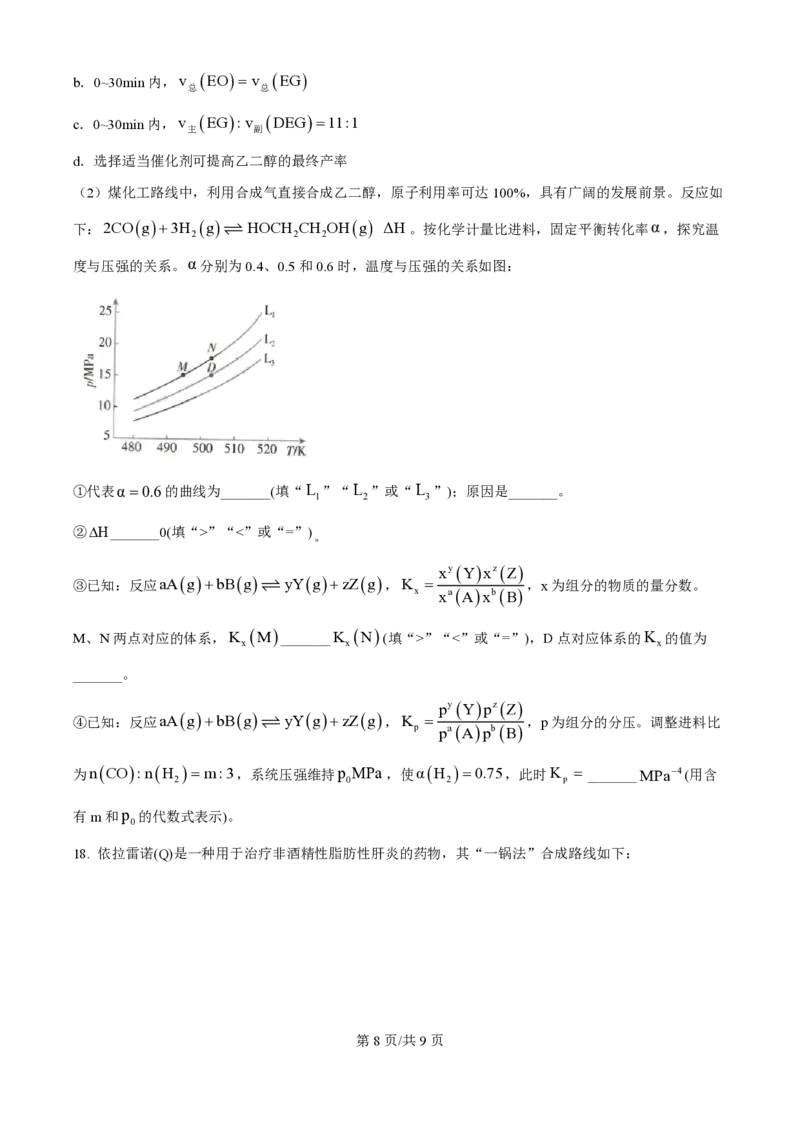
(2)煤化工路线中,利用合成气直接合成乙二醇,原子利用率可达100%,具有广阔的发展前景。反应如
下:2COg+3H g HOCH CH OHg ΔH。按化学计量比进料,固定平衡转化率α,探究温
2 ƒ 2 2
度与压强的关系。α分别为0.4、0.5和0.6时,温度与压强的关系如图:
①代表α=0.6的曲线为_______(填“L ”“L ”或“L ”);原因是_______。
1 2 3
②DH_______0(填“>”“<”或“=”)
。
xyYxzZ
③已知:反应aAg+bBg
ƒ
yYg+zZg ,K
x
=
xaAxbB
,x为组分的物质的量分数。
M、N两点对应的体系,K M _______K N (填“>”“<”或“=”),D点对应体系的K 的值为
x x x
_______。
pyYpzZ
④已知:反应aAg+bBg
ƒ
yYg+zZg ,K
p
=
paApbB
,p为组分的分压。调整进料比
为nCO:nH = m:3,系统压强维持p MPa,使αH =0.75,此时K = _______MPa-4(用含
2 0 2 p
有m和p 的代数式表示)。
0
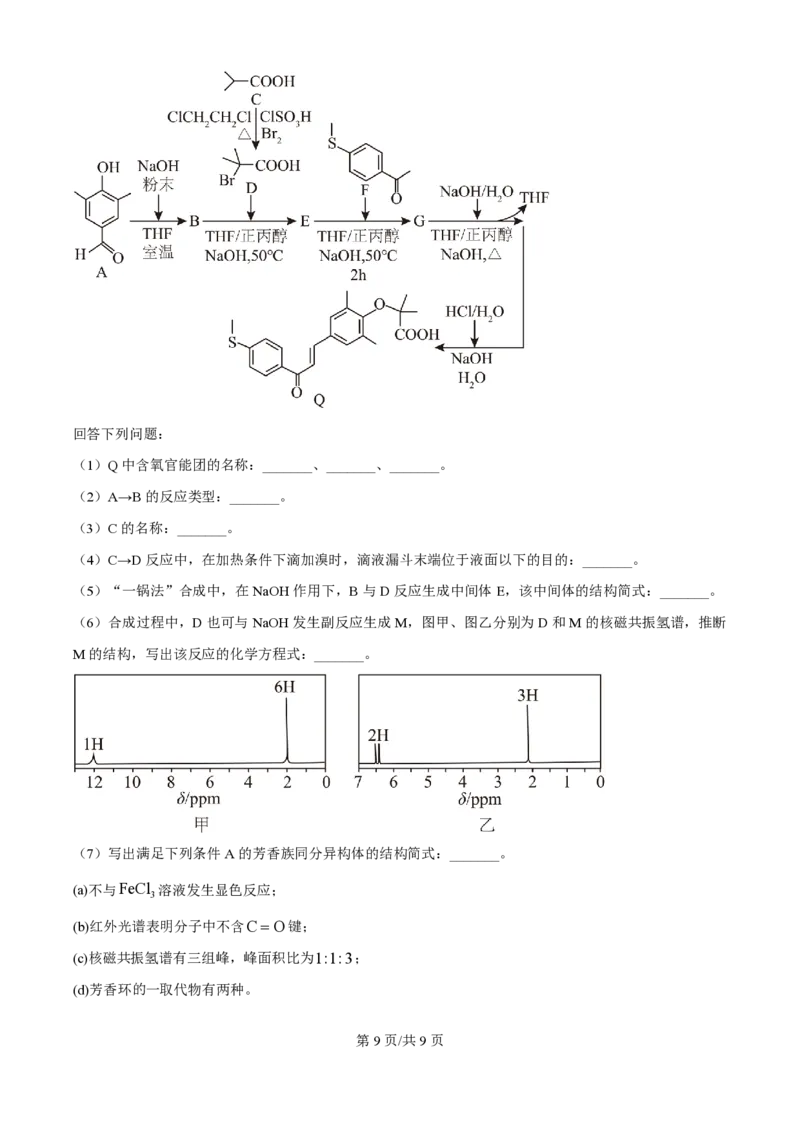
18. 依拉雷诺(Q)是一种用于治疗非酒精性脂肪性肝炎的药物,其“一锅法”合成路线如下:
第8页/共9页
学科网(北京)股份有限公司回答下列问题:
(1)Q中含氧官能团的名称:_______、_______、_______。
(2)A→B的反应类型:_______。
(3)C的名称:_______。
(4)C→D反应中,在加热条件下滴加溴时,滴液漏斗末端位于液面以下的目的:_______。
(5)“一锅法”合成中,在NaOH作用下,B与D反应生成中间体E,该中间体的结构简式:_______。
(6)合成过程中,D也可与NaOH发生副反应生成M,图甲、图乙分别为D和M的核磁共振氢谱,推断
M的结构,写出该反应的化学方程式:_______。
(7)写出满足下列条件A的芳香族同分异构体的结构简式:_______。
(a)不与FeCl 溶液发生显色反应;
3
(b)红外光谱表明分子中不含C=O键;
(c)核磁共振氢谱有三组峰,峰面积比为1:1:3;
(d)芳香环的一取代物有两种。
第9页/共9页
学科网(北京)股份有限公司