【指南文件】第二类医疗器械独立软件技术审评指南


请点我关注,亦可加微信拉入群互动。
请备注“器械注册里外事”。
【版权声明】本文由『 器械注册里外事 』整理/转载,欢迎转发。如需转载,请在醒目处标注来源于公众号『 器械注册里外事 』。
医疗器械人的专属工具
【适用人群】研发人员、RA人员、市场人员、销售人员、监管人员,其他医疗器械的爱好者
特此通告。



来源:上海器审
整理:器械注册里外事
『 精彩回顾』
【注册/法规汇总】
【临床评价】
-
西格玛医学洞见:一文读懂角膜塑形镜及临床试验设计
【答疑解惑】
【培训专栏】
-
【专栏12–回放汇总】影响体外诊断试剂设计开发思路的新老法规差异分析(1-6)线上课程部分回放汇总
-
【专栏13–回放汇总】医疗器械注册质量管理体系核查指南线上课程回放汇总
-
【专栏14–回放汇总】新法规下第一类医疗器械如何申报(1-4)线上课程回放汇总 -
【专栏15–回放汇总】医疗器械产品留样检查要点指南(1-2)线上课程回放汇总 -
【专栏16~专栏1–回放汇总】医疗器械生产企业质量控制与成品放行(16)~医疗器械监管条例条款讲解(1)线上课程回放汇总
【审评报告】
【分类界定】
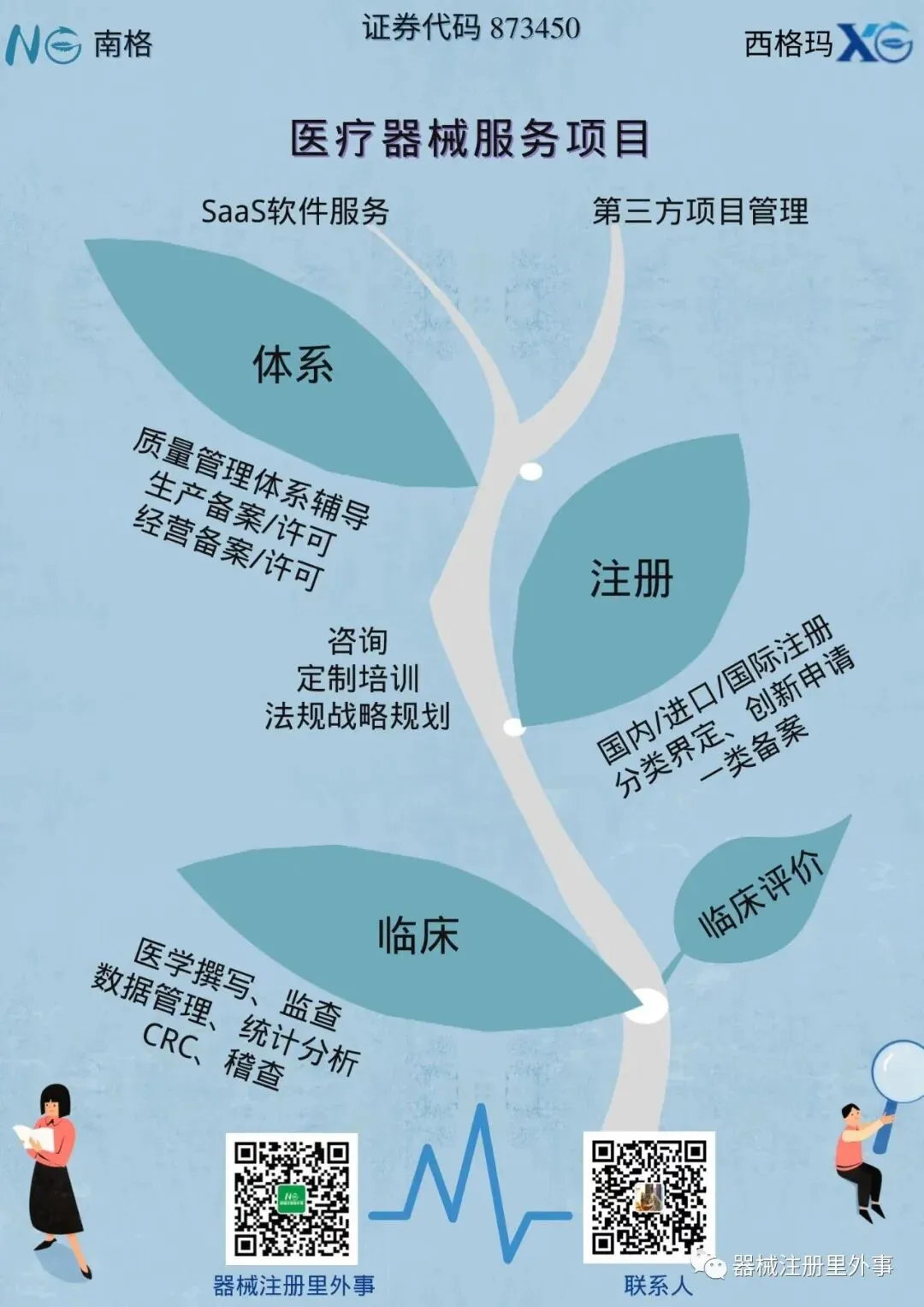


 长按识别二维码
长按识别二维码
『器械注册里外事』公众号
微信重要提示
目前,微信公众号浏览顺序已经不是按时间,而是随机推送。
所以,如果您对我们没有星标,或很少点在看,“器械注册里外事”将不会出现在您的公众号列表中,您可能看不到我们的推送消息了。
如果您觉得“器械注册里外事”有用
请把我们标记上星标(点亮)
或给我们一个「在看」(文末右下角)
或直接点击左下角「点赞」
感谢您一路陪伴和支持。
 夜雨聆风
夜雨聆风






