初三化学中考总复习知识点汇总(附word下载)




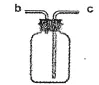
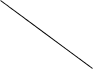
多功能瓶的使用:


  |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
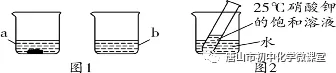
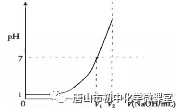 (3) 甲、乙两同学在盐酸中逐滴滴加氢氧化钠溶液过程中,多次测定溶液的pH,并据此画出如右图的曲线,请回答:
(3) 甲、乙两同学在盐酸中逐滴滴加氢氧化钠溶液过程中,多次测定溶液的pH,并据此画出如右图的曲线,请回答:|
|
|
|
|
|
|
|
|
|
|
链接(点击蓝色字迹即可)
1. 中考复习专题
2. 沪教版上下册全套微课
3. 人教版上下册全套微课
4. 在线测试中考真题全套
5.人教版说课稿上下册
6.在线测试一轮复习考点24套
7.化学复习基础知识(上)(下)答案版
8.2018、2019、2020中考真题分类汇编
9.人教版导学案上下册全套
10.全国初中化学优质课汇总
学生请加 QQ群:1065953380
初中化学老师:请添加我的微信号18633177917加我好友,就能加入全国初中化学老师群(微信)。

初三化学中考总复习知识点汇总:
链接:https://pan.baidu.com/s/1W_UEIkwdGc1b6fzTpiNlEw
提取码:8888
复制这段内容后打开百度网盘手机App,操作更方便哦

初三化学中考总复习知识点汇总:
链接:https://pan.baidu.com/s/1W_UEIkwdGc1b6fzTpiNlEw
提取码:8888
复制这段内容后打开百度网盘手机App,操作更方便哦
 夜雨聆风
夜雨聆风





