阿尔茨海默病(AD)诊断说明
随着人口老龄化的进程加快,老年性疾病居高不下,以本文提到的阿兹海默症为例,虽没有所谓的诊断金标准,目前阿尔茨海默病的诊断已从传统的“临床症状推测”升级为“临床症状+生物标志物+排除其他病因”的精准模式,根据2025年最新中国及国际诊疗指南,核心诊断逻辑如下:
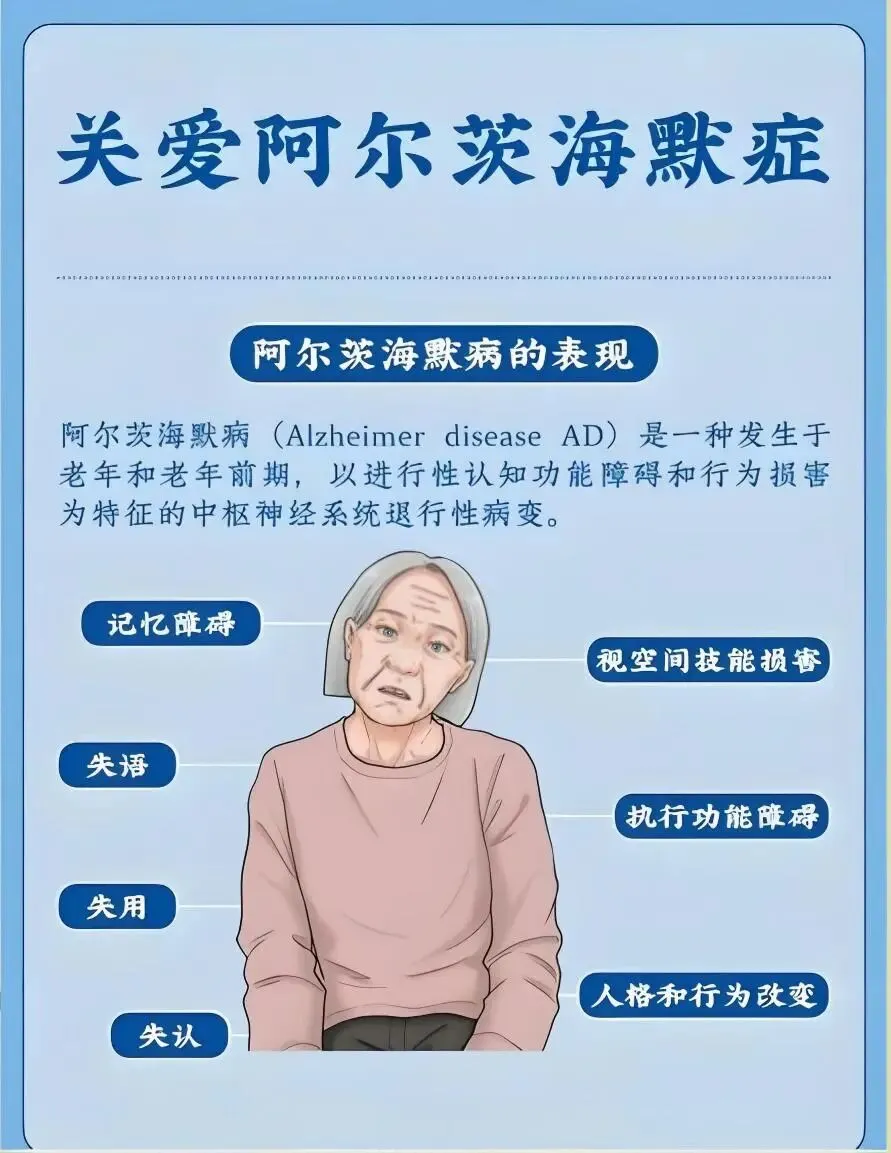
一、诊断核心依据
诊断需同时满足以下两类证据,准确率可达90%以上:
1. 临床症状证据
·核心表现:隐袭起病、持续进展的认知功能减退,首发症状以情景记忆障碍最典型(如记不住近期发生的事、重复询问同一问题),可伴随执行功能下降(如不会做饭、管不好钱)、语言障碍(找词困难)、视空间障碍(熟悉环境迷路)、精神行为改变(淡漠、多疑、易怒)。
·病程特点:症状持续≥6个月,且已影响日常独立生活能力。
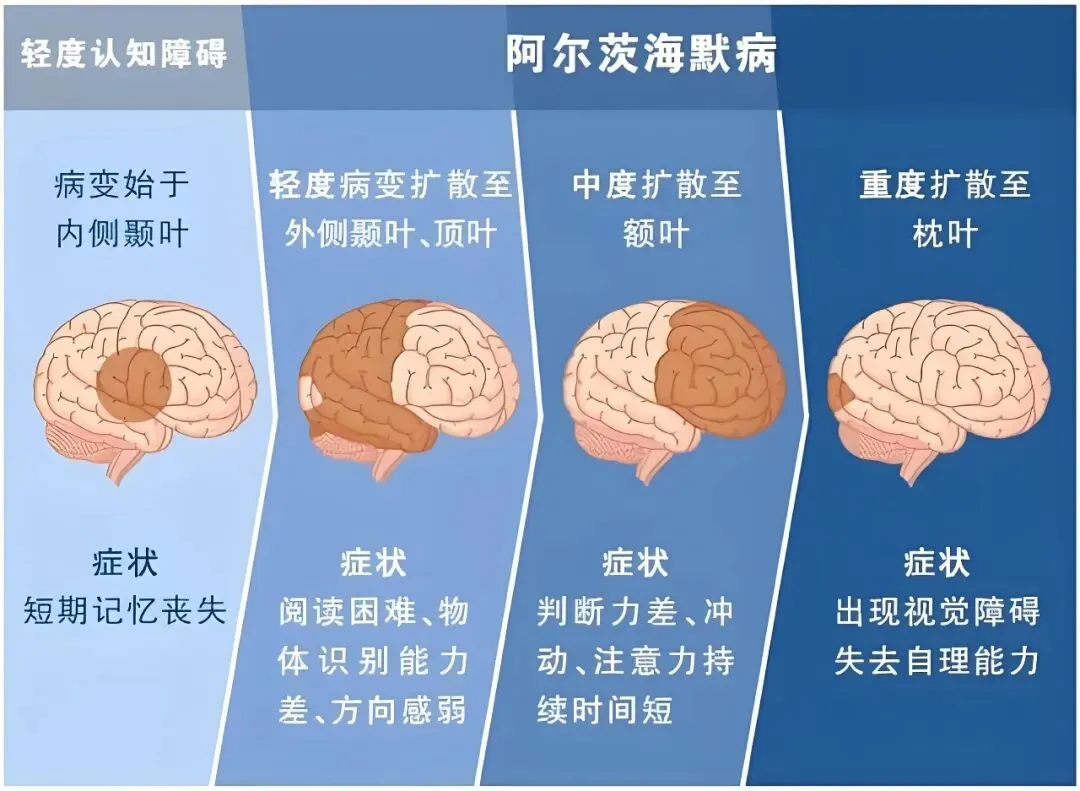
2. 生物标志物证据(病理确诊核心)
国际通用A/T/N生物标志物框架验证AD病理改变:
|
分类 |
标志物 |
检测方法 |
临床意义 |
|
A(β淀粉样蛋白病理) |
Aβ沉积 |
脑脊液Aβ42/40比值降低、淀粉样蛋白PET显像阳性 |
反映AD的核心病理启动因素,是靶向药物治疗的必要前提 |
|
T(tau蛋白病理) |
磷酸化tau蛋白升高 |
脑脊液p-tau181/p-tau217升高、血浆p-tau217升高、tau-PET显像阳性 |
与认知损害程度直接相关,可反映疾病进展速度 |
|
N(神经退行性变) |
神经元损伤 |
结构MRI显示海马/内侧颞叶萎缩、FDG-PET显示颞顶叶代谢降低、血液/脑脊液神经丝轻链(NfL)升高 |
反映大脑受损的严重程度,辅助鉴别其他类型痴呆 |
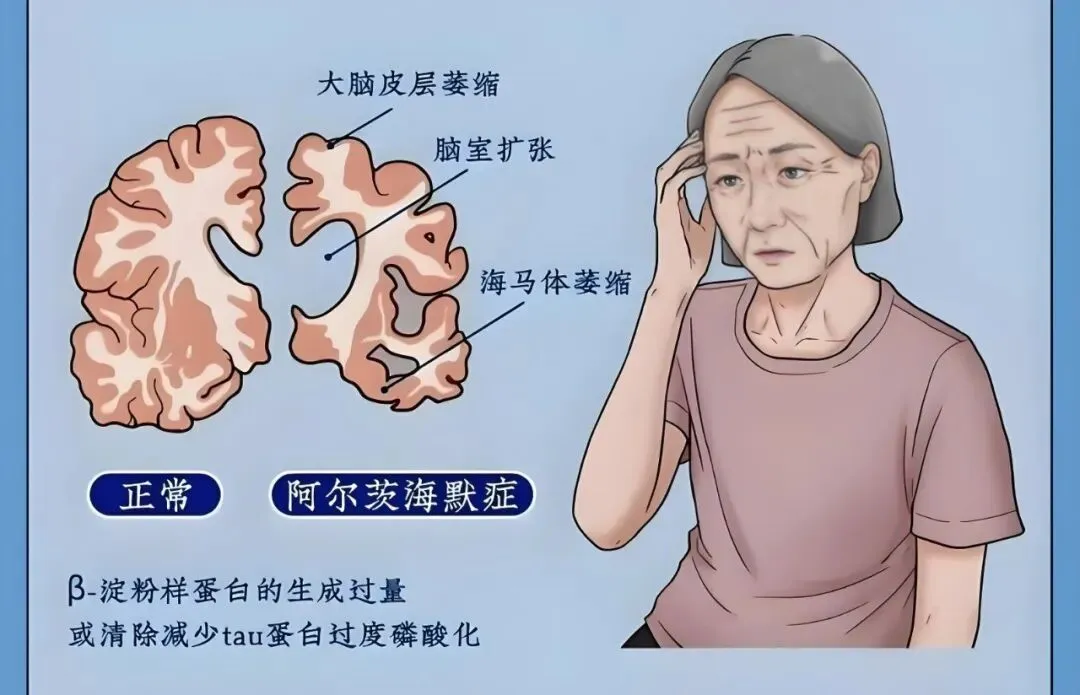
二、标准诊断流程
临床通常分三步完成诊断,适合各级医疗机构推广:
第一步:初筛识别(基层可完成)
1.症状筛查:通过询问患者及家属,排查AD早期10大警示信号:近记忆减退、熟悉事务完成困难、语言表达障碍、时间/地点定向力差、判断力下降、物品错置找不到、情绪性格突变、视空间能力下降(如上下楼梯踩空)、社交退缩、重复行为。
2.认知量表初筛:使用蒙特利尔认知评估量表(MoCA)或简易精神状态检查表(MMSE),MoCA对轻度认知障碍(MCI)更敏感,得分≤26分提示可能存在认知损害(需结合文化程度调整,文盲可适当放宽阈值)。
3.血液初筛:常规检查血常规、甲状腺功能、维生素B12/叶酸水平,排除甲状腺功能减退、维生素缺乏等可逆性认知障碍;有条件可联合血浆p-tau217+Aβ42/40比值检测,作为AD病理的无创初筛工具,准确率可达90%左右。
第二步:深度鉴别(二级以上医院完成)
1.全面神经心理学评估:通过专项记忆、执行功能、语言能力测试,明确认知损害模式(AD以“海马型遗忘综合征”为典型特征)。
2.结构影像学检查:常规做头颅MRI,观察是否存在海马、内侧颞叶萎缩,同时排除脑梗死、脑出血、脑肿瘤、正常压力脑积水等其他可导致认知障碍的脑部疾病。
3.排除其他痴呆类型:
o血管性痴呆:有卒中史,认知呈阶梯式下降,影像学可见多发梗死灶;
o路易体痴呆:伴随波动性认知障碍、反复视幻觉、帕金森样手抖症状;
o额颞叶痴呆:早期以性格改变、行为异常为首发,遗忘症状出现较晚,MRI显示额叶/颞叶前部萎缩。

第三步:病理确诊(三甲医院/记忆专科完成)
若前两步高度怀疑AD,可通过以下检查“一锤定音”:
·优先选择脑脊液检测:联合检测Aβ42、p-tau、总tau,是目前性价比最高的确诊手段;
·或选择淀粉样蛋白PET显像:可直接可视化脑内Aβ斑块沉积,适合无法耐受腰穿的患者;
·若以上两项均提示AD病理阳性,即可明确诊断。
三、诊断分层标准
根据证据充分程度,临床将诊断分为三个层级:
1.临床疑似AD:仅符合典型临床症状,无生物标志物支持;
2.很可能AD:符合临床症状+影像学/血液生物标志物提示AD特征,排除其他病因;
3.确定AD:符合临床症状+脑脊液/淀粉样蛋白PET生物标志物明确阳性,或尸检/脑活检发现AD特征性病理改变(老年斑、神经原纤维缠结)。
四、注意事项
1.不建议无症状人群筛查:目前不推荐对无认知症状的普通人群常规进行AD生物标志物检测,避免不必要的心理负担;
2.早期诊断价值最大:AD的病理改变在症状出现前10-20年就已启动,轻度认知障碍(MCI)阶段是干预黄金期,明确诊断后可尽早使用靶向药物(如抗Aβ单抗)延缓疾病进展;
3.诊断≠“判死刑”:AD是可干预的慢性病,明确诊断后通过药物+非药物联合干预,可有效延长患者独立生活时间,改善生存质量。
当然通过BIOKAT系统的相关内容,也可以做一些必要的检测和治疗,也是一种积极面对的方法。
物质信息诊疗
温柔精准疗法
恢复身体平衡
愿你我都被这个世界健康温柔以待
关注我,给您更多精彩

 夜雨聆风
夜雨聆风





